INTRODUCCIÓN
Según el Informe Mundial sobre la Discapacidad 95 millones de niños en todo el mundo presentan alguna discapacidad, de ellos 13 millones (el 0,7%) tienen una discapacidad grave.1 La parálisis cerebral infantil (PCI) es la causa más frecuen te de discapacidad motora durante la niñez.2,3
La PCI no es una enfermedad específica, se considera como un término descriptivo para un grupo de trastornos motores de origen cerebral que se ubican dentro de las discapacidades del desarrollo.4 Actualmente se describe como un grupo de trastornos permanentes del movimiento y de la postura que originan limitaciones en la actividad y que son atribuibles a alteraciones no progresivas ocurridas durante el desarrollo cerebral.5,6 Se acompaña frecuentemente de alteraciones sensoriales, de la percepción, de la cognición, de la comunicación, conductuales, de epilepsia o de problemas músculo-esqueléticos secundarios.7
La evidencia apunta hacia una etiología multifactorial con interacción entre componentes genéticos y los factores ambientales que actúan en tres períodos: prenatal, perinatal y postnatal.2,7
Su incidencia se ha mantenido estable en los últimos 10 años, como lo informan una revisión sistemática y un meta-análisis de 19 estudios en los que se esti mó que 2,11 niños por cada 1 000 nacidos vivos (NV) padece PCI.2 Según el Centro para el Control y la Prevención de las enfermedades del gobierno federal cada año cerca de 10 000 bebés nacidos en los Estados Unidos contraerán PCI. En países en desarrollo la incidencia de esa condición es mayor (siete casos por cada 1 000 nacimientos).3 En un estudio realizado en Cuba se informó que en los nacimientos ocurridos entre 1996 y 2002 la prevalencia de PCI encontrada fue de 1,81 casos por cada 1 000 NV.2
La PCI espástica congénita es la más frecuente, con una incidencia estimada en Estados Unidos de 1,7 casos por 1 000 NV sobrevivientes al año de edad y presenta, por lo menos, dos de las siguientes características: patrones de movimiento o postura anormales, hipertonía, reflejos patológicos como la hiperreflexia o signos piramidales positivos.2 La presión ejercida por los músculos y las contracturas progresivas puede originar malformación ósea y de articulaciones como la luxación de la cadera y la escoliosis.7,8
El abordaje integral del paciente por parte del equipo de salud es imprescindible. Se destaca el rol del nutricionista dietista porque su atención oportuna y regular permite evitar el deterioro del estado nutricional y el compromiso de la talla.9 Al utilizar ácidos grasos poliinsaturados de cadena larga omega 3 en pacientes con PCI se obtienen resultados con leve mejoría en el desarrollo psicomotor.10 El tratamiento del trastorno neuromotor se fundamenta en cuatro pilares: Fisioterapia, órtesis, medicamentos y Cirugía ortopédica. Existen otras terapias como la ocupacional, la del lenguaje, la crioterapia y la hidroterapia que resultarán benéficas.7
En relación con las correcciones ortopédicas la osteotomía de cuello astrágalo para la corrección del pie equino varo aducto rígido, la cirugía de partes blandas para la displasia de cadera y la cirugía de preservación de caderas son técnicas quirúrgicas que se han aplicado con buenos resultados.11,12,13,14
Para el tratamiento farmacológico de la espasticidad se emplean las benzodiacepinas, el baclofeno y la toxina botulínica tipo A (TBA).2,7 La TBA es considerada una de las principales opciones de tratamiento para las enfermedades neurológicas que cursan con espasticidad, hipertonía muscular y distonía focal.15 Además, un estudio mostró que el uso de TBA en las glándulas salivales (parótida y submaxilares) fue útil en el tratamiento de la sialorrea en niños con parálisis cerebral con un impacto positivo en la calidad de vida.16 El principal objetivo del tratamiento es lograr la mejoría de la función motora, la reducción del dolor y la prevención de complicaciones y mejorar la calidad de vida de los pacientes.15
Desde el año 2013 se comenzó a utilizar en el Hospital Pediátrico “José Luis Miranda” la TBA para el tratamiento de la espasticidad en niños con PCI, pero no se ha realizado, hasta el presente, ninguna investigación que evalúe los resultados de su empleo y de su efectividad.
Estos datos conducen a plantear la necesidad de aumentar los conocimientos sobre el tratamiento de la espasticidad con TBA, lo que implicaría tanto los aspectos relacionados con su dosificación y su distribución, como los efectos a largo plazo, que incluyen la reducción del número de intervenciones quirúrgicas en pacientes ambulantes y la disminución de los casos de luxación de la cadera en pacientes no ambulantes con espasticidad proximal de miembros inferiores.
En la actualidad se plantean una serie de cuestiones relacionadas con el tratamiento con TBA y su influencia en el tono muscular, la función motora y el nivel de dependencia de pacientes con PCI en este hospital. Esta investigación tiene el objetivo de evaluar la efectividad de la toxina botulínica tipo A en el tratamiento de niños con parálisis cerebral infantil espástica y de identificar en la respuesta la posible sinergia de la toxina botulínica tipo A con la fisioterapia y el tratamiento farmacológico coadyuvante.
MÉTODOS
Se realizó una investigación analítica longitudinal en niños con PCI paraparética en el Hospital Provincial Universitario Pediátrico “José Luis Miranda” de la Ciudad de Santa Clara, Provincia de Villa Clara, en el período comprendido entre enero de 2016 a enero de 2017.
La investigación comenzó con una revisión bibliográfica extensa sobre el tema para definir el problema científico. Posteriormente se procedió a definir el universo y la muestra. El universo de estudio estuvo conformado por todos los pacientes con PCI espástica de siete a 18 años de edad que se atendieron en la Consulta de Neurología. Se empleó el muestreo no probabilístico de tipo intencional y se aplicaron criterios de inclusión y exclusión. La muestra quedó conformada por 30 individuos. Se consideraron como criterios de inclusión: pacientes con diagnóstico de PCI espástica paraparética, con contracturas reductibles, edad de siete a 18 años, que acudieron por primera vez a la consulta en el período de estudio y que firmaron el consentimiento por los padres o los tutores legales. Se excluyeron los pacientes con contraindicaciones para el uso de la TBA, con Cirugía ortopédica de menos de 24 semanas, malformaciones óseas que alteren las valoraciones articulares, discapacidad cognitiva severa y presencia de ataxia o disquinesias y pacientes que no pudieron acudir a controles subsecuentes. Una vez seleccionados los pacientes se obtuvo el consentimiento de participación informado.
Inicialmente se procedió a la valoración del paciente libre del efecto de la TBA para evaluar su grado de espasticidad y su funcionalidad y se aplicaron las pruebas validadas internacionalmente: escala modificada de Ashworth, índice de Barthel y escala modificada de O’Brien.17
Tras esta valoración se seleccionaron los músculos que precisarían ser infiltrados y se les citó para el tratamiento con la toxina cada tres meses. Después de cada infiltración se realizaron sesiones de Fisioterapia, se siguió el método Bobath.18 La valoración post-infiltración se realizó en todos los pacientes al mes de la primera y última dosis en el período de un año.
Se empleó TBA Xeomeen/Xeomin (incobotulinumtoxina) en bulbos de 100 unidades internacionales (UI), que es la única presentación disponible en el país. Se solicitó consentimiento informado de los padres o tutores legales de los pacientes y se valoró la relación riesgo/beneficio para su aplicación. Se les explicaron a los familiares todos los efectos adversos del medicamento que han sido informados en otras poblaciones.
La dilución se realizó con solución fisiológica al 0,9% en dos y cuatro mililitros. La dosis administrada fue individualizada para cada paciente en dosis total de tres a 6U/kg distribuidas en los músculos afectados, sin pasar de 50U por músculos.
Se requirió, para realizar el procedimiento: solución salina sin preservadores, jeringas de insulina con agujas de 27 o 30 y de 25x32mm para inyecciones profundas, torundas de alcohol, gasas y guantes estériles.
Se tuvieron en cuenta variables como la edad, definida en dos grupos, de siete a 13 y de 14 a 18 años; el sexo, en masculino y femenino, y la terapia farmacológica coadyuvante en pacientes que emplearon baclofeno y pacientes que no lo emplearon.
A todos los pacientes se les evaluaron la espasticidad mediante la escala de Ashworth modificada, que consta de cinco puntos y califica la resistencia (aumento de tono) de los músculos al movimiento pasivo; el nivel de dependencia mediante el índice de Barthel, se consideraron valores que pueden oscilar entre cero y 100 puntos y la funcionalidad/tono muscular mediante la escala modificada de O’Brien, que evalúa cinco estadios y tiene en cuenta la valoración subjetiva de la respuesta al tratamiento según criterios de los familiares del paciente y de los Especialistas en Fisiatría y Neurología.
Como la escala de O’Brien deduce una mejoría subjetiva no se evaluó el momento antes de la aplicación de la toxina botulínica, sino que se compararon los cambios producidos desde la aplicación de la primera dosis hasta la última en el período de un año.
Se confeccionó, por parte del equipo de investigación, una hoja de recolección de datos para la inclusión de aspectos esenciales para la investigación. Los datos fueron almacenados y procesados en un fichero en el software SPSS versión 21.0 para Windows según los objetivos planteados.
Para determinar los posibles cambios en las esferas estudiadas por momento de aplicación de la toxina botulínica se utilizó el método no paramétrico para dos muestras relacionadas y se comparó siempre el momento inicial con la primera y la última aplicación de la toxina mediante la técnica de Wilcoxon debido a que las escalas a evaluar expresan ordinalidad.
Para la toma de la decisión estadística se prefijó un valor de significación alfa=0,05:
Si p<0,05 hubo cambios significativos en las esferas evaluadas
Si p>0,05 no hubo cambios significativos en las esferas evaluadas.
Los resultados se expusieron en gráficos y una tabla estadística para mejor comprensión. Se usaron distribuciones de frecuencias absolutas y relativas para las variables cualitativas.
El estudio se realizó de conformidad con los principios éticos de la Declaración de Helsinki 52, Asamblea General Edimburgo, Escocia, octubre 2000. El proyecto de investigación fue aprobado por el Consejo Científico del Hospital “José Luis Miranda”.
RESULTADOS
Entre ambos sexos 21 (70%) pacientes se distribuyeron en el grupo de edad de siete a 13 años. Los individuos del sexo masculino fueron 19 (63,3%) en total.
Antes de aplicar la primera dosis de la toxina botulínica tipo A 14 (46,7%) pacientes presentaban un marcado aumento del tono muscular con dificultad para el movimiento pasivo y 11 (36,6%) mostraban hipertonía moderada con conservación de los movimientos pasivos del miembro. En ninguno de los casos hubo variación del grado de espasticidad en su evaluación luego de la primera dosis con TBA.
Posterior a la evaluación, tras la última infiltración de TBA, se observó que en los 30 (100%) pacientes investigados ocurrió una mejoría del grado de espasticidad y hubo un cambio de categoría a un nivel inferior según la escala aplicada, lo que fue comprobado estadísticamente (Z=-5,477 p=0,000; p<0,05). Los 14 (46,7%) pacientes en los que predominaba un marcado aumento del tono lograron una mejoría clínica a hipertonía moderada, mientras que los 11 (36,6%) que presentaban una hipertonía moderada mejoraron al grado de hipertonía ligera (Figura 1).
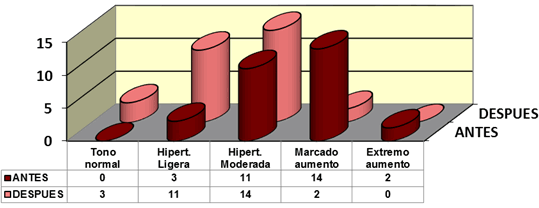
Figura 1 Comparación entre el grado de espasticidad según la escala de Ashworth antes y después del tratamiento con toxina botulínica tipo A
Antes del comienzo del tratamiento la totalidad de los pacientes mostraban grados de dependencia variables, 15 (50%) presentaban una dependencia grave, seguidos por los pacientes que tenían dependencia moderada (10, 33,3%). En ningún caso hubo variación en el nivel de dependencia luego de la primera dosis con TBA (Figura 2).
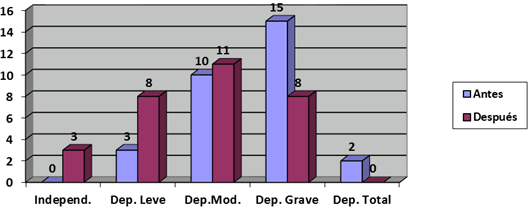
Figura 2 Comparación entre el nivel de dependencia según el índice de Barthel antes y después del tratamiento con toxina botulínica tipo A
Después de la infiltración de la última dosis con TBA se logró incrementar la cantidad de niños independientes y con dependencia leve desde cero a tres pacientes hasta tres y ocho respectivamente; paralelamente se logró una reducción significativa de la cantidad de niños con dependencia grave y dependencia total en relación con los resultados obtenidos después de la primera dosis (Z=-4,491 p=0,000; p<0,05).
De los 15 pacientes que presentaban un nivel de dependencia grave nueve (60%) lograron alcanzar un nivel de dependencia moderado y solo seis (40%) se mantuvieron en la misma categoría de dependencia que presentaban inicialmente seguidos, en orden de frecuencia, por los 10 que presentaban dependencia moderada, de los que ocho pasaron a dependencia leve (80%) y solo dos se mantuvieron en la categoría inicial, mientras que los tres que presentaban una dependencia leve pasaron a ser independientes y los dos pacientes que presentaban una dependencia total pasaron a un grado de categoría de dependencia inferior.
La evaluación subjetiva del tono y la función motora luego de un mes de la primera y la última aplicación de la TBA mostró que en 17 (56,7%) pacientes fue referida una mejoría moderada en el tono y también de la función y que en 10 (33,3%) se refirió una mejoría moderada en el tono sin cambio funcional y en tres (10%) una mejoría marcada del tono y de la función. Los cambios fueron demostrados estadísticamente (Z=-4,912 p=0,000; p<0,05).
En la relación de casos que llevaban terapia farmacológica se apreció que 11 (36,7%) pacientes tenían tratamiento coadyuvante para la espasticidad con baclofeno. En todas las escalas aplicadas se observó una mejoría estadísticamente significativa tanto en los pacientes que utilizaron tratamiento farmacológico con baclofeno como en los que solamente emplearon TBA, por lo que no hubo diferencias entre ambos grupos (Tabla 1).
DISCUSIÓN
El sexo masculino quedó representado con mayor frecuencia en esta serie, lo que coincide con otras investigaciones realizadas sobre el tema;6,19,20 no obstante, también existen investigadores que han presentado resultados diferentes. La PCI no tiene predilección por ningún género, salvo el tipo hemiplejia espástica que es más común en varones.21 Avellanet y colaboradores22 presentaron un predominio de pacientes del sexo femenino.
En esta investigación no ocurrieron modificaciones en la escala de Asworth al mes de administrada la toxina. Al evaluarse el grado de espasticidad posterior a la última aplicación de la TBA si se encontró una mejoría notable en la totalidad de los pacientes, lo que demuestra la efectividad de este tratamiento aplicado con regularidad.
La duración media del efecto clínico de la TBA oscila entre tres y seis meses, por lo que el intervalo mínimo aconsejado de infiltración es de tres meses; tanto en niños como en adultos no son adecuados intervalos más cortos porque los resultados son imprecisos y aumentan la posibilidad de aparición de anticuerpos.23
Una investigación sobre la respuesta de la espasticidad a la dosis inicial de la TBA informó una mejoría en la reevaluación al mes y a los tres meses de administrado el medicamento; sin embargo, se notó regresión al estado inicial, anterior al tratamiento, a medida que aumentaba el número de meses en el seguimiento y en el grupo con mayor puntuación del tono muscular.20 Respuestas similares se evidenciaron en un estudio realizado en un período de cuatro meses24 y en otro en el que la mayoría de sus pacientes retornaban a los 180 días a estadios anteriores a la colocación de TBA.25
En un trabajo reciente en el que se empleó Xeomeen/Xeomin, en presentación de 100UI, en pacientes con PCI, se realizaron varias aplicaciones acompañadas de Fisioterapia y se informaron que se objetivó mejoría de la espasticidad a partir de la primera aplicación, que se mantuvo en más de la mitad de los pacientes. Los que mostraron mejoría en los grados de movilidad articular (24%) tenían un mayor número de aplicaciones de la TBA, lo que recalca que la aplicación repetida se asocia con una eficacia sostenida.26 En esta investigación, al igual que en la presente, no se notificaron efectos adversos, lo que refuerza la seguridad de este tratamiento.
Los resultados obtenidos al mes de la primera dosis de toxina botulínica en los que no existieron cambios en el tono muscular parecen controversiales debido a que pudiera haber incidido la susceptibilidad individual al medicamento, la dosis empleada por los diferentes autores y el método de rehabilitación seleccionado. Con relación a los resultados obtenidos después de la última dosis la mejoría es consistente con la aplicación sistemática de TBA cada tres meses; fueron, en total, cuatro dosis a lo largo del año de estudio.
En los resultados se pudo apreciar que no existieron cambios en el nivel de dependencia (índice de Barthel) antes y después de la primera aplicación de la TBA, lo que coincide con los resultados obtenidos en el estudio realizado por Martín27 en 27 niños con PCI en el que se evidenció que no mejoraron su funcionalidad global para las actividades de la vida mediante el índice de Barthel pre y post infiltración de la TBA.
En el presente estudio, posterior a la última dosis de TBA en el período de un año, hubo cambios significativos en cuanto a la mejoría en el nivel de dependencia de los pacientes según el índice de Barthel, lo que podría estar relacionado a la mejoría del grado de espasticidad ya evidenciada en ese momento, así como la influencia de la Fisioterapia en un período de tiempo mayor.
Esta investigación reveló una mejoría en la valoración subjetiva del tono y la funcionalidad de la totalidad de los pacientes (escala de O´Brien) según el familiar y el personal médico (Especialista en Fisiatría y Neurología) después del tratamiento con TBA. En un estudio en el que se evaluó la efectividad de la toxina botulínica tipo A en el tratamiento de la espasticidad de los miembros inferiores en pacientes con parálisis cerebral infantil en una muestra de 53 pacientes con diferentes formas clínicas, grados de afectación y con contracturas dinámicas se obtuvo una puntuación igual o superior a tres en la escala de mejoría global de O’Brien posterior al tratamiento con TBA.28
En todas las escalas aplicadas se observó una mejoría estadísticamente significativa independientemente al uso de tratamiento farmacológico coadyuvante con baclofeno, sin existir diferencias entre ambos grupos.
Este resultado pudiera estar en relación con la baja biodisponibilidad que presenta el baclofeno oral empleado en los pacientes porque al ser un fármaco poco liposoluble tiene una pobre capacidad para cruzar la barrera hematoencefálica. En el caso del baclofeno intratecal (BIT) existe evidencia clase A y consenso en que reduce significativamente la espasticidad de los miembros superiores e inferiores; sin embargo, no existe igual nivel de evidencia respecto a los beneficios que esta terapia produciría en las dimensiones de actividad y participación de la Clasificación Internacional de Funcionamiento, Discapacidad y Salud de la Organización Mundial de la Salud en PCI. Una revisión sistemática exhaustiva reciente califica al BIT como opción terapéutica con evidencia disponible insuficiente en estos dominios en pacientes que padecen PCI. No obstante, con la terapia de BIT se han informado altos niveles de mejoría funcional en los niños con PCI y los estudios de costo-efectividad la apoyan, por lo tanto, debe ser consideradas dentro del arsenal terapéutico.29
CONCLUSIONES
La TBA es efectiva en el tratamiento de los pacientes con PCI espástica. La espasticidad, el nivel de dependencia y la funcionalidad asociada al tono muscular presentan mejoría con la administración de TBA de manera sistemática cada tres meses y asociada a Fisioterapia, con independencia del cumplimiento o no del tratamiento farmacológico coadyuvante.















