
Lupus eritematoso sistémico: calcio e inmunorregulación
Systemic lupus erythematosus: calcium and immunoregulation
Dr. Carlos Alberto Porras; Int. Harold Díaz; Dra. Carmen Delia Urbina; Dr. Rafael Pila Pérez
Hospital General del Oeste Dr. José Gregorio Hernández. Universidad Central de Venezuela. Caracas, Venezuela.
]]>
RESUMEN
La utilización del calcio in vitro se ha involucrado con la elevación de los niveles de interleucina sérica y estas moléculas estimulan la producción de los linfocitos. Se realizó un ensayo clínico fase II temprana, con el objetivo de determinar si la administración de calcio por vía oral a los pacientes con LUPUS, provoca un aumento del los niveles de linfocitos T, y en particular a los linfocitos T supresores, para mejorar la clínica. De ser así, se podría utilizar el calcio como parte del arsenal terapéutico en este grupo de pacientes. Se estudiaron 12 pacientes con lupus en el período de tres meses. Los pacientes fueron escogidos al azar y se conformaron dos grupos, uno que recibió 600 mgrs de calcio al día en forma de carbonato de calcio (A) (6 pacientes) y otro que recibió placebo (B) (6 pacientes). Antes de comenzar la administración del calcio o del placebo, a cada paciente se le practicó una evaluación clínica, hematología completa, subpoblación linfocitaria, creatinina sérica, examen simple de orina y electrocardiograma. Todos los pacientes fueron seguidos por tres meses y al final del estudio se repitieron las pruebas iniciales. No hubo diferencias clínicas entre los pacientes que recibieron calcio y los que recibieron placebo. Tres (50 %) de los pacientes que recibieron calcio mostraron una disminución de los leucocitos totales al igual que el grupo que recibió placebo. Cuatro (66, 6 %) de los pacientes del grupo A mostraron una disminución del conteo de linfocitos totales y sólo dos (33, 3 %) de los pacientes del grupo B (F = 0, 089). Cinco (83, 3 %) de los pacientes que recibieron calcio mostraron una elevación de los niveles de linfocitos CD3 en contra de dos
(33, 3 %) de los pacientes que recibieron placebo (F = 3, 2449). Tres (50 %) de los pacientes del grupo A elevaron los niveles de linfocitos CD4 y dos (33, 3 %) del grupo B (F = 0, 024). Cuatro (66, 6 %) de los pacientes que recibieron calcio presentaron elevación de los linfocitos CD8, en contra de uno (16, 6 %) de los que recibieron placebo (F = 2, 444). Todos los resultados se interpretaron en la tabla de Fisher con un nivel de 0, 05. No hubo diferencias estadísticas significativas entre los grupos respecto a los otros estudios paraclínicos realizados.
DeCS: LUPUS ERITEMATOSO SISTÉMICO; CALCIO.
ABSTRACT
The use of calcium in vitro has been involved with the increase of serum interleukin levels and these molecules stimulate lymphocyte production. A clinical assay early stage II was carried out with the objective to determine if calcium administration, by oral via, to the patients with Lupus, provokes an increase of T lymphocyte levels, particularly T lymphocyte suppressors, to improve the clinic. If it is true, calcium could be used as part of the therapeutic arsenal in this group of patients. Twelve patients with Lupus were studied in a period of three months. Patients were chosen at random, and two groups were conformed one of them received 600mgs of calcium daily, as calcium carbonate (A) (six patients) and the other one received placebo (B) (six patients). Before the administration of calcium or placebo a clinical evaluation, complete hematological exams, lymphocyte subpopulation, serum creatinine, simple urine analysis and electrocardiogram to each patient, were performed. All patients were followed by a period of three months and at the end of the study, initial exams were repeated again. There were no differences, from the clinical point of view, among patients that received calcium and those who received placebo. Three (50 %) of the patients that received calcium showed a decrease of the total leukocytes equal to the group that received placebo. Four (66, 6 %) of the patient groups (A) showed a decrease of total lymphocyte counting and only two (33, 3 %) of group (B) (F=0. 089). Five (83, 3 %) of the patients that received calcium showed an increase of lymphocyte CD3 levels versus two (33, 3 %) of the patients that received placebo (F=3, 2449). Three (50, 0 %) of the group (A) increase lymphocyte CD4 levels and two (33, 3 %) of the group (B) (F=0, 024). Four (66,6 %) of the patients that received calcium showed an increase of lymphocyte CD8, versus one (16, 6 %) of those that received placebo (F= 2, 444). All the results were expressed in the Fisher table with 0,05 level. There was no statistically significant difference among groups, regarding to other paraclinical studies performed.
DeCS: LUPUS ERYTHEMATOSUS SYSTEMIC; CALCIUM.
]]> INTRODUCCIÓN
En la fisiopatología del lupus eritematoso sistémico se señalan una gran variedad de alteraciones inmunológicas, en las cuales se incluyen las alteraciones celulares
y dentro de éstas las anormalidades de los linfocitos T, 1, 2 también se involucran la participación de ciertas moléculas como es el caso de las citokinas. 3
Las células T contribuyen de dos maneras en la patogénesis del lupus, estas fallan en la supresión de las células B y suministran una ayuda excesiva en la producción de autoanticuerpos por las células B.
Muchos estudios revelan la deficiencia de la función de las células T supresoras en pacientes con lupus, 3, 4 sin embargo, no está claro si esta deficiencia es debido a un defecto primario o secundario (por autoanticuerpos u otras moléculas donde podría estar involucrada la interleucina 2). 5, 6
La interleucina 2 (IL-2) es un importante factor de crecimiento autocrino para las células T y para la activación de las células T supresoras. Aunque los niveles séricos de IL-2 están elevados en los pacientes con enfermedad activa, la respuesta in vitro de las células T a la IL-2 está disminuida y reflejan, posiblemente, una refractariedad postactivación. Las anormalidades en la secreción de la IL-2, bajos niveles de receptores con alta afinidad para la IL-2, independientemente de la actividad de la enfermedad, pueden contribuir a la desregulación de la interleucina-2. Teóricamente, defectos de la secreción y en la respuesta de la IL-2 contribuyen al Lupus al interferir con la activación y la función de las células T. 7-9
Las células T periféricas del Lupus producen una cantidad subnormal de IL-2; sin embargo, in vitro, este estado puede ser revertido si se colocan en reposo a las células T por varios días o si se añade calcio iónico. 1 Quedará por saber si la administración de calcio iónico in vivo haría posible la reversión de este defecto.
Esta investigación se realizó con el objetivo de medir el producto de la activación de la interleucina y reflejar los niveles de linfocitos. Si los linfocitos aumentan, se puede pensar que la activación de los mismos es un proceso directamente relacionado con los niveles séricos de interleucina mediado por el calcio, aunque queda por conocer el mecanismo de interacción calcio e interleucina. En caso de no aumentar los niveles de linfocitos se puede tener en cuenta que esta respuesta celular no depende de la interleucina o que hay varios factores asociados. 1-4
Si el calcio iónico administrado permite que las células T periféricas sean capaces de producir una mayor cantidad de interleucina 2 y aumentar los niveles de linfocitos T supresores, se reflejarán en una mejoría de la sintomatología, pues el único mecanismo fisiopatológico involucrado es un trastorno en la producción de la interleucina. Por otra parte, si no se produce la activación del clon de células T, entonces el mecanismo fisiopatológico que involucra a la interleucina se relacionará con la falta de producción y la refractariedad postactivación.
]]> MÉTODO
Se realizó un ensayo clínico fase II temprana desde el 1ro de enero al 1ro de abril de 2002. Se incluyeron en la investigación a los pacientes con lupus, lúpicos, sin hallazgos clínicos y de laboratorio con insuficiencia hepática y/o renal, trastornos digestivos
y arritmias cardíacas, diagnosticados por clínica, por exámenes de laboratorio y con previo consentimiento del paciente.
Al momento del ingreso del paciente, se llenó una ficha clínica donde se recogió la identificación del mismo, el nombre, la edad, la fecha de ingreso al estudio, la procedencia, la dirección actual y teléfono (de habitación y/u oficina), el tratamiento al momento del ingreso al estudio, la fecha de diagnóstico del Lupus, los parámetros de laboratorio para lupus (anticuerpos anti-DNA y anti-Sm, niveles de CH50, C3 y C4 y las células LE, RA test y VDRL, el examen físico al momento del ingreso, las complicaciones clínicas presentes al momento del ingreso, los estudios paraclínicos al momento del ingreso: hematología completa y creatinina, las pruebas hepáticas (proteínas totales y fraccionadas, transaminasas, PT y PTT), el examen simple de orina, electrocardiograma y determinación de subpoblación linfocitaria.
Después del ingreso, se dividieron los pacientes al azar en dos grupos. Si a partir de este momento algún paciente presentó un determinado cuadro infeccioso, pues se inició tratamiento con antibióticos y continuó en observación.
Se observó a cada paciente por un período de tres meses. Durante el primer mes de observación se citaron a los pacientes a una consulta semanal donde se evaluaron clínicamente y se les entregaron la dosis semanal del medicamento. Después del primer mes de tratamiento se practicaron niveles de calcio sérico, hematología completa, creatinina y examen simple de orina. Al iniciar el segundo mes de evolución, se fijaron citas con intervalos de 15 días hasta el final del estudio. A finales del segundo mes se repitieron estudios paraclínicos controles que incluyeron niveles de calcio sérico, hematología completa, creatinina y examen simple de orina. Al cumplir los tres meses se repitieron todos los estudios paraclínicos iniciales a excepción de las pruebas hepáticas.
Se inició el trabajo con un total de 17 pacientes de los cuales un paciente del grupo placebo falleció a los tres días de incorporación al estudio y cuatro no continuaron el estudio.
La muestra final fue de 12 pacientes con lupus, quienes fueron distribuidos al azar en dos grupos de seis personas cada uno. Un grupo se designó con la letra A y el otro con la letra B. El grupo A recibió calcio en forma de carbonato de calcio y el grupo B recibió placebo. La dosis de calcio fue de 600mg al día.
Los procedimientos que se llevaron a cabo estuvieron de acuerdo con las normas éticas del Comité Académico del Postgrado de Medicina Interna del Hospital General del Oeste que evalúa los trabajos de investigación, y con las normas emanadas por la Comisión de Estudios de Postgrados de la Facultad de Medicina de la Universidad Central de Venezuela.
El método estadístico utilizado fue el análisis de covarianza, técnica que se basa en el procedimiento de regresiones y el análisis de varianza.
]]> Mediante este análisis se supo si la administración de calcio o de placebo presenta diferencias estadísticamente significativas en función de sus efectos sobre las poblaciones celulares hematopoyéticas, y principalmente sobre los linfocitos al igual que el efecto del calcio sobre la creatinina.En nuestra investigación, el calcio y el placebo son las variables independientes y los estudios paraclínicos (hemoglobina, leucocitos, linfocitos, plaquetas, examen de orina, y creatinina) representan las variables dependientes. Se trabajó con una población total de 12 pacientes (nt=12) dividida en dos grupos, identificados con la letra A para los que recibieron calcio y la letra B para los que recibieron el placebo, cada una con una muestra de seis pacientes (n=6). A cada grupo se le calculó la media. Posteriormente se calculó la gran media, esta representó la suma de las medias correspondientes a los grupos A y B respectivamente. La varianza de cada grupo de tratamiento se calculó dividiendo la suma de los cuadrados de las desviaciones de la media de cada grupo por (nA-1) y (nB-1) respectivamente. No fue necesario el cálculo de la varianza ponderada ya que todas las n son iguales. A cada grupo se le calculó la varianza intragrupal o residual para conocer la variación aleatoria que se presentó entre los pacientes en el estudio. Según la media y varianza que no se conocían, se utilizó la varianza intragrupal para estimar la varianza, la cual se obtuvo de la diferencias entre las medias de los grupos. Posteriormente se examinó si la estimación de la varianza obtenida de la media de los grupos es sólo una estimación de la varianza o si contenía un componente adicional por a las diferencias entre las medias ocasionado por efectos del calcio. Para esto se emplea una razón de varianza que tiene una distribución F interpretando el resultado en la tabla para valores críticos de F para un nivel de 0, 05.
En este análisis se introdujo una breve corrección, para eliminar únicamente la ventaja o desventaja en la medición inicial, inducida por los procesos infecciosos, como se observó en cuatro pacientes del grupo que recibió calcio, cuyos exámenes de orina revelaron datos compatibles con infecciones urinarias.
Además, en el caso de la población linfocitaria, se obtuvieron resultados en porcentajes, por lo que estos valores fueron transformados a arcosenos para posteriormente convertirlos en valores de ángulos, y así permitir su comparación.
RESULTADOS
Con respecto a la clínica, evolución y tratamiento, en el grupo A, tres pacientes (50 %) iniciaron el estudio con diagnóstico conocido de lupus, recibieron tratamiento a base de esteroides y permanecieron asintomáticos durante todo el estudio. Los otros tres pacientes ingresaron al estudio en el momento que se les diagnosticó el lupus, e inició tratamiento únicamente con calcio, con empeoramiento del cuadro clínico, hasta que se asoció tratamiento a base de esteroides, evolucionando a la mejoría clínica y persistiendo asintomáticos por el resto del estudio. Los seis pacientes del grupo B (100 %) ingresaron y permanecieron asintomáticos durante todo el proceso.
Cuatro pacientes (66, 6 %) del grupo A aumentaron las cifras de hemoglobina al final del estudio y dos pacientes (33, 3 %) de este mismo grupo mostraron cifras disminuidas de la mima al final del estudio también. En el grupo que recibió placebo, tres pacientes (50 %) presentaron aumento de las cifras de hemoglobina al final del estudio, un paciente (16, 6 %) no presentó modificaciones y dos (33, 3 %) mostraron disminución de las cifras de hemoglobina al final del estudio. Al comparar los dos grupos y practicar el análisis de varianzas se obtuvo un valor de F de 0, 0234 no significativo para un nivel de 0, 05. Puesto que el valor de F es menor que la unidad, se supone automáticamente una carencia de significación (Tabla 1).
Tres pacientes (50 %) del grupo B presentaron elevaciones de las cifras absolutas de plaquetas al final del estudio, dos (33, 3 %) de este mismo grupo no presentaron variaciones y uno (16, 6 %) presentó disminución del número de plaquetas. En el grupo A, tres (50 %) presentaron disminución de las cifras de plaquetas, dos (33, 3 %) permanecieron iguales y sólo uno (16, 6 %) presentó aumento del número de plaquetas. Al comparar los dos grupos y practicar un análisis de varianza se obtuvo un valor de F de 0, 0539 no significativo para un nivel de 0, 05. Puesto que el valor de F es menor que la unidad, se supone automáticamente una carencia de significación (Tabla 2).
]]>
Con respecto a los leucocitos, en los dos grupos, tres pacientes (50 %) presentaron un recuento de leucocitos en aumento al final del estudio, dos pacientes (33, 3 %) no presentaron modificaciones y sólo uno (16, 6 %), por grupo, mostró disminución del total de leucocitos. Al comparar los dos grupos se evidenció un F de 0, 7515 no estadísticamente significativo a un nivel de 0, 05 (Tabla 3).
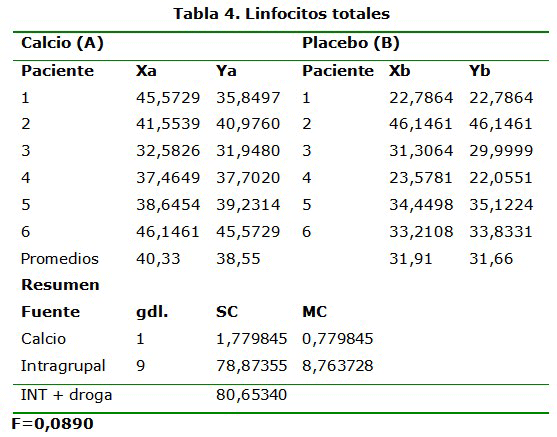
Con respecto a los linfocitos se observó que en el grupo A, cinco pacientes (83, 3 %) presentaron elevaciones de los linfocitos CD3 y sólo uno (16, 6 %) mostró disminución de los linfocitos CD3, cuatro pacientes (66, 6 %), de este mismo grupo presentaron elevaciones de linfocitos CD8, dos (33, 3 %) mostraron disminución de los linfocitos CD8 y tres pacientes (50 %) presentaron elevaciones de los linfocitos CD4, mientras dos (33, 3 %) no mostraron modificaciones de los CD4 y en uno (16, 6 %) hubo disminución de los CD4 (Tabla 4)
En el grupo B dos pacientes (33, 3 %) presentaron elevaciones de la subpoblación CD3, mientras que en tres (50 %) se mostró disminución de los linfocitos CD3. En este mismo grupo, sólo un paciente (16, 6 %) presentó elevaciones de los linfocitos CD8. Los CD4 no se modificaron en este grupo (Tabla 5)
.
Al practicar el análisis de covarianza e interpretar la F en un nivel de 0, 05 no hubo significación ya que se obtuvo para niveles de CD3 una F de 3, 2449, para CD4 una F de 0, 0024 y para los CD8 una F de 2, 440. Al practicar el análisis de covarianza a los valores transformados de los linfocitos igualmente no hubo significación estadística (Tabla 6).
]]> Cuando se sometieron al análisis estadístico los índices de linfocitos CD4/CD8 para los dos grupos se encontró una F de 2, 2153 no estadísticamente significativa para un nivel de 0, 05 (Tabla 7).Con respecto a los valores de creatinina se observó que, en el grupo que recibió calcio, dos pacientes (33, 3 %) presentaron elevaciones de las cifras de creatinina, dos (33, 3 %) permanecieron iguales y en los otros dos (33, 3 %) disminuyó. Es importante recalcar que las variaciones de las cifras de creatinina estuvieron dentro de los rangos de valores considerados normales. En el grupo que recibió placebo, dos pacientes (33, 3 %) presentaron elevaciones de las cifras de creatinina, tres (50, 0 %) no mostraron cambios y solo uno (16, 6 %) presentó disminución de las cifras de creatinina. En este grupo también se observó que los valores de creatinina variaron dentro de rangos normales (Tabla 8).
Al aplicar el análisis estadístico que permitió la comparación de los dos grupos se obtuvo una F de 1, 47 la cual no es significativamente estadística para un nivel de 0,05.
Con respecto a los exámenes de orina se observaron las siguientes variaciones en los dos grupos. En el grupo que recibió calcio, cuatro pacientes (66, 66 %) ingresaron al estudio con datos de infección urinaria y dos de estos (50 %) presentaron cristales de oxalato de calcio. Al finalizar el estudio cinco pacientes (83, 33 %) presentaron exámenes de orina dentro de límites normales y sólo un paciente (16, 66 %) persistió con el cuadro de infección urinario. Este examen de orina correspondió a una paciente embarazada. En el grupo que recibió placebo, un paciente (16, 66 %) inició el estudio con un examen de orina indicativo de infección urinaria mientras que el resto estuvo dentro de límites normales. Al finalizar el estudio todos los pacientes terminaron con exámenes de orina dentro de límites normales. Al realizar un análisis estadístico de los dos grupos no se observó una diferencia significativa.
Con respecto a los electrocardiogramas, cinco pacientes (83, 33 %) del grupo de calcio iniciaron el estudio sin alteraciones electrocardiográficas y sólo uno (16, 66 %) de este grupo presentó alteraciones electrocardiográficas indicativas de pericarditis, que se modificaron durante el estudio hacia la normalidad. Este paciente ingresó al estudio en el momento que se le diagnosticó el lupus. Los seis pacientes (100 %) del grupo que recibió placebo iniciaron y terminaron el estudio con electrocardiogramas dentro de límites normales. No hubo diferencia estadísticamente significativa entre los grupos.
DISCUSIÓN
Se debe considerar la presencia de varios factores que pueden influenciar los resultados obtenidos, pues se trabajó con pacientes en los cuales pudo haber más de una variable que alteró la respuesta al calcio, lo que llevó a considerar los efectos del calcio en individuos normales. 9, 10
]]> La dosis de calcio administrada probablemente no fue suficiente y no permitió alcanzar niveles séricos para la activación de linfocitos. De ser así, quedaría por determinar cuál es el nivel sérico adecuado.Según el tiempo de administración del medicamento, la sensibilidad de las pruebas de laboratorio que se utilizaron en la medición de los niveles de linfocitos originó un cierto margen de confianza que no se incluyó dentro de las mediciones porcentuales. Los medicamentos asociados al calcio alteran los niveles celulares y por lo tanto la interpretación de los mismos, como es la presencia de los esteroides.
Las condiciones asociadas, tales como los procesos infecciosos de base, alteran las poblaciones celulares, por lo que fue necesario el seguimiento de los pacientes para el control del cumplimiento del medicamento.
Con respecto al tamaño de la muestra, todo lo anterior, son factores que deberían corregirse para una mayor precisión de los resultados.
Por otra parte se puede hacer una discusión respecto a los mecanismos fisiopatológicos en el lupus eritematoso sistémico relacionados al calcio. 10-12
El defecto a nivel de los linfocitos T, con relación al lupus, puede medirse por una alteración en la cantidad de linfocitos normales y dentro de éstos los linfocitos T supresores regulan la actividad de los linfocitos B, también puede medirse el efecto de calidad, en el cual a pesar de producirse una cantidad suficiente de linfocitos T no son capaces de regular la actividad de otras células, y a la vez la interacción de estos dos fenómenos.
En la actualidad, para relacionar los linfocitos al calcio, sólo se puede realizar a través de la interleucina, por los siguientes mecanismos:
a) El calcio aumenta la producción de interleucina por parte de los linfocitos periféricos y posteriormente estas moléculas estimulan el clon celular.
b) El calcio facilita la interacción de la interleucina con los linfocitos para posteriormente activarlos.
c) Asociación de los dos procesos anteriores.
Debido a que el calcio no elevó los niveles de linfocitos, se hace más probable que el mecanismo fisiopatológico relacionado no sea solamente un trastorno en la producción de interleucina, como se pudo observar in vitro, sino que esté asociado a un proceso de activación de los linfocitos. 7-10
También se debe considerar, que, si se hubieran medido los niveles de interleucina sería más fácil precisar si la activación de los linfocitos es un fenómeno mediado exclusivamente por esta, como se observó in vitro y en estudios con animales o si depende de varios factores asociados, ya que es muy probable que en los pacientes con lupus exista más de un estímulo o agente relacionado a la actividad de los linfocitos. 1-3
Queda por dilucidar si el defecto de activación de los linfocitos es a nivel de una alteración en la estructura de la interleucina o si se trata de un defecto de receptores celulares a nivel de los linfocitos, determinado genética y ambientalmente. 4
Es factible considerar la probabilidad que en un individuo con una predisposición genética al lupus, pueda desarrollar la enfermedad en presencia de niveles deficientes de calcio. Si esto ocurre, esta observación apoya la teoría del origen multifactorial del lupus eritematoso sistémico. 5-8
Por otra parte, el uso de calcio, asociado a la terapia inicial en este grupo de pacientes, no provoca cambios en el curso de la enfermedad. 9-12
CONCLUSIONES
1. El calcio no modifica los niveles de linfocitos en los pacientes con lupus.
2. No se debe usar el calcio como monoterapia en los pacientes con lupus.
]]> 3. La elevación de la cantidad total de linfocitos circulantes en los pacientes con lupus, es un proceso donde no sólo está involucrada la interleucina y el calcio sino también otros factores.
REFERENCIAS BIBLIOGRÁFICAS
1. Steinberg A, Gourley MF, Klinman DM, Toscos GC, Scout DE, Krieg AM. Systemic lupus erythematosus annals of. Internal Medicine. 1996;115:548-57.
2. Morimoto C, Reinherz EL, Distaso JA, Steinberg AD, Scholossman SA. Relationship between systemic lupus erythematosus T cell subsets, anti-T cell antibodies and T cell functions. J Clin Invest. 1994;73:689-700.
3. Bresnihan B, Jasin HE. Suppressor function of peripheral blood mononuclearcells in normal individuals and patients with systemic lupus erythematosus. J Clin Invest. 1997;77:106-16.
4. Morimoto C. Loss of suppressor T lymphocyte function in patients with SLE. Clin Exp Inmunol. 1998;32:125-33.
5. Sakane T, Steinberg AD, Green I. Studies of immune function of patients with SLE. Dysfunction of suppressor T cell activity related to impaired generation of, rather than response to, suppressor cells. Arthritis Rheum. 1998;657-64.
6. Sagawa A, Abdou NI. Suppressor cell dysfunction in systemic lupus erythematosus. Cell involved and in vitro correction. J Clin Invest. 1997;789-96.
7. Linker IM, Bakke AC, Rodanthi C, Kitridou R, Gendler D, Gillis S, et al. Defective production of interleukin one and interleukin two in patients with systemic lupus erythematosus. The journal of Immunology. 2000;152:2651-55.
8. Mizel SB. Interleukin 1 and cell activation. Inmunol Rev. 2001;63:51.
9. Mohamed HA, Leroy E, Lantz O, Didier M, Brigitte A, Charpentier B, et al. Induced proliferation of human circulating NK cells and T lymphocytes: synergistic effects of IL and IL 2. The journal of Immunology. 1997;139:443-51.
10. Belizán JM, Villar J, González L, Campodonico L, Bergel E. Calcium supplementation to prevent hypertensive disorders. Annals of Internal Medicinal. 1997;116:1399-1405.
11. Schefler WC. Bioestadística. State University College at Buffalo. New York: Fondo Educativo Interamericano SA; 2001.
12. Guttman I, Wilks SS. Introductory Engineering Statistics. New York: State University College at Buffalo; 2001.
Recibido: 22 de septiembre de 2004. ]]> Aprobado: 21 de febrero de 2005.
Dr. Carlos Alberto Porras. Especialista de I Gradotr en Medicina Interna. Hospital General del Oeste Dr. José Gregorio Hernández. Universidad Central de Venezuela. Caracas, Venezuela.
]]>