
Anticuerpos antinucleosoma frente a marcadores inmunológicos convencionales en el diagnóstico de la actividad del lupus eritematoso sistémico
Anti-nucleosome antibodies against conventional Immunological markers in the diagnosis of SLE activity
Dra. Elena Kokuina, Dr. Miguel Estévez del Toro, Dra. Ángela Gutiérrez Rojas, Dr. Alfredo Ortiz Labrada, Dra. Yeniset Sánchez Bruzón, Dr. Dionisio Pérez Campos, Dra. Ana Argüelles Zayas, Dra. Nelsa Casas Figueredo, Dra. Araceli Chico Capote.
Hospital Clinicoquirúrgico "Hermanos Ameijeiras". La Habana, Cuba.
]]>
RESUMEN
Objetivos: examinar el perfil de anticuerpos en pacientes con lupus eritematoso sistémico y establecer la correlación entre los niveles de anticuerpos y la actividad de la enfermedad y de la nefritis lúpica.
Métodos: en 213 pacientes con lupus eritematoso sistémico, atendidos de forma consecutiva, se determinaron los anticuerpos anti-DNA de doble cadena (DNAdc), antinucleosoma (Nu), anti-Sm, anti-RNP, anti-Ro, anti-La y anti-Scl-70 por ensayo inmunoadsorbente ligado a enzima (ELISA), el C3 y el C4. La actividad de la enfermedad fue evaluada por el índice SLEDAI-2K, sin la contribución de anti-DNAdc, C3 ni C4. Los niveles de anticuerpos, el complemento y la actividad del lupus eritematoso sistémico fueron correlacionados.
Resultados: los niveles de todos los anticuerpos resultaron superiores significativamente en los pacientes en fase activa de la enfermedad con respecto a los que se hallaban en la fase inactiva. Los coeficientes de correlación de Spearman más altos con la puntuación de SLEDAI-2K correspondieron a los anti-Nu y anti-DNAdc (p= 0,856 y p= 0,616, respectivamente, p < 0,001 para ambos). Las áreas bajo de la curva (AUC) del análisis COR de la actividad del LES fueron en orden decreciente para los anti-Nu= 0,948, anti-DNAdc= 0,810, anti-RNP= 0,705, C4= 0,704, anti-Sm= 0,703, C3= 0,688, anti-Scl-70= 0,611, anti-La= 0,601 y anti-Ro= 0,593; y de la actividad renal para los anti-Nu= 0,845, anti-DNAdc= 0,755, C4= 0,694, C3= 0,670, anti-Sm= 0,641, anti-RNP= 0,630, anti-Scl-70= 0,611, anti-Ro= 0,593 y anti-La= 0,567.
Conclusión: los anticuerpos anti-Nu mostraron una capacidad discriminatoria excelente para la actividad del LES y de la actividad renal lúpica, superior a la de los anti-DNAdc y el resto de los marcadores.
Palabras clave: autoanticuerpo, antinucleosoma, anti-DNAdc, C3, C4, actividad del lupus eritematoso sistémico, SLEDAI-2K, nefritis lúpica.
ABSTRACT
Objectives: to examine the profile of antibodies in patients with systemic lupus erythematosus and establish the correlation between antibody levels and disease activity, and lupus nephritis. ]]>
Methods: anti-double stranded DNA (dsDNA), antinucleosoma (Nu), anti-Sm, anti-RNP, anti-Ro, anti-La, and anti-Scl-70 antibodies by enzyme-linked immunosorbent assay (ELISA) as well as C3 and C4 were determined in 213 patients with systemic lupus erythematosus who were treated consecutively. Disease activity was assessed by the SLEDAI 2K-index, without the contribution of anti-dsDNA, C3 or C4. The levels of antibodies, complement and activity of systemic lupus erythematosus were correlated.
Results: the levels of antibodies turned out to be remarkably higher in patients in the active phase of the disease compared to those who were in the inactive phase. The higher Spearman correlation coefficients with SLEDAI-2K score corresponded to the anti-Nu and anti-dsDNA (p = 0.856 and p = 0.616, respectively, p <0.001 for both). The areas under the ROC curve analysis of the activity of systemic lupus erythematosus were in descending order as follows: anti-Nu = 0.948; anti-dsDNA = 0.810; anti-RNP = 0.705; C4 = 0.704; anti-Sm = 0.703; C3 = 0.688; anti-Scl-70 = 0.611; = 0.601 anti-La. Anti-Ro = 0.593; and renal activity for anti-Nu = 0.845; anti-dsDNA = 0.755; C4= 0.694; C3 = 0.670; anti-Sm = 0.641; anti-RNP = 0.630; anti-Scl-70 = 0.611; anti-Ro = 0.593 and anti-La = 0.567.
Conclusion: the anti-Un exhibit excellent activity discriminating capacity of SLE lupus and renal activity, higher than the anti-dsDNA and other markers.
Key words: autoantibody, antinucleosoma, anti-dsDNA, C3, C4, activity of systemic lupus erythematosus, SLEDAI-2K, lupus nephritis.
INTRODUCCIÓN
El lupus eritematoso sistémico (LES) es una enfermedad autoinmune multisistémica crónica caracterizada por la producción de una gran variedad de autoanticuerpos entre los que predominan los anticuerpos antinucleares dirigidos frente a antígenos localizados en el interior de la célula. Entre estos, los anticuerpos anti-ácido desoxiribonucléico de doble cadena (DNAdc) se consideran la principal herramienta inmunológica del diagnóstico1 y seguimiento del LES2 aunque se presentan solo en 40-60 % de los pacientes y no siempre se correlacionan con la actividad de la enfermedad.3,4
Más recientemente se ha comunicado que el nucleosoma (Nu), unidad básica de la cromatina, es el inmunógeno principal del LES.5 La presencia de anticuerpos anti-Nu se ha asociado a la actividad de la enfermedad y a la nefritis en pacientes con LES.6,7 Autoanticuerpos dirigidos frente a otros antígenos nucleares y citoplasmáticos también han sido identificados en el LES, pero su significado clínico es menos claro. Los anticuerpos dirigidos frente a los originalmente denominados antígenos extraíbles nucleares (del inglés: ENA) incluyen las especificidades anti-Ro (SSA), anti-La (SSB), anti-Smith (Sm), anti-ribonucleoproteína (RNP) y anti-Scl-70. La presencia de los anticuerpos anti-ENA ayuda a establecer el diagnóstico, pero apenas se disponen evidencias a favor de que los anticuerpos anti-ENA puedan reflejar la actividad de la enfermedad del LES.8
La evolución del LES es impredecible, con fases de exacerbación o actividad que alternan con fases de remisión o relativa inactividad de la enfermedad. El diagnóstico de las fases de actividad del LES es uno de los retos más relevantes de la práctica clínica para optimizar el seguimiento clínico de los pacientes mediante el ajuste oportuno del tratamiento inmunosupresor. Hasta ahora, los niveles altos de anticuerpos anti-DNAdc y cifras bajas del complemento sérico son considerados como los marcadores inmunológicos más valiosos de la actividad del LES. 9
]]> Sobre la hipótesis de que las distintas especificidades de anticuerpos antinucleares no se asocian con la misma intensidad a las fases de actividad del LES nos propusimos evaluar los anticuerpos anti-DNAdc, anti-Nu, anti-Sm, anti-RNP, anti-Ro, anti-La y anti-Scl-70 para seleccionar los de mayor eficiencia diagnóstica de la actividad del LES y de la actividad renal lúpica.
MÉTODOS
Selección de pacientes
Se realizó un estudio transversal en 213 pacientes adultos consecutivos con un mínimo de 4 criterios para la clasificación del LES1 atendidos en el Servicio de Reumatología del Hospital Clinicoquirúrgico "Hermanos Ameijeiras" (HCQHA) en el período comprendido desde enero 2011 hasta enero 2013. Fueron excluidos los pacientes con diagnóstico adicional de otra enfermedad del tejido conectivo, así como los que han recibido terapia sistémica con corticosteroides, inmunosupresores o inmunomoduladores en los últimos 6 meses.
La presencia de los autoanticuerpos se analizó en un grupo control compuesto por 87 pacientes con diagnóstico de enfermedades reumáticas autoinmunes diferentes al LES: 24 con artritis reumatoide (AR); 12 con síndrome de Sjögren (SS); 29 con esclerosis sistémica (ES); 10 con enfermedad mixta del tejido conectivo (EMTC); 6 con miopatía inflamatoria (MI) y 6, con lupus cutáneo fijo discoide (LCFD).
La evaluación de la actividad del LES fue realizada por el cálculo del índice de actividad SLEDAI-2K2 con la exclusión de los datos de los anticuerpos anti-DNAdc, y el complemento por ser estos variables del estudio, los cuales de no estar excluidos pudieran redundar e invalidar los resultados.10 La evaluación de la actividad del LES incluyó el examen físico general, los síntomas referidos y las evaluaciones de laboratorio y de otros medios diagnósticos relevantes para el cálculo de SLEDAI-2K ocurridos en los 10 d precedentes a la consulta. Todos los pacientes fueron examinados por el mismo equipo de reumatólogos. La actividad de la enfermedad fue dividida en 2 categorías respecto a la puntuación del SLEDAI-2K: mínima o leve (0 £ SLEDAI-2K £ 5), correspondiente a la fase inactiva del LES y moderada o grave (SLEDAI-2K > 5), correspondiente a la fase activa.11 Se consideró como nefritis lúpica activa la presencia de cualquiera de las siguientes alteraciones si reproducibles: proteinuria > 0,5 g/24 h; piuria (> 5 leucocitos/campo en ausencia de infección), hematuria (> 5 hematíes/campo en ausencia de infección o litiasis), cilindruria y cifras de creatinina sérica superiores a las del rango normal.
Autoanticuerpos y complemento
La toma de la muestra biológica para determinar los autoanticuerpos se realizó simultáneamente con las pruebas de laboratorio protocolizadas para el seguimiento de la actividad del LES en los 10 d precedentes a la consulta de reumatología y anterior al aumento de las dosis de glucocorticoides o fármacos inmunosupresores en pacientes con la enfermedad activa. Las muestras de suero fueron fraccionadas y conservadas a -20 °C hasta la fecha de la determinación. Las determinaciones de los autoanticuerpos anti-DNAdc, anti-Nu, anti-Sm, anti-RNP, anti-Ro, anti-La y anti-Scl-70 se realizaron por el método de ELISA dirigido a la detección de los anticuerpos de isotipo IgG (Orgentec Diagnostika, Mainz, Germany). Los resultados se expresaron en U/mL. Los valores de corte para todas las determinaciones de autoanticuerpos fueron los recomendados por el fabricante. Las concentraciones séricas de las proteínas C3 y C4 fueron cuantificadas por inmunoturbifimetría automatizada estándar (Roche/Hitachi cobas c, Mannheim, Alemania). El rango normal para el C3 fue 0,9 - 1,8 g/L y para C4 0,1 - 0,4 g/L, según las recomendaciones del fabricante. Se consideró como carga de autoanticuerpos (Nº autoacs) el total de las especificidades antinucleares positivas; y como carga de biomarcadores (Nºautoacs, C3yC4) la suma de las especificidades antinucleares positivas, C3 y C4 inferior al rango normal.
]]>La estadística descriptiva se expresó como media y desviación estándar (DE) para las variables continuas y como frecuencia y porcentaje para las variables categóricas. Las variables continuas de distribución asimétrica se calcularon con medianas. Los autoanticuerpos y el SLEDAI-2K demostraron una distribución asimétrica en el histograma de frecuencia y la prueba de Kolmogorov-Smirnov. La sensibilidad y la especificidad de los autoanticuerpos para el LES respecto al grupo de pacientes con otras conectivopatías se calcularon con las tablas de contingencia de 2 X 2. La sensibilidad fue calculada por el cociente de verdaderos positivos (VP) entre la suma de VP + falsos negativos (FN). La especificidad fue el cociente de verdaderos negativos (VN) dividido entre la suma de VN + falsos positivos (FP).
Las diferencias en los niveles de autoanticuerpos y componentes del complemento entre los pacientes en fase de actividad (SLEDAI-2K > 5) y en fase de inactividad del LES (SLEDAI-2K £ 5) fueron determinadas por la prueba de Mann-Whitney. La correlación entre 2 variables continuas se realizó con la correlación no paramétrica de Spearman (coeficiente de correlación ρ [rho]).
Se realizaron los análisis de las curvas COR (del inglés: receiver-operating characteristics curve, ROC) para todos los autoanticuerpos, C3 y C4 con el objetivo de determinar los puntos de corte óptimos para discriminar entre los pacientes en fase de actividad e inactividad del LES. Las curvas COR se construyeron mediante el cálculo de la sensibilidad y la especificidad de múltiples puntos de corte. El área debajo de la curva (AUC) es el valor que indica la probabilidad de que un paciente en fase de actividad del LES seleccionado al azar tenga cifras más elevadas del biomarcador que un paciente en fase de inactividad; un valor de AUC de 0,5 indica ninguna discriminación y un valor de 1 indica discriminación perfecta. La exactitud de cada biomarcador en predecir la actividad del LES y la actividad de la nefritis lúpica fue clasificada en sobresaliente, muy buena, buena, regular y mala si el AUC estaba en el rango de 0,9 - 1,0; 0,81 - 0,90; 0,71 - 0,80; 0,61 - 0,70 y 0,50 - 0,60, respectivamente.12
La significación estadística fue definida como p < 0,05 calculado bilateralmente (2-tailed). El análisis estadístico se realizadó con el paquete estadístico SPSS v 13.0 para Windows Xp.
RESULTADOS
Características demográficas de la población de estudio
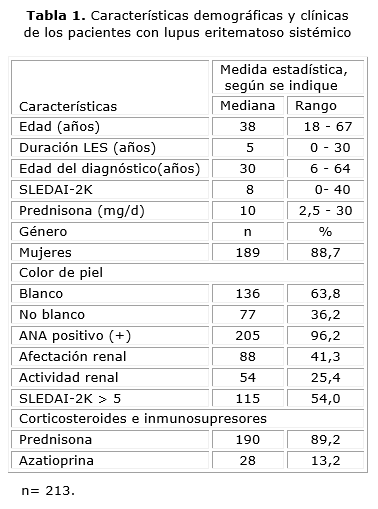
Las características de la población de estudio se presentan en la tabla 1. La mediana del tiempo de evolución de la enfermedad fue de 5 años. El 41 % de los pacientes presentaba nefritis lúpica y de estos, el 61,4 % (54/88) se encontraba en la fase activa de la enfermedad renal. La mediana de la puntuación de SLEDAI-2K fue 8 y 54 % (115/213) de los pacientes estaban en fase de actividad (SLEDAI-2K > 5).
]]>
Presencia de los autoanticuerpos en pacientes con lupus eritematoso sistémico y otras conectivopatías
Los autoanticuerpos anti-DNAdc y anti-Nu fueron poco frecuentes en las conectivopatías diferentes al LES (7/87 y 8/87, respectivamente), estas reactividades se correspondieron con el diagnóstico de ES, AR y EMTC. Los anticuerpos anti-Sm fueron exclusivos del LES, lo que se correspondió con una especificidad de 100 % (tabla 2), mientras que los anti-RNP se encontraron en los pacientes con EMTC (10/87). Los anticuerpos anti-Ro y anti-La se presentaron en los pacientes con SS, AR y ES (22/87 y 15/87, respectivamente) y los anti-Scl-70 en los de ES (15/87).
La especificidad para el diagnóstico del LES se calculó respecto al grupo de OCpt.
Niveles de autoanticuerpos, C3 y C4 en pacientes en fases activa y no activa del LES
Los niveles de todos los autoanticuerpos resultaron significativamente superiores en los pacientes en fase activa del LES que en aquellos en fase inactiva (tabla 3). Los anticuerpos anti-Nu y anti-DNAdc mostraron las diferencias mayores entre los que se hallaban en fase activa e inactiva del LES ( Z= -11,29 y -7,79, respectivamente; p < 0,001).
Correlación de los autoanticuerpos, C3 y C4 con la puntuación de SLEDAI y la proteinuria
La correlación de Spearman fue directa y significativa entre todas las especificidades de autoanticuerpos y la puntuación del SLEDAI-2K, e inversa y significativa entre los factores C3 y C4 del complemento y el SLEDAI-2K (tabla 4). Se encontró, además, correlación directa y significativa entre los niveles séricos de los anticuerpos anti-DNAdc, anti-Nu, anti-Sm y anti-RNP y la concentración de proteínas en orina de 24 h e inversa y significativa entre los factores de complemento C3 y C4 y la proteinuria de 24 h (tabla 4). Las concentraciones de los anticuerpos anti-DNAdc y anti-Nu se correlacionaron directamente entre sí (ρ= 0,630, p < 0,001) e inversamente con C3 (ρ= -0,381; ρ= -0,463, respectivamente, p < 0,001 para ambos) y C4 (ρ= -0,469; ρ= -0,467, respectivamente, p < 0,001 para ambos).
Relación entre los anticuerpos anti-DNAdc y anti-Nu en los pacientes con LES activo
Los anticuerpos anti-Nu se encontraron presentes en 111 (96,5 %) de los 115 pacientes en fase de actividad del LES; mientras que los anti-DNAdc se encontraron en 75 (65,2 %) de los pacientes activos. De los 115 pacientes en fase de actividad del LES, 74 (64,3 %) presentaron niveles positivos de ambos anticuerpos, 37 (32,2 %) fueron positivos de anti-Nu en ausencia de anti-DNAdc y solo 1 paciente (0,9 %) resultó positivo de anticuerpos anti-DNAdc en ausencia de anti-Nu.
Análisis COR de los autoanticuerpos, C3 y C4 respecto a la actividad del LES
La mayor exactitud diagnóstica para la actividad del LES correspondió a los anticuerpos anti-Nu y anti-DNAdc con las AUC de 0,948 y 0,810, clasificable como sobresaliente y muy buena, respectivamente (Fig. 1). El resto de los biomarcadores se caracterizó por las AUC consideradas como no satisfactorias (< 0,71) (tabla 5). El AUC de la suma de los niveles de los anticuerpos anti-DNAdc y los anti-Nu (AUC= 0,939; IC 95 %= 0,906 – 0.972) no resultó superior al AUC de los anticuerpos anti-Nu. La cifra mayor de sensibilidad con la especificidad fijada en 95 % fue la de los anticuerpos anti-Nu que alcanzó el 90 % (tabla 5).
]]>
Análisis COR de los autoanticuerpos, C3 y C4 respecto a la actividad renal del LES
La mayor exactitud diagnóstica para la nefritis lúpica activa le correspondió a los anticuerpos anti-Nu y anti-DNAdc con las AUC de 0,845 y 0,755, respectivamente (Fig. 2). El resto de los biomarcadores se caracterizó por AUC no satisfactorias (< 0,71) (tabla 6). El AUC de la suma de los anticuerpos anti-DNAdc y los anti-Nu resultó de 0,850 (IC 95 %= 0,789 - 0,911). La cifra mayor de sensibilidad con la especificidad fijada en 95 % fue la de los anticuerpos anti-DNAdc que se situó en 33 % (tabla 6).
DISCUSIÓN
El presente estudio proporciona un análisis del perfil de los autoanticuerpos en el LES y de la correlación entre la reactividad de los autoanticuerpos y la actividad de la enfermedad lúpica. Del análisis han emergido 3 conclusiones clave. Primero, es el anti-Nu y luego el anti-DNAdc los autoanticuerpos que se encontraron más fuertemente asociados a la actividad del LES y a la de nefritis lúpica. Segundo, los anticuerpos anti-Nu estuvieron presentes en una proporción notable de pacientes en fase de actividad negativos de anti-DNAdc. Tercero, la relación inversa que se observó entre los niveles de los anticuerpos anti-Nu y anti-DNAdc y los factores de complemento C3 y C4 indica el carácter patogénico de ambos autoanticuerpos.
El análisis de la prevalencia de los autoanticuerpos en pacientes con LES y con otras conectivopatías mostró que los anticuerpos anti-Nu fueron los de mayor sensibilidad diagnóstica para el LES (78 %), solo superados por la reactividad de los ANA. La sensibilidad de los anticuerpos anti-Nu resultó muy superior a la de los anti-DNAdc, que estuvieron presente solo en 45 % de los pacientes con LES. La sensibilidad parece ser una clara ventaja de los anticuerpos anti-Nu sobre el resto de los biomarcadores, y en algunos estudios ha llegado al 100 %.6
]]> Los anticuerpos anti-Nu igual que los anti-DNAdc se han considerado muy específicos del LES, aunque la especificidad de los anti-Nu se mueve entre el 80 y 99 %.7 La especificidad de los anticuerpos anti-Nu y anti-DNAdc en este estudio fue similar, 91 y 92 %, respectivamente (tabla 2). Ninguno de los 2 anticuerpos fueron exclusivos del LES y se presentaron en una pequeña proporción de pacientes con ES, AR y EMTC. La prevalencia baja de los anti-Nu en la ES, AR y EMTC ha sido descrita anteriormente.13-16La presencia y la elevada especificidad de los anticuerpos anti-Nu en el LES sugiere que los anticuerpos anti-Nu pudieran desempeñar un papel en el proceso patogénico en esta enfermedad. Los anticuerpos anti-Nu estuvieron presentes en casi todos los pacientes en fase de actividad del LES (97 %) y, al mismo tiempo, los niveles de los anticuerpos anti-Nu fueron significativamente más altos en los pacientes en fase activa de la enfermedad que en los que se hallaban en la fase inactiva. Por otra parte, aunque los títulos de los anticuerpos anti-DNAdc fueron también superiores en los pacientes en fase activa del LES, los anticuerpos anti-DNAdc estuvieron presentes solo en 65 % de estos pacientes.
La fase de actividad clínica del LES se caracterizó por la actividad serológica, manifestada por niveles séricos superiores de todas las especificidades de autoanticuerpos y por la mayor carga de autoanticuerpos. Los anticuerpos que más se elevaron en la fase activa del LES fueron los anti-Nu y anti-DNAdc (tabla 3).
Un número considerable de autores han comunicado asociación entre los anticuerpos anti-Nu y la actividad del LES revelada por niveles aumentados de anticuerpos anti-Nu en pacientes con LES activo.6,11,17-23 Sin embargo, es controversial el lugar que ocupan en el podio lo anticuerpos anti-Nu y los anti-DNAdc. Mientras que algunos estudios destacan a los anti-Nu como marcadores de actividad del LES,17-19,22 otros defienden la superioridad de los anticuerpos anti-DNAdc como los más fuertemente asociados a la actividad del LES y a la de nefritis lúpica.11,24-26 La detección de anticuerpos anti-DNAdc de gran avidez, que es el subconjunto de mayor potencial patogénico, pudiera explicar la asociación más fuerte de los anti-DNAdc con la actividad del LES observada en algunas investigaciones.11,25
La sobreproducción de múltiples especificidades de autoanticuerpos asociada a la fase de actividad clínica del LES se puede atribuir a la activación policlonal de las células B.27,28 Si consideramos la compleja naturaleza a modo de espectro en el plano clínico y serológico del LES29 es posible que cada especificidad antinuclear sea marcador de actividad de un subgrupo de pacientes. Desde un enfoque práctico, la actividad serológica asociada a la actividad clínica del LES advierte que la identificación de un biomarcador único de la actividad del LES puede no ser la solución definitiva para el seguimiento clínico de la enfermedad, la cual posiblemente dependa de un perfil amplio de biomarcadores, obtenible con la nueva tecnología proteómica que incluye además del perfil de autoanticuerpos, análisis de genes, perfiles de transcripción, análisis de las vías de señales y expresión de citocinas y quimiocinas.9
La estrecha asociación de los niveles séricos de los anticuerpos anti-Nu con la actividad del LES fue demostrada también en el análisis de correlación con la puntuación de SLEDAI-2K (tabla 4), un reconocido índice de medición de la actividad del LES.2 El coeficiente de correlación más alto con SLEDAI-2K le correspondió a los anticuerpos anti-Nu, seguidos por los anti-DNAdc (0,856 y 0,616, respectivamente; p < 0,001 para ambos). Las correlaciones de los anticuerpos anti-Nu con la actividad del LES superan en el coeficiente a las de otros estudios,11,22,23,30 lo cual se puede atribuir a las diferencias en el tamaño y a las características de la muestra, considerando no solo los criterios de inclusión y exclusión, sino también el nivel asistencial del centro de salud, así como las diferencias étnicas de la población derivadas de la diversidad genética, ambiental y socio-demográfica.
Son pocas las publicaciones que han podido demostrar asociación entre los autoanticuerpos y las manifestaciones clínicas del LES. En relación con la asociación entre los anticuerpos anti-Nu y anti-DNAdc con la proteinuria diaria, las opiniones están divididas entre una correlación positiva,25,30 a la que apoyan nuestros resultados, y ausencia de correlación.16,21,31 La correlación positiva de los anticuerpos anti-Nu y los anti-DNAdc con la pérdida renal de proteínas indica la contribución de estos anticuerpos a la producción de la lesión renal lúpica.
Los anticuerpos anti-Nu y los anti-DNAdc se correlacionaron directamente entre ellos, lo que evidencia que pertenecen a la misma familia de anticuerpos dirigidos a la cromatina.11,19,20,32 Tanto los anticuerpos anti-Nu como los anti-DNAdc se correlacionaron de forma inversa con los factores C3 y C4, lo que enfatiza su papel patogénico en el LES. Los anticuerpos anti-Nu han sido asociados con el consumo de complemento en estudios anteriores, ya sea del C3,19 C411 o ambos.21,30
Para determinar mejor la exactitud de la discriminación de los autoanticuerpos entre la fase de actividad y la de remisión del LES se construyeron las curvas COR. En este marco, donde el área debajo de la curva (AUC) es el criterio de la exactitud de la prueba, los anticuerpos anti-Nu han demostrado ser un excelente marcador para la actividad del LES y de la nefritis lúpica con AUC de 0,948 y 0,845, respectivamente.
Los anticuerpos anti-Nu y anti-DNA demostraron mayor exactitud para el diagnóstico de la actividad del LES que para la actividad de la nefritis lúpica, lo que indica que estos anticuerpos pudieran estar implicados, además de en la lesión renal, en las manifestaciones extrarrenales del LES. Al respecto, Hung y otros y Shabana y otros encontraron también una correlación mayor de los anticuerpos anti-Nu con la actividad del LES que con la actividad de la nefritis lúpica.21,32 De hecho, la asociación de los anti-Nu con SLEDAI, pero no con la actividad de la nefritis lúpica ha sido descrita en varios estudios,24,26,33 lo que se debe a la contribución de diversas manifestaciones extrarrenales.6,20,24,30,32,33
]]> Como conclusión, vale destacar que la actividad del LES estuvo relacionada con la producción aumentada de múltiples especificidades de autoanticuerpos, entre los cuales los anticuerpos anti-Nu han mostrado la asociación más significativa con la actividad de la enfermedad, y con la actividad de la nefritis lúpica. Los anticuerpos anti-Nu detectaron una proporción considerable de pacientes activos con LES negativos para los anticuerpos anti-DNAdc. La estrecha asociación entre los anticuerpos anti-Nu y la actividad de la enfermedad del LES y de la nefritis lúpica puede obedecer al papel patogénico de estos anticuerpos, sustentado por la correlación con el consumo de complemento y la pérdida renal de proteínas. Nosotros recomendamos firmemente la determinación de los anticuerpos anti-Nu en el seguimiento clínico del LES, tanto para la evaluación de la actividad de la enfermedad como de la nefritis lúpica. Aunque los anticuerpos anti-Nu parecen ser un biomarcador esencial de la actividad del LES, se requieren estudios adicionales longitudinales para comprobar el valor de predicción de estos anticuerpos en el manejo clínico de los pacientes con LES.
REFERENCIAS BIBLIOGRAFICAS
1. Tan EM, Cohen AS, Fries JF, Masi AT, McShane DJ, Rithfield NF, et al. The 1982 revised criteria for the classification of systemic lupus erythematosus. Arthritis Rheum. 1982;25:1271-7.
2. Gladman DD, Ibanez D, Urowitz MB. Systemic lupus erythematosus disease activity index 2000. J Rheumatol. 2002;29:288-91.
3. Esdaile JM, Abrahamowicz M, Joseph L, MacKenzie T, Li Y, Danoff D. Laboratory tests as predictors of disease exacerbations in systemic lupus erythematosus. Why some tests fail. Arthritis Rheum. 1996;39:370-8.
4. Gladman DD, Hirani N, Ibanez D, Urowitz MB. Clinically active serologically quiescent systemic lupus erythematosus. J Rheumatol. 2003;30:1960-2.
5. Mohan C, Adams S, Stanik V, Datta SK. Nucleosome: a major immunogen for pathogenic autoantibody-inducing T cells of lupus. J Exp Med. 1993;177:1367-81.
6. Simon JA, Cabiedes J, Ortiz E, Alcocer-Varela J, Sanchez-Guerrero J. Antinucleosome antibodies in patients with systemic lupus erythematosus of recent onset. Potential utility as a diagnostic tool and disease activity marker. Rheumatology. 2004;43:220-4.
7. Gómez-Puerta JA, Burlingame RW, Cervera R. Antichromatin (anti-nucleosome) antibodies: diagnostic and clinical value. Autoimmun Rev. 2008;7:606-11.
8. Agarwal S, Harper J, Kiely PDW. Concentration of antibodies to extractable nuclear antigens and disease activity in systemic lupus erythematosus. Lupus. 2009;18:407-412.
9. Liu CC, Kao AH, Manzi S, Ahearn JM. Biomarkers in systemic lupus erythematosus: challenges and prospects for the future. Ther Adv Musculoskel Dis. 2013;5:210-33.
10. Villegas-Zambrano N, Martínez-Taboada VM, Bolívar A, San Martin M, Álvarez L, Marín MJ, et al. Correlation between clinical activity and serological markers in a wide cohort of patients with systemic lupus erythematosus: an eight-year prospective study. Ann NY Acad Sci. 2009;1173:60-6.
11. Andrejevic S, Jeremic I, Sefik-Bukilica M, Nikolic M, Stojimirovic B, Bonaci-Nikolic B. Immunoserological parameters in SLE: high-avidity anti-dsDNA detected by ELISA are the most closely associated with the disease activity Clin Rheumatol. 2013,32:1619-26.
13. Amoura Z, Koutouzov S, Chabre H, Cacoub P, Amoura I, Musset L, et al. Presence of antinucleosome autoantibodies in a restricted set of connective tissue diseases. Antinucleosome antibodies of the IgG3 subclass are markers of renal pathogenicity in systemic lupus erythematosus. Arthritis Rheum. 2000;43:76-84.
14. Benucci M, Saviola G, Baiardi P, Cammelli E, Manfredi M. Antinucleosome antibodies as prediction factor of development of autoantibodies during therapy with three different TNF alpha blocking agents in rheumatoid arthritis. Clin Rheumatol. 2008;27:91-5.
]]>15. Ferreira FGM, Skare TL, Nisihara RM, Utiyama SR. Antinucleosome antibodies in scleroderma patients. Indian J Med Res. 2011;133:341-2.
16. Quattrocchi P, Barrile A, Bonanno D, Giannetto L, Patafi M, Tigano V, et al. The role of anti-nucleosome antibodies in systemic lupus erythematosus. Results of a study of patients with systemic lupus erythematosus and other connective tissue diseases. Reumatismo. 2005;57:109-13.
17. Souza A, da Silva LM, Oliveira FR, Roselino AMF, Louzada-Junior P. Anti-nucleosome and anti-chromatin antibodies are present in active systemic lupus erythematosus but not in the cutaneous form of the disease. Lupus. 2009;18:223-9.
18. Suleiman S, Kamaliah D, Nadeem A, Naing NN, Che Maraina CH. Anti-nucleosome antibodies as a disease activity marker in patients with systemic lupus erythematosus. Intern J Rheum Dis. 2009;12:100-6.
19. Saisoong S, Eiam-Ong S, Hanvivatvong O. Correlations between antinucleosome antibodies and ant-double-stranded DNA antibodies, C3, C4, and clinical activity in lupus patients. Clin Exp Rheumatol. 2006;24:51-8.
21. Hung WT, Chen YM, Lan JL, Chen HH, Chen YH, Chen DY, et al. Antinucleosome antibodies as a potential biomarker for the evaluation of renal pathological activity in patients with proliferative lupus nephritis. Lupus. 2011;20:1404-10.
22. Kiss E, Lakos G, Szegedi G, Poor G, Szodoray P. Anti-nucleosome antibody, a reliable indicator for lupus nephritis. Autoimmunity. 2009;42:393-8.
23. Düzgün N, Sahin M, Genç Y, Tutkak H. Antinucleosome antibodies and systemic lupus erythematosus. Ann N Y Acad Sci. 2007;1109:421-8.
24. Kim HA, Jeon JY, Choi GS, Sung JM, Kim MJ, Yun JM, et al. The antichromatin antibodies can be useful as a diagnostic tool and disease activity marker of systemic lupus erythematosus in Koreans. Clin Immunol. 2008;128:277-83.
25. Manson JJ, Ma A, Rogers P, Mason LJ, Berden JH, van der Vlag J, et al. Relationship between anti-dsDNA, anti-nucleosome and anti-alpha-actinin antibodies and markers of renal disease in patients with lupus nephritis: a prospective longitudinal study. Arthritis Res Ther. 2009;11:R154.
26. Mok CC, Ho LY, Leung HW, Wong LG. Performance of anti-C1q, antinucleosome and anti-dsDNA antibodies for detecting concurrent disease activity of systemic lupus erythematosus. Trans Res. 2010;156:320-5.
27. Dorner T, Heimbacher C, Farner NL, Lipsky PE. Enhanced mutational activity of Vkappa gene rearrangements in systemic lupus erythematosus. Clin Immunol. 1999;92:188-96.
28. Furtado J, Isenberg DA. B cell elimination in systemic lupus erythematosus. Clin Immunol. 2013;146:90-103.
29. Agmon-Levin N, Mosca M, Petri M, Shoenfeld Y. Systemic lupus erythematosus one disease or many? Autoimmun Rev. 2012;11:593-595
30. Su Y, Jia RL, Han L, Li ZG. Role of anti-nucleosome antibody in the diagnosis of systemic lupus erythematosus. Clin Immunol. 2007;122:115-20.
]]>31. Grootscholten C, Dieker JW, McGrath FD, Roos A, Derksen RH, van der Vlag J, et al. A prospective study of anti-chromatin and anti-C1q autoantibodies in patients with proliferative lupus nephritis treated with cyclophosphamide pulses or azathioprine/methylprednisolone. Ann Rheum Dis. 2007;66:693-6.
32. Shabana AA, El-Ghawet AE, Machaly SA, Abu Hashim EM, El-Kady BA, Shaat R. Anti-chromatin and anti-histone antibodies in Egyptian patients with systemic lupus erythematosus. Clin Rheumatol. 2009;28:673-8.
33. Bose N, Wang X, Gupta M, Yao Q. The clinical utility of anti-chromatin antibodies as measured by BioPlex 2200 in the diagnosis of systemic lupus erythematosus versus other rheumatic diseases. Int J Clin Exp Med. 2012;5:316-20.
Recibido: 13 de mayo de 2014.
Aceptado: 1 de agosto de 2014.
Dra. Elena Kokuina. Hospital Clinicoquirúrgico "Hermanos Ameijeiras", San Lázaro No. 701 entre Belascoaín y Marqués González, Centro Habana, La Habana, Cuba. CP 10 300. inmunologia@hha.sld.cu
]]>