]]>
Se realizó, además, Ultrasonografía Doppler de las arterías uterinas en la consulta inicial que permitió incluir un número de casos. Se consideró alterada si cumplía uno de los siguientes parámetros:
- Índice de pulsatilidad (IP)> 0,58
- Índice de resistencia (IR)> 0,45
- Relación sístole/diástole> 3 o presencia de notch16 ]]>
- Hipertensión arterial crónica: ____
- Diabetes mellitus:___
- Enfermedad renal:___
- Síndrome antifosfolípido: ___
- Lupus eritematoso sistémico: ___ ]]> Asma bronquial: ___
- Úlcera péptica: ___
- Enfermedad inflamatoria intestinal: ___
- Artritis reumatoidea: ___
- Trastornos tromboembólicos: ___
- Trastorno de la coagulación: ___
- PE agravada: si: ___ no:___
- Historia de sangramiento previa al parto: si: ___ no:___ ]]> Hemorragia post parto: si: ___ no:___
- Hematoma retroplacentario: si: ___ no:___
- Trastornos gastrointestinales si: ___ no:___
- Episodios hemorrágicos: si: ___ no:___ ]]> Hemorragia intraventircular: si: ___ no:___
Los datos del estudio fueron almacenados utilizando el paquete estadístico SPSS. Se realizaron distribuciones frecuencia y porcentajes, aplicando la estadística descriptiva. La prueba de Chi cuadrado se empleó para determinar relación entre variables cualitativas y determinar la significación estadística de los datos obtenidos según valor de p.
En cuanto a las consideraciones éticas, se le explicó los objetivos del estudio a cada paciente para garantizar respuestas ajustadas a nuestros intereses y se solicitó su colaboración, bajo el compromiso de utilización de la información sólo en el contexto de la investigación. Esta investigación fue aprobada por el Consejo Científico de la Institución.
RESULTADOS
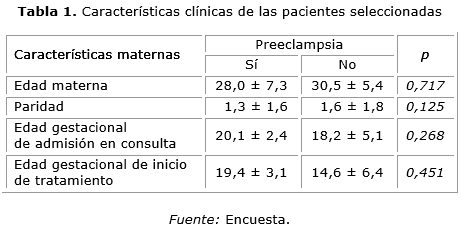
En la tabla 1 se realiza una caracterización de la muestra estudiada. En ella, la edad materna y la paridad no mostraron diferencias estadísticas entre las pacientes que desarrollaron PE o no.
Con relación a la edad gestacional de admisión en la consulta, en el grupo de pacientes con PE la edad gestacional promedio fue de 20,1 ± 2, 4 semanas, lo cual difiere del grupo que no desarrolló la enfermedad, que fue menor.
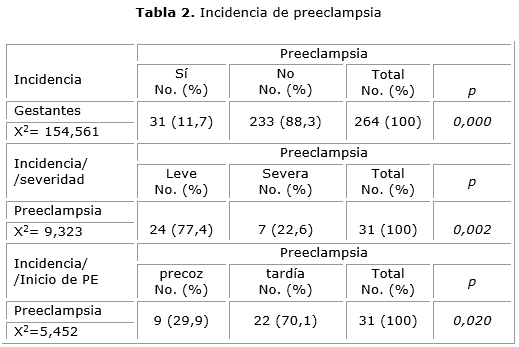
En el grupo de pacientes estudiadas, todas de alto riesgo, 11,7 % presentó PE a pesar de la terapéutica empleada, con una diferencia muy significativa del 88,3 % de pacientes que lograron un desarrollo normal del embarazo, como se evidencia en la tabla 2.
En este trabajo de las pacientes que desarrollaron PE, solo 22,6 % fue de forma grave; mientras 77,4 % fue leve, con un predominio estadísticamente significativo de los casos leves.
Cuando en la presente investigación se analiza la influencia del tratamiento sobre el inicio de PE, se encontró que solo en un tercio de las pacientes, la PE tuvo un inicio antes de las 32 semanas de gestación. El resto de las pacientes con PE de aparición tardía (70,1 %) con una diferencia significativa desde el punto de vista porcentual y estadístico.
Los valores estadísticos arrojados refuerzan el papel "preventivo" de la ASA y el Calcio en la aparición de la PE y sus formas severas.
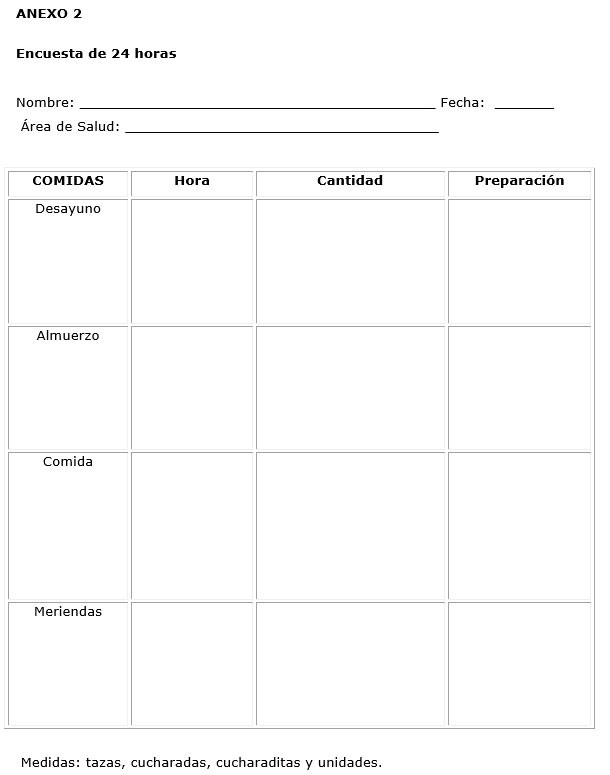
Todas las pacientes estudiadas tenían suplementación con carbonato de calcio (1 g/día) al ser consideradas como pacientes de alto riesgo para la PE. Pero de ellas, solo 14 % tenían -según la encuesta alimentaria-, una baja ingesta de calcio. El resto de las pacientes tenían una ingesta dentro de valores considerados como normales (86 %). Esto se relacina con el nivel educativo de las pacientes encuestadas para recordar de forma precisa la ingesta alimentaria del día anterior al interrogatorio (tabla 3).
En este trabajo no existieron diferencias significativas en la incidencia de PE en las pacientes que se les administró calcio, ya que 13,5 % de las que presentaron baja ingesta de calcio desarrollaron PE contra 11,5 % de las de ingesta normal.
Cuando analizamos cada uno de los grupos específicos, se observa en la tabla 4, que existieron diferencias porcentuales estadísticamente significativas en grupos de riesgo determinados. Del total de pacientes hipertensas crónicas, 90,5 % no desarrolló preeclampsia frente al 9,5 % que presentó la enfermedad. Estas diferencias son muy significativas que inducen a pensar en el papel protector de la terapéutica empleada en este grupo de riesgo.
]]>
Otro de los grupos de riesgo que tuvieron un alto beneficio con valor estadístico fueron las pacientes con obesidad, antecedentes de PE en el embarazo anterior, pacientes con ecografía Doppler patológica; mientras que las pacientes que mostraron un beneficio moderado son las pacientes con síndrome antifosfolípidos, lupus eritematoso sistémico y diabetes mellitus. Sus resultados auguran una mejora en el riesgo de preeclampsia en estas pacientes por los bajos porcientos de pacientes que la desarrollan después de recibir la suplementación del ASA y Calcio.
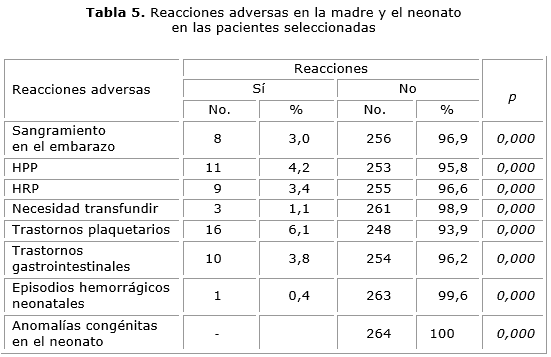
La tabla 5 describe los eventos que presentaron las pacientes que consumieron la suplementación de Calcio y ASA, los cuales, en su mayoría no pueden atribuírseles como consecuencias de la terapéutica empleada y sí a la evolución propia de la enfermedad en análisis, como el HRP con frecuencia elevada en la PE.
No obstante, hay trastornos como los gastrointestinales (3,8 %) y los de función plaquetaria (6,1 %) que se le adjudicaron al uso de salicilatos y llevaron en ocasiones la suspensión del tratamiento antes de las 36 semanas.
DISCUSIÓN
La PE es una enfermedad multisistémica, cuyo único tratamiento definitivo es la interrupción del embarazo, el parto del feto y la expulsión de la placenta.1
Estos resultados nos permiten apoyar lo señalado en la bibliografía, al referir que la edad gestacional de inicio de tratamiento tiene una relación directa a la aparición de la preeclampsia (PE), en la que a mayor edad gestacional mayor probabilidad de ocurrencia de la misma.2,3
]]> El hecho de que la consulta funcione a nivel de atención secundario, puede influir en que la admisión e inicio del tratamiento aún sea después de las 16 semanas de gestación, y a pesar de estar pautadas por las normas de atención prenatal cubanas aún persista un grupo pacientes que se les indica el tratamiento después de la edad gestacional ideal.Varios estudios sobre la ASA en mujeres con alto riesgo de PE sugieren que la eficacia está fuertemente relacionada con la edad gestacional de inicio de tratamiento. Estos han demostrado que cuando el tratamiento es iniciado antes de las 16 semanas de gestación, el riesgo de PE se reduce en un 50 % [RR 0,47,95 % IC 0,36-0,62]. Mientras, cuando el tratamiento es después de esta edad gestacional, es solo en un 20 %, la reducción del riesgo de PE (RR 0,78,95 % CI 0,61-0,99).6,12
En los embarazos normales, la invasión del trofoblasto al miometrio y la transformación de las arterias espirales uterinas en vasos angostos con pérdida de la muscular generalmente empiezan a la semana ocho de la gestación y son terminadas por las 16 a 20 semanas completamente.5 Este proceso fisiológico de placentación está reducido en PE, particularmente en PE pretérmino, RCIU y en menor grado en el parto de pretérmino espontáneo. Estudios de las biopsias de placentas en mujeres con PE, han informado que solamente 0-40 % de las arterias espirales uterinas son transformadas totalmente, comparado con 80-100 % en mujeres con embarazo normal.17
Las evidencias recientes de nivel I (revisiones sistemáticas) han encontrado beneficios leves-moderados con el uso de bajas dosis de ASA para prevención de la PE en pacientes con elevado riesgo de PE. Estos estudios destacan que la ASA a bajas dosis, reduce entre un 10-27% el riesgo de PE.4,18
Varios autores como Bujold,12 Mone F,18 Roberge19 han reportado en sus series el efecto de esta terapia combinada sobre la severidad de la PE.
El estudio PREDO,6 de "Predicción y prevención de la preeclampsia" que agrupó a 1064 mujeres, el cual se llevó a cabo en 10 países, sugirió en su informe final que la ASA puede reducir el riesgo de PE (RR 0,6, 95 % CI 0,4-0,8) y la PE severa (RR 0,3, 95 % CI 0,1-0,7) cuando el tratamiento se inicia antes de las 16 semanas.
Roberge19 señala que el inicio de la terapia antes de las 16 semanas reduce el riesgo de PE severa pero no de la PE leve-moderada. Ello avala la hipótesis que la administración de ASA antes de esa edad gestacional puede reducir los trastornos de la placentación y con ello disminuir las formas severas y tempranas de la PE.
Uno de los dilemas actuales está en determinar para qué grupo de mujeres ofrecer la prevención de la PE puede ser más provechoso, si para todas las mujeres o sólo para aquellas con los factores de riesgo muy importantes, o para aquellas con alguna prueba de screening positiva. Esto explica las opiniones diferentes en las pautas internacionales sobre las cuales es más apropiado brindar dosis baja de ASA.
Un estudio reciente ha demostrado que es más fructífero tratar todos universalmente con dosis bajas de ASA que tratar solo las que se obtengan por un algoritmo bien pautado de detección.20
Un método de selección de pacientes de alto riesgo es a través del Doppler color de las arterias uterinas y la demostración de un aumento en la media del IP. La alta incidencia de complicaciones en este grupo de alto riesgo que incluye PE en 18 % de los casos y RCIU en 23 %, confirma la confiabilidad del Doppler uterino en el diagnóstico en la placentación anormal. Este alto valor predictivo positivo le confiere un mayor valor profético comparado con el de la historia previa del embarazo, que es el método de selección de grupos de alto riesgo en la mayoría de los estudios randomizados existentes de ASA.18
]]> Las reducciones de la PE, de la morbilidad severa y de la mortalidad materna, avalan el uso de suplementos de calcio durante el embarazo en mujeres con bajo consumo dietético. Pero en el caso de las mujeres con adecuado consumo dietético, la evidencia del beneficio del suplemento de calcio no es concluyente. Varios trabajos han demostrado la importancia de los niveles de calcio en la dieta. Estos estudios con mujeres con altos niveles de ingesta (1200 mg/d) no han mostrado una reducción en el riesgo de PE.2,3,10La ASA, además de ser vista como una droga segura en el embarazo, tiene un bajo costo y está ampliamente disponible. Por lo que, al sopesar los elevados costos por los servicios médicos mundialmente para el tratamiento de la PE y sus secuelas, que abarca el cuidado para la madre y el neonato, se sugiere que la provisión universal de ASA para la prevención de PE es más económicamente más viable.18
La literatura describe que ASA, administrada a dosis de 100 miligramos por día no es suficiente para afectar la función de plaquetaria en la madre.19 Sin embargo, existen reportes de estudios en que se enrolaron mujeres tratadas con bajas dosis de ASA y otras no (grupo control), en los que el uso de ASA se asoció significativamente con un incremento del riesgo de episodios gastrointestinales y sangramientos cerebrales (5,58 frente a 3,60 por cada 1000 personas al año).13
Aunque tales riesgos son pequeños, consideramos que durante la administración de ASA debe preferirse la tableta con protección entérica y no debe ser rutinariamente ofrecida, sino que debe ser reservada esta terapia para las mujeres con alto riesgo de PE.13
La mayoría de las evidencias relacionan que dosis bajas de aspirina (ASA), es el agente anti plaquetario que se debe usar en la práctica para prevenir la PE. La decisión de tomar o no ASA durante el embarazo debe ser tomada en la consulta, entre la paciente y su médico. La implementación de estos resultados en la práctica clínica de rutina requiere mayor habilidad para identificar el subgrupo de mujeres en las que el beneficio es mayor (las de alto riesgo para preeclampsia), y quizás el uso de dosis mayores sea seguro. Aun así, la estrategia de tratar las de alto riesgo, tiene el límite de que un número importante de casos usualmente ocurre en las de bajo riesgo, que no serían cubiertas por la terapia con ASA. Sin embargo, desde el punto de vista de salud pública, aún con estos beneficios leves-moderados valen la pena su uso ampliamente. Cualquier intervención que prevenga esta enfermedad y/o sus complicaciones es de valor inestimable.
Se concluye que el uso de la aspirina y el calcio, a las dosis empleadas, influyeron en la disminución de la incidencia de preeclampsia y sus formas severas. Existieron beneficios mayores, con las medidas preventivas empleadas, para algunos grupos específicos de riesgo como: HTA crónica, obesidad, historia de preeclampsia previa y ecografía Doppler alterada. No se observó un incremento de eventos adversos sobre la madre y el neonato en las pacientes tratadas.
CONFLICTO DE INTERESES
Los autores no declaran tener conflictos de intereses.
]]> REFERENCIAS BIBLIOGRÁFICAS
1. World Health Organization. WHO recommendations for Prevention, treatment of pre-eclampsia, and eclampsia. World Health Organization 2014. Disponible en: http://whqlibdoc.who.int/publications/2011/9789241548335_eng.pdf
2. Duley L, Henderson-Smart D, Knight M, King J. Antiplatelet agents for preventing preeclampsia and its complications. (Cochrane Review). In: The Cochrane Library, Issue 2. 2009. Oxford: Update Software. Disponible en: http://www.update-software.com/BCP/BCPGetDocument.asp?DocumentID=CD004659
3. Souza EV, Torloni MR, Atallah AN, Dos Santos GMS, Kula L, Sass N. Aspirin plus calcium supplementationto prevent superimposed preeclampsia: a randomized trial. Braz J Med Biol Res. 2014;47(5).
4. Briceño C, Briceño L. Aspirina, calcio y prevención de preeclampsia. Rev Obstet Ginecol Venez. 2009;69(4):262-8. Disponible en: http://www.scielo.org.ve/pdf/og/v69n4/art08.pdf
5. Orizondo R. Novedades y controversias en relación con la preeclampsia/eclampsia. Rev cubana med [revista en la Internet]. 2007;46(2): Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0034-75232007000200009&lng=es
6. Villa P, Kajantie E, Ra¨ikko¨nen K, Pesonen AK, Ha¨ma¨la¨inen E, Vainio M, et al. Aspirin in the prevention of pre-eclampsia in high-risk women: a randomised placebo-controlled PREDO Trial and meta-analysis of randomized trials. BJOG. 2013;120:64-74.Disponible en: http://www.sigo.it/pdf_esterni/aspirin-prevention-preeclampsia2012_13-11.pdf
7. Lorenzo P, Moreno A, Leza JC. Velázquez. Farmacología básica y clínica. 17 a ed. España: Editorial Médica Panamericana; 2005.
]]>8. Velásquez M, Gil-Villa AM, Cadavid AP. Lipoxinas inducidas por la aspirina: una alternativa para modular los procesos proinflamatorios en la preeclampsia. Rev Cubana Obstet Ginecol. 2013;39(3):292-305. Disponible en: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0138-600X2013000300009&lng=es
9. GoodlinRC, Haesslein HO, Fleming J. Aspirin for the treatment of recurrent toxaemia. Lancet. 1978;2(8079):51.
10. Askie LM, Duley L, Henderson-Smart DJ, Stewart LA. Antiplatelet agents for prevention of pre-eclampsia: a metaanalysis of individual patient data. Lancet. 2007;369:1791-8. Disponible en: doi:10.1016/S0140-6736(07)60712-0.
11. Henderson JT, Whitlock EP, O'Conner E, Senger CA, Thompson JH, Rowland MG. Low-Dose Aspirin for the Prevention of Morbidity and Mortality From Preeclampsia: A Systematic Evidence Review for the U.S. Preventive Services Task Force. Rockville (MD): Agency for Healthcare Research and Quality (US); 2014. Report No.: 14-05207-EF-1.
12. Bujold E, Roberge S, Nicolaides K. Low-dose aspirin for prevention of adverse outcomes related to abnormal placentation. Prenatal Diagnosis. 2014;34:642-8.
13. Roberge S, Villa P, Nicolaides K, Giguère Y, Vainio M, Bakthi A, et al. Early Administration of Low-Dose Aspirin for he Prevention of Preterm and Term Preeclampsia: A Systematic Review and Meta-Analysis. Fetal Diagn Ther. 2012;31:141-6.
]]>14. Hofmeyr GJ, Lawrie TA, Atallah ÁN, Duley L. Calcium supplementation during pregnancy for preventing hypertensive disorders and related problems (Review).The Cochrane Library. 2011. Disponible en: http://apps.who.int/rhl/reviews/CD001059.pdf
15. Cuba. Ministerio de Salud Pública. Manual de Obstetricia y Perinatología 2012.
16. Lorente M, Navarro G. Prevención de la preeclampsia con aspirina. Prog Obstet Ginecol. 2015. Disponible en: http://dx.doi.org/10.1016/j.pog.2015.06.004
17. Papageorghiou AT, Yu CK, Cicero S, Bower S, Nicolaides KH. Second-trimester uterine artery Doppler screening in un selected populations: a review. J Matern Fetal Neonatal Med. 2002;12:78-88. Disponible en: doi: 10.1080/jmf.12.2.78.88.
18. Mone F, Mulcahy C, McParland P, McAuliffe FM. Should we recommend universal aspirin for all pregnant women?. Am Journal of Obstetrics and Gynecology. 2017;216(2):141.e1-141.e5. doi:10.1016/j.ajog.2016.09.086
19. Roberge S, Sibai B , Mc Caw-Binns A , Bujold E . Low-Dose Aspirin in Early Gestation for Prevention of Preeclampsia and Small-for-Gestational-Age Neonates: Meta-analysis of Large Randomized Trials. Am J Perinatol. 2016;33(8):781-5. doi: 10.1055/s-0036-15724951.
20. O'Gorman N, Wright D, Rolnik DL, Nicolaides KH, Poon LC. Study protocol for the randomized controlled trial: combined multimarket screening and randomized patient treatment with Aspirin for evidence-based preeclampsia prevention (ASPRE). BMJ Open. 2016;6:e011801.
]]>
Recibido: 8 de abril de 2017.
Aprobado: 14 de mayo de 2014.
Vivian de las Mercedes Cairo González. Hospital Universitario Ginecobstétrico "Mariana Grajales". Santa Clara, Villa Clara. Cuba.
Correo electrónico: viviancg@infomed.sld.cu
]]> HISTORIA CLÍNICA INDIVIDUAL
Datos generales de la paciente
Nombre: ________________________________ Edad: _____ años HC: __________
Raza: B: ___ N: ___ M:___ Área de Salud:______________________ Fecha:________
Hábitos tóxicos: Café __ Tabaco__ Alcohol___
Historia obstétrica
Edad gestacional: _______semanas
FUM: __________ FPP: __________
Gesta: ________ Para:________ Aborto:________
]]>Antecedentes patológicos personales
1. Historia personal de PE (en embarazos anteriores): si: ___ no:___
· Tipo de preeclampsia en embarazo anterior: grave ____ leve:___
2. Presencia de algunas enfermedades crónicas:
3. Examen físico:
Talla: ___ Peso: ___ IMC:_____
TA: ___ FC: ___ Edemas: __Sí __No
]]> Altura uterina: ___ Presentación: ___ Foco fetal: ___ FC fetal: ___4. Complementarios:
Ultrasonografía Doopler:
___________________________________________________________________
___________________________________________________________________
___ Normal ___Patológica
Creatinina: ____ Ácido úrico: ____ Proteinuria de 24 horas: ____
5. Con relación al uso de Aspirina:
Fecha de inicio consumo de aspirina: _____________ semanas.
]]> Dosis:__________________
6. En relación con el calcio:
Escasa ingesta calcio previo. Si: _______ No:______
Escasa ingesta de calcio en la gestación: Si: _______ No:______
Fecha de inicio consumo de calcio: _____________ semanas.
Dosis:__________________
7. Resultados:
Maternos
]]> - Preeclampsia: si: ___ no:___· PE ≤ 32 semanas:___ PE ≥ 32 semanas: :___
- Enfermedad hipertensiva gestacional: si: ___ no:___
- Hematoma retroplacentario: si: ___ no:___
- Edad gestacional momento del parto: ___________ semanas
- Eclampsia: si: ___ no:___
- Insuficiencia hepática: si: ___ no:___
- Insuficiencia real. si: ___ no:___
]]> - CID: si: ___ no:___Perinatales
- Muerte perinatal:
- Muerte fetal: si: ___ no:___ Muerte neonatal: si: ___ no:___
- Retardo crecimiento fetal si: ___ no:___
- Peso al nacer: __________
8. Efectos indeseables:
En la madre:
· Necesidad de transfusiones de sangré o sus derivados. si: ___ no:___
· Otras relacionadas con la administración de aspirina y/o suplementos de calcio: ______________________________________________________________________
______________________________________________________________________
En el feto o RN:
· Otras relacionadas con la administración de aspirina y/o suplementos de calcio: _____________________________________________________________________
______________________________________________________________________
]]>