Instituto de Medicina Tropical "Pedro Kourí"
Dra. Blanca E. Duménigo Ripoll1 y Dr. Carlos M. Finlay Villalvilla2
Se presenta el diagnóstico de fascioliasis hepática ovina mediante un ensayo inmunoenzimático tipo sandwich con el uso del anticuerpo monoclonal ES78 (sandwich ELISA) previamente reportado para el diagnóstico de fascioliasis bovina. El ensayo fue aplicado a las heces de 40 ovinos infectados con Fasciola hepatica, 88 ovinos con otras infecciones parasitarias probadas por coproparasitología y 100 animales negativos coprológicamente. Fueron detectados antígenos de excreción-secreción de Fasciola hepatica en 38 de los 40 ovinos con fascioliasis y en ninguno de los animales negativos o con otras parasitosis. Los resultados indican que el ES78-sandwich ELISA, al igual que en bovinos, es rápido, simple y útil para el diagnóstico de la infección activa por Fasciola hepatica en el ganado ovino.
Descriptores DeCS: FASCIOLIASIS/diagnóstico; FASCIOLIASIS/veterinaria; FASCIOLA HEPATICA/inmunología; ANTIGENOS HELMINTICOS/análisis; OVINOS/parasitología; ANTICUERPOS MONOCLONALES; HECES/parasitología; TEST DE ELISA/métodos.
En Cuba, la fascioliasis hepática es enzoótica en los ganados bovino y ovino, por tanto, causa grandes pérdidas económicas en la industria pecuaria. Aunque la cría de ovino no está tan extendida en nuestro país como en otros, está demostrado que el ovino es más susceptible a la infección por Fasciola hepatica que otras especies animales.1 Estos antecedentes, unidos a la baja sensibilidad mostrada por los métodos coproparasitológicos en el diagnóstico de esta parasitosis, y a los exitosos resultados obtenidos por nosotros en el diagnóstico de la fascioliasis bovina mediante un ensayo inmunoenzimático de captura tipo sandwich (sandwich ELISA) con el uso del anticuerpo monoclonal ES78 (AcMES78),2,3 hacen que el objetivo del presente trabajo sea la aplicación de éste en la detección y cuantificación de coproantígenos para el diagnóstico de fascioliasis hepática en ganado ovino. En este estudio se describe un procedimiento similar, con pequeñas modificaciones, al utilizado para la detección de antígenos de excreción-secreción (ES) en heces de ganado bovino.3
Para el análisis de las heces se procedió a suspender 1 g de heces frescas en 7 mL de agua y homogenizarlo mediante un depresor lingual de madera. Una vez homogenizado, se centrifugó a 900 rpm durante 3 min. El sobrenadante se colectó y guardó a -20 oC hasta su uso. Se sensibilizaron placas de microtitulación de poliestireno (Maxisorp, NUNC) con el AcMES78 a una concentración de 5 Fg por mL diluido en una solución tampón de carbonato- -bicarbonato 0,1M; pH 9,6 e incubados durante 16 h a 4 oC. Una vez finalizada la incubación, las placas fueron lavadas 3 veces con solución salina tamponada con fosfato que contenía 0,05 % de Tween 20 (SSTF-T) y se bloquearon los sitios libres de antígeno con leche descremada (Oxoid) al 2,5 % diluida en SSTF-T durante 1 h a 37 oC. Una vez secadas las placas por succión, se añadieron 100 ml de cada suspensión fecal y se incubaron 2 h a temperatura ambiente (TA). Posteriormente, las placas fueron lavadas 6 veces son SSTF-T y se les añadió el conjugado (IgG antiantígenos de ES de F. hepatica conjugado con peroxidasa de rábano) a una dilución de 1:500 en SSTF-T que contenía 10 % de suero de ternera y se incubaron por 1h a TA. Las placas fueron lavadas posteriormente como se describe en el paso anterior y se les añadió la solución de sustrato (20 mL de H2O2 al 30 % + 20 mg de O-fenilendiamina hidroclórica + 50 mL de tampón citrato-fosfato 0,1 M; pH 5,0) e incubadas 30 min a TA en oscuridad. La reacción fue detenida con 50 mL de ácido sulfúrico al 12,5 % y los resultados obtenidos fueron leídos en un lector de microELISA (Organon Technika) a 492 nm. Las concentraciones de antígenos (ng/mL de suspensión fecal) fueron estimadas al comparar los valores de densidad óptica (DO) obtenidos, con una curva estándar generada por la dilución seriada de concentraciones previamente conocidas (desde 5 a 500 ng/mL) de antígenos de ES.4 Los resultados fueron analizados estadísticamente mediante la distribución t de Student de comparación de medias.
Para la detección de coproantígenos por sandwich ELISA se colectó una muestra fecal por separado a 40 ovinos de la raza Pelibuey naturalmente infectados, pertenecientes al Plan Genético "Niña Bonita" y a 100 ovinos de igual raza con repetidos análisis parasitológicos negativos, utilizados como controles, procedentes de los bioterios de diferentes centros de investigación. El ensayo también fue aplicado, para conocer la existencia de reacciones cruzadas, a 88 muestras fecales de ovinos infectados con otras parasitosis: Haemonchus contortus, 33; Tricostrogilídeos, 20; Eimeria sp., 18; Trichuris ovis, 14 y Dicrocoelium dentriticum, 3. El número de huevos por gramo de heces estuvo en el rango de 1 a 198 determinado por la técnica de sedimentación y cuantificación descrita por Dennis y otros.5 La correlación entre el número de huevos y los valores de absorbancia observada con el sandwich ELISA fue estudiada mediante la prueba de correlación de rangos de Spearman.
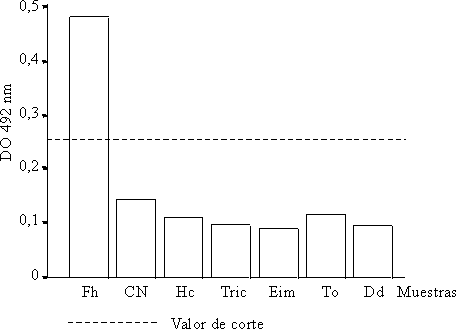
Los valores de absorbancia del grupo control negativo (fig.) oscilaron entre 0,08-0,22 para un valor medio de 0,142 (± 0,04). El valor de corte estimado para este ensayo fue de 0,24 según el criterio de 0,142 + 2 (0,04) ( 12 ng mL-1) por encima del cual se consideró toda muestra estudiada como positiva. Los valores de DO de las muestras de animales con fascioliasis estuvieron en un rango de 0,28-1,15; con un valor medio de 0,46 (±0,22); mientras que los valores de absorbancia de las muestras de animales con otros parásitos estuvieron en el rango de 0,07-0,12 (0,07<DO<0,12) (0,02<DE<0,04). Se obtuvieron diferencias altamente significativas entre los niveles de antígenos detectados en las heces (p<0,001) de los animales con fascioliasis, con respeto a los diferentes grupos estudiados, no se observaron reacciones cruzadas. Para medir las cantidades aproximadas de antígenos de ES en las heces de ovinos con F. hepatica, las densidades ópticas fueron comparadas con la curva patrón. Las muestras fecales de 38 de los 40 animales con fascioliasis tuvieron antígenos detectables en heces en concentraciones superiores a 12 ng/mL. La concentración media de los antígenos en heces fue de 22 ng/mL. La correlación entre el número de huevos por gramo de heces y coproantígenos fue significativa (r=0,24; p<0,005). Al no ser posible realizar el estudio en animales de matadero no pudo correlacionarse el número de parásitos adultos en el hígado con el número de huevos por gramo de heces y la concentración de antígenos, y tampoco determinar el número mínimo de parásitos que excretan antígenos capaces de ser detectados por el ES78-sandwich ELISA. Esto también podría explicar el hecho de que aunque la concentración mínima de antígenos detectada por nuestro método es similar a la detectada en las heces de bovinos, 2 de los ovinos resultaron negativos y ninguno tuvo concentraciones mayores de 50 ng mL-1 de antígenos, mientras que en los bovinos, el 100 % tuvo antígenos detectables en heces, de los cuales el 38 % tuvo concentraciones de antígeno 50 ng/mL. Estudios futuros en ovinos que se infecten experimentalmente permitirán definir esto y, por tanto, el límite de detección del ensayo.
]]> Fig. Especificidad del sandwich ELISA mediante el AcM ES78 para la captura de antígenos en heces de animales infectados con: Fasciola hepatica (Fh), Haemonchus contortus (Hc), Tricostrongilídeos (Tric), Eimeria sp. (Eim), Trichuris ovis (To), Dicrocoelium dendriticum (Dd). Controles negativos (CN).También habrá que tener en cuenta que, debido a la capacidad de absorción de agua que tienen las heces de ovinos, fue necesario diluir las muestras en 7mL de agua a diferencia de las heces de bovinos que fueron diluidas en 2 mL, lo que podría disminuir la sensibilidad del ensayo y las infecciones ligeras ya no ser detectables por el ES78-sandwich ELISA. Por último, los resultados de este trabajo indican que la detección de coproantígenos mediante el sandwich ELISA con la utilización del AcM ES78, al igual que para el ganado bovino, es un método rápido, simple y útil para el diagnóstico de fascioliasis en el ganado ovino.
The diagnosis of ovine fascioliasis hepatica is presented by a sandwich ELISA with the use of monoclonal antibody ES78 previously reported for the diagnosis of bovine fascioliasis. The assay was applied to faeces of 40 sheeps infected with Fasciola hepatica, 88 sheeps with other parasitary infections tested by coproparasitology and 100 caprologically negative animals. Antigens of excretion-secretion of Fasciola hepatica were detected in 38 of the 40 sheeps with fascioliasis and in none of the negative animals or with other parasitosis. The results show that ES78 sandwich ELISA, as in bovines, is fast, simple and useful for the diagnosis of the active infection caused by Fasciola hepatica among ovines.
Subject headings: FASCIOLASIS/diagnosis; FASCIOLASIS/veterinary; FASCIOLIASIS HEPATICA/immunology; ANTIGENS, HELMINTH/analysis; SHEEP/parasitology; ANTIBODIES, MONOCLONAL; FAECES/parasitology; ENZYME-LINKED IMMUNOSORBENT ASSAY/methods.
Dra. Blanca E. Duménigo Ripoll. Instituto de Medicina Tropical" Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba.
1 Médica veterinaria. Investigadora Titular.
2 Doctor en Ciencias Biológicas. Especialista de II Grado en Bioquímica. Investigador Titular. Subdirector de Parasitología.