Instituto de Medicina Tropical "Pedro Kourí"
Lic. Rosabel Falcón Márquez,1 Lic. Gilda Toraño Peraza,2 Lic. Berta Victoria Martínez3 y Lic. Isis Tamargo Martínez4
Se ensayó un novedoso esquema de inmunización dirigido a la elevación de anticuerpos para Haemophilus influenzae tipo b, en el que se combinaron como inmunógenos un antígeno celular inactivado con formaldehído 0,5 %, y un antígeno lipopolisacarídico parcialmente purificado mediante un método de precipitación selectiva con solventes orgánicos. Se obtuvieron anticuerpos de elevada especificidad y actividad biológica con títulos de hasta 1:256 por contrainmunoelectroforesis, que fueron purificados mediante precipitación selectiva con sulfato de amonio y cromatografía de intercambio iónico con la utilización de una columna de DEAE-Sepharose. La metodología propuesta en este trabajo permite la producción de anticuerpos purificados, útiles en la optimización de técnicas de diagnóstico serológicas y de serotipaje de cepas de H. influenzae b.
DeCs: HAEMOPHILUS INFLUENZAE TIPO B; ESQUEMA DE INMUNIZACIÓN; CONTRAINMUNOELECTROFORESIS//métodos; LIPOPOLISACÁRIDOS.
Haemophilus influenzae tipo b (Hib) es el agente causal de 99 % de las infecciones invasivas causadas por su especie.1 Dentro de estas, las meningitis constituyen el mayor problema de salud al ocasionar altas tasas de morbilidad y mortalidad en niños menores de 5 años.2 Diversos componentes celulares, así como sustancias extracelulares, desempeñan un papel importante en la patogenia de Hib. Dentro de estos, el lipopolisacárido (LPS), componente de la membrana externa de las bacterias gramnegativas, es un potente factor de virulencia, cuyo efecto ciliostático favorece la colonización y diseminación de este microorganismo en el tracto respiratorio. El LPS constituye un antígeno timoindependiente pobremente inmunogénico, que contiene en su estructura varios determinantes antigénicos capaces de estimular la producción de anticuerpos bactericidas.3,4
Con el objetivo de contribuir a la optimización de sistemas útiles en el inmunodiagnóstico de Hib, el laboratorio de Infecciones Respiratorias Agudas Bactericidas (IRAB) del Instituto de Medicina Tropical "Pedro Kourí" (IPK) se propuso obtener inmunoglobulinas purificadas a partir de anticuerpos específicos contra el LPS de Hib, mediante un esquema de inmunización totalmente novedoso.
Se utilizaron como inmunógenos un antígeno celular (Agc) y un antígeno lipopolisacarídico (Ag-LPS), producidos a partir de la cepa Hib ATCC 10211. Para la preparación del Agc, la cepa fue cultivada en placas de agar chocolate por 24 h a 37 °C en atmósfera de CO2 5 %, la biomasa obtenida fue resuspendida en solución salina estéril e inactivada con formaldehído 0,5 %, y la concentración celular se ajustó a 1,5 × 109 células/mL. Para la preparación del Ag-LPS la cepa fue cultivada en caldo cerebro-corazón suplementado con 0,2 mg/mL de hemina, NAD y 0,04 g/mL de glucosa. El Ag-LPS fue parcialmente purificado por medio del método fenol-H2O descrito por Westphal y Jann5 y el rendimiento estimado fue de 1,56 mg/mL de polisacárido, con la utilización del método fenol-sulfúrico.6 La concentración de proteínas determinada por el método de Lowry fue de 0,12 mg/mL7 y el contenido de ácidos nucleicos, calculado según Maniati, fue de 87,9 mg/mL.8
Para la obtención de anticuerpos específicos anti-LPS, se ensayó un esquema de inmunización en conejos albinos de 2,5 kg de peso y 3 meses de edad que constó de 2 etapas. Durante la primera, al tomar como referencia otros esquemas de inmunización desarrollados en el laboratorio IRAB del IPK en la producción de anticuerpos específicos para Hib (Tamargo I, observaciones inéditas), se utilizó como inmunógeno el Agc. Este fue administrado por vía endovenosa y en dosis de 0,5; 1; 1,5 y 2 mL, con intervalos entre dosis de 3 d, hasta obtener sueros con títulos mayores o iguales a 1:16 por contrainmunoelectroforesis (CIE). En una segunda etapa del esquema se procedió a la inoculación del Ag-LPS 2 veces por semana, en dosis ascendentes desde 0,1 hasta 1 mL.
]]> Al finalizar la primera etapa del esquema se obtuvo un título de anticuerpos de hasta 1:32 frente al Agc, y en la segunda fase los títulos ascendieron hasta la dilución 1:256 frente al Ag-LPS parcialmente purificado, en la misma medida fue disminuyendo la respuesta de anticuerpos frente al Agc y llegó a desaparecer al concluir las inmunizaciones.Iniciar el esquema de inmunización con el empleo del Agc garantiza una potente proliferación linfocitaria, y la posterior inoculación del antígeno parcialmente purificado estimula una respuesta inmunológica más específica.9,10 Con esta com-binación se logra superar la baja inmunogenicidad que presenta el Ag-LPS.3,4 No se tiene referencia de la utilización de un método de inmunización similar al propuesto por los autores de este estudio.
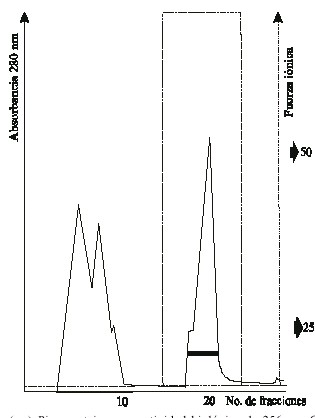
Las inmunoglobulinas G (IgG) anti-LPS de Hib fueron purificadas con la utilización de los métodos de precipitación selectiva con sulfato de amo-nio 50 % y tecnología FPLC mediante una cromatografía de intercambio aniónico en DEAE-Sepharose. La electroforesis en geles de polia-crilamida en presencia de dodecil sulfato de sodio (SDS-PAGE) en condiciones de reducción,11 realizada como criterio de pureza, reveló solo las 2 bandas (25 y 50 kDa) correspondientes a la IgG tratada con b-mercaptoetanol (fig.). Como resultado de la purificación se incrementó en 2 veces el grado de pureza del antisuero anti-LPS, sin grandes pérdidas de la actividad biológica (título 1:64, determinado por CIE).
(- ) Pico proteico con actividad biológica de 256 por CIE. Lateral derecho: Perfil electroforético de los anticuerpos específicos contra Hib obtenidos en SDS-PAGE.
Fig. Perfil de elusión de la IgG anti-LPS de Haemophilus influenzae tipo b en cromatografía de intercambio aniónico DEAE-Sepharose.
Con este trabajo se logró obtener por primera vez en Cuba, a través de un novedoso esquema de inmunización y un proceso de purificación con la utilización de la tecnología FPLC, IgG anti-LPS de Hib, útil como herramienta en la optimización de métodos serológicos para el diagnóstico de Hib, estudios epidemiológicos y de caracterización de cepas.12
A novel immunization schedule was tested to increase antibodies to Haemophilus influenzae type B in which a 0.5 % formaldehyde-inactivated cellular antigen and a partially purified lipopolysacharid antigen obtained from a selective precipitation with organic solvents were combined as immunogens. High specificity and biological activity antibodies with titers up to 1:256 were obtained by counterinmunoelectrophoresis; they were purified through a selective precipitation with ammonium sulphate and an ion-exchange chromatography using a DEAE-Sapharose column. The method proposed in this paper facilitates the production of purified antibodies useful for the improvement of serological diagnosis and H. influenzae b strain serotyping techniques.
Subject headings: HAEMOPHILUS INFLUENZAE TYPE B; IMMUNIZATION SCHEDULE; COUNTERIMMUNO-ELECTROPHORESIS/methods; LIPOPOLYSACCHA-RIDES.X
Recibido: 2 de septiembre de 1999. Aprobado: 2 de octubre del 2000.
Lic. Rosabel Falcón Márquez. Instituto de Medicina Tropical "Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba. Correo electrónico: ciipk@ipk.sld.cu