ARTÍCULO ORIGINAL
Actividad antiplasmodial in vivo de las esponjas Mycale laxissima y Clathria echinata
In vivo antiplasmodial activity of Mycale laxissima and Clathria echinata sponges
]]>
MSc. Judith Mendiola Martínez,I Dr. C. Erik Luis Regalado Veloz,II MSc. Aymé Fernández-Calienes Valdés,I Téc. Deyanira Acuña Rodríguez,I Dr. C. Lázara Rojas Rivero,I MSc. Olga Valdés IglesiasIII Instituto de Medicina Tropical "Pedro Kourí". La Habana, Cuba.
II Centro de Bioactivos Marinos. La Habana, Cuba.
Introducción: la búsqueda de nuevas sustancias antimaláricas incluye entre sus retos el desarrollo de alternativas para el tratamiento de la malaria cerebral, debido a la alta mortalidad y las deficiencias neurológicas persistentes después del tratamiento con los medicamentos recomendados actualmente.
Objetivos: evaluar la actividad de fracciones orgánicas de Mycale laxissima y Clathria echinata en el modelo de malaria cerebral producida por la infección de ratones C57BL/6 con Plasmodium berghei ANKA.
Métodos: se evaluaron fracciones orgánicas obtenidas mediante cromatografía flash en fase inversa a partir de los extractos crudos de las dos especies. Se realizó un análisis químico cualitativo para detectar la presencia de saponinas, triterpenos/esteroides y alcaloides en estas fracciones. El efecto esquizonticida de las fracciones se determinó mediante la prueba de supresión de la parasitemia al inicio de la infección. Se evaluaron la supervivencia, los síntomas neurológicos y la reducción del peso corporal en los días subsiguientes.
Resultados: las fracciones orgánicas de Mycale laxissima a dosis de 200 mg/kg y Clathria echinata a100 mg/kg no mostraron una disminución sustancial del peso de los animales o muertes hasta el día 4; para las cuales se obtuvieron reducciones significativas de las medianas de la parasitemia de 45 % y 53 %, respectivamente. La fracción de Mycale laxissima a 200 mg/kg produjo un incremento significativo en el tiempo de supervivencia hasta 20 d, mientras los animales tratados con Clathria echinata a 100 mg/kg presentaron una mediana de tiempo de supervivencia de 16 d. Ambos incrementos fueron superiores a 7 d. En este período, los animales tratados con las fracciones orgánicas de Clathria echinata y Mycale laxissima no presentaron los síntomas neurológicos observados en los controles. Esta prolongación de la supervivencia fue similar a la observada en presencia de dosis de 7,5 mg/kg de cloroquina.
Conclusiones: las fracciones orgánicas de Mycale laxissima y Clathria echinata mostraron actividades antimaláricas, promisorias en el modelo de infección de ratones C57BL/6 con Plasmodium berghei ANKA, que sugieren el estudio de sus constituyentes químicos activos.
Palabras clave: Plasmodium berghei, malaria cerebral, modelos animales, Mycale, Clathria.
Introduction: the search of new antimalarial compounds comprises, among its challenges, the development of therapeutic alternatives for cerebral malaria; due to the high mortality and neurological deficiencies that persist after treatment with recommended drugs.
Objectives: to evaluate the activity of organic fractions of Mycale laxissima and Clathria echinata in the cerebral malaria model of infection of C57BL/6 mice with Plasmodium berghei ANKA.
Methods: preparative fractions of both species were obtained by reverse-phase flash chromatography. In order to detect the presence of saponins, triterpenods/steroids and alkaloids, a qualitative chemical analysis was performed. The schyzontocidal effect of the extracts was determined by the suppression test at the beginning of the infection. Survival, neurological symptoms and body weight changes were evaluated in subsequent days.
Results: the organic fractions of Mycale laxissima at 200 mg/kg and Clathria echinata at 100 mg/kg showed neither substantial reductions of body weights, nor deaths of animals until day 4; but caused significant reductions of median parasitemia of 45 % and 53 % respectively. The fraction of Mycale laxissima at 200 mg/kg caused a significant increase in the median survival time up to day 20, whereas animals treated with Clathria echinata at 100 mg/kg presented a survival of 16 days. Both increases the survival time 7 days. Neurological alterations were not observed in the groups treated with organic fractions when compared to the control group. This survival extension was similar to the effect of administration of 7.5 mg/kg of chloroquine.
Conclusions: the organic fractions of Mycale laxissima and Clathria echinata exhibited promising antimalarial activities in the infection model of C57BL/6 mice with Plasmodium berghei ANKA. This indicates that their active chemical constituents should be studied.
Key words: Plasmodium berghei, cerebral malaria, animal model, Mycale, Clathria.
]]>
INTRODUCCIÓN
La resistencia actual de Plasmodium falciparum y Plasmodium vivax a los fármacos antimaláricos y de los mosquitos frente a los insecticidas constituyen amenazas importantes para las estrategias de control del paludismo que se han establecido cada vez con mayor éxito en una gran parte de los países endémicos.1 Esto ha motivado el desarrollo de intensos esfuerzos de investigación en la búsqueda de nuevas sustancias antimaláricas o para la modificación de las ya existentes. El tratamiento de la malaria cerebral, una de las más importantes complicaciones de la malaria severa producida por P. falciparum, representa un reto porque produce alta mortalidad, así como deficiencias neurológicas persistentes después del tratamiento con los medicamentos recomendados.2 Aislamientos parasitarios de la zona de Cambodia-Tailandia presentan una reducción de la susceptibilidad frente a los derivados de artemisinina, lo que pudiera comprometer su eficacia para el tratamiento de esta infección.1
En el tratamiento de la malaria cerebral se aplican combinaciones de algunos fármacos convencionales con otros tratamientos terapéuticos3 y diversas formas de inmunomodulación o neuroprotección han sido propuestas como tentativas experimentales.4 Este enfoque se basa en las evidencias de que la malaria cerebral es un proceso inmunopatológico,5 por lo que requiere el análisis de la interacción hospedero-parásito, junto con la inhibición de dianas en el parásito para la exploración de nuevas alternativas terapéuticas.
Las investigaciones acerca de intervenciones terapéuticas para la malaria cerebral se realizan, principalmente, en modelos murinos de infección con Plasmodium berghei ANKA. Estos facilitan la identificación de compuestos antimaláricos efectivos y de posibles sustancias inmunomoduladoras, que además pueden sugerir importantes vías relacionadas con la patogenia.5 Los experimentos in vivo también permiten determinar cuáles productos naturales pueden ser convertidos metabólicamente en sustancias bioactivas.6
Estudios previos identificaron a fracciones orgánicas de las esponjas Mycale laxissima y Clathria echinata, con actividad inhibidora sobre el crecimiento in vitro de P. berghei en el rango entre 10 y 50 µg/mL, con niveles de selectividad de 9,45 y 4,24, respectivamente. El análisis químico cualitativo realizado resultó en la determinación de glicósidos esteroidales entre los componentes detectables de M. laxissima, así como de alcaloides y triterpenos/esteroides para C. echinata.7 Algunas saponinas extraídas de plantas presentan una gran potencialidad para el tratamiento de enfermedades cerebrales,8 por sus propiedades antioxidantes, antiinflamatorias, anti-apoptosis e inmunomoduladoras.9 Los glicósidos esteroidales de organismos marinos presentan una variedad de estructuras diferentes a los terrestres y aunque no han sido investigados de modo adecuado en varios aspectos, atraen la atención por su capacidad de unirse a algunos receptores.10 Resultados anteriores informan la actividad antimalárica in vitro de alcaloides de guanidina aislados de C. calla.11 Estas sustancias, además, presentan un amplio perfil de bioactividad, sobre todo como inhibidores enzimáticos.12 Estas evidencias sugieren evaluar la actividad de fracciones orgánicas de M. laxissima y C. echinata en modelos murinos de malaria cerebral.
Este estudio tuvo como objetivo determinar el efecto in vivo de fracciones orgánicas de M. laxissima y C. echinata sobre la reducción inicial de la parasitemia y en la supervivencia de ratones de la cepa C57BL/6 infectados con P. berghei ANKA.
]]>
MÉTODOS
Extracción y separación del material biológico
Los ejemplares de las esponjas M. laxissima Duchassaing & Michelotti, 1864, familia Mycalidae y C. echinata Alcolado, 1984, familia Microcionidae, se colectaron a una profundidad entre 10 y 25 m en Boca de Calderas, La Habana (23º 05' 55" N 82º 28' 30" W) en marzo de 2008; se identificaron por el doctor Pedro M. Alcolado (Instituto de Oceanología, La Habana, Cuba). Los ejemplares de referencia se encuentran ubicados en la colección del Acuario Nacional de Cuba y se clasificaron con los números de catálogo IdO 192 para M. laxissima e IdO 602 para C. echinata. Las esponjas se lavaron con agua de mar en el laboratorio para eliminar los organismos asociados en su superficie y después se conservaron en congelación hasta el proceso de extracción. Cada ejemplar se liofilizó y pulverizó para obtener 50 g de material seco, el cual se extrajo en baño ultrasónico con una mezcla de MeOH/CH2Cl2 (1:1). A continuación, los extractos crudos fueron fraccionados mediante cromatografía flash en fase inversa (RP-C18) según la metodología previamente descrita,13 en la cual se procedió a colectar la elución correspondiente a la aplicación de diclorometano/metanol 1:1 como fracción orgánica y los productos de la elución con agua se eliminaron. Las fracciones orgánicas obtenidas se evaluaron mediante un análisis químico cualitativo según Harborne,14 para detectar la presencia de saponinas, triterpenos/esteroides y alcaloides en estas fracciones; a continuación se determinó su actividad antimalárica in vivo.
Actividad antimalárica in vivo
Los parásitos de la cepa ANKA de Plasmodium berghei provinieron del Laboratorio de Microbiología, Parasitología e Higiene de la Universidad de Amberes, Bélgica. Los experimentos se realizaron con ratones hembras de la cepa C57BL/6 Cenp (peso promedio 16,55 ± 1,424 g) procedentes del Centro Nacional de Producción Animales de Laboratorio (CENPALAB), con edad de 6 a 8 semanas, las cuales se mantuvieron en condiciones de luz y humedad requeridas y acceso libre a los alimentos y agua. Se cumplieron las normas internacionales para el cuidado de los animales en la experimentación biomédica y el proyecto general se aprobó por el Comité de ética del Instituto "Pedro Kourí". El efecto esquizonticida de las fracciones se determinó mediante la prueba de supresión de la parasitemia de Peters y otros.15 Grupos de 5 animales se infectaron por la vía intraperitoneal con 1- 2 x 105 eritrocitos parasitados de un donante homólogo, en el día 0. La actividad de las fracciones orgánicas se estudió inicialmente a dosis de 50, 100 y 200 mg/kg según valores descriptivos internacionales;16 por los resultados de baja toxicidad y mayor reducción de la parasitemia se seleccionaron para el estudio las dosis de 100 mg/kg para C. echinata y 200 mg/kg para M. laxissima, las cuales se administraron los días 0 (4 h después de la infección), 1, 2 y 3, por la vía intraperitoneal, en un volumen de 0,2 mL. Las fracciones se disolvieron en solución de dimetilsulfóxido (DMSO) 10 % diluido en cloruro de sodio 0,9 % estéril. El grupo control negativo recibió el mismo volumen de vehículo. El grupo control positivo se trató con 7,5 mg/kg de cloroquina (Sigma, EE: UU:) disuelta en solución estéril de cloruro de sodio 0,9 %. Cambios en el peso corporal y la eficacia en la reducción de la parasitemia se determinaron el día 4 posterior a la infección en todos los grupos de estudio. La parasitemia se evaluó en extensiones finas de 2 µL de sangre tomada de la cola, que se colorearon con Giemsa y se examinaron con microscopio óptico para realizar el conteo de parásitos en un total aproximado de 3 000 eritrocitos. Los experimentos se repitieron tres veces. ]]>
La evaluación de la supervivencia se realizó desde el inicio de los experimentos y a continuación en los días 6 al 10 posteriores a la infección, en los cuales aparece la severidad de la malaria y la muerte. Estas características están bien establecidas para el modelo de infección C57BL/6-P. berghei ANKA y se describen como principales síntomas neurológicos a evaluar la ataxia, parálisis límbica, respiración anormal, posición anormal del cuerpo, locomoción disminuida y convulsiones. Debido a que la administración de DMSO se ha reportado antes que reduce de manera parcial la aparición de malaria cerebral en los animales,17 se incluyó un estudio de las características típicas mostradas por animales no tratados. Los animales que presentaron algún síntoma neurológico, con una reducción rápida de su peso corporal y con una parasitemia menor que 25 %, se consideró que presentaron malaria cerebral18 y se sacrificaron. Este día fue considerado como día de la muerte, porque el progreso rápido a enfermedad terminal es característico de este modelo.
Análisis estadístico
Se calcularon medianas para los valores de parasitemia y pesos corporales que se compararon mediante la prueba U de Mann-Whitney. Los datos de supervivencia se presentaron como curvas de Kaplan-Meier y se analizaron mediante la prueba de Gehan-Breslow-Wilcoxon. Valores de p menores que 0,05 se consideraron como significativos. Se utilizó el programa estadístico Graph Pad Prism 5.00.
RESULTADOS
Los efectos de la administración de ambas fracciones hasta el día 4 posterior a la infección se muestran en las figuras 1 y 2. ]]>
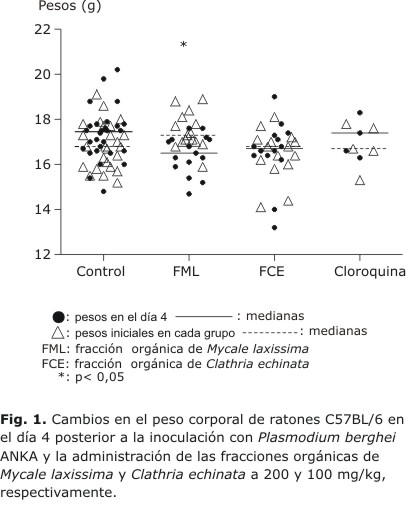
La fracción orgánica de Mycale laxissima a 200 mg/kg produjo una diferencia significativa (p< 0,05) en el peso corporal inicial de los animales (n= 15) equivalente a 4,62 % (Fig. 1), sin muertes registradas en el día 4. La fracción orgánica de C. echinata no causó disminución significativa del peso de los animales (n= 15; Fig. 1) o muertes. El grupo de animales que recibieron la fracción orgánica de M. laxissima (n= 10) a 200 mg/kg presentó una disminución significativa de la parasitemia (p< 0,001) en comparación con el grupo control de su serie experimental (n= 16) y se determinó un descenso de 45 %. La administración de la fracción orgánica de C. echinata a 100 mg/kg mostró medianas significativamente diferentes de la parasitemia en los animales (n= 9) (p< 0,01), comparadas a su grupo control b (n= 10), con reducción equivalente a 53 %. No se observaron parásitos en el día 4 para el grupo que recibió cloroquina a 7,5 mg/kg (n= 11) (Fig. 2).
Las observaciones posteriores al día 4, mostraron los efectos de la administración de las fracciones de las esponjas, el vehículo utilizado y el fármaco de referencia al inicio de la infección sobre el período crítico del día 6 al 10. Los ratones infectados y que no se les administró ninguna sustancia desarrollaron un incremento de la parasitemia de un valor de mediana igual a 0,773 % (0,422/2,17 %) (25/75 percentiles) en el día 4, a 11,92 % (5,77/26,51 %) en el día 7. Se observó una disminución del peso inicial de los animales de un valor de mediana igual a 17,35 g (15,88/18,3 g) a 14,15 g (12,88/16,6 g), estimada en 18,4 %. La mediana del tiempo de supervivencia resultó de 8 d y la mortalidad para el período crítico de 75 %, sin diferencias significativas del tiempo de supervivencia registrado de 9 d y la mortalidad de 72,5 % para el grupo de animales que recibieron el vehículo (Fig. 3). Se observó que estos animales presentaron en su mayoría síntomas neurológicos como ataxia, parálisis límbica, posición anormal del cuerpo y dificultad respiratoria. La observación de convulsiones fue menos frecuente. Estos cambios se presentaron con una reducción rápida de su peso corporal y una parasitemia menor que 25 %, por lo que se consideró que los animales en su mayoría mostraron malaria cerebral. Algunos animales presentaron características de enfermedad terminal, sobre todo la limitación de su movimiento, unida a la pérdida de peso significativa aun con parasitemias menores que 25 %, pero no pudieron detectarse los principales síntomas neurológicos. La cloroquina a 7,5 mg/kg produjo una prolongación significativa de la supervivencia con mediana de 24 d (p< 0,01) (Fig. 3).
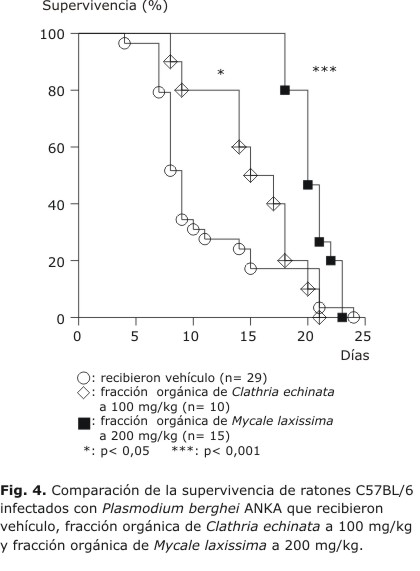
La administración de la fracción de M. laxissima a 200 mg/kg produjo un incremento significativo en el tiempo de supervivencia hasta 20 d comparada a los controles que solo recibieron el vehículo (p< 0,001); mientras los animales tratados con C. echinata a 100 mg/kg presentaron una mediana de tiempo de supervivencia de 16 d, también significativamente diferente al grupo control (p< 0,05) (Fig. 4). Estos efectos fueron similares a los observados en presencia de dosis de 7,5 mg/kg de cloroquina. Los tratamientos aplicados no lograron la cura de los animales, inclusive se manifestó recrudescencia en el grupo tratado con cloroquina desde el día 10. Los animales tratados con las fracciones orgánicas y cloroquina rebasaron el período crítico, no presentaron alteraciones neurológicas, pero posteriormente mostraron hiperparasitemia y anemia severa.
]]>
El análisis cualitativo resultó positivo para la detección de saponinas en la fracción orgánica de M. laxissima y para alcaloides y triterpenos/esteroides en la fracción orgánica de C. echinata.
DISCUSIÓN
La actividad antimalárica mostrada por las fracciones orgánicas de C. echinata y M. laxissima en el modelo de infección de ratones C57BL/6 con P. berghei ANKA, alcanza valores de dosis efectivas comparables a los recomendados para la continuidad del estudio de extractos de plantas,6 así como para compuestos purificados o sintéticos;16 esta reducción de la parasitemia se produjo sin variaciones sustanciales del peso de los animales y muertes. Es también un resultado importante de la bioactividad de estas fracciones, la prolongación del tiempo de supervivencia, similar a la observada en presencia de dosis de 7,5 mg/kg de cloroquina, con una diferencia mayor de 7 d16 cuando se comparó con la mediana de los controles. En este período, los animales tratados con las fracciones orgánicas de C. echinata y M. laxissima no presentaron los síntomas neurológicos observados en los controles. Estos efectos se obtuvieron a dosis superiores a la cloroquina, pero las fracciones orgánicas de ambas esponjas son muestras complejas, en las que los posibles principios activos pueden encontrarse en menor concentración.
Estos resultados son consistentes con investigaciones previas que señalan la importancia del desarrollo de la parasitemia en el progreso de la enfermedad.17,19 En el presente estudio se observó un efecto de reducción de la parasitemia al inicio de la infección (día 4), que sugiere un retraso temporal en el incremento de la parasitemia. Mc Quillan y otros20 han planteado como hipótesis para este modelo, que el momento de arranque en el crecimiento del parásito debe coincidir con determinada activación inmune, para que se desarrolle la malaria cerebral. Con vistas a explicar los fundamentos de los efectos observados en ambas fracciones, será necesario separar sus componentes activos y estudiar sus efectos sobre los perfiles de células inmunes y citoquinas en tejidos relacionados con la malaria severa en este modelo, así como evaluar la acción de estos productos mediante estudios histopatológicos.
La actividad antimalárica presentada por las fracciones orgánicas de C. echinata y M. laxissima en el modelo de infección de ratones C57BL/6 con P. berghei ANKA que se caracteriza por producir malaria severa, afectar fundamentalmente el cerebro y producir la muerte entre 50 y 100 % de los animales infectados,19 no ha sido descrita con anterioridad. El análisis cualitativo resultó positivo para la detección de saponinas en la fracción orgánica de M. laxissima, y de alcaloides y triterpenos/esteroides en la fracción orgánica de C. echinata. De M. laxissima han sido aisladas 11 saponinas esteroidales llamadas mycalósidos A-K, pero la información sobre su bioactividad es escasa.10 La actividad biológica de saponinas de origen marino ha sido poco estudiada, cuyas estructuras presentan diferencias significativas con las aisladas de plantas,10 en las que se pueden encontrar reportes de actividad antimalárica in vivo,21 pero aún se desconocen sus mecanismos de acción. Los alcaloides del género Clathria fueron solo evaluados in vitro en experimentos previos.11 Los resultados de este trabajo refuerzan el interés en investigar las potencialidades antimaláricas de estos compuestos y sus posibles derivados.
En resumen, consideramos que las fracciones orgánicas de M. laxissima y C. echinata mostraron actividades antimaláricas promisorias en el modelo de infección de ratones C57BL/6 con P. berghei ANKA, que sugieren el estudio de sus constituyentes químicos activos. ]]>
REFERENCIAS BIBLIOGRÁFICAS
1. World Health Organization. Global report on antimalarial drug efficacy and drug resistance: 2000-2010. Geneva: WHO Press; 2010.
2. Dondorp AM, Fanello CI, Hendriksen IC, Gomes E, Seni A, Chhaganlal KD, et al. Artesunate versus quinine in the treatment of severe falciparum malaria in African children (AQUAMAT): an open-label, randomised trial. Lancet. 2010;376(9753):1647-57.
3. World Health Organization. Guidelines for the treatment of malaria. Geneva: WHO Press; 2006. ]]>
4. White NJ, Turner GDH, Medana IM, Dondorp AM, Day NPJ. The murine cerebral malaria phenomenon. Trends Parasitol. 2009;26(1):11-5.
5. De Souza JB, Hafalla JCR, Riley EM, Couper KN. Cerebral malaria: why experimental murine models are required to understand the pathogenesis of disease. Parasitology. 2010;137(5):75572.
6. Wells TC. Natural products as starting points for future anti-malarial therapies: going back to our roots? Malar J. 2011;10(Suppl 1):S3.
7. Mendiola BJ, Regalado EL, Laguna A, Valdes O, Fernandez-Calienes A, Acuña D, et al. In vitro and in vivo inhibitory activities against Plasmodium berghei of Cuban marine sponges extracts. Vaccimonitor. 2010;19(Suppl 2):227.
8. Radad K, Moldzio R, Rausch WD. Ginsenosides and their CNS targets.CNS Neurosci Ther. 2011;17(6):761-8. ]]>
9. Yuan CS, Wang CZ, Wicks SM, Qi LW. Chemical and pharmacological studies of saponins with a focus on American ginseng. J Ginseng Res. 2010;34(3):160-7.
10. Ivanchina NV, Kicha AA, Stonik VA. Steroid glycosides from marine organisms. Steroids. 2011;76(5):425-54.
11. Laville R,Thomas OP, Berrue F, Marquez D, Vacelet J, Amade P. Bioactive guanidine alkaloids from two caribbean marine sponges. J Nat Prod. 2009;72(9):1589-94.
12. Berlinck RG, Burtoloso AC, Kossuga MH. The chemistry and biology of organic guanidine derivatives. Nat Prod Rep. 2008;25(5):919-54.
13. Regalado E, Laguna A, Mendiola J, Thomas O, Nogueiras C. Bromopyrrole alkaloids from the Caribbean sponge Agelas cerebrum. Quim Nova. 2011;34(2):289-91. ]]>
14. Harborne JB. Phytochemical methods. London: Chapman and Hall, Ltd; 1973.
15. Peters W, Portus JH, Robinson BL.The chemotherapy of rodent malaria. XXII. The value of drug-resistant strains of Plasmodium berghei in screening for blood schizontocidal activity. Ann Trop Med Parasitol. 1975;69(2):155-71.
16. Nwaka S, Ramirez B, Brun R, Maes L, Douglas F, Ridley R. Advancing drug innovation for neglected diseases-criteria for lead progression. PLoS Negl Trop Dis. 2009;3(8):e440.
17. Waknine-Grinberg JH, Hunt N, Bentura-Marciano A, McQuillan JA, Chan HW, Chan WC, et al. Artemisone effective against murine cerebral malaria. Malar J. 2010;9:227-41.
18. Dai M, Reznik SE, Spray DC, Weiss LM, Tanowitz HB, Gulinello M, et al. Persistent cognitive and motor deficits after successful antimalarial treatment in murine cerebral malaria. Microbes Infect. 2010;12(14-15):1198-207. ]]>
19. Martins YC, Werneck GL, Carvalho LJ, Silva BP, Andrade BG, Souza TM, et al. Algorithms to predict cerebral malaria in murine models using the SHIRPA protocol. Malar J. 2010;9:85-97.
20. Mc Quillan JA, Mitchell AJ, Ho YF, Combes V, Ball HJ, Golenser J, et al. Coincident parasite and CD8 T cell sequestration is required for development of experimental cerebral malaria. Int J Parasitol. 2011;41(2):155-63.
21. Han H, Chen Y, Bi H, Yu L, Sun C, Li S, et al. In vivo antimalarial activity of ginseng extracts. Pharm Biol. 2011;49(3):283-9.
Recibido: 3 de mayo de 2012. ]]> Aprobado. 28 de junio de 2012.
Judith Mendiola Martínez. Laboratorio de Malaria Experimental, Departamento de Parasitología. Instituto de Medicina Tropical "Pedro Kourí". Autopista Novia del Mediodía Km 6 ½. AP 601. Lisa, La Habana, Cuba. Correo electrónico: mendiola@ipk.sld.cu ]]>