ARTÍCULO DE INVESTIGACIÓN
Detección de anticuerpos IgG contra el ADN de doble cadena mediante ELISA utilizando como recubrimiento ADN xenógeno, alógeno y autólogo
]]>
Detection of IgG antibodies to ELISA-double-chain DNA using xenogenous, allogenic and autologous
Gipsis Suárez RománI; Antonio Mario González GriegoII; Tammy Fernández RomeroI; Mónica Romero SáezIII
I Doctora en Medicina. Especialista de I Grado en Bioquímica clínica. Instructor. Departamento de Bioquímica. Instituto de Ciencias Básicas y Preclínicas "Victoria de Girón".
IIDoctor en Medicina. Doctor en Ciencias Médicas. Especialista de II Grado en Inmunología. Profesor Académico y Titular. Departamento de Inmunología. Centro Nacional de Genética Médica. ]]>
IIIDoctora en Medicina. Especialista de I Grado en Inmunología. Asistente. Departamento de Inmunología. Centro Nacional de Genética Médica.
RESUMEN
]]>
El ADN xenógeno empleado como recubrimiento de un enzimoinmunoensayo indirecto, para la detección de anticuerpos IgG contra el ADN de doble cadena es de difícil obtención y muy costoso.
Palabras clave: Anti-ADNdc(doble cadena), ELISA (prueba de inmunoadsorción ligada a enzima), LES (lupus eritematoso sistémico).
ABSTRACT
Xenogenous DNA used as coating of an indirect enzyme-immunoassay for detection of IgG to double-chain DNA is very difficult to obtain and it is very expensive. ]]>
OBJECTIVE: To assess usefulness of allogenic and autologous DNA coating antigen to determine these antibodies.
Key words: anti-DNAdch (double chain),ELISA (enzyme-linked immunosorbant assay), SLE (systemic lupus erythematosus).
]]>
INTRODUCCIÓN
Los anticuerpos contra el ADN de doble cadena tipo IgG (IgG anti-ADNdc) constituyen marcadores de actividad del Lupus Eritematoso Sistémico (LES), una enfermedad autoinmune sistémica. 1 Para la detección de dichos anticuerpos mediante ELISA, se emplean como antígenos diferentes ADN xenógenos.2-4 También se ha utilizado ADN humano (alógeno), o sea, ADN de individuos de la misma especie.3,5 Para efectuar el diagnóstico del LES, basándose en el concepto de autoinmunidad propiamente dicho, este trabajo persigue el objetivo de evaluar la utilidad del ADN humano tanto alógeno (de la misma especie) como autólogo (ADN de los individuos enfermos) también recubrimiento del enzimoinmunoensayo para la determinación de IgG anti-ADNdc.
MÉTODOS
Muestras: se recogió suero de 4 pacientes con diagnóstico de LES, según criterios de la Asociación Americana de Reumatología modificados en 1982 y revisados en 1997. Se obtuvo sangre total fresca de 2 individuos supuestamente sanos y de los 4 enfermos lúpicos, destinados a la obtención del antígeno. Se empleó suero de personas supuestamente sanas utilizado como control negativo en los ensayos, procedente del banco de sangre ubicado en el municipio Marianao. Se utilizó suero de individuos enfermos con más de 100 DS o unidades de positividad como control positivo.
Obtención del antígeno: extracción de ADN genómico humano alógeno y autólogo. 5
Determinación de IgG anti-ADNdc mediante ELISA indirecto. 5 ]]>
En cada placa de microtitulación se corrió un control negativo, un control positivo y cuatro muestras. Cada placa se consideró un ensayo. Se efectuaron dos ensayos. En el primer ensayo se utilizó un ADN alógeno diferente al empleado en el segundo. Estos antígenos habían sido usados en un estudio anterior. 5Estudios de precisión: repetibilidad, intraensayo e interensayos.
Se montaron 2 réplicas de los controles positivo y negativo y 4 réplicas de las muestras para evaluar repetibilidad intraensayos. El ensayo 1 se repitió dos veces, en días diferentes, pero manteniendo las mismas condiciones para evaluar la reproducibilidad del mismo.
Análisis de los resultados
Se calculó la capacidad de discriminación (K) para cada antígeno y los coeficientes de variación (CV) según los métodos estándares. La cuantificación de anticuerpos IgG anti-ADNdc (CA) se determinó mediante la aplicación de la siguiente fórmula: 5
CA=Xm - Xc- / DSc-
Xm ? Densidad óptica media de la muestra.
Xc-? Densidad óptica media del control negativo.
DSc-? Desviación estándar del control negativo.
]]>
RESULTADOS
Los criterios con los que se trabajó para un 99,9 % de confianza fueron los siguientes: se tomó como valor negativo de referencia cuando CA=3 DS (unidades de positividad). Se consideró ideal si K=10, aceptable si 5=K<10 y desfavorable si K<5. La obtención de un CVK =10% indicaría la no existencia de diferencias notables en los resultados, un 10 %<CVK=20 % significaría la existencia de diferencias poco notables en los resultados y si CVK>20 % implicaría la existencia de diferencias notables. Se tomó un CV intraensayo e interensayo como ideal si CV=10 %, aceptable si 10 %<CV=20 % y desfavorable si CV>20 %.
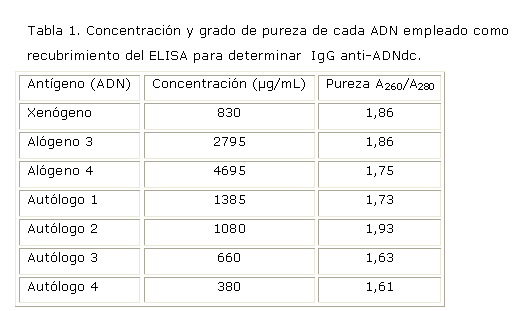
El grado de pureza de los tres tipos de ADN empleados en el estudio se encontró dentro del rango aceptado como ideal (1.6-2.0). Esto indica que el ADN no estaba contaminado con proteínas (Tabla 1).
Se analizó el suero de 4 pacientes con LES. Hubo un 100 % de concordancia en cuanto a los resultados cualitativos obtenidos con los diferentes antígenos empleados. Los cuatro pacientes resultaron negativos con la utilización del ADN xenógeno, del ADN alógeno y del ADN autólogo (Tablas 2 y 3).
Las K con el empleo de los diferentes antígenos (ADN xenógeno, ADN alógeno y ADN autólogo) resultaron aceptables. En el ensayo 1 con el ADN xenógeno fue de 6,1, con el ADN alógeno 4 de 6,0 y con los ADN autólogos 1, 2, 3 y 4 de 6,2, 6,3, 6,0 y 6,3 respectivamente. En el segundo ensayo la K del método con la utilización del ADN de timo de ternera y con el ADN alógeno 3 fue de 6,9. Con el empleo de los ADN autólogos 1 y 2 se obtuvieron los valores de 6,6 y 7,5 respectivamente.
El coeficiente de variación entre las capacidades de discriminación (CVK) con el empleo de cada antígeno se mantuvo por debajo del 10 % en ambos ensayos.
Los coeficientes de variación de los controles negativos y de las muestras, en su mayoría, estuvieron por debajo del 10 %. Solo una pequeña parte estuvo comprendida en el rango aceptable (Tablas 4 y 5).
]]>
DISCUSIÓN
Como país en vías de desarrollo, necesitamos disponer de antígenos menos costosos y fáciles de obtener, que puedan ser empleados como recubrimiento en los enzimoinmunoensayos de nuestros laboratorios clínicos y de investigación. Estos antígenos deben contribuir a incrementar la capacidad de discriminación, la sensibilidad y especificidad del método. Por esta razón en este estudio se evaluó la utilidad del empleo de ADN xenógeno (timo de ternera) y ADN genómico humano (alógeno y autólogo) como recubrimiento del ELISA para detectar anticuerpos anti-ADNdc en el diagnóstico del LES.
Janyapoon y otros reportaron que el ELISA utilizando ADN genómico humano (alógeno) fue de mejor sensibilidad y especificidad que el ELISA que empleaba ADN genómico bacteriano (xenógeno). 3 Wigand y otros reportaron que el ELISA con ADN recombinante humano logró ser más específico que los ELISA que usaban ADN plasmídico y ADN de huevos de salmón como recubrimiento. 4
En un trabajo anterior, en el que se empleó ADN de timo de ternera y ADN alógeno se obtuvo una capacidad de discriminación del método aceptable con ambos antígenos. Además no hubo diferencias notables en cuanto a la K con el uso de los dos tipos de ADN. 5
]]>
En nuestro estudio sólo se determinaron anticuerpos anti-ADNdc de tipo IgG ya que son más específicos para el LES que los de tipo IgM. 1 Se obtuvo un 100 % de coincidencia en cuanto a los resultados con el empleo de los tres tipos de ADN, lo cual indica que cualquiera de ellos puede emplearse como recubrimiento en el método ELISA. Esto avala lo reportado en la literatura acerca de que los anticuerpos anti-ADNdc reaccionan contra epítopes conformacionales del eje pentosa-fosfato que es común a todos los ADN. 1
Los 4 pacientes a los que se les extrajo su ADN tuvieron resultados negativos, a pesar de que presentaban síntomas de actividad de la enfermedad. Estos individuos no eran pacientes de debut (no era objetivo de este estudio evaluar la sensibilidad y especificidad del método) y todos estaban con tratamiento con esteroides. En la literatura se reporta que la terapéutica negativiza a los anticuerpos anti-ADNdc. 6
La K obtenida con cada tipo de antígeno en los dos ensayos llevados a cabo fue aceptable. En esto influye si se utilizan sustancias antes del recubrimiento, si los reactivos están en buen estado, la pureza del antígeno y su grado de polimerización, si el antígeno es modificado, la calidad de las soluciones empleadas, etc. 7-10
En el ELISA que se realiza en este laboratorio no se emplea ninguna sustancia pre-recubrimiento como sulfato de protamina, polihitidina o polilisina, etc, que pueden conllevar a la aparición de falsos positivos. 7-9 Además el ADN se utiliza en su forma intacta, o sea, no es fragmentado. Cuando el antígeno es fragmentado se pueden producir reacciones no específicas con dichos fragmentos que conducen a resultados falsos positivos. 7, 10
Las soluciones reguladoras o amortiguadoras usadas fueron preparadas y almacenadas cuidadosamente para evitar su contaminación bacteriana, ya que las que contienen fosfato y Tris constituyen un medio excelente para saprófitos, bacterias, etc. No se adicionaron a las soluciones amortiguadoras ningún agente antimicrobiano como azida o mercurio, pues los mismos tienen un efecto devastador sobre la actividad enzimática en sistemas, que como este, usan peroxidasa. Ninguno de los reactivos utilizados sobrepasaba la fecha de vencimiento. 7- 9
Tanto el ADN xenógeno (de timo de ternera) como el ADN genómico humano alógeno y autólogo poseían grados de pureza adecuados. A mayor grado de pureza mayor cantidad de ADN se adhiere al pocillo, el riesgo de interferencias disminuye y se produce una mejor señal. 7 Ello contribuye a lograr una buena capacidad de discriminación del método. Precisamente, la utilización de un antígeno altamente purificado constituye uno de los requisitos que debe tenerse en cuenta a la hora de realizar un enzimoinmunoensayo. 7 ]]>
El ADN de timo de ternera presentó un grado de pureza (1,86) igual al del ADN alógeno 3. Basado en lo expuesto en el párrafo anterior se explica que ambos ADN presentaran la misma K (6,1). En ambos ensayos con el empleo del ADN autólogo 2, que tenía mejor grado de pureza que el ADN de timo de ternera, se logró mayor K del método con respecto al ADN xenógeno.
A pesar de que el ADN xenógeno presentó un grado de pureza mayor al del ADN alógeno 4, la K con ambos antígenos resultó muy similar (6,1 y 6,0 respectivamente). Se obtuvieron valores de K con los ADN autólogos 1, 3 y 4 muy próximos e inclusive mayores que con el ADN xenógeno, a pesar de que el grado de pureza de los primeros era inferior al del ADN xenógeno. Estos hallazgos están relacionados con el hecho de que se gana en especificidad con el uso del ADN de la misma especie y del propio paciente.
Si importante es la relación entre el grado de pureza del antígeno y la capacidad de discriminación del método, también el grado de polimerización del antígeno influye notablemente sobre la K. A mayor grado de polimerización se incrementa la posibilidad de que no se pierdan los epítopes conformacionales contra los que se supone reaccionan los anti-ADNdc. 7 Se conoce que el ADN de timo de ternera posee un elevado grado de polimerización (según Directorio Linscott de reactivos inmunológicos y biológicos), el cual no fue determinado en los ADN alógenos y autólogos usados.
A pesar de estas diferencias los coeficientes de variación entre la capacidad de discriminación del método con los antígenos empleados en cada ensayo demostraron que estas no son importantes. Por tal motivo se concluye que el ADN genómico humano tanto alógeno como autólogo es tan útil como antígeno en este método ELISA como el ADN xenógeno. Se hace necesario ampliar esta investigación sobre la base de evaluar otras variables como la especificidad y la sensibilidad clínicas.
]]>
REFERENCIAS BIBLIOGRÁFICAS
1. Hahn BH. Antibodies to DNA. N Engl J of Med. 1998;338(19):1359-68.
2. Gonzalez C, Guevara P, Garcia-Berrocal B, Navajo J, Gonzalez-Buitrago J. Clinical evaluation of cobas core anti-dsDNA EIA quant. J Clin Lab Anal. 2004;18(3):200-5.
3. Janyapoon K, Jivakanont P, Surbrsing R, Siriprapapan W, Tachawuttiwat T, Korbsrisate S. Detection of anti-dsDNA by ELISA using different sources of antigen. Pathology. 2005 Feb;37(1):63-8.
4. Wigand R, Gottschalk R, Falkenbach A, Matthias T, Kaltwasser JP, Hoelzer D. Detection of dsDNA antibodies in diagnosis of systemic lupus erythematosus—comparative studies of diagnostic effectiveness of 3 ELISA methods with different antigens and a Crithidia luciliae immunofluorescence test. Z Rheumatol. 1997;56(2):53-62.
5. Suárez G, González A, Romero T, González VE. Determinación de anticuerpos IgG contra el ADN de doble cadena mediante ELISA utilizando como recubrimiento ADN xenógeno y alógeno. Rev Cubana Invest Biomed. 2007;26(4).
6. Brounwald E, Hauser Stephin L, Fauli Anthony S, Kasper Dennis L, Longo Dan L, Jameson J, editores. Harrison. Principios de Medicina Interna. Vol II. 15th ed. New York: Mc Graw Hill; 2001.
7. Rose NR, Hamilton RG, Detrick, editors. Manual of Clinical Laboratory Immunology. 6th ed. Washington: Editorial ASM Press; 2002.
8. Kroubouzos G, Tosca A, Konstadoulakis M, Varelzidis A. Poly-L-lysine causes false results in ELISA methods detecting anti-dsDNA antibodies. J Immunol Methods. 1992;148:261-3.
9. Janyapoon K, Siriprapapun W, Techawuttiwat T, Jivaganon P. Evaluation of optimal conditions for dsDNA coating on microtiter plates for anti-dsDNA detection by ELISA. Bull Health Sci Tech. 2003;6:31-8.
]]>
10. Pitsetsky D, González T. The influence of DNA size on the binding of antibodies to DNA in the sera of normal human subjets and patient with systemic lupus erythematosus (SLE). Clin Exp Immunol. 1999;116:334-9.
Recibido: 20 febrero de 2008.
Aprobado: 10 de junio de 2008.
]]>
Dra. Gipsis Suárez Román. Instituto de Ciencias Básicas y Preclínicas "Victoria de Girón". Calle 146 No. 3102 esquina ave. 31. Cubanacán, Playa. Ciudad de la Habana. Teléfono: 208- 48- 77. E-mail: gipsis@giron.sld.cu
]]>
]]>