5cm, eritema, rinitis y la asociación de rinitis y asma, estos predominaron en el grupo etáreo de cinco a nueve años, sexo femenino, vía subcutánea, con la mezcla de Dermatophagoides pteronyssinus y Blomia tropicalis (VALERGEN DP + VALERGEN BT) y con concentración de 20 000 UB/ml. Conclusiones: la inmunoterapia con vacunas VALERGEN propicia una evolución clínica favorable en la mayoría de los pacientes, con un bajo índice de eventos adversos, lo que confirma su efectividad y seguridad en el tratamiento del asma.]]>
5cm, erythema, rhinitis and the rhinitis association and asthma, these prevailed in the ages from 5 to 9 years, feminine sex, subcutaneous route, with the mixture of Dermatophagoides pteronyssinus and Blomia tropicalis (VALERGEN DP + VALERGEN BT) and with concentration of 20 000 UB/ml. Conclusion: immunotherapy with VALERGEN vaccines provides a positive clinical evolution in the majority of the patients, with a low rate of adverse events which confirms its effectiveness and safety in the treatment of asthma.]]>
Vigilancia de la efectividad y seguridad de las vacunas VALERGEN en el tratamiento del asma
Surveillance of the effectiveness and safety of the VALERGEN vaccines in the treatment of asthma
Dra. Circe Pagés Rubio; Dra. Osaida Calderín Marín; Dra. María Morales Menéndez
Hospital Universitario Manuel Ascunce Domenech. Universidad de Ciencias Médicas de Camagüey. Camagüey, Cuba.
]]>
RESUMEN
Fundamento: la inmunoterapia es la única estrategia terapéutica para cambiar el rumbo de la fisiopatología de las enfermedades alérgicas, de aquí la importancia del estudio de su aplicación, las posibles reacciones adversas y su efectividad en dichas enfermedades.
Objetivo: evaluar la efectividad y seguridad de las vacunas VALERGEN en el tratamiento del asma.
Métodos: se realizó un estudio observacional de cohorte en pacientes con diagnóstico de asma intermitente, persistente leve y moderada a los que se les indicó la administración de las vacunas VALERGEN tanto por vía sublingual como por vía subcutánea. Se estableció un sistema de seguimiento prospectivo activo de los pacientes asmáticos vacunados, se empleó el método de farmacovigilancia monitoreo de eventos adversos en una cohorte. Se tomó una muestra de 100 pacientes que cumplieron los criterios de selección. Los datos se recolectaron a través de cuestionarios. Para el análisis de los mismos se utilizó estadística descriptiva e inferencial. El procesamiento de la información se realizó mediante el paquete estadístico SPSS versión 15.0. Los resultados obtenidos fueron ilustrados en tablas y gráficos.
Resultados: se encontró un predominio de pacientes con disminución de síntomas de asma y de la medicación con el uso de inmunoterapia, resultado que mostró una alta significación estadística (p=0,000). Los eventos adversos que más se presentaron fueron el habón >5cm, eritema, rinitis y la asociación de rinitis y asma, estos predominaron en el grupo etáreo de cinco a nueve años, sexo femenino, vía subcutánea, con la mezcla de Dermatophagoides pteronyssinus y Blomia tropicalis (VALERGEN DP + VALERGEN BT) y con concentración de 20 000 UB/ml.
Conclusiones: la inmunoterapia con vacunas VALERGEN propicia una evolución clínica favorable en la mayoría de los pacientes, con un bajo índice de eventos adversos, lo que confirma su efectividad y seguridad en el tratamiento del asma.
DeCS: FARMACOVIGILANCIA; DESENSIBILIZACIÓN INMUNOLÓGICA; ASMA/terapia; NIÑO; ESTUDIOS DE COHORTES.
ABSTRACT
Background: immunotherapy is the sole therapeutic strategy used to change the direction of physiopathology of allergic illnesses, hence the importance of this study, its application, the possible adverse reactions and its effectiveness in these conditions. ]]>
Objective: to evaluate the effectiveness and safety of the VALERGEN vaccines in the treatment of asthma.
Methods: an observational study of cohort was carried out in patients with diagnosis of mild to moderate persistent and intermittent asthma on which the administration of the VALERGEN vaccines were indicated by sublingual route or subcutaneously. An active prospective approach of the patients with asthma was used and the method of pharmacosurveillance monitoring of adverse events in a cohort was established. A sample of 100 patients fulfilling the selection criteria was conformed. The data were gathered through questionnaires. The analysis of data was done using descriptive and inferential statistics. The prosecution of information was carried out by means of the statistical package SPSS version 15.0. The obtained results were illustrated in charts and graphics.
Results: a prevalence of patient with decreased asthma symptoms was found and also the need for medication with the use of immunotherapy, this result that showed a high statistical significance (p=0,000). The adverse events presented more often were, the weal >5cm, erythema, rhinitis and the rhinitis association and asthma, these prevailed in the ages from 5 to 9 years, feminine sex, subcutaneous route, with the mixture of Dermatophagoides pteronyssinus and Blomia tropicalis (VALERGEN DP + VALERGEN BT) and with concentration of 20 000 UB/ml.
Conclusion: immunotherapy with VALERGEN vaccines provides a positive clinical evolution in the majority of the patients, with a low rate of adverse events which confirms its effectiveness and safety in the treatment of asthma.
DeCS: PHARMACOVIGILANCE; DESENSITIZATION, IMMUNOLOGIC; ASTHMA/therapy; CHILD; COHORT STUDIES.
INTRODUCCIÓN
Las vacunas terapéuticas para la alergia, también llamadas inmunoterapia alergeno-específica, consisten en la administración de dosis progresiva del alergeno al cual el individuo está sensibilizado, en pacientes con afecciones mediadas por la inmunoglobulina E (IgE). 1-3 El objetivo es modificar la respuesta inmunitaria e inducir un estado de tolerancia a la exposición alergénica con la consiguiente disminución de los síntomas alérgicos y de las reacciones inflamatorias asociadas con la exposición natural a dichos alérgenos. 2 La inmunoterapia alérgeno-específica ha sido utilizada en el tratamiento de enfermedades alérgicas desde 1911, citado por Lockey R, Ledford DK 4 y Calderón M, et al. 5
El uso de la inmunoterapia provoca en un inicio aumento de la IgE específica, seguida por una disminución a niveles menores que los basales en la segunda mitad del primer año de tratamiento. Esta reducción va seguida de un aumento en los niveles de inmunoglobulina G (IgG), de forma especial en el IgG4. Entre sus funciones está la de bloquear la IgE fijada a la célula cebada con el alérgeno, al inicio de la reacción alérgica. Un tercer mecanismo probable es la co-fijación al alérgeno de la IgG junto con la IgE, lo que causa una coestimulación simultánea de receptores para ambas inmunoglobulinas, receptor de baja afinidad para la IgE (FcεRII) y receptor de alta afinidad para la IgE (FcεRI), de forma individual en la superficie de la célula cebada, donde el primero es un receptor inhibitorio que frena la actividad de la IgE mediante mecanismos intracelulares, donde impide la degranulación de la célula cebada. En etapas muy temprana de la inmunoterapia, se ha visto además un aumento de las inmunoglobulinas G por el alérgeno, donde se vuelven más eficaces para fijarlo. 6
]]> A partir de las últimas décadas se ha acumulado una gran cantidad de datos que documentan la eficacia clínica de la inmunoterapia, a través de la ejecución de ensayos clínicos controlados a doble ciegas para las diferentes manifestaciones alérgicas, en los cuales se reportan logros positivos entre 60 y 80 % de los pacientes después de tres años de tratamiento. En especial en el tratamiento del asma, su eficacia ha sido demostrada en diferentes ensayos clínicos. 7 La inmunoterapia tiene el potencial de cambiar el curso de la enfermedad alérgica y prevenir el agravamiento de la misma a largo plazo. En el caso de las alergias respiratorias, se ha demostrado que previene la aparición de nuevas sensibilizaciones alérgicas, así como el desarrollo del asma en pacientes con rinitis o asma ligera. 8El riesgo de las reacciones adversas de carácter sistémico constituye aún una seria limitación de la inmunoterapia y restringe su uso a servicios especializados de alergia, no obstante, se reconoce que con el desarrollo actual y uso de vacunas de alérgenos de calidad, bien caracterizadas y estandarizadas manera biológica, se ha incrementado su eficacia y seguridad. 9 La inmunoterapia alérgeno-específica ha demostrado ser una alternativa costo-efectiva en varios estudios realizados en países desarrollados. 10, 11 La misma está indicada cuando el alérgeno causante no puede ser eliminado del ambiente del paciente a pesar de las medidas de control tomadas para ello. Los ácaros del polvo doméstico, son un ejemplo claro al respecto. El papel de los mismos en el desarrollo del asma ha sido demostrado de manera amplia a escala mundial. 12, 13 Varios trabajos han demostrado la efectividad de la inmunoterapia en pacientes asmáticos donde se utilizan extractos alergénicos de ácaros. 7 En Cuba, los ácaros domésticos de mayor importancia alergénica son Dermatophagoides pteronyssinus, Dermatophagoides siboney y Blomia tropicalis. 14 Estas tres especies tienen una gran importancia como agentes sensibilizantes en individuos alérgicos y en particular asmáticos, en un grado similar. 15
Se tuvo en cuenta, los riesgos implicados en la administración de la inmunoterapia alérgeno-específica, así como su introducción creciente en los servicios de alergia con el empleo de las vacunas industriales VALERGEN en ambas variantes de administración, inyectable y sublingual, resulta necesario disponer de un sistema de farmacovigilancia activa, que permita identificar los posibles acontecimientos clínicos que puedan estar asociados con el empleo de las mismas y dar seguimiento a su efectividad en la práctica clínica habitual, razón por la cual se llevó a cabo la investigación, con el objetivo de evaluar la efectividad y seguridad de las vacunas VALERGEN en el tratamiento del asma.
MÉTODOS
Se realizó un estudio observacional de cohorte, se estableció un sistema de seguimiento prospectivo activo de los pacientes asmáticos vacunados con alguna/s de las vacunas VALERGEN, en la consulta de Alergología del Hospital Universitario Manuel Ascunce Domenech, de la ciudad de Camagüey de febrero de 2011 a diciembre de 2014. Se empleó el método de farmacovigilancia monitoreo de eventos adversos en una cohorte (cohort event monitoring). De un universo de 537 enfermos con asma que acudieron a consulta de Alergología, se tomó una muestra de 100 pacientes que cumplieron los criterios de selección.
Criterios de inclusión
Pacientes con diagnóstico confirmado de asma intermitente y persistente leve a moderada, asociada a sensibilización alérgica a los ácaros Dermatophagoides pteronyssinus, Dermatophagoides siboney o Blomia tropicalis, con indicación médica de inmunoterapia con vacunas VALERGEN según instrucciones del fabricante.
Pacientes monosensibilizados y polisensibilizados.
Ambos sexos. ]]>
Mayores de cinco años de edad.
Pacientes con la capacidad para responder a las preguntas de la entrevista o con cuidador/tutor que pueda contestar por él.
Consentimiento de participación.
Criterios de exclusión
Pacientes con contraindicaciones para la aplicación de la inmunoterapia con vacunas VALERGEN, de acuerdo a las instrucciones del fabricante.
Pacientes tratados de manera previa con inmunoterapia con extractos alergénicos en los dos años anteriores.
Pacientes que no acuden de forma regular a las consultas de seguimiento.
Los datos se recolectaron a través de cuestionario aplicados al inicio, a los seis y a los 12 meses de tratamiento.
Se aplicó el tratamiento donde se empleó la pauta indicada por el fabricante. Sin embargo, se aceptaron los cambios personalizados previstos en la posología que se refleja en el prospecto, propios de la inmunoterapia alérgeno-específica. Para la vía subcutánea, se consideró como paciente tratado aquel que alcanzó la fase de mantenimiento con una dosis en el rango de 1 000-6 000 UB. Para la sublingual se consideró tratado si alcanzó al menos la dosis de mantenimiento indicada (2 000 UB). No obstante, los pacientes que no alcanzaron estas dosis no fueron excluidos del estudio en cuanto a las variables de seguridad.
Se vigiló la variación de la frecuencia, severidad de las crisis de asma y consumo de medicamentos, así como los eventos asociados con el uso de las vacunas VALERGEN.
]]> Se utilizó la estadística descriptiva e inferencial para el análisis de los datos, estos fueron procesados mediante la prueba de Ji cuadrado, se demostró significación estadística en algunos de los resultados encontrados. Los resultados se presentan en texto, tablas de contingencia y gráficos, y fueron analizados y discutidos de acuerdo a los valores estadísticos obtenidos. Se empleó el Microsoft Excel y SPSS versión 15.0 para procesar datos y el Microsoft Word para la redacción del informe final.Para la investigación se utilizaron extractos alergénicos VALERGEN® de Dermatophagoides pteronyssinus, Dermatophagoides siboney y Blomia tropicalis producidos por el centro nacional de biopreparados (BIOCEN), estandarizados en unidades biológicas (UB) 100 000 UB/ml (equivalentes a histamina HCL 10mg/ml), liofilizados. Diluyente albúmina sérica humana 0,2 %, solución tampón fosfato con fenol al 0,4 % como preservante. Los extractos utilizados son fabricados en instalaciones industriales de acuerdo a las buenas prácticas de producción biológica, con licencia de producción otorgada por el centro para el control estatal de la calidad de los medicamentos (CECMED). Estos productos han sido registrados como vacunas terapéuticas tanto para la vía subcutánea inyectable (ITSC) o sublingual en gotas (ITSL), los mismos están incluidos en el cuadro básico de medicamentos del sistema nacional de salud.
RESULTADOS
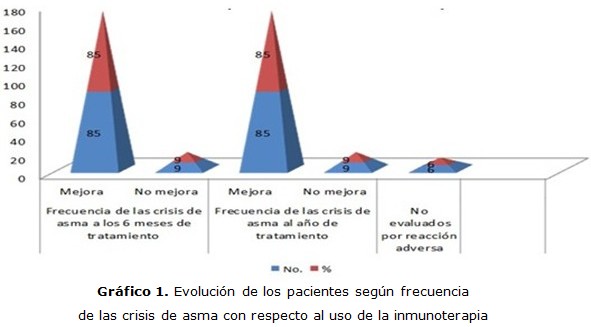
La evolución de los pacientes según la frecuencia de las crisis de asma fue favorable, donde se notó una mejoría en el 85 % de casos, tanto a los seis meses como al año de haber iniciado el tratamiento con inmunoterapia con las vacunas alergénicas de ácaros VALERGEN, resultado que mostró una alta significación estadística (p=0,000) (gráfico 1).
De manera general, se encontró mejoría en el número de las crisis al evaluar la severidad en el tiempo de uso de la inmunoterapia, donde predominó el número de pacientes que mejoraron a los seis meses y al año de iniciado el tratamiento con 84 y 85 pacientes de manera equitativa.
El consumo de medicamentos disminuyó en la mayoría de los pacientes, donde se pudo observar un consumo menor en 84 pacientes a los seis meses y en 85 al año de tratamiento con vacunas alergénicas (gráfico 2).
Los eventos adversos se presentaron en 11 pacientes para un 11 % de la muestra estudiada, así como predominó el habón >5 cm con tres pacientes, seguido de eritema, rinitis, y la asociación de rinitis y asma con dos casos cada uno, lo que evidencia la seguridad de las vacunas VALERGEN (gráfico 3).
]]>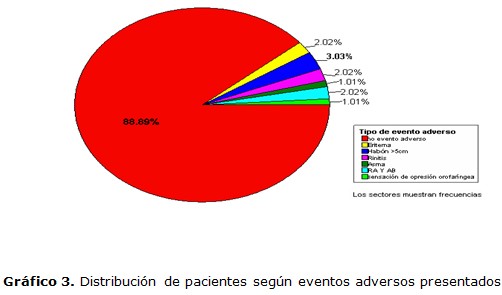
Existió un predominio de eventos adversos en el grupo etáreo de cinco a nueve años con cinco casos del total de pacientes tratados. El sexo femenino fue el de mayor incidencia con un 8 %. La vía subcutánea predominó sobre la sublingual con un 6 %. La vacuna alergénica que más efectos adversos provocó fue la mezcla de Dermatophagoides pteronyssinus y Blomia tropicalis (VALERGEN DP + VALERGEN BT) en seis pacientes. La mayor parte de los eventos adversos se presentaron con una concentración de 20 000 UB/ml en un 5 % de pacientes (tabla 1).
DISCUSIÓN
El primer estudio nacional de farmacovigilancia en inmunoterapia realizado en Cuba, plantea que el comportamiento de las variables de eficacia mostró mejorías muy significativas. 16 Labrada Rosado A 17 en su tesis doctoral realizó un meta-análisis donde confirma que el efecto promedio en cuanto a reducción de síntomas fue del 56,4 % y la reducción de la medicación fue del 58,4 %, mientras que el efecto de ambas variables sumadas: síntomas y medicación, fue incluso algo mayor 60,3 %. El efecto fue consistente entre los diferentes ensayos y significativo tanto a los seis como a los 12 meses de tratamiento.
Keles S, et al, 18 plantean que la inmunoterapia disminuye la frecuencia de las crisis de asma. Tanto en la subcutánea como sublingual, donde los síntomas de asma han sido evaluados, se han mostrado resultados positivos. 19 Hay alguna evidencia que la inmunoterapia puede prevenir la progresión de la enfermedad, el desarrollo de nuevas sensibilizaciones y disminuir las crisis de asma. 3
La inmunoterapia alérgeno-específica es efectiva en pacientes con asma leve o moderada, y es un tratamiento satisfactorio que está asociado a la reducción de síntomas, 20 además contribuye a disminuir la mortalidad de los pacientes con asma. 21
Capella A y Durham SR 22 expresan en su trabajo que la eficacia clínica de la inmunoterapia alérgeno-específica ha sido demostrada tanto en adultos como en niños. En un meta-análisis reciente se evidencia una notable mejoría en cuanto a los síntomas de asma, así como una reducción significativa de la necesidad de medicación en estos pacientes. 22-24
Jutel M 25 en su artículo Allergen-apecific immunotherapy in asthma cita que una evidencia creciente de estudios doble ciego controlados con placebo, demuestra que tanto la inmunoterapia sublingual como la inmunoterapia subcutánea son eficaces para reducir las puntuaciones por síntomas y uso de medicamentos, mejoran la calidad de vida e inducen cambios favorables en los marcadores inmunológicos específicos.
]]> Las enfermedades alérgicas son uno de los problemas más comunes encontrados en la práctica clínica. Medicamentos tales como los corticoesteroides y antihistamínicos pueden proporcionar un alivio de los síntomas, pero no cambian el curso de la enfermedad. 26-28Múltiples estudios realizados por Labrada Rosado A, 17 Castro Almarales RL, 27, 28 Sugrañes Montalván A, et al, 29 evidencian un bajo porciento de eventos adversos en los pacientes con inmunoterapia, lo que demuestra las reacciones locales más frecuentes en ambos tipos.
El ácaro Dermatophagoides pteronyssinus es el más utilizado en la elaboración de las vacunas, lo que se corresponde con la mayor sensibilización a este ácaro encontrado en la población cubana. 1 Calderón MA, et al, 30 le atribuye a este ácaro un papel preponderante como agente sensibilizante, de particular importancia en la primera infancia. Le siguió Blomia tropicalis, ácaro que también muestra alta sensibilidad en Cuba. 1 Esto pudiera explicar el predominio de efectos adversos en las vacunas alergénicas de mezcla de VALERGEN DP con VALERGEN BT que se encontró en la investigación.
La gran heterogeneidad en la clasificación y presentación de informes de eventos adversos sobre inmunoterapia, tanto en ITSC como ITSL, hace que el análisis y las comparaciones sobre seguridad sea difícil. Aunque ninguna forma de inmunoterapia está exenta de riesgos, la ITSL parece ser mejor tolerada que la ITSC y debe ser prescrita sólo por médicos entrenados en alergia, que deben brindar instrucciones a los pacientes sobre su tratamiento, para que aprendan a reconocer los eventos que pueden encontrar con su uso. 1
La experiencia recogida con el empleo de ITSL muestra menor número de reacciones adversas, tanto en niños como en adultos, con una frecuencia internacional de un evento adverso por 1 000 dosis y en menos de un 10 % de los pacientes tratados. 1 En estudios realizados por Castro Almarales RL, 27 Canonica GW, et al, 31 demuestran la eficacia y seguridad de la inmunoterapia alérgeno-específica, tanto subcutánea como sublingual, en el tratamiento del asma.
Las reacciones alérgicas son inherentes a la inmunoterapia con alérgenos, o sea, no son un efecto colateral. La frecuencia de reacciones adversas durante la misma se ha estimado entre 0,84 % y 10 % de las inyecciones administradas, entre 0,05 % y 0,27 % de reacciones sistémicas, de manera especial, de naturaleza leve o moderada. 17
CONCLUSIONES
La evolución clínica en los pacientes expuestos a las vacunas VALERGEN como tratamiento del asma, en términos de reducción de la frecuencia, severidad de las crisis de asma y consumo de medicamentos fue favorable, se pudo observar una mejoría clínica evidente en la mayoría de los casos.
Los efectos adversos que más se presentaron fueron el habón >5cm, seguido de eritema, rinitis, y la asociación de rinitis y asma.
]]> Las reacciones adversas predominaron en los niños del grupo etáreo de cinco a nueve años, sexo femenino, vía subcutánea, con la mezcla DP+BT y con concentraciones de 20 000 UB/ml.
REFERENCIAS BIBLIOGRÁFICAS
1. Álvarez Castelló M, Castro Almarales RL, Labrada Rosado A, Enríquez Domínguez I, Ronquillo Díaz M, Ronquillo M, et al. Prescripción y Vigilancia de la inmunoterapia sublingual con vacunas estandarizadas de ácaros domésticos en un servicio de alergología. VacciMonitor [Internet]. 2012 [citado 3 Feb 2014];21(3):[aprox. 4 p.]. Disponible en: http://www.finlay.sld.cu/publicaciones/vaccimonitor/Vm2012/a18.pdf
2. Saranz RJ, Lozano A, Cáceres ME, Arnolt RG, Máspero JF, Bozzola CM, et al. Inmunoterapia con alergenos para la prevención y el tratamiento de las enfermedades alérgicas respiratorias de la infancia. Arch Argent Pediatr [Internet]. May-Jun 2010 [citado 3 Feb 2014];108(3):[aprox. 2 p.]. Disponible en: http://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S0325-00752010000300020
3. Meadows A, Kaambwa B, Novielli N, Huissoon A, Fry-Smith A, Meads C, et al. A systematic review and economic evaluation of subcutaneous and sublingual allergen immunotherapy in adults and children with seasonal allergic rhinitis.Health Technol Assess. 2013;17(27):1-322.
4. Lockey R, Ledford DK. Allergens and Allergen Immunotherapy. Clinical Allergy and Immunology. 4ª ed. New York: Healthcare; 2008.
5. Calderon M, Cardona V, Demoly P. One hundred years of allergen immunotherapy European Academy of Allergy and Clinical Immunology celebration: review of unanswered questions. Allergy [Internet]. 2012 [citado 2013 May 10];67(4):[about 15 p.]. Available from: http://onlinelibrary.wiley.com/doi/10.1111/j.1398-9995.2012.02785.x/pdf
6. Larenas Linnemann D, Pereira C, Rodríguez Pérez N. Mecanismos de inmunoterapia. En: Méndez de Inocencio J, Huerta López J, Bellanti JA, Ovilla Martínez R, Escobar Gutiérrez A, editores. Alergia: Enfermedad Multisistémica. Fundamentos básicos y clínicos. México: Editorial Panamericana; 2008. p. 395-401.
7. Abramson MJ, Puy RM, Weiner JM. Allergen immunotherapy for asthma. Cochrane Database Syst Rev. 2003;(4):CD001186.
8. Burks AW, Calderon MA, Casale T, Cox L, Demoly P, Jutel M, et al. Update on allergy immunotherapy: American Academy of Allergy, Asthma & Immunology/European Academy of Allergy and Clinical Immunology/PRACTALL consensus. J Allergy Clin Immunol. 2013 May;131(5):1288-96.
9. Van Ree R. Indoor allergens: Relevance of major allergen measurements and standardization. J Allergy Clin Immunol. 2007 Feb;119(2):270-7.
10. Berto P, Frati F, Incorvaia C. Economic Studies of immunotherapy: a review. Curr Op Allergy Clin Immunol. 2008 Dec;8(6):585-9.
]]>11. Nasser S, Vestenbaek U, Beriot-Mathiot A, Poulsen PB. Cost effectiveness of specific immunotherapy with Grazx in allergic rhinitis co-existing with asthma. Allergy. 2008 Dec;63(12):1624-9.
12. Edwin EA, Ronmark E, Wickens K, Perzanowski M, Barry D, Lundback B, et al. Contribution of dust mite and cat specific IgE to total IgE: Relevance to asthma prevalence. J Allergy Clin Immunol. 2007 Feb;119(2):359-65.
13. Platts-Mills TA. The role of Indoor Allergens in chronic allergic disease. J Allergy Clin Immunol. 2007 Feb;119(2):297-302.
14. Ferrándiz R, Casas R, Dreborg S. Sensitisation to Dermatophagoides siboney, Blomia tropicalis, and other domestic mites in asthmatic patients. Allergy [Internet]. 1996 [citado 2012 May 30];51(7):[about 11 p.]. Available from: http://onlinelibrary.wiley.com/doi/10.1111/j.1398-9995.1996.tb04656.x/pdf
15. Castro Almarales RL, Mateo Morejón M, Naranjo Robalino RM, Navarro Viltre BI, Álvarez Castelló M, Ronquillo Díaz M, et al. Correlation between skin tests to Dermatophagoides pteronyssinus, Dermatophagoides siboney and Blomia tropicalis in Cuban asthmatics. Allergol Immunopathol (Madr). 2006 Jan-Feb;34(1):23-6.
16. Inmunoterapia. Avances del primer estudio nacional de Farmacovigilancia en inmunoterapia [Internet]. La Habana: Inmunoterapia; 2012 [citado 3 Feb 2014]. Disponible en: http://articulos.sld.cu/inmunoterapia/category/nacionales
17. Labrada Rosado A. Desarrollo a ciclo completo de las primeras vacunas estandarizadas de alergenos de ácaros para la inmunoterapia en Cuba. [tesis doctoral]. La Habana: Instituto Superior de Ciencias Médicas; 2009.
18. Keles S, Karakoc Aydiner E, Ozen A, Izgi AG, Tevetoglu A, Akkoc T, et al. A novel approach in allergen-specific immunotherapy: combination of sublingual and subcutaneous routes. J Allergy Clin Immunol. 2011 Oct;128(4):808-15.
19. Passalacqua G, Canonica GW. Specific immunotherapy in asthma: efficacy and safety. Clin Experimen Allerg [Internet]. 2011 [citado 2014 Feb 3];41(9):[about 7 p.]. Available from: http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2222.2010.03688.x/full
20. Kopp MV. Role of immunmodulators in allergen-specific immunotherapy. Germany Allergy [Internet]. 2011 [citado 2013 Feb 3];66(9):[about 7 p.]. Available from: http://onlinelibrary.wiley.com/doi/10.1111/j.1398-9995.2011.02553.x/pdf
21. Wayne T. House dust allergy and immunotherapy. Hum Vaccin Immunother [Internet]. 2012 Oct 1 [citado 2013 Oct 15];8(10):[about 10 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3660285
22. Capella A, Durham S. Allergen immunotherapy for allergic respiratory diseases. Hum Vaccin Immunother [Internet]. 2012 Oct 1 [citado 2013 Oct 15];8(10):[about 12 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3660772
23. Díaz Rodríguez A, Labrada Rosado A, Castro Almarales RL, Álvarez Castelló M. Current status and future perspectives of immunotherapy in Latin America and Cuba. WAOJ [Internet]. 2014 [citado 2014 Oct 21];7(1):[about 4 p.]. Available from: http://www.waojournal.org/content/pdf/1939-4551-7-28.pdf
24. Kim JM, Lin SY, Suárez-Cuervo C, Chelladurai Y, Ramanathan M, Segal JB, Erekosima N. Allergen-Specific Immunotherapy for Pediatric Asthma and Rhinoconjunctivitis: A Systematic Review. Pediatrics [Internet]. 2013 Jun [citado 2013 Oct 15];131(6):[about 11 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4074663
25. Jutel M. Allergen-Specific Immunotherapy in Asthma. Curr Treat Options Allergy [Internet]. 2014 Mar [citado 2014 Jun 10];1(2):[about 9 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4032467/.
26. Young-Yuen Wu A. Immunotherapy - Vaccines for allergic diseases. J Thorac Dis [Internet]. 2012 Apr 1 [citado 2013 Feb 3];4(2):[about 8 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3378232
27. Castro Almarales RL, Álvarez Castello M, Ronquillo Díaz M, González León M, Labrada Rosado A, Rodríguez Canosa JS, et al. Immunotherapy 2072. Therapeutic effect and higher safety profile for allergic asthma in Cuban patients with sublingual immunmotherapy using tropical domestic mite allergen vaccines. WAOJ [Internet]. 2013 [citado 2014 Ene 10];6(Suppl 1):[about 4 p.]. Available from: http://www.waojournal.org/content/pdf/1939-4551-6-S1-P154.pdf
28. Castro Almarales RL, Ronquillo Díaz M, Álvarez Castello M, González León M, Labrada Rosado A, Rodríguez Canosa JS, et al. Immunotherapy 2073. Therapeutic effect of mite allergen vaccines by subcutaneous route in allergic Cuban asthmatic patients. WAOJ [Internet]. 2013 [citado 2014 Ene 10];6(Suppl 1):[about 5 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3643624/.
29. Sugrañes Montalván A, Hernández Veiga M, Morales Menéndez M, Barreto Suárez E, Sugrañes Montalbán A, Ramírez Torres A. Uso de vacuna Valergen DP en la rinitis alérgica. AMC [Internet]. Jul-Ago 2011 [citado 3 Feb 2013];15(4):[aprox. 7 p.]. Disponible en: http://scielo.sld.cu/scielo.php?pid=S1025-02552011000400005&script=sci_arttext
30. Calderón MA, Linneberg A, Kleine Tebbe J, De Blay F, Hernandez Fernandez de Rojas D, Virchow JC, et al. Respiratory allergy caused by house dust mites: What do we really know? J Allergy Clin Immunol. 2015 Jul;136(1):38-48.
31. Canonica GW, Cox L, Pawankar R, Baena Cagnani CE, Blaiss M, Bonini S, et al. Sublingual immunotherapy: World Allergy Organization position paper 2013 update. WAOJ [Internet]. 2014 Mar 28 [citado 2014 May 10];7(1):[about 6 p.]. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3983904
Recibido: 31 de mayo de 2016
Aprobado: 10 de noviembre de 2016
Dra. Circe Pagés Rubio. Especialista de I grado en Alergología. Especialista de I grado en Medicina General Integral. Hospital Universitario Manuel Ascunce Domenech. Universidad de Ciencias Médicas de Camagüey. Camagüey, Cuba. Email: circepr@nauta.cu
]]>