 ]]>
]]>
ARTÍCULO ORIGINAL
Prescripción y vigilancia de la inmunoterapia sublingual con vacunas estandarizadas de ácaros domésticos en un servicio de alergología
Prescription and surveillance of the sublingual immunotherapy with standardized domestic mite vaccines in allergology service
Mirta Álvarez, 1* Raúl Lázaro Castro, 2 Daniel Ramón Gutiérrez,1 Alexis Labrada,2 Irene Enríquez,1 Mercedes Ronquillo,1 José Rodríguez 1
1 Hospital Universitario "General Calixto García". La Habana, Cuba. ]]>
2 Departamento de Alergenos. Centro Nacional de Biopreparados (BIOCEN). Carretera Beltrán km 1/2. Bejucal, Mayabeque, Cuba.
email:mirtaac@infomed.sld.cu
* Especialista de I Grado en MGI, II Grado en Alergología. MSc en Enfermedades Infecciosas y Salud Ocupacional.
RESUMEN
Las vacunas terapéuticas para la alergia, también llamadas inmunoterapia alergeno específica, consisten en la administración de dosis progresivamente crecientes del alergeno al cual el individuo está sensibilizado, con el objetivo de alcanzar tolerancia al mismo y disminuir la sintomatología clínica. Se realizó un estudio descriptivo, de corte transversal para determinar la seguridad de las vacunas de ácaros domésticos (VALERGEN), administradas mediante gotas por vía sublingual. Se verificaron sus eventos adversos en pacientes alérgicos, atendidos en el Departamento de Alergología del hospital universitario "Calixto García", que asistieron a cambios de vacunas en el mes de septiembre de 2010, así como la frecuencia de prescripción de vacunas alergénicas en el período enero-septiembre del mismo año. Se incluyeron 130 pacientes con tratamiento de inmunoterapia sublingual con VALERGEN, con una edad media de 19,6 años (rango 1-75); el 40,7% tenía 17 años o menos. El tipo de vacuna más empleada resultó ser la multialergénica (63,8%). El ácaro más empleado fue el Dermatophagoides pteronyssinus, seguido de Blomia tropicalis . El 71,55% de los casos se encontraban en fase de mantenimiento. Se reportaron cuatro eventos adversos (3,1%) locales leves, que no requirieron tratamiento ni cambio de pauta de vacunación. Se comprobó que las vacunas sublinguales VALERGEN son seguras y bien toleradas en los pacientes alérgicos.
Palabras clave: inmunoterapia, vacunas sublinguales, eventos adversos, VALERGEN, alergia
Allergen-specific immunotherapy consists of administering gradually increasing doses of the allergen, to which the patient is sensitized, aiming at achieving tolerance to it and decreasing clinical symptoms. The sublingual immunotherapy (SLIT) was introduced as an alternative to subcutaneous route. The objective was to assess the safety of sublingual standardized vaccines of three domestic mite species (VALERGEN, Cuba) and its adverse events in allergic patients from the Calixto García University Hospital in Havana, as well as the frequency of the vaccine prescription. A descriptive and cross sectional study design included 130 patients with treatment of SLIT with VALERGEN (BIOCEN, Cuba), who attended the Allergy Service in the period from January to September 2010. Age distribution: mean 19.6 years (range 1-75), 40.7% was younger than 18 years. The multiallergen vaccine was the most used (63.8%). The most common allergen was D. pteronyssinus followed by B. tropicalis . 71.55% of administered allergens vaccines were in maintenance phase. We found 4 adverse events (3.1% of patients), all local, mild, and not requiring treatment or change of dosing schedule. The VALERGEN vaccines by sublingual route were shown to be safe and well tolerated in Cuban allergic patients.
Keywords : immunotherapy, sublingual vaccines, adverse events, VALERGEN, allergy.
INTRODUCCIÓN
La inmunoterapia sublingual (ITSL) cada día gana más terreno en la práctica alergológica. Son muchos los estudios que avalan su eficacia y su seguridad, tanto en niños como en adultos (1-9), al igual que la clásica inmunoterapia subcutánea. La inmunoterapia (IT) cumple ya 100 años de duro batallar, la cual ha demostrado su validez en el tratamiento de las enfermedades alérgicas IgE mediadas y se ha consolidado, hasta hoy, como el único tratamiento capaz de modificar el curso natural de estas enfermedades (1, 9).
]]>
Estudios recientes han mostrado que la ITSL mantiene sus efectos hasta cinco años después de descontinuada y previene la aparición de nuevas sensibilizaciones. Tiene más aceptación entre los pacientes, pues se evitan el pinchazo y puede administrársele en el hogar. Se considera una terapia segura y ha sido validada recientemente por un panel de expertos y la Organización Mundial de la Salud, para uso clínico rutinario en niños y adultos (7, 8).
La IT se indica al demostrarse una sensibilización alérgica mediante pruebas cutáneas o determinación de IgE sérica específica y si dicha sensibilización se corresponde con la sintomatología que presenta el paciente. Como en cualquier tratamiento se reportan efectos adversos con su uso. Su frecuencia de aparición es baja comparada con la inmunoterapia subcutánea (ITSC) y son generalmente locales. Son atributos de superioridad para las vacunas sublinguales su administración oral y sencillez, además de la administración en el hogar sin necesidad de personal sanitario.
Con la ITSL también se minimiza el efecto psicológico de la carga familiar y personal que supone una terapia larga y costosa como la terapia subcutánea. Todo esto facilita una mayor adhesión al tratamiento y, por tanto, mayor posibilidad para el control de la enfermedad, que es el objetivo principal para obtener mejor calidad de vida (9).
En nuestro país se viene utilizando por algunos alergólogos desde hace años esta modalidad de administración sublingual de vacunas alergénicas, cuyo reporte inicial de uso data de los primeros años del pasado siglo XX, apareciendo las primeras publicaciones en 1980.
Recientemente se logró, por primera, el registro sanitario estatal por el Centro para el Control Estatal de la Calidad de los Medicamentos (CECMED) de las primeras vacunas sublinguales para la alergia (VALERGEN), producidas en el Centro Nacional de Biopreparados (BIOCEN). La forma más extendida y la única utilizada en nuestro servicio es la sublingual deglutida, donde el paciente mantiene la vacuna debajo de la lengua 1 o 2 minutos y después es ingerida.
]]>
El objetivo de esta investigación fue determinar la frecuencia de prescripción de estas vacunas, VALERGEN, por vía sublingual y sentar las bases para la vigilancia activa de eventos adversos de las mismas en nuestro servicio.
MATERIALES Y MÉTODOS
Estudio descriptivo, transversal, que se realizó revisando la historia clínica de todos los pacientes alérgicos, sin discriminación y el registro de elaboración de vacunas alergénicas, entre enero y septiembre del 2010 e igual periodo del 2009, del servicio de alergología del hospital universitario "General Calixto García", en La Habana, Cuba.
El equipo médico registró de forma estandarizada toda la vacunación prescrita para las enfermedades alérgicas y los eventos adversos observados por los pacientes durante el curso de los tratamientos. La inmunoterapia se prescribió de acuerdo con las recomendaciones de la Organización Mundial de la Salud (8). La prueba de alergia a los diferentes alergenos se realizó de acuerdo con la historia clínica individual y una prueba cutánea por punción positiva. La severidad de las enfermedades alérgicas se estableció según las guías internacionales (7, 8).
Los eventos adversos los clasificamos en: inesperados o esperados. Los inesperados fueron aquellos eventos no descritos en el registro de estos productos con anterioridad, o descritos, pero con un aumento en frecuencia, severidad o progresión de la enfermedad. Mientras los esperados fueron los que por su naturaleza o severidad estaban descritos en el registro de las vacunas investigadas.
]]>
Además, los eventos adversos esperados se clasificaron de acuerdo con las recomendaciones de la Organización Mundial de Alergia (9) en: locales: prurito lingual u oral, edema de labios o lengua, náuseas, epigastralgia o diarrea, y sistémicos: Grado 0: síntomas no específicos como cefalea, malestar general, cansancio, artralgia probablemente, no mediada por IgE; Grado I: rinitis o asma ligera, urticaria localizada que responden a los antihistamínicos o b-2 broncodilatadores; Grado II: asma moderada, urticaria generalizada de aparición lenta después de 15 min que responden a los antihistamínicos o b-2 broncodilatadores; Grado III: asma severa, angioedema, urticaria generalizada de aparición rápida antes de 15 min que no responden a los antihistamínicos o b-2 broncodilatadores; Grado IV (Shock anafiláctico): picor, enrojecimiento, eritema, broncoespasmo, hipotensión o paro cardiorespiratorio de aparición rápida, provocada antes de 15 min, que requiere un tratamiento intensivo.
Por otro lado, todos los eventos adversos se registraron por el paciente si aparecieron antes (inmediatas) o después de los 30 min (tardías). En el caso de presentar eventos adversos los pacientes o sus familiares fueron instruidos para reconocer los eventos que aparecieran en el curso de la inmunoterapia sublingual, registrar en su modelo individual de eventos adversos e informar al equipo médico de sus características. El equipo médico los clasificó y registró en la historia clínica individual, teniendo en cuenta las características demográficas y clínicas del paciente y fase del tratamiento. La frecuencia de prescripción sublingual o subcutánea de las vacunas VALERGEN-DP (ácaro Dermatophagoides pteronyssinus ), VALERGEN-DS ( D. siboney ) y VALERGEN-BT ( Blomia tropicalis ), se determinó de acuerdo con el número de pacientes que se les asignó por una u otra vía el total de prescripciones realizadas en cada periodo investigado. Las vacunas alergénicas, según composición, se clasificaron como: simples, si estaban compuestas por un solo alérgeno y mixtas cuando se incluyeron varios alérgenos.
A todos los pacientes se les administró volúmenes (comenzando por 1 gota hasta alcanzar las 10 gotas) sublinguales en forma creciente de la vacunas investigadas mediante diferentes dosis (20, 200, 2000 y 20000 UB/mL), por tres semanas en la fase de incremento. Posteriormente, en la fase de mantenimiento se administró una dosis fija (10 gotas de la dosis de 20000 UB/mL, dosis máxima tolerada, 10000 UB), dos veces por semana (lunes y viernes).
La vigilancia sobre los eventos adversos (EA) ocurridos con la ITSL se estableció seleccionando a los pacientes alérgicos, sin discriminación del servicio, que concurrieron a cambio de vacunas durante el mes de septiembre del 2010 y que utilizaron inmunoterapia con productos VALERGEN.
El procesamiento de los datos se realizó empleando las funciones estadísticas del programa Microsoft Excel 7.0 y con el paquete estadístico Statistica 4.0 se calculó la media, desviación estándar, porcentaje y se realizó el análisis de los eventos adversos según sexo, edad y enfermedad tratada, aplicando tablas de contingencia (Prueba de c 2 y exacto de Fisher); el valor significativo fue de p<0,05.
]]>
RESULTADOS
En el período comprendido entre enero y septiembre de este año 2010 se prescribieron 12 932 vacunas alergénicas, de ellas el 40,7% eran sublinguales. En la Tabla 1 se observan los datos en igual período del año anterior, en el cual las vacunas sublinguales constituyeron el 32% de un total de 13 089 vacunas alergénicas prescritas. A pesar de prescribirse 157 vacunas menos este año, con respecto al anterior período, el porcentaje de vacunas sublinguales aumentó en un 8%.
De un total de 776 vacunas producidas en el mes de septiembre, el 16,8% utilizaba solo productos VALERGEN en su composición. Las características de los pacientes con vacunas sublinguales VALERGEN se resumen en la Tabla 2.
Los eventos adversos se reportaron en cuatro pacientes, dos por cada sexo con una media de edad de 24,4 que correspondieron al 3,08% del total de pacientes con ITSL. La diferencia entre ambos grupos no fue estadísticamente significativa (p>0,05) para la edad y el sexo.
Los cuatro eventos adversos se registraron en pacientes con asma, con una difererencia estadísticamente significativa (p=0,005). Por lo tanto, el asma en este estudio constituyó un factor de riesgo para desarrollar un EA. El grupo con mayor prescripción fue el de adultos entre 18 y 60 años, 61 casos (46,9%), seguido del grupo pediátrico, 53 pacientes, que representó el 40,7%.
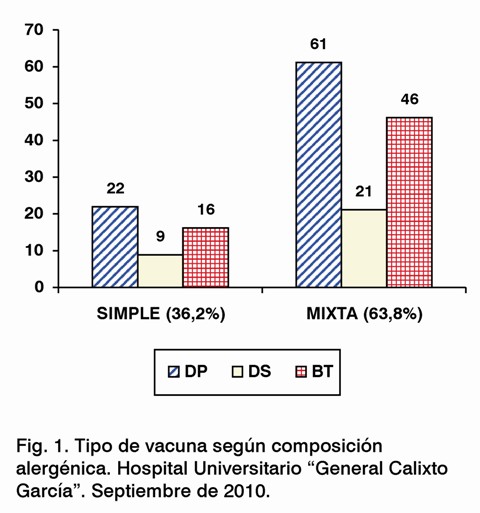
La mayoría de las vacunas utilizadas en nuestro servicio son mezclas de alérgenos (63,8%). El ácaro más indicado en las vacunas, ya sea simple o mixta, es el Dermatophagoides pteronyssinus (DP). La distribución por ácaros, según composición de alérgenos (Fig. 1) fue similar para los dos tipos de vacunas sublinguales empleadas. Se muestran las vacunas VALERGEN con relación a la fase de IT en que se encontraban los pacientes (Fig. 2). La mayor parte de los casos estaban en fase de mantenimiento (71,5%), lo que habla a favor de la buena adherencia al tratamiento por esta vía.
Se muestra la ocurrencia de EA con estas vacunas VALERGEN reportadas en nuestro estudio (Fig. 3). Los cuatro eventos fueron locales, leves e inmediatos (3,1% de los casos) y en fase de incremento de dosis. El prurito sublingual se reportó en tres casos y uno presentó naúseas. Ninguno necesitó reducción de la dosis ni variación en la pauta de vacunación y la resolución fue espontánea.
DISCUSIÓN
La vacunación por vía sublingual es ampliamente utilizada en el mundo, fundamentalmente en Europa, y es de gran aceptación por médicos y pacientes. Esta se desarrolló buscando una vía más segura y rápida de administración que evitara las reacciones adversas graves y mortales, así como la degradación gastrointestinal del extracto.
]]>
Aunque se ha demostrado que las cantidades absorbidas de extracto alergénico no son relevantes, su eficacia está ampliamente avalada por un gran número de ensayos clínicos (5, 10, 11).
El incremento de la prescripción de la ITSL, observado en este estudio, impresiona que está asociado a una preferencia creciente del equipo médico por esta vía, al constatar un mayor perfil de seguridad.
Las enfermedades alérgicas aumentan en todo el mundo y, según estimados de la OMS, en el año 2050 la mitad de la población mundial presentará un trastorno alérgico. En la reciente revisión del documento de posición sobre ITSL, los expertos encontraron resultados muy variables, desde eventos leves, no trascendentes, hasta análisis exhaustivos de eventos sistémicos severos. No se ha descrito ningún caso fatal, aunque se recogen seis casos de reacciones anafilácticas serias con el uso de vacunas sublinguales (12-15), no existiendo reportes de estos eventos en nuestro país.
El ácaro D. pteronissinus fue el más utilizado en la elaboración de las vacunas, lo que se corresponde con la mayor sensibilización a este ácaro encontrado en la población cubana por varios autores (16, 17). Reportes internacionales le atribuyen a este ácaro un papel preponderante como agente sensibilizante, de particular importancia en la primera infancia (18, 19). Le siguió Blomia tropicalis , ácaro que muestra alta sensibilidad en la población cubana, sobre todo en zonas costeras, como la reportada en el municipio Habana del Este, de la capital (20) y que es atendido de manera regular en nuestro servicio de alergología.
La modalidad de administración sublingual es de amplia aceptación por los niños y sus padres debido a la administración en su hogar y la eliminación del doloroso pinchazo. Su utilización debe hacerse desde edades tempranas, ya que es el único tratamiento capaz de modificar el curso natural de las enfermedades alérgicas y evita el desarrollo de nuevas sensibilizaciones. Una consideración con la ITSL es que la mayoría de las dosis se administran fuera del entorno clínico sin supervisión médica directa y la exactitud de la información del EA depende del paciente o la interpretación de la familia. Por lo tanto, se debe orientar e instruir a los pacientes y familiares a conocer, describir y registrar las características de los eventos adversos que ocurran en su hogar e informar rápidamente a su equipo médico.
]]>
La gran heterogeneidad en la clasificación y presentación de informes de EA sobre inmunoterapia, tanto ITSC como ITSL, hace que el análisis y las comparaciones sobre seguridad sea difícil. Aunque ninguna forma de IT está exenta de riesgos, la ITSL parece ser mejor tolerada que la ITSC y debe ser prescrita solo por médicos entrenados en alergia, que deben brindar instrucciones a los pacientes sobre su tratamiento, para que aprendan a reconocer los eventos que pueden encontrar con su uso (8).
Debe ser una prioridad también de los servicios de alergología de todas las provincias difundir conocimientos entre los profesionales de atención primaria para que reconozcan los eventos adversos que pueden presentarse con esta modalidad terapéutica, aplicada por el propio paciente o su familia en el hogar, pues son ellos los que primero se enfrentan a los EA que ocurren.
La experiencia internacional recogida con el empleo de ITSL muestra menor número de reacciones adversas, tanto en niños como en adultos, con una frecuencia internacional de un evento adverso por 1000 dosis (21) y en menos del 10% de los pacientes tratados, lo que está acorde con nuestros resultados.
Podemos concluir que las vacunas alergénicas VALERGEN para uso sublingual, ampliamente utilizadas en el servicio de alergología de nuestro hospital, provocan escasos eventos adversos de tipo local leves, por lo que se consideran un tratamiento seguro en los pacientes alérgicos.
Recomendamos diseñar ensayos clínicos fase IV en niños y adultos y generalizar el registro de las reacciones adversas a la inmunoterapia en todos los niveles de atención de salud y en los servicios de alergología de todo el país.
]]>
REFERENCIAS
1. Bousquet J, Lockey R, Malling HJ. WHO position paper Allergen immunotherapy: therapeutic vaccines for allergic diseases. J Allergy Clin Immunol 1998;102:558-62.
2. Rodríguez SO. Inmunoterapia sublingual en rinitis alérgica y asma en niños de dos a cinco años sensibilizados con ácaros. Revista Alergia México 2008;55(2):71-5.
3. Di Rienzo V, Pagani A, Parmiani S, Passalacqua G, Canonica WG. Post-marketing surveillance study on the safety of sublingual immunotherapy in pediatric patients. Allergy 1999;54:1110-3.
4. Gidaro GB, Marcucci F, Sensi L, Incorvaia C, Frati F, Ciprandi G. The safety of sublingual-swallow immunotherapy: an analysis of published studies. Clin Exp Allergy 2005;35:565-71. 5. Penagos M, Passalacqua G, Compalati E, Baena-Cagnani CE, Orozco S, Pedroza AY, et al. Metaanalysis of the Efficacy of Sublingual Immunotherapy in the Treatment of Allergic Asthma in Pediatric Patients, 3 to 18 Years of Age. Chest 2008;133:599-609.
6. Ulrich W, Tabar A, Kuna P, Halken S, Montagut A, Beaumont O, le Gall M. Efficacy and safety of 5-grass-pollen sublingual immunotherapy tablets in pediatric allergic rhinoconjunctivitis. The Journal of Allergy and Clinical Immunology 2009;123(1):160-6.
7. Passalacqua G, Lombardi C, Canonica GW. Sublingual Immunotherapy: An Update. Current Opinion in Allergy & Clinical Immunology 2004;4(1):31-6.
8. Canonica GW, Bousquet J, Casale T, Lockey R, Baena-Cagnani CE, Pawankar R, et al. Sub-Lingual Immunotherapy. World Allergy Organization Position Paper World Allergy Organization Journal 2009; 2(11):233-81.
9. Canonica GW, Baena-Cagnani CE, Bousquet J, Bousquet PJ, Lockey RF, Malling HJ, et al. Recommendations for standardization of clinical trials with Allergen Specific Immunotherapy for respiratory allergy. A statement of a World Allergy Organization (WAO) taskforce. Allergy 2007;62:317-24.
10. Gómez VJ, Flores SG, Orea SM, López TJ, Jiménez SN. Inocuidad y eficacia de la inmunoterapia sublingual específica en pacientes con asma y alergia a Dermatophagoides pteronyssinus. Revista Alergia México 2005;52(6):231-6.
11. Passalacqua G, Guerra L, Fumagalli F, Compatali E, Canonica W. An Update of Sublingual Immunotherapy. Allergy Clin Immunol Int J World Allergy Org 2005;17(5):181-5.
12. De Groot H, Bijl A. Anaphylactic reaction after the first dose of sublingual immunotherapy with grass pollen tablet. Allergy 2011;64:961-7.
13. Dunsky EH, Goldstein MF, Dvorin DJ, Belecanech GA. Anaphylaxis to sublingual immunotherapy. Allergy 2006; 61: 1235-1244.
14. Eifan AO, Keles S, Bahceciler NN, Barlan IB. Anaphylaxis to multiple pollen allergen sublingual immunotherapy. Allergy 2007;62 (5):567-8.
15. Antico A, Pagani M, Crema A. Anaphylaxis by latex sublingual immunotherapy. Allergy 2006; 61:1236-7.
16. Pérez PM, García DA, Sabina DA, Vega GM, Macías CV. Sensibilización a diferentes tipos de ácaros en pacientes adultos. Rev Cubana Med 2002;41(2):75-8.
17. Castro Almarales RL, González León M, Labrada Rosado A, Navarro Viltre BI, Álvarez Castelló M, García Gómez I. Sensibilización a Dermatophagoides pteronyssinus, Dermatophagoides siboney y Blomia tropicalis en niños de tres consultorios. Rev Cubana Med Gen Integr 2005;21(3-4). Disponible en: http://scielo.slcu/scielo.php?script=sci_arttext&pid=S0864 -21252005000300022&lng=es.
18. Sánchez-Borges M, Capriles-Hulett A, Malka S. Inhalant allergens clinically significant in Latin America. Allergy Clin Immunol Int: J World Allergy Org 2004;16:28-32.
19. Platts-Mills TAE, Vervloet D, Thomas WR, Aalberse RC, Chapman MD. Indoor allergens and asthma: Report of the Third International Workshop. J Allergy Clin Immunol 1997;100(6):1-24.
20. Castro ARL, Álvarez CM, Ronquillo DM, Rodríguez CJS, García GI, González LM, et al. Sensibilización a tres especies de ácaros en pacientes alérgicos de la zona costera de la ciudad de La Habana. Rev Alerg Mex 2009;56(2):31-5.
21. Campbell D S. Sublingual immunotherapy for children: Are we there yet? Defining its role in clinical practice. Paediatric Respiratory Reviews 2009;10(2):69-74.
Recibido: Febrero de 2012
Aceptado: Mayo de 2012