Cáncer de ovario en el Instituto Nacional de Oncología y Radiobiología de Cuba: 2001 a 2005
Ovarian cancer at the National Institute of Oncology and Radiobiology of Cuba: 2001-2005
]]>
I Especialista de I Grado en Oncología. Investigador Agregado. Instituto Nacional de Oncología y Radiobiología (INOR). La Habana, Cuba.
II Especialista de I Grado en Ginecología y Obstetricia. Diplomada en Ginecología Oncológica. Hospital Ginecoobstétrico Docente «Ramón González Coro». La Habana, Cuba.
III Especialista de I Grado en Cirugía General. Diplomado en Ginecología Oncológica. Instituto Nacional de Oncología y Radiobiología (INOR). La Habana, Cuba.
IV Especialista de II Grado en Oncología. Instructor de Oncología. Investigador Agregado. Instituto Nacional de Oncología y Radiobiología (INOR). La Habana, Cuba.
V Especialista de II Grado en Oncología. Asistente de Oncología. Investigador Agregado. Instituto Nacional de Oncología y Radiobiología (INOR). La Habana, Cuba.
VI Especialista de I Grado en Ginecología y Obstetricia. Especialista de II Grado en Oncología. Asistente de Ginecoobstetricia. Investigador Agregado. Instituto Nacional de Oncología y Radiobiología (INOR). La Habana, Cuba.
VII Especialista de II Grado en Oncología. Investigador Agregado. Instituto Nacional de Oncología y Radiobiología (INOR). La Habana, Cuba. ]]>
RESUMEN
INTRODUCCIÓN. El cáncer de ovario ocupa el tercer lugar entre los cánceres ginecológicos y a él se debe el 5 % de todas las muertes por cáncer. El objetivo del presente estudio fue conocer la incidencia hospitalaria, la respuesta al tratamiento y la supervivencia global del cáncer de ovario en nuestra institución, durante un quinquenio.
MÉTODOS. Se realizó un estudio retrospectivo, descriptivo, lineal con 192 mujeres con tumores de ovario. Se excluyeron aquellas con tumores benignos o tumores no extirpables, y las que no recibieron tratamiento oncoespecífico o lo recibieron y fueron seguidas en otros hospitales. ]]>
Palabras clave: Cáncer de ovario, incidencia hospitalaria, respuesta al tratamiento, supervivencia global.
ABSTRACT
INTRODUCTION. Ovarian cancer occupies the third place among the gynecological cancers, and it causes 5 % of all the deaths from cancer. The objective of this study is to know the hospital incidence, the response to the treatment and the global survival of ovarian cancer in our institution during a five-year term.
METHODS. A descriptive, retrospective and lineal study was carried out among 192 females with ovarian tumors. Those with benign or non resectable tumors were excluded, as well as the patients that did not receive oncospecific treatment or that received it, but were followed-up in another hospital.
RESULTS. The most affected age groups were in the fifth and sixth decades of life (40.4 %). Mean age was 48 years old. The most common clinical stage was the stage III (261 % of the females). 44.2 % were at stage IIIc. The most frequent histological type was the serous papillary adenocarcinoma (H" 70 %) among the epithelial cancers (49; 94.23 %). The global mean survival of the patients that received surgical treatment was 31 months. At the end of the study, the survival rate was under 40 %. Survival after the 36 months was null among the patients that did not respond to chemotherapy.
CONCLUSIONS. The behavior of ovarian cancer at the National Institute of Oncology and Radiobiology does not differ to much from what is reported by the world medical literature
Key words: Ovarian cancer, hospital incidence, response to treatment, global survival.
]]>
El cáncer de ovario ocupa el tercer lugar entre los cánceres ginecológicos, representa el 4 % de los cánceres de la mujer y a él corresponde la mayor mortalidad entre ellos (5 % de todas las muertes ocasionadas por cáncer). Se presenta en todas las edades, incluidas la niñez y la adolescencia. Su incidencia ha aumentado en las últimas décadas, pero la evolución insidiosa o silente que lo caracteriza entorpece el diagnóstico temprano, lo que hace que más del 60 % de las enfermas se diagnostiquen en etapa avanzada.1-6
En el 2004 en la Unión Europea, se diagnosticaron cerca de 48 000 casos nuevos y murieron 31 000 pacientes;3 en los Estados Unidos se diagnosticaron 25 580 casos nuevos y murieron 16 090 mujeres por su causa.7 La media de la edad al diagnóstico fue de 63 años y el 70 % de las enfermas tenían enfermedad avanzada. Se estimó que en el 2007 en EE. UU. habría 20 180 casos nuevos y que morirían 15 310 mujeres.8 La incidencia aumenta con la edad y la mayor prevalencia se encuentra entre la séptima y la octava décadas de la vida.4,9
La mayoría de los cánceres de ovario se encuentran en la posmenopausia; sólo del 10 al 15 % se presentan en la premenopausia.2,10 Aproximadamente el 70 % son diagnosticados entre los 40 y 70 años de edad. Más del 80 % (≈ 90%) son cánceres epiteliales; el resto deriva de las células germinales y del estroma de los cordones sexuales.1-3,11,12 La incidencia de los tumores de acuerdo con su estirpe histológica varía según la edad. Menos del 1 % de las neoplasias epiteliales de ovario aparecen antes de los 30 años; la mayoría son tumores de células germinales. Alrededor del 20 al 30 % de las neoplasias ováricas encontradas en la posmenopausia son malignas, mientras que sólo el 7 % de las encontradas en las premenopausia lo son.2 El riesgo de desarrollar cáncer de ovario durante la vida de la mujer es de aproximadamente 1,7 %; una de cada 55 mujeres desarrollará cáncer de ovario a lo largo de su vida y aproximadamente 1 de cada 60 mujeres morirá por esta causa. La incidencia es mayor en nulíparas y en mujeres con historia familiar de cáncer de ovario.1,2 La tasa de incidencia es de 15 a 16 × 105 en el grupo etario de 40 a 44 años y asciende hasta 57 × 105 entre los 70 y 74.1,13 La tasa de incidencia del cáncer ovárico es más alta en los países occidentales industrializados4,6 y se estima en torno al 14 × 105. La mortalidad anual por cáncer del ovario es aproximadamente del 65 % de la tasa de incidencia.8 En los países con alta incidencia de cáncer de ovario la supervivencia global (SV) es inferior al 50 % a los 5 años.3 La SV mediana a los 5 años (SV5 años), incluyendo todos los estadios, es de aproximadamente 42 %. La SV5 años en mujeres menores de 45 años es del 70 %, mientras que en las mayores de 75 años es del 20 %.5 La tasa de SV ha mejorado discretamente en los últimos 30 años desde 36 % hasta 45 %.9 La SV5 años de los carcinomas serosos en etapa I es del 70 %, cuando afectan el peritoneo cae al 25 %; la de los endometrioides es del 40 al 50 % y la de los de células claras es casi nula14.
En Cuba, en el 2003, se reportaron 383 casos para una tasa cruda de 8,2 × 105, que aumenta hasta 19,4 en las mayores de 60 años. En el 2005, 219 mujeres murieron por cáncer de ovario; la tasa de mortalidad aumenta cada 5 años a partir de los sesenta años de edad y declina a partir de los 80. Ocupa el octavo lugar entre los cánceres que afectan a la mujer y es la décima causa de muerte entre ellas.5,15
Los carcinomas ováricos epiteliales representan entre el 80 y más del 90 % de todos los cánceres del ovario y son más frecuentes entre las caucásicas. En los Estados Unidos la tasa de incidencia en las mujeres blancas varía entre 12 y 15 × 105 frente a 8 y 10 entre las razas no blancas. La edad mediana al diagnóstico es de 56 años. Los serosos son los más comunes (40 a 50 %), le siguen los carcinomas endometrioides (20 %); los mucinosos, los de células claras y los indiferenciados (5 a 10 %) y los de Brenner, que son muy raros (2 %). Los tumores de células germinales predominan en las mujeres jóvenes y en las niñas; constituyen el 90 % de los tumores prepuberales y el 60 % se presenta antes de los 20 años. Representan menos del 5 % de los cánceres ováricos y el disgerminoma es su variedad más común; el 50 % de estos aparece en mujeres menores de 20 años y el 80 % en menores de 30. Le siguen los tumores del seno endodérmico y el teratoma inmaduro, que representa el 25 % de los tumores germinales y predomina en las dos primeras décadas de la vida. Entre los tumores derivados de los cordones sexuales y del estroma gonadal (8 %) predominan los de células granulosas, los cuales en la mujer adulta tienen un pico de incidencia en los 50 años y aproximadamente el 67 % aparece en la posmenopausia. Constituyen el 95 % de todos los tumores de la granulosa y entre el 1 y el 2 % de todos los tumores ováricos. Las otras variedades son raras.1,6,12,14 ]]>
Cerca del 70 % de las enfermas con cánceres epiteliales se presenta en las etapas III y IV, mientras que el 70 % de las pacientes con cánceres de células germinales acuden en la etapa I.1Son factores de riesgo para el cáncer ovárico: la nuliparidad, la ovulación incesante, (menarquía precoz y menopausia tardía), la infertilidad y la historia personal o familiar de cáncer de mama, ovario y colon.11,12
El cáncer de ovario no es un asesino silencioso. Se ha demostrado que el 95 % de las mujeres tienen síntomas abdominales inespecíficos (malestar abdominopélvico y sensación de llenura), síntomas gastrointestinales vagos (dispepsia, saciedad temprana, meteorismo, cambios del hábito intestinal) y síntomas urinarios (urgencia miccional o polaquiuria), desde muchos meses antes del diagnóstico. A diferencia de los cánceres epiteliales, los de células germinales tienden a provocar dolor intenso cuando están aún confinados al ovario. Los signos más frecuentes son el tumor y la ascitis, pero son tardíos. Se observa derrame pleural en el 10 % de las enfermas y sangrado vaginal anormal en el 30 % de ellas.1,6,7,9,12
El examen ginecológico ultrasonográfico, abdominal y transvaginal, es el estudio más útil para evaluar los tumores ováricos debido a su capacidad de distinguir la morfología del ovario, y con el efecto Doppler se pueden identificar los vasos de neoformación. La sonografía tridimensional amplifica la visualización de la estructura de los ovarios. Los niveles del antígeno CA 125 están elevados en más del 80 % de los cánceres epiteliales, pero en menos de la mitad de los casos en estadios tempranos; los niveles del CA 19-9 están elevados en muchos carcinomas mucinosos; los del antígeno carcinoembrionario, de la α-feto proteína y de la gonadotropina coriónica β se elevan en los cánceres derivados de las células germinales y del estroma.1,2,5,6,12,13
El pronóstico del cáncer de ovario está íntimamente relacionado con la etapa clínica en el momento del diagnóstico. La estadificación es quirúrgica y se realiza utilizando el sistema de la Federación Internacional de Ginecología y Obstetricia (FIGO). Un ejemplo de la importancia de realizar una estadificación adecuada es la presencia de metástasis ganglionares en el 24 % y en el 50 % de los tumores en supuestos estadios I y II, lo que los clasifica correctamente como estadio III. La distribución de los casos en los estadios del I al IV es H" 20 %, 5 %, 58 % y 17 %, respectivamente.8,9,16,17
El tratamiento inicial del cáncer de ovario es quirúrgico. La cirugía óptima pretende reducir la enfermedad macroscópica a lesiones menores de 1 cm, mejor a 0; incluye: panhisterectomía con doble anexectomía, omentectomía y apendicectomía, y pueden agregarse la disección radical de la pelvis, una resección intestinal o hepática segmentaria, la esplenectomía, la denudación del diafragma o una peritonectomía. La citorreducción óptima puede lograrse, en manos experimentadas, en el 90 % de las enfermas y constituye una variable pronóstica independiente para la supervivencia; en manos inexpertas el porcentaje puede caer hasta 20. Una revisión de la literatura médica demostró que las pacientes con citorreducción óptima tuvieron una supervivencia promedio de 39 meses frente a una de solamente 17 meses en las pacientes con enfermedad residual subóptima. Cuando se desee y sea posible conservar la fertilidad, podrá conservarse el útero y el ovario contralateral en pacientes con cánceres epiteliales cuidadosamente seleccionadas, con cánceres germinales o estromales en estadios IA y IB, bien diferenciados (grado 1) de bajo riesgo y en cánceres de bajo potencial maligno «en el límite». Se excluyen los tumores de células claras, los del seno endodérmico y los carcinomas embrionarios, si bien algunos autores incluyen estos dos últimos y los grado 2. Posteriormente, en los cánceres epiteliales, se administrará quimioterapia adyuvante basada en platino + taxano, complementada con aplicaciones intraperitoneales, lo que incrementa la SV (por 16 meses en los estadios III). En los tumores de células germinales la quimioterapia (QTP) consistirá en platino + etopósido + bleomicina; la combinación de platino + taxano puede utilizarse, pero se prefiere en las recaídas. En los cánceres de estirpe estromal puede emplearse indistintamente uno u otro de los esquemas expuestos. Los tumores mesodérmicos müllerianos mixtos (carcinosarcomas) son tumores extremadamente raros que se tratan como los sarcomas uterinos " cirugía + quimioterapia basada en ifosfamida/platino ± radioterapia o, con frecuencia, como los cánceres ováricos epiteliales.1,12,13 En las pacientes con tumores bien diferenciados (grado 1) en estadios IA y IB no se utiliza quimioterapia complementaria, excepto en las sometidas a cirugía conservadora. En los casos considerados no extirpables, a priori o durante la exploración quirúrgica, en los que no se logró la citorreducción óptima y en las pacientes en las que existen contraindicaciones formales para la cirugía en el momento de hacer el diagnóstico, se utilizará quimioterapia neoadyuvante con cirugía de intervalo después de 3 ciclos, o relaparotomía al final del tratamiento citotóxico según sea el caso.1,2,5-9,11-13,17-26
Las pacientes operadas por cirujanos no entrenados en ginecología oncológica requieren un enfoque diferenciado, dependiente de si existen dudas sobre la estadificación y la intervención quirúrgica (IQ) realizada. Generalmente es necesario reintervenir a la enferma para estadificarla correctamente, completar una IQ incompleta u optimizar la cirugía, después de lo cual, o si no existen dudas, se someten al tratamiento habitual con las mismas consideraciones. Sin embargo, en algunos casos se puede iniciar la quimioterapia (QTP) indicada y realizar citorreducción de intervalo, o llevar cabo al final del tratamiento una laparotomía «de revisión» o una relaparotomía para completar la cirugía óptima [Colectivo de autores. Guía para el tratamiento del cáncer ovárico. INOR. La Habana, 2007].13
La mayoría de las mujeres tratadas con esta sistemática terapéutica logran una remisión clínica, pero lamentablemente, la mayoría de ellas sufrirá una recaída y sucumbirá por la enfermedad. La persistencia y las recidivas son muy frecuentes en los cánceres epiteliales del ovario; ocurren en la mayoría de las enfermas, y se encuentra una persistencia en el 75"85 % de las mujeres tratadas (H" 20 % sin respuesta alguna) y recurrencia hasta en el 50 % después de una relaparotomía negativa. El 80 % de las mujeres con recidiva tienen enfermedad macroscópica susceptible de citorreducción quirúrgica. La quimioterapia es el arma fundamental para tratar la enfermedad persistente o recurrente; lo primero es determinar si la paciente es sensible al platino o, por el contrario, resistente al platino: se consideran sensibles al platino las mujeres cuya enfermedad recurre después de 6 meses de terminar el tratamiento. En estas enfermas el tratamiento estándar continúa siendo platino + paclitaxel o gemcitabina, u oxaliplatino + docetaxel. En las pacientes con resistencia, los fármacos más utilizados son los taxanos, el topotecán, la gemcitabina, la altretamina, la doxorrubicina liposomal, el etopósido, la vinorelbina y la ifosfamida; generalmente utilizados como agentes únicos.
Varios nuevos fármacos se encuentran en ensayos clínicos: bevacizumab, canfosfamida, trabectedina, etc.1,2,5,6,8,9,13,27-2
En caso de tumores de células germinales las persistencias y recurrencias se tratan con platino + ifosfamida + paclitaxel o etopósido o vinblastina. Cuando se trate de tumores derivados de células del estroma, otra vez puede elegirse entre los esquemas diseñados para los de células germinales o los correspondientes a los cánceres epiteliales.13,23 ]]>
Se realizó un estudio retrospectivo, descriptivo, lineal, de las pacientes con diagnóstico histopatológico de cáncer de ovario que recibieron tratamiento oncoespecífico en el INOR, en el quinquenio comprendido entre el 2001 y el 2005. De las 192 mujeres con diagnóstico de tumores de ovario, se excluyeron aquellas con tumores benignos (101), con tumores no extirpables y las que no recibieron tratamiento oncoespecífico o lo recibieron o fueron seguidas en otros hospitales (49).
Nuestro universo y muestra quedaron constituidos por 52 enfermas de cuyas historias clínicas obtuvimos los datos siguientes: edad al diagnóstico, diagnóstico histopatológico, etapa clínica, cirugía realizada (óptima o no óptima), esquema de quimioterapia utilizado (con o sin taxanos), tipo de respuesta objetiva (completa o parcial) y última notificación del estado del paciente. Los datos se tabularon y se analizaron, y se compararon con los de la literatura médica. Para el análisis se utilizaron medidas de resumen para datos cualitativos (tasas, porcentajes y razones) y cuantitativos (media aritmética, desviación estándar), y se aplicó la prueba de ji al cuadrado en los casos necesarios. Las funciones de supervivencia fueron estimadas por el método de Kaplan Meier y contrastadas con la prueba de Log Rank. Además, se determinaron las medianas de la supervivencia y los intervalos de confianza (95 %) correspondientes. Se empleó un nivel de significación de 0,05 en las estadísticas de inferencias. En algunos casos la información se presenta resumida en gráficos.
Para la confección del trabajo y el análisis de los datos utilizamos los programas de Microsoft Office Professional Edition, versión 11 (2003) y SPSS v11,5 para Windows.
RESULTADOS
En el período analizado se atendieron en el Servicio de Ginecología del INOR 3732 mujeres. Fueron inscritas 192 pacientes (5,1 %) con el diagnóstico clínico e imagenológico de tumor de ovario; 91 de ellas (47,4 %) fueron diagnosticadas histológicamente como cánceres de ovario. La incidencia promedio fue de 2,4 × 102, con fluctuaciones entre 1,3 y 7,2. ]]>
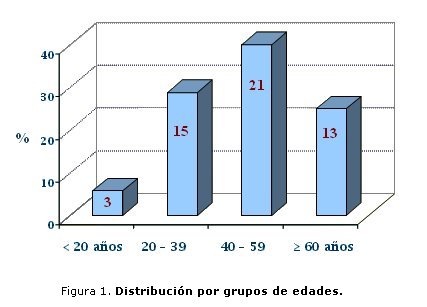
El grupo etario más afectado fue el comprendido entre los 40 y los 59 años (quinta y sexta décadas de la vida) y el menos afectado el de las menores de 20 años (figura 1). La edad media fue de 48,04 años con una desviación estándar de 14,44 años (de la cuarta a la séptima décadas).
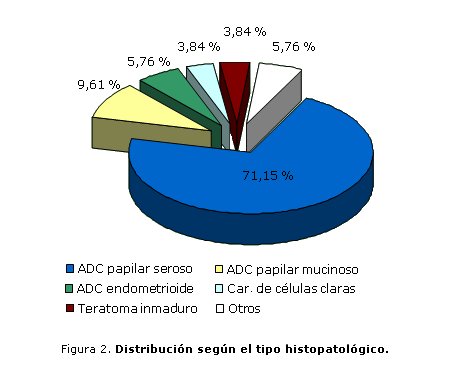
Los cánceres más frecuentes fueron los epiteliales (49; 94,23 %) y entre ellos, el adenocarcinoma papilar seroso (37; 71,15 %) (figura 2). Solo 3 no eran epiteliales: un teratoma inmaduro, un tumor de células granulosas y un disgerminoma.
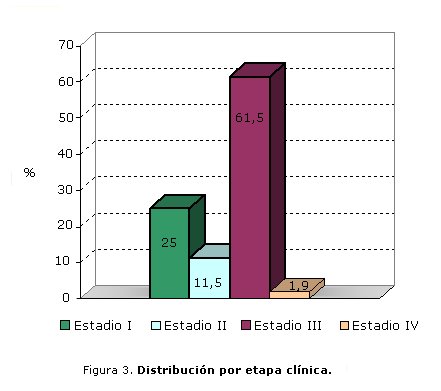
La mayor parte de las pacientes estaban en estadio III (32; 61,54 %); de ellas 23 (44,23 %) en etapa IIIc (figura 3).
La supervivencia global media de las pacientes con cáncer de ovario fue de 31 meses (IC al 95 % de 17 45) con una tasa de supervivencia a los 36 meses de 35,1 %. ]]>
La supervivencia media en pacientes con cáncer de ovario en las cuales se logró la cirugía óptima fue de: 34 meses (IC 95 %: 28 39), y la tasa de supervivencia a los 36 meses del 75,7 %; con cirugía no óptima la media fue de 23 meses (IC 95 %: 13 33) y la tasa de supervivencia a los 36 meses del 15,3 %. La diferencia entre los dos grupos fue estadísticamente significativa (p = 0,0277).
En nuestra serie, 30 enfermas (57,69 %) mostraron respuesta completa a la QTP entre ellas, en 25 (83,33 %) se había logrado la cirugía óptima. Hubo 10 mujeres que mostraron progresión de la enfermedad en 8 de ellas no se logró realizar la cirugía óptima. El resto de las pacientes mostró una respuesta parcial.
La supervivencia media en pacientes con respuesta a la QTP fue de 35 meses (IC 95 %: 31 40) y en las pacientes sin respuesta, de 16 meses (IC 95 %: 12 20) (p = 0,0000). La tasa de supervivencia a los 36 meses, en las primeras, fue de un 76,5 %; mientras que en el grupo de pacientes sin respuesta no hubo sobrevivientes.
La supervivencia media en pacientes con cirugía óptima y respuesta a la QTP fue de 36 meses (IC 95 %: 32 41), con una tasa de supervivencia del 85,9%. En el grupo de pacientes con cirugía óptima sin respuesta a la QTP la supervivencia media fue de 12 meses (IC 95 %: 0 24) y no hubo sobrevivientes a los 36 meses (p = 0,0012). Por otro lado, la supervivencia media en pacientes con cirugía no óptima y respuesta a la QTP fue de 31 meses (IC 95 %: 21 41) con una tasa del 53,3 % a los 36 meses; mientras que en pacientes sin respuesta fue de 16 meses (IC 95 %: 14 18) y no hubo sobrevivientes a los 36 meses.
En nuestro estudio 29 enfermas (55,77 %) recibieron QTP sin taxanos y el resto (23; 44,23 %) con ellos. Se obtuvo respuesta completa en 17 (73,91 %) de las pacientes tratadas con taxanos y solo en 13 (44,83 %) de las tratadas sin ellos. En las primeras, la supervivencia media fue de 33 meses (IC 95 %: 27 39) con una tasa de supervivencia a los 36 meses de 61,2 %; y en las otras, la supervivencia media fue de 23 meses (IC 95 %: 9 37), con un 39,4 % de sobrevivientes a los 36 meses; la diferencia, sin embargo, no fue estadísticamente significativa (p = 0,1036).
DISCUSIÓN
El incremento de la incidencia promedio se debió al menor número de casos atendidos, así como al mayor número de mujeres remitidas desde los consultorios de los médicos de familia y otros hospitales, y también, por la asistencia espontánea de pacientes de otras provincias. ]]>
La distribución etaria se corresponde, en parte, con lo reportado en la literatura médica, pero los anglosajones encuentran mayor incidencia en edades más tardías, así como una edad media más avanzada.1,2,5-9,11-13,17,29La literatura médica revisada concuerda con el predominio de los cánceres epiteliales, aunque en nuestra serie la proporción de adenocarcinomas papilares serosos es superior a la generalmente reportada.1,2,5-9,11-13,17,29,30
Todos los autores concuerdan en que el cáncer ovárico epitelial se diagnostica en etapas tardías de su evolución. Como se aprecia en el siguiente cuadro, resalta la mínima cantidad de mujeres diagnosticadas en estadio IV lo que ha de deberse, entre otros factores, a las bondades de nuestro sistema de salud.1,2,5"9,12,14,19
Cuadro. Diagnóstico del cáncer ovárico epitelial
según datos de la literatura médica internacional e INOR
| Etapa | I | II | III | ]]> IV |
| Literatura médica | 20,0 | 5,0 | 58,0 | 17,0 |
| INOR | 25,0 | 11,5 | 61,5 | ]]> 1,9 |
Empero, solo menos del 40 % de los cánceres epiteliales del ovario se curan.13 No ocurre así con los tumores derivados de células germinales y con los tumores del estroma que tienen mayor tasa de curabilidad.1,2,6,12,13,17,20,23 La tasa de supervivencia a los 36 meses está por debajo de la SV reportada en la bibliografía revisada. Se estima que la SV5 años está en torno al 80-90 % para los estadios I, 40-60 % para los estadios II, 10-20 % para los III y < 5 % para los IV (etapa I - 73 %; etapa II - 45 %; etapa III - 21 %; etapa IV < 5 %); aunque algunos consideran que es mayor, 80 a 95 %, en las etapas I y II, y menor de 10 a 30 % en las III y IV.2,7,9
La diferencia significativa que, en cuanto a supervivencia, existe entre las pacientes con cirugía óptima en comparación con la no óptima, con respuesta completa a la QTP en comparación a la ausencia de respuesta, y entre las que tenían cirugía óptima + respuesta completa frente a las otras combinaciones posibles, confirman en menor escala la validez del arquetipo para el tratamiento del cáncer ovárico derivado de células epiteliales.
En resumen, nuestros resultados en cuanto a distribución etaria, frecuencia de tipos histológicos y estadio al inicio, confirman lo reportado en la literatura médica. También confirman la validez del arquetipo terapéutico de los cánceres ováricos epiteliales. La SV5 años es menor que la reportada en la bibliografía revisada.
REFERENCIAS BIBLIOGRÁFICAS
1. Parlan BY, Markman MA, Eifel PJ. Ovarian Cancer, Peritoneal Carcinoma, and Fallopian Tube Carcinoma. In: DeVita VT Jr. Hellman S, Rosenberg SA (Eds.) Cancer: Principles & Practice of Oncology. 7th Edition. Philadelphia: Lippincott Williams & Wilkins; 2005. CD-ROM Edition.
2. Mendiola C, Gómez H, Martínez-Salmeán J, Martín Lf, Ojeda B. Cáncer De Ovario. En: Cortés H, Díaz E, García J, Germà JR, Guillem V, López JJ, Moreno JA, Pérez G, (Editores). Oncología Médica 1ª Edición. Madrid: Nova Sidonia Oncología (Grupo Aula Médica, S.A.); 2000. Edición en CD-ROM
3. Globocan Database. 2004 Available on internet at: http://www-dep.iarc.fr/globocan/database.htm
4. American Cancer Society Inc. Cancer Facts & Figures 2006. Atlanta, 2006. Available on internet at: http://www.cancer.org/downloads/STT/CAFF2006PWSecured.pdf
5. Pérez M. Ginecología Oncológica Pelviana. Primera Parte. 1ª Edición. La Habana: Editorial Ciencias Médicas; 2006.
6. Helm CW, Edwards RP. Malignant Lesions of the ovaries. WebMD. [Monograph on internet] 2005; Available at: http://www.emedicine.com/med/topic3306.htm .
7. Cannistra SA. Cancer of the ovary. N Engl J Med 2004;351:2519-29.
8. National Cancer Institute. Cáncer epitelial de los ovarios (PDQ®). USA National Institutes of Health. [monograph on internet] 2008; Available at: http://www.nci.nih.gov/cancertopics/pdq/treatment/ovarianepithelial/healthprofessional/allpages
9. García AA. Ovarian Cancer. WebMD. [Monograph on internet] 2007; Available at: http://www.emedicine.com/med/topic1698.htm .
10. Fernández del Castillo C. Cáncer Genital Femenino. Programa de Actualización Continua en Ginecología y Obstetricia. 1ª Edición. Intersistemas S.A. de C.V. Mexico; 1998. [Monografía en Internet]. Disponible en: http://www.drscope.com/pac/gineobs/g8/g8_pag45.htm#ovario
11. del Carmen MG. Primary Epithelial Ovarian Cancer: Diagnosis and Management. In: Perry MC (Ed). Am Soc Clin Oncol Ed Book; 2006. CD-ROM Edition.
12. Cass I, Karlan BY. Neoplasms of the Ovary and Fallopian Tube. In: Scott JR, Gibbs RS, Karlan BY, Haney AF, Danforth DN (Eds). Danforth's Obstetrics and Gynecology. 9th Ed. . New York: Lippincott Williams & Wilkins Publishers; 2003.
13. Morgan RJ Jr, Álvarez RD, Armstrong DK, Boston B, Chen Lee-may, Copeland L, Fowler J, et al. Ovarian Carcinoma. NCCN Practice Guidelines in Oncology. [Monograph on internet] 2007. Available at: http://www.nccn.org
14. Crum CP. Aparato Genital Femenino. En: Robbins' Patología Estructural y Funcional. Capítulo 23°. 5ª ed. Madrid: Mc Graw-Hill Interamericana de España S.A. Editores; 1995.
15. MINSAP. Anuario Estadístico. [monografía en Internet]. Disponible en: http://bvs.sld.cu/cgi-bin/wxis/anuario
16. Green FL, Compton CC, Fritz AG, Shah JP, Winchester DP. AJCC Cancer Staging Atlas. 1ª ed. New York: Springer Science plus Business Media, LLC.; 2006.
17. Ibáñez E, Rdez-Escudero FJ. Clínica, Diagnóstico y tratamiento de los Tumores Ováricos Malignos. En: Cabero-Roura L. Tratado de Ginecología, Obstetricia y Medicina de la Reproducción. 1ª Edición. Capítulo 196. Sociedad Española de Ginecología y Obstetricia. Barcelona: Editorial Médica Panamericana; 2003.
18. Vermorken JB. Intraperitoneal chemotherapy in advanced ovarian cancer: recognition at last. Ann Oncol 2006;17(Suppl 10):2416.
19. Krasner CN. New Approaches for Intraperitoneal Therapy. In: Perry MC (Ed). Am Soc Clin Oncol Ed Book; 2006. CD-ROM Edition.
20. Colombo N, Parma G. Sex-Cord Stromal Tumors. In: Govindan R (Ed). Am Soc Clin Oncol Ed Book; 2007. CD-ROM Edition.
21. Sugiyama T, Fujiwara K. Clear Cell Carcinoma of the Ovary. In: Govindan R (Ed). Am Soc Clin Oncol Ed Book; 2007. CD-ROM Edition.
22. Armstrong DK, Bundy B, Wenzel L, Huang HQ, Baergen R, Lele S, Copeland LJ, et al. Intraperitoneal Cisplatin and Paclitaxel in Ovarian Cancer. N Engl J Med 2006;354:34-43.
23. Gershenson DM. Management of Ovarian Germ Cell Tumors. J Clin Oncol 2007;25:2938-43.
24. Pomela C, Jeyarajaha A, Orama D, Shepherda J, Millikena D, Dauplatb J, Reynoldsa K. Cytoreductive Surgery in Ovarian Cancer. Cancer Imaging 2007;7:210-5.
25. Morrison J, Swanton A, Collins S, Kehoe S. Chemotherapy versus surgery for initial treatment in advanced ovarian epithelial cancer. Cochrane Database of Systematic Reviews 2007; Issue 4. Art. Nº: CD005343.
26. Chi DS, Ramirez DT, Teitcher JB, Mironov S, Sarasohn DM, Iyer RB, Eisenhauer EL, et al. Prospective Study of the Correlation Between Postoperative Computed Tomography Scan and Primary Surgeon Assessment in Patients With Advanced Ovarian, Tubal, and Peritoneal Carcinoma Reported to Have Undergone Primary Surgical Cytoreduction to Residual Disease 1 cm or Less. J Clin Oncol 2007;25:4946-51.
27. Modesitt SC, Jazaeri AA. Recurrent epithelial ovarian cancer: pharmacotherapy and novel therapeutics. Expert Opin Pharmacother 2007;8(14):2293-305.
28. E. A. Eisenhauer EA. New targets and non-cytotoxics in ovarian cancer. Ann Oncol 2006;17(Suppl 10):247-50.
29. Sessa C, De Braud F, Perotti A, Bauer J, Curigliano G, Noberasco C, Zanaboni F, et al. Trabectedin for women with ovarian carcinoma after treatment with platinum and taxanes fails. J Clin Oncol. 2005 Mar 20;23(9):1867-74.
30. Naora H. The heterogeneity of epithelial ovarian cancers: reconciling old and new paradigms. Expert Rev. Mol. Med 2007;9(13):1-12.
]]>
Juan Edmundo Rodríguez Reigosa. Calle 19 núm. 1160, Apto. 4 entre 16 y 18. El Vedado. CP 10400. La Habana, Cuba. ]]>