Adenocarcinoma gástrico y tumor estromal del estómago sincrónico incidental
Gastric adenocarcinoma and incidental synchronous incidental gastrointestinal stromal tumor
José Luis Guerra Mesa, Janet Lamadrid García, Ivanis Ruíz Calderón
Servicio de Cirugía Esplácnica. Instituto Nacional de Oncología y Radiobiología. La Habana. Cuba.
]]>
RESUMEN
Se presenta el caso de un paciente masculino de 73 años de edad operado por adenocarcinoma del antro gástrico. Se practicó gastrectomía subtotal distal más linfadenectomía D2. Durante el examen anatomopatológico de la pieza quirúrgica se encontró otro tumor pequeño en el espesor de la pared del antro cubierto por mucosa normal, separado del adenocarcinoma. El análisis histológico confirmó otra neoplasia incidental sincrónica, un tumor del estroma gastrointestinal de tipo fusiforme, positivo para el marcador tumoral CD117. El objetivo del trabajo es presentar esta asociación tumoral sincrónica, revisar sus características y las teorías etiopatogénicas actuales de esta condición sincrónica según la literatura especializada.
Palabras clave: adenocarcinoma gástrico; tumor estromal gastrointestinal; tumores sincrónicos; gastrectomía; quimioterapia perioperatoria.
ABSTRACT
A case is presented of a 73-year-old male patient who was operated for a gastric adenocarcinoma of the antrum. A distal subtotal gastrectomy plus D2 lymphadenectomy were practiced. During the anatomic and pathologic examination of the surgical piece, a second tiny tumor was found in the wall of the antrum and that was covered with a normal mucosa separated from the adenocarcinoma. The histologic examination confirmed another synchronous incidental neoplasm, a spindle-cell gastrointestinal stromal tumor, positive for the tumor marker CD117. This paper is aimed at presenting synchronous tumor entity, to review its characteristics and the current etiologic and pathogenic theories of this synchronic condition according to the specialized literature.
Keywords: gastric adenocarcinoma; gastrointestinal stromal tumor; synchronous tumors; gastrectomy; perioperative chemotherapy.
]]> INTRODUCCIÓN
El término tumor del estroma gastrointestinal (GIST, por sus iniciales en inglés) fue enunciado por Mazur y Clark en 1983.1 Los adenocarcinomas gástricos representan el 95 % de las neoplasias malignas del estómago.2 El GIST es el tumor mesenquimal más frecuente del tractus gastrointestinal, representa entre 0,2 % y 1 % de los cánceres que en él se originan, con una incidencia estimada de 10 a 20 por millón de habitantes. La mayoría de los GIST (60-70 %) asientan en el estómago.3-6 Los GIST gástricos y los adenocarcinomas del estómago se originan en distintas capas del órgano. Los primeros derivan de una célula madre, precursora de las células intersticiales de Cajal, situadas, estas últimas, en la capa muscular en toda la longitud del tubo digestivo,7,8 los segundos se originan en las glándulas del estrato mucoso del estómago. Los GIST se clasificaron como una entidad individual a partir del descubrimiento mediante inmunohistoquímica del gen c-kit (CD117) en la década de 1990.9 El primer caso de tumor sincrónico epitelial y estromal del estómago fue descrito en el año 2000.10
PRESENTACIÓN DE CASO
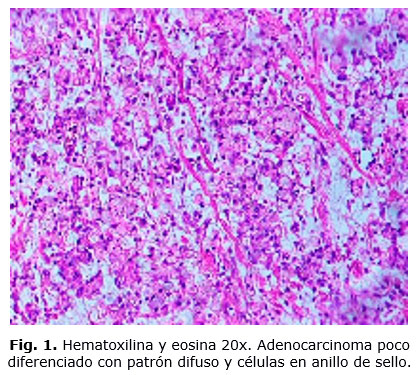
Paciente masculino, blanco, de 73 años de edad, con antecedentes de padecer hipertensión arterial. Acudió al Instituto Nacional de Oncología y Radiobiología por síntomas digestivos del tipo de dispepsia, epigastralgia, plenitud gástrica, náuseas, y además pérdida de peso de 5 kg en un término de seis meses. En el examen físico practicado sólo se encontraron las características de un hombre de la tercera edad aparentemente sano. Los estudios que evalúan al paciente de manera general y los de extensión neoplásica fueron normales. La panendoscopia de tractus digestivo superior mostró una lesión ulcerada sin convergencia de los pliegues gástricos hacia dicha lesión y zona rígida periulcerosa. Esta lesión estaba situada en el tercio inferior del estómago, en su curvatura menor, se extendía hacia las caras anterior y posterior del antro, de tipo III de la clasificación macroscópica de Borrmann.11 La biopsia endoscópica arrojó como resultado la presencia de un adenocarcinoma gástrico de tipo difuso, pobremente diferenciado con células en anillo de sello, según las clasificaciones de Lauren12 y las de los tumores del estómago propuestas por la Organización Mundial de la Salud.13
El plan terapéutico consistió en quimioterapia perioperatoria a base de 5-fluoruracilo en infusión continua de 24 h durante cinco días con cisdimetildiaminoplatino más cirugía. La operación quirúrgica consistió en una gastrectomía subtotal distal junto con omentectomía mayor y menor y linfadenectomía regional tipo D2 de los grupos ganglionares números 1, 3, 4, 5, 6, 7, 8, 9, 11p y 12a. El restablecimiento de la continuidad digestiva se hizo mediante técnica de Billroth II, con anastomosis gastroyeyunal antecólica, tipo Polya junto con anastomosis yeyunal laterolateral de Braun. El informe anatomopatológico de la pieza quirúrgica corroboró el diagnóstico de la biopsia endoscópica (Fig. 1).
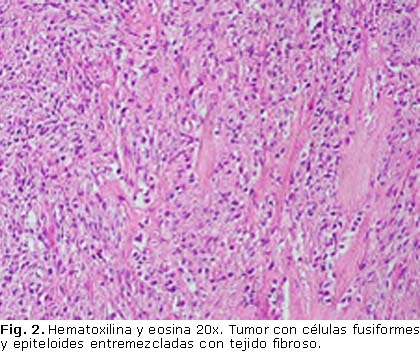
Fueron extirpados diez grupos ganglionares regionales para un total de 27 ganglios linfáticos con un solo ganglio metastásico del grupo número 5 producido por el adenocarcinoma gástrico. No se identificaron ganglios metastásicos a consecuencia del GIST gástrico sincrónico. Durante el examen macroscópico del estómago los patólogos encontraron otra lesión en el espesor de la pared gástrica de 8 mm de diámetro mayor, cubierta por mucosa normal, situada también en el antro, e independiente del adenocarcinoma. El estudio microscópico reveló un GIST con patrón celular fusiforme y epitelioide (Fig. 2).
Los análisis de inmunohistoquímica confirmaron el diagnóstico con el marcador tumoral CD117 positivo (Fig. 3), con un Ki67 menor de 5 % y un índice mitótico de menos de 5 mitosis por cada 50 campos de gran aumento.
]]>
Se logró una resección R0. La estadificación posquirúrgica se realizó atendiendo a los sistemas TNM de la Asociación Japonesa para el cáncer g ástrico14 y del Instituto Nacional de Cáncer de los Estados Unidos de Norteamérica:15 el adenocarcinoma gástrico se clasificó como pT2 N1 M0 (P0, H0, CY0), estadio IIA y el GIST gástrico como pT1 N0 M0 con bajo índice mitótico, estadio IA.
DISCUSIÓN
En años recientes, la ocurrencia de tumores sincrónicos de diferentes histologías originados en el mismo órgano se ha reportado con más frecuencia. Los GIST sincrónicos con adenocarcinomas gástricos es una de estas asociaciones. Los GIST reportados de manera sincrónica con otras neoplasias del tracto gastrointestinal incluyen: adenocarcinomas gástricos, linfomas, cánceres de esófago, de colon, de páncreas, el hepatocarcinoma y los tumores carcinoides. La asociación sincrónica con los adenocarcinomas de estómago es la más frecuente, 47 %.16,17 Cuando se analizan grupos de pacientes de GIST sincrónicos con otros cánceres del tubo digestivo y de GIST aislados, se encuentra que los GIST más pequeños y con bajo o muy bajo riesgo de comportamiento maligno son más frecuentes en el grupo sincrónico que en el de los GIST aislados.18 Los síntomas de los GIST dependen del tamaño del tumor y de su localización en el tubo digestivo. Los GIST son sintomáticos en 60 % de los casos.8,19 Las manifestaciones clínicas pueden ser de diferente tipo. Los clínicamente manifiestos habitualmente son mayores de 2-3 cm de diámetro y se pueden presentar con sangrado digestivo, dolor, anemia, masas abdominales palpables, e incluso síntomas de abdomen agudo en los ancianos.20 En los pacientes con GIST sincrónico con adenocarcinoma gástrico, los síntomas del GIST están a menudo enmascarados por los síntomas del adenocarcinoma gástrico, debido al pequeño tamaño del GIST gástrico sincrónico.17 Este último concepto es completamente aplicable a nuestro caso.
El diagnóstico preoperatorio de los GIST es particularmente difícil.16 En un estudio de Shen y otros sólo 3 casos (4,92 %) de 61 pacientes con GIST sincrónicos asintomáticos con otros cánceres del tubo digestivo pudieron ser diagnosticados de forma preoperatoria. Du21 y Ferreira,22 en investigaciones individuales y separadas, señalan que la mayoría de los GIST sincrónicos (95,7 %) se descubrieron accidentalmente durante la cirugía de otros cánceres gastrointestinales. Sólo 4,3 % de los GIST coexistentes se identificaron durante los estudios preoperatorios.
]]> Por ese motivo, siempre se debe hacer una búsqueda cuidadosa de GIST sincrónicos durante otras cirugías por cánceres gastrointestinales. Zhou señala que la mayoría de sus 13 casos de GIST sincrónicos con otros cánceres del tubo digestivo se diagnosticaron de forma posoperatoria.23 El diagnóstico de los GIST a menudo es incidental en el curso de los estudios imagenológicos, durante la cirugía o en el examen anatomopatológico de las piezas quirúrgicas. Esta última situación está reportada en la serie de Ferreira y otros23 y fue la que ocurrió en nuestro caso. La TAC es uno de los estudios más importantes para la evaluación de los tumores sólidos. Los GIST de estómago, menores de 1 cm de diámetro, no pueden ser detectados con la tomografía axial computarizada (TAC) preoperatoria, porque estos tumores son difíciles de diferenciar de los ganglios linfáticos metastásicos perigástricos, lo que sólo puede ser confirmado mediante análisis histológico. Las características individuales de los GIST y de las adenopatías regionales metastásicas de los carcinomas gástricos, que son un hallazgo significativamente más común, se sobreponen. Por eso, la TAC no puede diferenciar de forma correcta y confiable entre ambos basada en el tamaño o las características de sus contornos solamente.24Se han propuesto disímiles hipótesis que tratan de explicar la génesis de la coincidencia de los GIST con los adenocarcinomas gástricos. Estas hipótesis incluyen las relacionadas con la predisposición genética, factores de riesgo ambiental, efecto mutagénico de la quimioterapia y la radioterapia previa, infección por Helicobacter pylori, gastritis crónica atrófica y hallazgos coincidentes.10,25-27
Se ha especulado que el Helicobacter pylori está relacionado con la génesis de los adenocarcinomas gástricos.28 Otros han dicho que no existe evidencia de su vinculación con la génesis de los GIST.29 Las mutaciones genéticas de los tejidos gástricos vecinos afectados por un carcinógeno común a ambas neoplasias es otra hipótesis reportada en la literatura, así como una desregulación genética combinada parece estar involucrada en la patogenia de estas dos entidades.18 En el caso de la hipótesis del gen común parece ser que este afecta de forma diferente al tejido mesenquimal y al epitelial, ya que en esta asociación sincrónica los adenocarcinomas gástricos están en un estadio mucho más avanzado que los GIST porque estos últimos tienen menor tamaño con muy bajo potencial para transformación maligna. Kawanowa y otros analizaron 100 casos de cáncer gástrico; ellos encontraron una alta incidencia de GIST microscópicos (35 %), sugiriendo que otros cambios genéticos, además del gen c-kit, sean necesarios para su evolución hacia la malignidad. Estas alteraciones están probablemente involucradas también en la génesis de los carcinomas gástricos.
Se sugiere igualmente que la coexistencia de estas neoplasias puede ser atribuida a mutaciones de genes metalotionínicos. Su ausencia reduce la oncosupresión celular necesaria para bloquear el surgimiento y la progresión de los GIST, así como de otros tumores epiteliales.30-32 Liszka y otros encontraron que el riesgo de invasión y que el diámetro de los GIST sincrónicos incidentales con carcinomas gástricos era menor que el de los GIST aislados. Los pequeños GIST sincrónicos incidentales eran de muy bajo riesgo y consideraron que la biología de los GIST sincrónicos podría estar inhibida por el cáncer gástrico.33 Esto no pasa de una mera teoría aún no comprobada.
También se ha planteado la posibilidad de que estos GIST se originen de una célula progenitora capaz de diferenciarse hacia linajes mesenquimales y epiteliales. Otra posible explicación del sincronismo, es que los factores carcinógenos ambientales pudieran afectar vías moleculares compartidas tanto por las células mesenquimales como por las epiteliales del tubo digestivo.22 Sin embargo, hasta el momento, a falta de evidencias certeras, la simple coincidencia parece ser la explicación más probable.
En relación con la incidencia de los GIST y adenocarcinomas gástricos sincrónicos, Liu muestra en un estudio retrospectivo que la coexistencia de GIST gástricos con adenocarcinomas de estómago ocurrió en 9,96 % (24/241) de los pacientes con GIST gástricos.17 Ferreira señala que de seis casos de GIST sincrónicos con otros cánceres digestivos, 3 (50 %) se asociaron al de estómago.24 Varios autores señalan que el por ciento de los pacientes con GIST que es diagnosticado de forma sincrónica con otro cáncer digestivo está en el rango de 17,1 a 37,9 %.19,34,35
Otros autores son más categóricos al plantear que hasta el momento no se ha determinado la incidencia exacta de la coexistencia de los GIST con otros carcinomas.20,24 La mayoría de las publicaciones, tratan sobre reportes de casos aislados y algunas pocas, con series de pocos pacientes. Por ello, la incidencia exacta de la asociación sincrónica entre los GIST y los carcinomas gástricos no ha sido aún determinada con exactitud. Aunque según lo reportado, parece ser que este fenómeno no es tan aislado como generalmente se considera.
Los GIST pueden aparecer en cualquier parte del estómago, pero la mayoría de los GIST sincrónicos incidentales se han reportado en el antro,2,18,21,35 tal como sucedió en nuestro paciente. El tamaño de los GIST sincrónicos varía entre 2 mm y 7,5 cm de diámetro, pero el diámetro promedio de los GIST sincrónicos incidentales es de 8,5 mm.18-20 El de nuestro caso tenía 8 mm. Los GIST gástricos sincrónicos con los carcinomas de estómago ocurren en ambos sexos, pero son más frecuentes en pacientes masculinos de edad avanzada con una edad promedio de 72 años y un rango de entre 60 y 86 años.17,21,24,36 Nuestro paciente es un hombre de 73 años de edad.
Se ha reportado que el subtipo histológico de los adenocarcinomas gástricos sincrónicos con GIST de estómago más frecuentemente encontrado es el poco diferenciado con células en anillo sello, aunque todavía se necesita investigar un mayor número de pacientes para que esta afirmación tenga más certeza. El adenocarcinoma gástrico de nuestro paciente también era de tipo difuso, pobremente diferenciado con células en anillo se selló.24 En el estudio de Liu Z. y otros de coexistencia de GIST y adenocarcinomas gástricos, 93,3 % (14/15) de los GIST tuvo un bajo índice mitótico de menos de 5/50 campos de gran aumento y un Ki67 menor de 5 %. El caso que presentamos tuvo idénticas características.17 El porciento de metástasis ganglionares regionales producidas por los GIST se estima en el rango de entre 1 y 3.4 %.37-39 Nuestro paciente no tuvo metástasis ganglionares regionales derivadas del GIST, sino sólo una derivada del adenocarcinoma gástrico, que es la situación más frecuente.
Si bien los GIST son tumores poco frecuentes en la práctica clínica, existen indicios que hacen pensar que no sean tumores tan poco frecuentes; sino que puede suceder, entre otras muchas hipótesis posibles, que una vez aparecidos tengan un muy lento desarrollo o que necesiten de otros estímulos para su crecimiento ulterior una vez que ya se originaron. Entre algunos reportes que tratan este aspecto está el de Kawanowa y otros que encontraron GIST microscópicos sincrónicos en 35 % de piezas quirúrgicas de gastrectomías por adenocarcinomas gástricos.32 Agaimy y otros descubrieron GIST microscópicos en 22,5 % de pacientes de 50 años de edad o mayores, en varias series de autopsias consecutivas.14
]]> En el caso de los tumores sincrónicos, los planes terapéuticos en ocasiones tienen que ser cambiados en relación a como hubieran sido aplicados si estos mismos tumoreshubieran sido metacrónicos. Esta decisión estará determinada por varios factores entre los que se encuentran: el estadio clínico, el tipo histológico, el índice de estado general del paciente, el conocido comportamiento biológico de cada uno de estos cánceres.
En el caso que nos ocupa se continuó, después de la gastrectomía, con la segunda fase de la quimioterapia perioperatoria planificada para el adenocarcinoma gástrico, por tener un estadio avanzado (pT2 N0 M0, estadio IIA). El GIST encontrado de forma incidental fue clasificado como de bajo grado de malignidad, por lo que no requirió tratamiento adyuvante alguno, sino sólo vigilancia durante el seguimiento periódico estipulado para su estadio clínico, pT1N0 M0, estadio IA.
El Instituto Nacional de Cáncer de los Estados Unidos de Norteamérica señala que todos los GIST de 2 cm o más en su diámetro mayor deben ser resecados. Sin embargo, el manejo de los GIST menores de 2 cm, encontrados incidentalmente, aún permanece en discusión.15 No es frecuente descubrir los GIST sincrónicos de menos de 2 cm de diámetro durante una gastrectomía; si es encontrado, no debe dudarse en su resección en ese acto quirúrgico, ya sea incluido en el segmento gástrico a resecar o mediante una resección en cuña de la pared gástrica que incluya al GIST, independiente del segmento de estómago a resecar por el carcinoma. No se requieren amplios márgenes de resección para lograr bordes de sección quirúrgica negativos, dado que los GIST tienden a crecer localmente o hacia fuera del estómago, más que infiltrando difusamente la pared gástrica.
Consideramos que estos tumores no deben dejarse sin extirpar por dos razones principales: aunque los GIST de menos de 2 cm de diámetro exhiben un bajo o muy bajo riesgo de progresión hacia la malignidad, no se puede excluir su potencial maligno. Por otro lado, en caso de crecimiento ulterior su resección estará dificultada por la fibrosis y las adherencias intraabdominales secuelas de la gastrectomía previa por el adenocarcinoma. Los GIST gástricos sincrónicos incidentales con adenocarcinomas de estómago habitualmente son pequeños, asintomáticos, con bajo o muy bajo potencial maligno y su probabilidad de recidiva es nula o como mínimo considerablemente más baja que la de los adenocarcinomas gástricos sincrónicos. Por esta razón, los GIST sincrónicos incidentales no deben ser tratados de manera adyuvante con inhibidores de la tirosin quinasa, para no interferir con el tratamiento complementario de quimioterapia, o de radioterapia más quimioterapia de los adenocarcinomas gástricos sincrónicos. Pero como tienen potencial para transformación maligna, es necesario el seguimiento estrecho de estos pacientes. El perfeccionamiento futuro de los sistemas de estratificación de riesgo incrementará la precisión de estos sistemas para predecir la recidiva, lo que permitirá mejorar el manejo personalizado de los pacientes con esta enfermedad.
La evolución de los cánceres sincrónicos está determinada, generalmente, por el tumor cuyo estadio clínico sea más avanzado. El pronóstico de los GIST gástricos sincrónicos con adenocarcinomas de estómago es peor que el pronóstico para los GIST primarios aislados, pero es comparable con el de los adenocarcinomas de estómago aislados.17,36 En relación con la sobrevida, se considera que los cánceres sincrónicos del tubo digestivo cursan con índices de pobre sobrevida global en análisis univariados.19 De igual manera que con el pronóstico, la sobrevida también estará, cuando menos, si no determinada, al menos influenciada por el tumor cuyo estadio clínico esté más avanzado.
En resumen, los GIST sincrónicos habitualmente son descubiertos de manera incidental durante los estudios endoscópicos, de imágenes o en la operación quirúrgica realizada por otros cánceres. Son más pequeños que los GIST aislados. Generalmente tienen bajo o muy bajo riesgo para transformación maligna. La causa exacta de la asociación entre los GIST y los adenocarcinomas no está aún determinada. En la mayoría de los casos esta asociación es probablemente sólo una coincidencia. La resección quirúrgica es el tratamiento estándar. Son necesarios estudios adicionales para dilucidar los mecanismos exactos genéticos y moleculares que subyacen en la carcinogénesis y progresión de los GIST con otros cánceres sincrónicos.
La asociación sincrónica entre los GIST y los carcinomas gástricos parece ser más común de lo que previamente se estimaba. Conociendo que uno de los factores relacionados con la aparición del cáncer es la edad avanzada, este hecho, asociado al impresionante aumento del envejecimiento poblacional, obliga al médico a tener en cuenta la posibilidad creciente del aumento de la incidencia de los cánceres en general y de los cánceres sincrónicos en particular, como es el caso de la asociación sincrónica de los adenocarcinomas gástricos y los GIST del estómago.
REFERENCIAS BIBLIOGRÁFICAS
]]>1. Mazur MT, Clark HB. Gastric stromal tumors. Reappraisal of histogenesis. Am J Surg Pathol. 1983;7:507-19.
2. Khoshnevis J, Rakhshan A, Sobhiyeh MR, Gholizadeh B, Rahbari A, Farideh A, et al. Simultaneous Gastric Adenocarcinoma and Gastrointestinal Stromal Tumor of the Stomach: A Case Report. Iran J Cancer Prev. 2013;6(1):55-8.
3. Feng F, Liu Z, Zhang X. Comparison of endoscopic and open resection for small gastric gastrointestinal stromal tumor. Transl Oncol. 2015;8:504-8.
4. Sheppard K, Kinross KM, Solomon B. Targeting PI3 kinase/AKT/mTOR signaling in cancer. Crit Rev Oncog. 2012;17:69-95.
5. Tzen CY, Wang JH, Huang YJ. Incidence of gastrointestinal stromal tumor: a retrospective study based on immunohistochemical and mutational analyses. Dig Dis Sci. 2007;52:792-7.
]]>6. DeMatteo RP, Lewis JJ, Leung D, Mudan SS, Woodruff JM, Brennan MF. Two hundred gastrointestinal stromal tumors: recurrence patterns and prognostic factors for survival. Annals of Surgery. 2000;231(1):51-8.
7. Koelz M, Wick N, Winkler T, L¨angle F, Wrba F. The impact of c-kit mutations on histomorphological risk assessment of gastrointestinal stromal tumors. European Surgery. 2007;39(1):45-53.
8. Miettinen M, Lasota J, Gastrointestinal stromal tumors - definition, clinical, histological, immunohistochemical, and molecular genetic features and differential diagnosis. Virchows Archiv. 2001;438(1):1-12.
9. Hirota S, Isozaki K, Moriyama Y. Gain-of-function mutations of c-kit in human gastrointestinal stromal tumors. Science. 1998;279(5350):577-80.
10. Maiorana A, Fante R, Maria Cesinaro A, Adriana Fano R. Synchronous occurrence of epithelial and stromal tumors in the stomach: a report of 6 cases. Arch Pathol Lab Med. 2000;124:682-6.
]]> 11. Borrman R. Geschwulste des Magens. En: Handbuch der speziellen pathologischen Anatomie und Histologie, O.H Fal, editor Berlin, Verlag Von Julius Springer; 1926.12. Lauren P. The two main histologic types of gastric carcinoma: diffuse and so-called intestinal type carcinoma: an attempt at histo-clinical classification. Acta Pathol Microbiol Scand. 1965;64:31-49.
13. Fléjou JF . WHO classification of digestive tumors: the fourth edition. Ann Pathol. 2011;31(5 Suppl):27-31. doi: 10.1016
14. Japanese Gastric Cancer Association. Japanese classification of gastric carcinoma: 3rd English edition. Gastric Cancer. 2011;14:101-12.
15. PDQ® Adult Treatment Editorial Board. PDQ Gastrointestinal Stromal Tumors Treatment. Bethesda, MD: National Cancer Institute. Updated <12/23/2016>. Available at: http://www.cancer.gov/types/soft-tissue-sarcoma/hp/gist-treatment-pdq . Accessed <02/18/2017>. [PMID: 26389157]
16. Agaimy A, Wunsch PH, Sobin LH. Occurrence of other malignancies in patients with gastrointestinal stromal tumors. Semin Diagn Pathol. 2006;23:120-9.
17. Liu Z, Liu S, Zheng G, Yang J, Hong L, Sun L, et al. Clinicopathological features and prognosis of coexistence of gastric gastrointestinal stromal tumor and gastric cancer. Medicine. 2016;95:45. Disponible en: http://dx.doi.org/10.1097/MD.0000000000005373
18. Shen C, Chen H, Yin Y, Chen J, Han L, Zhang B, et al. Synchronous occurrence of gastrointestinal stromal tumors and other digestive tract malignancies in the elderly. Oncotarget. 2015;6(10). Disponible en: www.impactjournals.com/oncotarget
19. Nilsson B, Bumming P, Meis-Kindblom JM. Gastrointestinal stromal tumors: the incidence, prevalence, clinical course, and prognostication in the preimatinib mesylate era- a population-based study in western Sweden. Cancer. 2005;103(4):821-9.
20. Marano L, Arru GM, Piras M, Fiume S, Gemini S. Surgical management of acutely presenting gastrointestinal stromal tumors of the stomach among elderly: Experience of an emergency surgery department. Int J Surg. 2014;S1:145-7.
21. Du J, Shen N, He HS, Fu XL, Wang JZ, Mao CZ. Synchronous gastrointestinal cancer and gastrointetinal stromal tumors: a single institution experience. World Journal of Surgical Oncology. 2016;14:130 DOI 10.1186/s12957-016-0882-9
22. Ferreira SS, Werutsky G, Garcia Toneto M, Machado Alves J, Duarte Piantá C, Cristine Breunig R, et al. Synchronous gastrointestinal stromal tumors (GIST) and other primary cancers: Case series of a single institution experience. International Journal of Surgery. 2010;8:314-7.
23. Zhou G, Lou N, Wu L, Yu H, Zhang Q. Gastrointestinal stromal tumor with synchronous gastric cancer: report of a case and review of literature. Int J Clin Exp Pathol. 2016;9(1):363-6. Disponible en: www.ijcep.com /ISSN:1936-2625/IJCEP0018196
24. Shi Z, Zhuang Q. Computed tomography imaging characteristics of synchronous gastrointestinal stromal tumors in patients with gastric cancer and correlation with clinicopathological findings. Molecular and Clinical Oncology. 2015;3:1311-4.
25. Woodall 3rd CE, Brock GN, Fan J. An evaluation of 2537 gastrointestinal stromal tumors for a proposed clinical staging system. Arch Surg. 2009;144:670-8.
26. Kaffes A, Hughes L, Hollinshead J. Synchronous primary adenocarcinoma, mucosa-associated lymphoid tissue lymphoma and a stromal tumor in a Helicobacter pylori-infected stomach. J Gastroenterol Hepatol. 2002;17:1033-6.
27. Tada I, Zeze K, Nakashima K. Two cases of the independent coexistence of early cancer and leiomyosarcoma in the same stomach. Gan No Rinsho. 1984;30:1812-8.
28. Lin YL, Tzeng JE, Wei CK, Lin CW. Small gastrointestinal stromal tumor concomitant with early gastric cancer: a case report. World J Gastroenterol. 2006; 12:815-7.
29. Al-Brahim N, Radhi J, Gately J. Synchronous epithelioid stromal tumour and lipoma in the stomach. Can J Gastroenterol. 2003;17:374-5.
30. Pedersen MO, Larsen A, Stoltenberg M, Penkowa M. The role of metallothionein in oncogenesis and cancer prognosis. Progress in Histochemistry and Cytochemistry. 2009;44(1):29-64.
31. Soo ETL, Nog CT, Yip GWC. Differential expression of metallothionein in gastrointestinal stromal tumors and gastric carcinomas. Anatomical Record. 2011;294(2):267-72.
32. Kawanowa K, Sakuma Y, Sakurai S. High incidence of microscopic gastrointestinal stromal tumors in the stomach. Hum Pathol. 2006;37:1527-35.
33. Liszka Ł, Zielińska-Pajak E, Pajak J, Gołka D, Huszno J. Coexistence of gastrointestinal stromal tumors with other neoplasms. J Gastroenterol. 2007;42:641-9.
34. Murphy JD, Ma GL, Baumgartner JM. Increased risk of additional cancers among patients with gastrointestinal stromal tumors: A population based study. Cancer. 2015;121(17):2960-7.
]]>35. Cai R, Ren G, Wang DB. Synchronous adenocarcinoma and gastrointestinal stromal tumors in the stomach. World J Gastroenterol. 2013;19(20):3117-23.
36. Lin M, Lin JX, Huang CM, Zheng CH, Li P, Xie JW, et al. Prognostic analysis of gastric gastrointestinal stromal tumor with synchronous gastric cancer. World J Surg Oncol. 2014;12:25.
37. Aparicio T, Boige V, Sabourin JC. Prognostic factors after surgery of primary resectable gastrointestinal stromal tumours. Eur J Surg Oncol. 2004;30(10):1098-103.
38. Tashiro T, Hasegawa T, Omatsu M, Sekine S, Shimoda T, Katai H. Gastrointestinal stromal tumour of the stomach showing lymph node metastases. Histopathology. 2005;47(4):438-9.
39. Sista F, Abruzzese V, Schietroma M, Amicucci G. Concomitant Gastrointestinal Stromal Tumor of the Stomach and Gastric Adenocarcinoma in a Patient with Billroth II Resection. Case Reports in Surgery. 2013;583856:5. http://dx.doi.org/10.1155/2013/583856
]]>
Recibido: 16 de marzo de 2017.
Aprobado: 15 de abril de 2017.
José Luis Guerra Mesa. Servicio de Cirugía Esplácnica. Instituto Nacional de Oncología y Radiobiología. La Habana. Cuba.
Correo electrónico: josel.guerra@infomed.sld.cu