REVISIÓN BILIOGRÁFICA
Metaloproteinasas de la matriz en Odontología y sus consideraciones desde el campo de la química computacional
Matrix metalloproteinases and their considerations in Dentistry from the field of computational chemistry
]]>
PhD. Antonio Díaz Caballero, PhD. Darío Méndez Cuadro, MSc. Emiliano Martínez Serrano, Dra. Jennifer Orozco Páez, Lic. Margarita Rosa Velásquez
Facultad de Odontología. Universidad de Cartagena. Colombia.
RESUMEN
Las metaloproteinasas de la matriz son una familia de proteasas zinc-dependientes encargadas de la remodelación de los componentes proteicos de la matriz extracelular de todos los tejidos, su actividad catalítica es controlada por inhibidores tisulares de metaloproteinasas de la matriz. En condiciones patológicas se pierde el equilibrio existente entre MMPs con respecto a la de estos inhibidores endógenos, este desequilibrio es evidente en enfermedades orales como la caries dental, gingivitis, periodontitis, entre otras, por lo tanto la posibilidad de lograr una inhibición selectiva de la actividad de estas enzimas con inhibidores sintéticos constituye un enfoque prometedor en el tratamiento de distintas enfermedades de la cavidad oral. Se presenta a continuación una revisión bibliográfica cuyo objetivo es analizar el papel que juegan las metaloproteinasas de la matriz en el desarrollo de patologías orales e identificar el aporte que ha hecho el análisis computacional de estas enzimas en el campo de la odontología. Para tal fin se llevó a cabo una búsqueda de la literatura disponible en bases de datos como Pubmed, Sience Direct, Ovid y Ebsco Host empleando palabras claves como: patologías orales, cáncer oral, adhesión dentinaria, metaloproteinasas de la matriz, inhibidor sintético de metaloproteinasas y modelado molecular. Se seleccionaron 35 artículos para orientar la presente revisión. Al terminar se pudo concluir que existe correlación positiva entre la desregulación de determinadas MMPs y la progresión de ciertas enfermedades orales, esto ha impulsado la identificación y el diseño insílico de inhibidores efectivos para estas proteínas, partiendo de análisis relación estructura-actividad y acoplamiento molecular computacional. Hasta la fecha se ha logrado demostrar que los inhibidores de MMPs más potentes presentan grupos hidroxamatos. Teniendo en cuenta lo anterior, el diseño de compuestos que bloqueen la actividad representa una estrategia quimiopreventiva racional encaminada a la inhibición de las MMPs.
Palabras clave: metaloproteinasas de la matriz, inhibidores tisulares de metaloproteinasas, biología molecular computacional.
ABSTRACT
Matrix metalloproteinases are a family of zinc-dependent proteases responsible for the remodeling the protein components of extracellular matrix of all tissues; its catalytic activity is controlled by tissue inhibitors of matrix metalloproteinases. At pathological conditions the balance between MMPs regarding these endogenous inhibitors is lost, this imbalance is evident in oral diseases including dental caries, gingivitis, periodontitis, among others, hence the possibility of achieving selective inhibition of activity of these enzymes with synthetic inhibitors is a promising approach in the treatment of various diseases of the oral cavity. A literature review aimed at analyzing the role of matrix metalloproteinases in the development of oral diseases and identify the contribution made by the computational analysis of these enzymes in the field of dentistry is presented below. To this end a search of the literature available was conducted in databases such as Pubmed, Sience Direct, Ovid, and Ebsco Host using keywords like: oral pathology, oral cancer, dentin bonding, matrix metalloproteinases, synthetic inhibitor of metalloproteinases, and molecular modeling. 35 items were selected to guide this review. At the end it was concluded that there is positive correlation between deregulation of certain MMPs and progression of certain oral diseases, this has boosted in silico identifying and designing effective inhibitors for these proteins, based on structure-activity relationship analysis and molecular docking computational. To date it has successfully demonstrated that the most potent inhibitors of MMPs have hydroxamate groups. So far it has successfully demonstrated that the most potent inhibitors of MMPs have hydroxamate groups. Considering the above, the design of compounds that block the chemopreventive activity represents a rational strategy for the inhibition of MMPs.
Keywords: matrix metalloproteinases, tissue inhibitors of metalloproteinases, computational molecular biology.
INTRODUCCIÓN
Las enzimas juegan un papel importante en todos los procesos celulares y tisulares del cuerpo humano. Existe un grupo de enzimas denominadas metaloproteinasas de la matriz (MMPs) cuya función principal es la remodelación de la matriz extracelular de los diferentes tejidos. Se expresan tanto en procesos fisiológicos como patológicos del cuerpo humano, de allí que la importancia de su estudio radica en la amplia expresión de estas enzimas en diversas patologías del cuerpo humano y en enfermedades de la cavidad oral.1
]]>
La actividad catalítica de las MMPs es controlada por los inhibidores tisulares de metaloproteinasas de la matriz (TIMPs). En condiciones patológicas se pierde el equilibrio existente entre MMPs con respecto a la de TIMPs, este desequilibrio es evidente en enfermedades orales como la caries dental, gingivitis, periodontitis, cáncer oral y degradación del tejido pulpar. Aunque son diversos los enfoques terapéuticos de cada patología, el estudio y análisis a nivel computacional de las MMPs y de los TIMPs ofrece una nueva área para el desarrollo de novedosas alternativas terapéuticas encaminadas a la inhibición de MMPs involucradas en las patologías orales mencionadas.2,3El empleo de programas computacionales resulta ventajoso ya que permite analizar con relativo bajo costo diferentes aspectos de la estructura de una MMP como por ejemplo su secuencia, niveles de organización de la proteína, eventos de dimerización y su asociación con componentes de la matriz e inhibidores. Por lo tanto, el análisis computacional de las estructuras de estas enzimas puede contribuir significativamente al desarrollo de nuevos inhibidores eficaces y selectivos de las MMPs, mediante acoplamieno y cribado virtual de nuestros compuestos de interés con fármacos diseñados insilico.2,4 Es por ello que el objetivo de la presente revisión bibliográfica es realizar un abordaje del papel que juegan las MMPs en el desarrollo de enfermedades orales e identificar los inhibidores diseñados insílico que se proponen actualmente para modular la actividad de estas enzimas.
MÉTODOS
Se realizó una búsqueda electrónica de literatura en bases de datos como: MEDLINE (Ovid), Pubmed, Sience Direct, Ovid y Dentistry & Oral Sciences Source (EBSCO-Host) desde el año 2000 hasta la 4ta. semana de enero de 2013, con descriptores como: oral diseases, chronic periodontitis, cáncer oral, adhesión dentinaria, Matrix metalloproteinases, tissue inhibitors of metalloproteinases, extracellular matrix, caries dental, docking y modelado molecular computacional. Cabe resaltar que se incluyeron 2 grupos de artículos, un grupo con los cuales se dio respaldo a los conceptos bioquímicos, aspectos generales y el mecanismo de acción de las MMPs y su relación con algunas enfermedades orales de gran prevalencia, se incluyeron artículos que expusieron claramente la metodología usada, pacientes con patologías orales y definieron la proteína a investigar, en este caso las MMPs. Se trabajó con un segundo grupo de artículos que suministraron la descripción de análisis computacionales de nuestras proteínas de interés. Posterior a esto se realizó un tamizaje con la aplicación de criterios a los artículos encontrados en las bases de datos, con lo cual se seleccionaron 36 artículos que cumplieron con los criterios de inclusión.
ANÁLISIS E INTEGRACIÓN DE LA INFORMACIÓN
Las metaloproteinasas de la matriz (MMPs) son una familia de proteasas que participan en la remodelación de la matriz extracelular de manera dependiente de zinc y calcio. Estas enzimas son sintetizadas por diferentes células del tejido conectivo, como fibroblastos, osteoblastos, odontoblastos y también células de defensa como los leucocitos (polimorfonucleares y macrófagos). Ellas digieren distintos componentes de la matriz extracelular, contribuyendo con diversos procesos fisiológicos, como el remodelado normal de tejidos, la angiogénesis, el desarrollo embrionario del tejido conjuntivo, la ovulación, la apoptosis y la cicatrización de heridas.5 ]]>
La función fisiológica principal de estas proteasas se atribuyó originalmente a la modulación y regulación del recambio de la matriz extracelular (MEC) por la degradación proteolítica directa de las proteínas que la constituyen (por ejemplo, colágeno, fibronectina y proteoglicanos), pero también se encontró que actúan como mediadores químicos, regulando la función de moléculas bioactivas como las citoquinas y quimioquinas, e intervienen en la destrucción del tejido y la respuesta inmune relacionada con la inflamación, produciéndose un aumento drástico en la expresión y actividad de estas enzimas.6
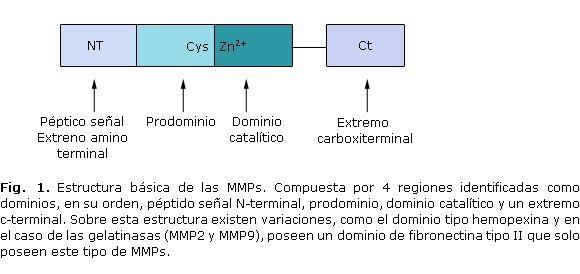
Todas las MMP se sintetizan con una secuencia señal N-terminal conformada por 20 residuos de aminoácidos que orienta la excreción de la enzima, esta secuencia se retira en el retículo endoplasmático dando las proenzimas latentes. Las proenzimas presentan una estructura básica que contiene al menos un prodominio, un dominio catalítico y un extremo C-terminal (Fig. 1).2
El prodominio consta aproximadamente de 80-90 aminoácidos (propéptido), contiene una cisteína conservada y es el encargado de mantener la latencia de la enzima. Este segmento de aminoácidos blinda al dominio catalítico y es susceptible de escisión. Interactúa con la región catalítica a través de un residuo de cisteína conservado y el ion Zn2+ en una región tipo bolsillo.7 El zinc es uno de los iones metálicos más importantes encontrados en las MMPs. La Geometría de coordinación del ión zinc en el sitio activo de los complejos ligando-metaloproteinasa plantea un reto en la determinación de las afinidades de unión de ligando en la estructura basada en el diseño de fármacos. Este hecho se debe a que el Zn existe generalmente en 4, 5 o 6 coordenadas geométricas, con ligandos tales como, His, Cys, Asp, Glu, sustrato / inhibidor y moléculas de agua. Por lo tanto la modelación de la unión del ligando al ion zinc es muy problemático debido a la polarización, la transferencia de carga de varias coordenada geométricas y la falta de campos de fuerza precisas. Estas limitaciones han dificultado la estructura basada en estudios de diseño de fármacos dirigidos a diseñar nuevos ligandos potentes y selectivos de zinc-metaloproteinasas. Por otra parte, el dominio catalítico es conformado por 175 aminoácidos aproximadamente, presenta un motivo altamente conservado de unión a zinc con secuencia HEXXHXXGXXH y otro motivo «interruptor de cisteína'' PRCGXPD, que posee tres histidinas que coordinan un átomo de zinc dentro del dominio catalítico. El dominio catalítico también contiene una metionina conservada, formando una "vuelta-Met'' 8 residuos después del motivo de unión a zinc, que forma una base para soportar la estructura alrededor del zinc catalítico.8
Esta coordinación Cys-Zn2+ mantiene las pro-MMPs inactivas previniendo la catálisis mediante la unión de una molécula de agua al átomo de zinc. Aunque el dominio catalítico de MMPs es estructuralmente muy similar, existen diferencias con respecto a la especificidad de sustrato, localización celular, la unión de la membrana y la regulación que hacen de esta una familia de enzimas muy versátil con una multitud de funciones fisiológicas, muchas de los cuales todavía no se comprenden totalmente.8
Por último, el extremo C-terminal de tipo hemopexina funciona principalmente como una secuencia de reconocimiento para el sustrato y lo presentan todas las MMPs a excepción de la MMP-7, MMP-23 y MMP 26. Existe también un dominio de fibronectina tipo II, que solo poseen las gelatinasas. Inicialmente las MMPs se clasificaron según el tipo de componente de la MEC que son capaces de degradar. Así, las MMPs quedaron agrupadas en: colagenasas (MMP-1, -8, -13), gelatinasas (MMP-2, -9), estromelisinas (MMP-3, -10, -11, -7), y matrilisinas. Sin embargo, esta clasificación ha quedado obsoleta, ya que se han descrito nuevos sustratos dentro y fuera de la MEC, por lo que actualmente las MMPs se clasifican según su número y estructura.9,10 ]]>
Las MMPs son detectables con alta frecuencia en las células, tejidos y líquidos intersticiales implicados en una amplia variedad de funciones biológicas, en estado de salud y en condiciones patológicas. A nivel oral, la expresión de estas proteínas puede cuantificarse en diferentes fluidos como la saliva, el fluido gingival crevicular (FGC) o muestras de enjuagues bucales y algunos tejidos como la encía, mucosa y dentina. Son consideradas como posibles biomarcadores, los cambios cuantitativos de estas enzimas pueden reflejar el estado de salud oral de un sujeto y emplearse no solo en el diagnóstico y tratamiento de enfermedades orales sino también como indicadores del proceso de adhesión de diferentes biomateriales dentales.11,12
Dentro de las MMPs que se elevan con mayor frecuencia se pueden mencionar la MMP-8 en encías con gingivitis; las MMP-1, MMP-3 y MMP-9 en encías sanas pero inflamadas; la MMP-2 y predominantemente la MMP- 9 en pacientes con periodontitis, la MMP2 y MMP9 en cáncer oral.13,14 Es importante anotar que el estudio de las MMPs radica en una adecuada selección de técnicas para el aislamiento y purificación de estas enzimas.15
Cambios en los niveles de algunas MMPs se han relacionado con el progreso de la lesión cariosa, brindando una nueva perspectiva de patología. En ella, las MMPs del huésped, de origen odontoblástico (pulpar), actuarían en la capa profunda de la lesión cariosa coadyuvando al proceso proteolítico de la matriz orgánica de la dentina, (ligeramente alterada por las colagenásas bacterianas) e interactuando y perpetuándose su actividad proteolítica gracias a diversos factores de crecimiento, presentes en la matriz orgánica de la dentina que estimulan su transcripción y activación, alternándose y sucediendo simultáneamente a los momentos altamente desmineralizantes, consecuencia de la producción bacteriana de toxinas y ácidos carboxílicos.16 Los odontoblastos producen metaloproteinasas MMPs -2,-8,-9,-14,-20, la más abundante en la dentina es la MMP -8. Por otra parte los cambios de pH que tienen lugar en la lesión de caries son activadores muy potentes para MMPs. Estos resultados forman una base a la teoría de una secuencial desmineralización-MMP activación y degradación de matriz de dentina que tiene lugar en la lesión dentina.17
De igual manera varias MMPs se encontraron implicadas en el desarrollo de la enfermedad periodontal, patología oral de alta prevalencia considerada como una inflamación que se extiende a profundidad en los tejidos y causa pérdida de tejido de soporte conectivo y hueso alveolar. El mecanismo fisiopatológico por el cual ocurre esta sucesión de fenómenos tiene explicación en la respuesta inmune del hospedero frente a los microorganismos productores de toxinas (endotoxinas bacterianas) conocidos ampliamente como periodontopatógenos.18
Se demostró que la formas zimogénicas o inactivas de las MMPs -8, -9 y -13 presentes en periodontitis son activadas por cascadas independientes y/o cooperativas que incluyen la participación de otras proteinasas del hospedadero.12 Aunque no es evidencia causal de enfermedad periodontal, es un hecho que las metaloproteinasas están participando activamente en procesos de salud y su producción se ve aumentada en estadios inflamatorios de gingivitis y enfermedad periodontal.19
Por otro lado, en cáncer oral se evidenció alta expresión de MMPs, esta patología se caracteriza por un alto grado de invasión local y una alta tasa de metástasis a los ganglios linfáticos cervicales, esta propagación del cáncer es producida por la degradación de la matriz extracelular (ECM) donde las MMPs especialmente la MMP-9, se encuentran involucradas. Romper la ECM permite no solo que el cáncer se propague, sino que también se liberan factores diversos de sus sitios críticos, incluyendo citoquinas.20
]]>
La expresión de MMPs no solamente se ciñe a procesos patológicos, estudios in vitro e in vivo han demostrado la degradación de las fibras de colágeno en y debajo de las capas adhesivas de restauraciones de resina, donde las MMPs presentes en la dentina parecen ser las responsables de la degradación.21 Los monómeros resinosos y/o las aminas terciarias presentes en los sistemas adhesivos resinosos SAR y cementos resinosos que se emplean actualmente juegan un papel en la activación de las MMPs sea por: la inhibición de TIMPs, activando las formas latentes de MMPs interfiriendo en el grupo cisteína de su estructura molecular zinc dependiente, o estimulando a los odontoblastos para la expresión y secreción de nuevas MMPs. Teniendo en cuenta estas consideraciones el trabajo futuro mostrará si la inhibición de MMPs puede ser utilizado para prevenir la pérdida de adhesión.22
Debido a sus variadas funciones fisiológicas, las MMPs deben estar estrictamente reguladas en múltiples niveles, de forma que únicamente se expresen y sean activas en el tipo celular, momento y lugar adecuados, uno de estos puntos de regulación es a través del bloqueo de su actividad enzimática, este puede llevarse a cabo por la interacción de las MMP con alguno de sus inhibidores fisiológicos.23 La principal familia de inhibidores específicos endógenos de las MMPs son los TIMPs, el complejo resultante de la unión de la MMP con su inhibidor es inactivo e incapaz de fijar un sustrato. Los TIMPs son proteínas que tienen capacidad para inhibir la actividad de todas las MMP, pero cada uno de ellos muestra una afinidad diferente para cada proteasa. Actualmente se reconocen 4 tipos de TIMP que son capaces de unirse a la región catalítica de la enzima e inhibir su acción. Sin embargo, la vida media de los inhibidores endógenos es muy corta, por lo que no se han utilizado en la práctica clínica.24
A la fecha, cuatro inhibidores endógenos han sido aislados en vertebrados TIMP-1, TIMP-2, TIMP-3 y TIMP- 4. Actúan específicamente sobre las formas activas de las MMPs, incluso sobre ciertas formas latentes. Los TIMPs se encuentran presentes en una relación 1:1 en comparación con las MMPs, condición que permite obtener un adecuado remodelamiento de la MEC, gracias al balance entre síntesis y degradación de esta.4
Como se mencionó anteriormente, existe una correlación positiva entre la desregulación de determinadas MMPs y la progresión de ciertas patologías orales como el cáncer. Es así como la identificación y el diseño de inhibidores efectivos para estas proteínas representa una estrategia quimiopreventiva racional y es un área activa de investigación en la actualidad.25
Anteriormente, la búsqueda de nuevos fármacos implicaba la síntesis ardua a través de varias rutas sintéticas de los posibles compuestos con la propiedad de interés o el cribado de productos naturales, lo cual implicaba tiempo y costos elevados. Paulatinamente, estos gastos se han hecho cada vez menores debido al desarrollo y la evolución de las herramientas computacionales, las cuales vienen evolucionado de tal forma que se han transformado en tecnologías importantes para la búsqueda de moléculas candidatas a fármacos mediante la selección de moléculas cabezas de serie o leads a partir de bases de datos. El campo de la química computacional abarca enfoques computacionales para el diseño, desarrollo y síntesis de compuestos farmacológicamente activos. Por ejemplo, métodos para ligandoreceptor automatizado de acoplamiento y técnicas para la búsqueda de similitud molecular.26,27
En Odontología, el análisis computacional y el estudio de complejos enzima/inhibidor mediante cristalografía de rayos X o resonancia magnética nuclear aumenta las expectativas de obtener o diseñar un inhibidor terapéutico efectivo, teniendo en cuenta las condiciones locales de la cavidad oral a las cuales va a actuar el inhibidor diseñado, como el pH, solubilidad, presencia de proteínas o agentes inactivantes, entre otros aspectos.28,29 ]]>
En estudios previos donde se aplican estas herramientas para el estudio de inhibidores de MMPs se obtuvieron hallazgos importantes. En primera instancia, se encontraron 3 componentes o requerimientos esenciales para que una molécula actúe como inhibidor efectivo de MMPs: (1) un grupo funcional capaz de quelar el ion zinc presente en el sitio activo de estas enzimas se le conoce como grupo de unión a Zinc ZBG, (2) al menos un grupo funcional que forme puentes de hidrógeno con el esqueleto de la enzima27 y una o más cadenas laterales que establezcan interacciones de Van der Waals con subsitios específicos dentro del sitio activo. Comúnmente, este tipo de inhibidores son clasificados de acuerdo a su grupo de unión al Zn, dada la importancia de esta interacción, ya que define el modo de unión y así la potencia relativa del inhibidor. Así, por ejemplo, se encuentran aquellos que contienen el grupo hidroxamato, carboxilato, tiolato, fosfinil, entre otros.30.31
La mayoría de los inhibidores de MMP desarrollados por compañías farmacéuticas se encuentran en el grupo de los hidroxamatos (Fig. 2). Esta preferencia está basada en estudios previos de relación estructura actividad y en datos de cristalografía que sugieren que los inhibidores de MMPs más potentes pueden ser obtenidos insertando un grupo hidroxamato en medio de una secuencia peptídica dada.32
De un estudio de Relación Estructura Actividad32 específico para una serie de ácido hidroxámicos con sustituyentes hidroxilo cuaternarios se obtuvo lo siguiente: la orientación estereoquímica de P1 es esencial para la actividad, el grupo fenilpropil se estableció como el mejor sustituyente de la región P1 y sustituyentes hidrofóbicos en P2 y N-metilamidas en P3 se encontraron óptimos. Hanessian y otros definieron exitosamente la alta hidrofobicidad del bolsillo S1, el cual está rodeado por Tyr-155, His-166 y Tyr-168. Al realizar la simulación del acoplamiento entre la molécula 4-bencilsulfanil-N-hydroxi-2-[isobutil-(4-metoxibenzenosulfonil)-amino] butiramida y el sitio activo de la MMP-3, se obtiene que el bolsillo S1 es ocupado por el grupo bencil (Fig. 3).33
Por otra parte, Okada y otros sugieren por una parte que una larga cadena en la posición P1´ es preferible para que se de la unión a las MMP-2, -3 y 9 y MT1-MMP, un grupo alquil ramificado en la posición P2´ es crítica para la unión al domino de transmembrana (DMT1), mientras que la introducción de un grupo voluminoso en la posición á del grupo hidroxamato parece disminuir la actividad contra DMT1.34
]]>
Pei y otros, investigaron el efecto de dos tioles no proteicos, el glutatión (GSH) y N-acetilcisteina (NAC), sobre la activación, función e interacciones célula - matrix extracelular de la gelatinasa degradante de membrana basal, MMP-9. Estos estudios revelaron que el NAC y GSH emplean la S-tiolación de proteínas para inhibir la activación organomercurial de MMP-9. En este estudio se realizaron ensayos experimentales utilizando líneas celulares cancerígenas de la cavidad oral. Los hallazgos encontrados fueron corroborados utilizando modelado molecular computacional. Específicamente, se realizó un acoplamiento molecular entre los tioles y la MMP-9 y se realizó una búsqueda conformacional usando el método de Monte Carlo.25 Para el acoplamiento molecular se extrajo de protein Data Bank (PDB) la estructura cristalina de la proteína MMP9 acomplejada con el ligando NFH (N-2-[(2R)-2-{[formil(hidroxi)amino]metil}-4-metilpentanoil]-N,3-dimetil-L-valinamida) identificada con el código 1GKC y resolución 2.3 Å (Fig. 4).
Como ya se mencionó, los inhibidores sintéticos generalmente contienen un grupo de quelante (ZBG) que se unen al átomo de zinc catalítico en el sitio activo de la MMP. Otros sustituyentes de estos inhibidores generalmente están diseñados para interactuar con varios bolsillos de enlace sobre la MMP de interés, haciendo al inhibidor más o menos específico para determinadas MMP's.35
CONCLUSIONES
El estudio computacional de moléculas se propone como herramienta para la evaluación de nuevas medidas terapéuticas. Durante la revisión se pudo apreciar la posibilidad de inhibición selectiva de MMPs por inhibidores sintéticos como un método para evitar la actividad de estas enzimas, lo que constituye un enfoque prometedor en el tratamiento de distintas enfermedades de la cavidad oral, teniendo en cuenta la alta expresión de estas enzimas y el papel central que juegan en el desarrollo de cada patología. Sumado a esto se ha evidenciado que los niveles de TIMPs (inhibidores tisulares de las MMPs) son bajos e inadecuados para inhibir las MMPs elevadas, por lo tanto proponer y diseñar nuevas alternativas terapéuticas empleando herramientas computacionales, puede ser un nuevo paso a consolidar entre la Odontología y la química computacional. ]]>
REFERENCIAS BILIOGRÁFICAS
1. Mora J, Manzur A, Ramírez T, Herzog D. Papel de las Metaloproteinasas de la Matriz en la Degradación del Tejido Pulpar: Una revisión literaria. Rev Cient Ondontol. 2006;1(1):20-6.
2. Tallant C, Marrero A, Gomis-Rüth FX. Matrix metalloproteinases: Fold and function of their catalytic domains. Biochimica et Biophysica Acta. 2010;1803(1):20-8.
3. Sorsa T, Tjaderhane L, Salo T. Matrix metalloproteinases (MMPs) in oral diseases. Oral Dis. 2004;10(6):311-8.
4. Cheng T, Li Q, Zhou Z, Wang Y, Bryant SH. Structure based virtual screening for drug discovery: a problem-centric review. AAPS J. 2012;14(1):133-41.
5. Kuula H, Salo T, Pirilä E, Tuomainen AM, Jauhiainen M, Uitto VJ, Tjäderhane L, Pussinen PJ, Sorsa T. Local and systemic responses in matrix metalloproteinase 8-deficient mice during Porphyromonas gingivalis-induced periodontitis. Infect Immun. 2009 Feb;77(2):850-9.
6. Sorsa T, Tjäderhane L, Konttinen YT, Lauhio A, Salo T, Lee HM, et al. Matrix metalloproteinases: contribution to pathogenesis, diagnosis and treatment of periodontal inflammation. Annals of medicine. 2006;38(5):306-21.
7. Klein T, Bischoff R. Physiology and pathophysiology of matrix metalloproteases. Amino Acids. 2011;41(2):271-90.
8. Jain T, Jayaram B. Computational protocol for predicting the binding affinities of zinc containingmetalloprotein -ligand complexes. Proteins. 2007;67(4):1167-78.
9. Bildt MM, Bloemen M, Kuijpers-Jagtman AM, Von den Hoff JW. Matrix metalloproteinases and tissue inhibitors of metalloproteinases in gingival crevicular fluid during orthodontic tooth movement. Eur J Orthod. 2009;31(5):529-35.
10. Brew K, Nagase H. The tissue inhibitors of metalloproteinases (TIMPs): An ancient family with structural and functional diversity. Biochimica et Biophysica Acta. 2010;1803(1):55-71.
11. Al-Azri A, Gibson R, Keefe D, Logan R. Matrix metalloproteinases: do they play a role in mucosal pathology of the oral cavity? Oral Dis. 2013;19(4):347-59.
12. Hernández P MP, Tervahartiala T, Sorsa T, Hernández M. Análisis de MMPs en fluidos orales en el diagnóstico complementario de las enfermedades periodontales. Rev Clin Periodoncia Implantol Rehabil Oral. 2012;5(3):150-3.
13. Rai B, Kaur J, Jain R, Anand SC. Levels of gingival crevicular metalloproteinases-8 and -9 in periodontitis. Saudi Dent J. 2010;22(3):129-31.
14. Costa JE, Lorentz TC, Costa FO. Association between maternal periodontitis and an increased risk of preeclampsia. J Periodontol. 2006;77(12):2063-9.
15. Cheng XC, Fang H, Xu WF. Advances in assays of matrix metalloproteinases (MMPs) and their inhibitors. J Enzyme Inhib Med Chem. 2008;23(2):154-67.
16. Hidalgo R. Las metaloproteinasas y el progreso de la lesión cariosa en dentina. Rev Estomatol Herediana. 2006;16(1):64-72.
17. Palosaari H WJ, Larmas M, Rönkä H, Sorsa T, Salo T, Tjäderhane L. The expression of MMP-8 in human odontoblasts and dental pulp cells is downregulated by TGF-beta1. J Dent Res. 2000;79(1):77-84.
18. Simancas M, Arévalo L, Díaz A. Periodontitis crónica: una visión desde la proteómica. Duazary. 2010;7(1):106-16.
19. Teles RP, Sakellari D, Konstantinidis A, Socransky SS, Haffajee AD. Application of the checkerboard immunoblotting technique to the quantification of host biomarkers in gingival crevicular fluid. Journal of periodontology. 2009;80(3):447-56.
20. Singh RD HN, Patel JB, Shah FD, Shukla SN, Shah PM, Patel PS. Matrix Metalloproteinases and Their Inhibitors: Correlation with Invasion and Metastasis in Oral Cancer. Ind J Clin Biochem. 2010;25(3):250-9.
21. Pashley DH TF, Yiu C, Hashimoto M, Breschi L, Carvalho RM, Ito S. Collagen degradation by host-derived enzymes during aging. J Dent Res. 2004; 83(3):216-21.
22. Hidalgo-Lostaunau R. Reacción de la dentina a los sistemas adhesivos resinosos: aspectos biológicos relacionados y biodegradación de la capa híbrida. Rev Estomatol Herediana. 2008;18(1):50-64.
23. Trojanek J. Matrix metalloproteinases and their tissue inhibitors. Postepy Biochem. 2012;58(3):353-62.
24. Xiang J, Cao Z, Dong W, Li C. Manifestación del inductor de las metaloproteinasas de matriz extracelular (EMMPRIN) en la encía humana sana e inflamada. Quintessence. 2010;23(7):311-8.
25. Pei P, Horan MP, Hille R, Hemann CF, Schwendeman SP, Mallery SR. Reduced nonprotein thiols inhibit activation and function of MMP-9: implications for chemoprevention. Free Radic Biol Med. 2006;41(8):1315-24.
26. Reddy AS PS, Kumar PP, Pradeep HN, Sastry GN. Virtual screening in drug discovery-a computational perspective. Curr Protein Pept Sci. 2007; 8(4):329-51.
27. Schneider G. Computational medicinal chemistry. Future Med Chem. 2011;3(4):393-4.
28. Terp GE, Christensen IT, Jorgensen FS. Structural differences of matrix metalloproteinases. Homology modeling and energy minimization of enzyme-substrate complexes. J Biomol Struct Dyn. 2000;17(6):933-46.
29. Hou T, Zhang W, Xu X. Molecular docking studies of a group of hydroxamate inhibitors with gelatinase-A by molecular dynamics. J Comput Aided Mol Des. 2002;16(1):27-41.
30. Kontogiorgis CA, Papaioannou P, Hadjipavlou-Litina DJ. Matrix metalloproteinase inhibitors: a review on pharmacophore mapping and (Q)SARs results. Curr Med Chem. 2005;12(3):339-55.
31. Wang J, Uttamchandani M, Li J, Hu M, Yao SQ. Rapid assembly of matrix metalloprotease inhibitors using click chemistry. Org Lett. 2006;8(17):3821-4.
32. Cuniasse P DL, Makaritis A, Beau F, Georgiadis D, Matziari M, Yiotakis A, et al. Future challenges facing the development of specific active-site-directed synthetic inhibitors of MMPs. Biochimie 2005;87(3-4):393-402.
33. Hanessian S, Moitessier N, Gauchet C, Viau M. N-Aryl sulfonyl homocysteine hydroxamate inhibitors of matrix metalloproteinases: further probing of the S(1), S(1)', and S(2)' pockets. J Med Chem. 2001;44(19):3066-73. ]]>
34. Verma RP, Hansch C. Matrix metalloproteinases (MMPs): chemical-biological functions and (Q)SARs. Bioorg Med Chem. 2007;15(6):2223-68.
35. Gill SE PW. Metalloproteinases and their inhibitors: Regulators of wound healing. J Biochem Cell Biol. 2008;40:133-447.
Recibibo: 27 de febrero de 2013.
Aprobado: 17 de julio de 2013.
]]>
Antonio Díaz Caballero. Facultad de Odontología. Universidad de Cartagena. Teléfono: +57+6698172 Ext. 110. Fax: +57+6698193 Ext. 124. Correo electrónico: adiazc1@unicartagena.edu.co ]]>