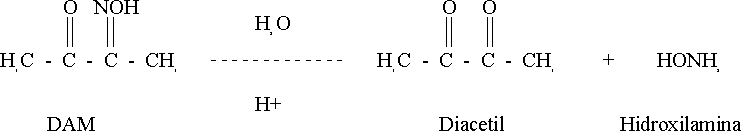
1 Licenciada en Química. Investigadora Auxiliar.
2 Licenciada en Bioquímica.
3 Licenciada en Química.
4 Técnica en Química.
5 Licenciada en Ciencias Farmacéuticas.
Descriptores DeCS: COLORIMETRIA/métodos; JUEGO DE REACTIVOS PARA DIAGNOSTICO; UREA/sangre; QUIMICA CLINICA; FENOLES; TIMOL; SALICILATO DE SODIO; HIPOCLORITO DE SODIO; CALIBRACION; ESTANDARES DE REFERENCIA.
La determinación de urea reviste gran importancia para el diagnóstico clínico de diversas afecciones generalmente de origen renal; por lo que contar con un juego de reactivos que permita obtener valores confiables en esta determinación es un objetivo básico en la producción de reactivos para química clínica.
Por la estructura de la molécula de urea, diversos autores han encaminado los métodos para su determinación en 2 grandes grupos: métodos directos y métodos indirectos.
En los métodos directos la reacción transcurre con la molécula sin previa transformación, especialmente por los grupos amino de ésta, según la ecuación de la figura 1. ]]>
Así ocurre la reacción de Fearon con la diacetil monoxima-tiosemicarbazida (DAM-TSC) en un medio ácido fuerte y con un agente oxidante,1 y es en la década de los 70 que se introduce el empleo de la antipiridina.
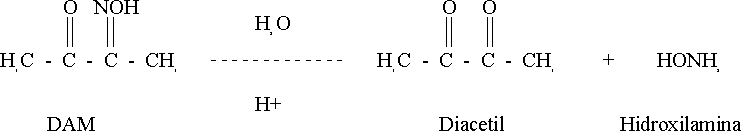
La cuantificación colorimétrica en los métodos indirectos es utilizada por Cam, Barrier y Lawny,2 quienes estudiaron una selección de derivados fenólicos capaces de formar un reactivo estable con la ureasa y su aplicación en química clínica, como son: timol, m-cresol, ácido salicílico y sus derivados.
Hanadas y Yamanishi,3 por una parte, y Tabacco, Meiattini y Moda4 estudiaron la reacción colorimétrica para cuantificar urea con un reactivo que contiene fenol o sus derivados como cromógenos y agentes oxidantes.
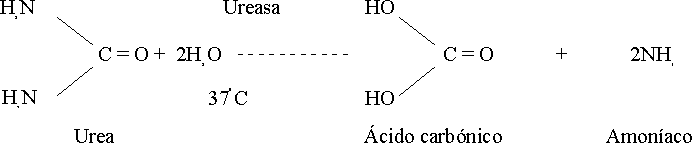
Un estudio de la espectrofotometría y la cinética de la reacción en estos métodos se plantea por Patton y Crouch;5 la reacción transcurre según la ecuación general de la figura 2.
La coloración del producto final (indofenol) de la reacción depende del derivado fenólico utilizado.

Preparación de los reactivos
Las muestras se desproteinizaron con el RT1-2 y se prepararon diluciones de 1:10 para las soluciones de referencia de urea.
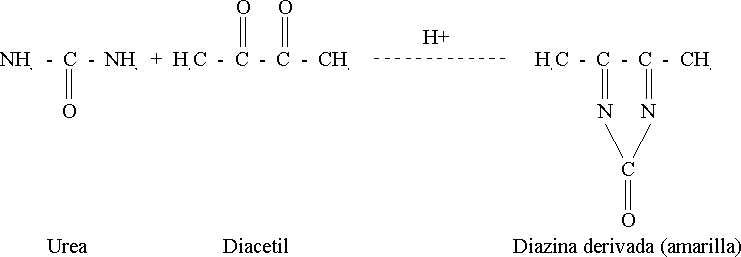
Reacción de coloración
| | | ]]> Ensayo referencia | |
| Solución de referencia | | | |
| Suero | | | |
| Agua destilada | | | |
| RT3-4 | ]]> 5 mL | | |
Método de Berthelot y sus modificaciones
La preparación de los reactivos se presentó de la manera siguiente:
| | | | |
| Agua destilada | | ]]> 1 mL | |
| RT1 | | | |
| Suero | | | |
| RT2 | | | ]]> 100 mL |
RT3 ó RT4 ó
RT5 1,5 mL 1,5 mL 1,5 mL
RT6 1,5 mL 1,5 mL 1,5 mL
Se mezcló e incubó por 15 min a 37 oC.
La longitud de onda varía de acuerdo con el derivado fenólico utilizado (RT3 620 nm; RT4 600 nm; RT5 580 nm).
Estudio de la linealidad y selección del tiempo óptimo de lectura
Se utilizó la curva de calibración en un rango de concentraciones de urea desde 4,9950 hasta 24,9750 mmol/L, evaluando distintos tiempos de reacción, y se calculó el coeficiente de correlación.
Imprecisión
Se evaluaron cada uno de los métodos descritos en 80 muestras de suero control lote 7010. Se estudió en todos los casos la imprecisión, calculando el coeficiente de variación entre los valores obtenidos en el día para conocer la repetibilidad y entre las corridas para determinar la reproducibilidad. ]]>
InexactitudSe determinó el coeficiente de correlación entre cada uno de los métodos ensayados mediante el análisis de 15 muestras durante 5 d. Los valores obtenidos fueron comparados con los de DAM, método que se utilizó como referencia para llevar a cabo este estudio.
| | | | | | ]]> r | | |
| | | | | | | ]]> 10 | |
| | | | | | | | |
| ]]> 60 | | | | | | | |
| | | ]]> ! | | |
| Métodos | | | ||||
| | | | ]]> 4 | | ||
| DAM | | | | | | |
| Fenol-hipoclorito | | | ]]> 6,54 | | | |
| Timol | | | | | | |
| Salicilato de sodio | ]]> 3,97 | | | | | |
El comportamiento de los 3 métodos estudiados nos permite utilizarlos indistintamente en la determinación de urea en suero.
De estos datos se pudo concluir que la coloración era estable hasta 1 h, y se definió que el tiempo óptimo para cada ensayo se obtenía en:
En los sistemas estudiados se pudo apreciar que los valores del coeficiente de correlación obtenidos para los 3 métodos y tomando como referencia el de la DAM, eran buenos ya que estaban muy cercanos a 1, lo que nos indicó que los 3 métodos eran adecuados para la determinación de urea en suero.
En todos los casos estudiados la manipulación es sencilla, aspecto fundamental para el trabajo de rutina del laboratorio clínico, siendo el más práctico entre ellos el del salicilato de sodio.
Se recomienda evaluar el método menos complejo para su elaboración industrial.
Subject headings: COLORIMETRY/methods; REAGENT KITS, DIAGNOSTIC; UREA/blood; CHEMISTRY, CLINICAL; PHENOLS; THYMOL; SODIUM SALICYLATE; SODIUM HYPOCHLORITE; CALIBRATION; REFERENCE STANDARDS.
Li. Lilliam Valdés Diez. Empresa de Productos Biológicos "Carlos J. Finlay". Infanta No. 1162, municipio Centro Habana, La Habana, Cuba. ]]>