Descriptores DeCS: PROPRANOLOL/analogos & derivados; CROMATO-GRAFIA EN CAPA DELGADA/métodos; ESPECTROMETRIA DE FLUORESCENCIA/método; COLORIMETRIA/método; CROMATOGRAFIA LIQUIDA DE ALTA PRESION/método.
El propranolol es un bloqueador b-adrenérgico muy utilizado en el tratamiento clínico. Este medicamento se une competitivamente a los adrenorreceptores, disminuye la eficacia de los b -agonistas y consecuentemente la presión sanguínea, el impulso y la fuerza de contracción cardíaca.1 La estructura química del propranolol indica la presencia de un centro quiral que es el sitio específico por el cual ocurre la unión al receptor para realizar su acción biológica. Cada isómero presenta un efecto farmacológico distinto; en una mezcla racémica el isómero d-propranolol es 40 veces más potente como antiarrítmico y antihipertensivo que el 1-propranolol,2 de aquí se deriva la importancia de la resolución y la determinación del contenido de este principio activo en medicamentos.
El objetivo de este trabajo es presentar el resultado de la revisión bibliográfica de los métodos más actuales de detección y resolución enantiomérica del clorhidrato de propranolol y sus ésteres.
Para la selección de los artículos relacionados con la temática se revisaron las bases de datos MEDLINE (1986-1994), Analytical Abstracts (1985-1994), Chemicals Abstracts (1990-1992) y los Current Contents (Life Science y Physical, Chemical & Earth Sciencies) desde 1990-1996, tanto en disquete como en papel.
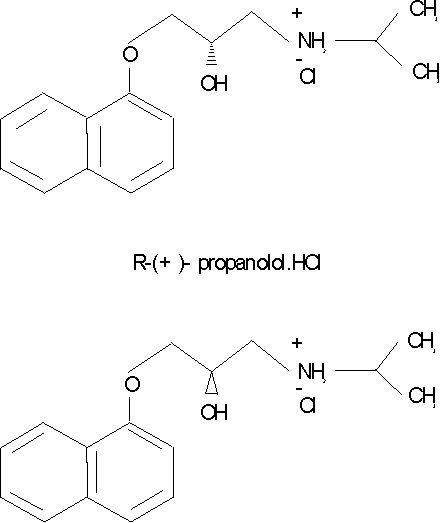
El (R/S)-propranolol clorhidrato cuyo nombre químico es 1-(isopropilamina)-3-(-1-naftiloxi)-2-propranolol clorhidrato, también puede ser nombrado 1-[(1-metiletil (amino))]-3-(-1-naftaleniloxi)-2-propanol, su fórmula estructural se representa según se muestra en la figura 1 y la empírica es C16H22ClNO2 con un peso molecular de 295,81 g/mol y un punto de fusión entre 162-165 oC. Este compuesto es un sólido blanco, soluble en agua y alcohol, ligeramente insoluble en cloroformo y prácticamente insoluble en éter.3 En soluciones acuosas el propranolol se descompone con oxidación de la cadena de isopropilamina, acompañada por una disminución del pH y decoloración de la solución. Las soluciones son más estables a pH=3 y se descomponen rápidamente a pH alcalino. El valor del pka es 9,45.

Los efectos adversos más comúnmente vistos son: náuseas, vómitos, otros disturbios gastrointestinales y fatiga. Sobre el sistema cardiovascular produce bradicardia e hipotensión, y en el sistema nervioso central causa alucinaciones, confusión, disturbios del sueño y la visión. Puede ocurrir broncoespasmo particularmente en individuos susceptibles (asmáticos). Otros efectos adversos reportados son: reacciones alérgicas, disturbios metabólicos, retención de líquido, alopecia, miopatías y estomatitis.
Para la detección del propranolol clorhidrato se encontraron varios métodos, dentro de los que se encuentra el realizado por Sungur y otros5 en 1989 al detectar algunos ß-bloqueadores por cromatografía de placa delgada (CCD), después de una de-rivatización con dabsil (4-dimetil-ami-noazobenceno). Los ß-bloqueadores se hicieron reaccionar con dabsil en una solución acetona-agua (3:1) bufereada con una solución de hidrogenocarbonato de sodio. Para la separación de los derivados dabsílico de los ß-bloqueadores se probaron diferentes sistemas de solventes, mostrando la mejor separación el sistema de solvente cloroformo-acetona-etanol (95 %) con una proporción de 10:0,5:0,5, siendo el propranolol el ß-bloqueador más sensible a la detección por CCD. Los valores de Rf para cada muestra son reportados en la literatura. Se señala que las propiedades cromóforas de los derivados dabsílicos permiten una estimación espectrofotométrica en la región visible, cuyo monitoreo evita las interferencias causadas por sustancias que absorben en la región ultravioleta (UV). La coloración de los derivados dabsílicos de los ß-bloqueadores permite una determinación densitométrica por CCD de los compuestos en fluidos biológicos y formas dosificadas. ]]>
Otro método empleado para la detección y determinación del racemato de propranolol es la cromatografía líquida de alta resolución (CLAR) reportada en la USP XXII,6 en la cual se utiliza una fase móvil formada por dodecil sulfato de sodio (SDS) en ácido fosfórico (0,15 mol/L), acetonitrilo: metanol: agua (36:36:28). La técnica reportada empleó una columna RP-18 de 25 cm x 4 mm, con un flujo de 1,5 mL/min y detección a 290 nm.La CLAR también fue utilizada por Henry y Repta7 para medir la estabilidad de una suspensión del clorhidrato de propranolol realizada a partir de tabletas. Para llevar a cabo esta técnica fue necesaria la detección y determinación del propranolol en la suspensión. Se utilizó una columna de octadecilsilano de fase reversa (15 cm x 5 mm) y una precolumna de 5 cm con el mismo empaquetamiento. El detector ultravioleta fue fijado a 280 nm. La fase móvil consistió en 30 % de acetonitrilo, octanosulfonato de sodio (4 mmol/L), hidrogenosulfato de tetrabutilamonio (3,5 mmol/L) y 0,1 % de ácido sulfúrico en agua estéril. El flujo utilizado fue de 1 mL/min. Con las condiciones antes mencionadas, el tiempo de retención obtenido para el propranolol fue de 6,3 min. La determinación de la concentración del propranolol clorhidrato en las muestras se obtuvo por el método de cuantificación del estándar externo utilizando como patrón el propranolol . HCl, USP, y la ecuación de la recta de regresión de la curva de calibración se utilizó para determinar la concentración de las muestras basándose en la medición de la altura de los picos.
Guiberteau-Cabanillas y otros,8 utilizaron el extracto acuoso de tabletas pulverizadas para la detección del propranolol; se analizó una alícuota de 10 mL del extracto en una columna Pecosphere C18 (3,3 cm x 4,6 mm); como fase móvil emplearon acetonitrilo / SDS (0,01 mol/L) (3:2) con 1 % de ácido acético a un flujo de 2 mL/min y la detección se realizó a 230 nm.
Un método cromatográfico más novedoso llamado cromatografía de fluido supercrítico (CFS) es realizado por Ruane y Tomkinson,9 en 1990, para la detección del propranolol. En la técnica se efectuó el análisis de alícuotas de una solución de 1 mg/mL de [14C] propanolol (propranolol marcado con isótopo radiactivo) en metanol o acetonitrilo sobre una columna de silicagel enlazada a aminopropil (15 cm x 4,6 mm), operada a 50 oC. A la fase móvil compuesta por dióxido de carbono líquido se le adicionó 10 % de metanol como modificador orgánico y 0,1 % de trietilamina, a una presión de 3200-3400 psi y una velocidad de flujo de 5 mL/min. La detección radioactiva se realizó con un monitor radiactivo Berthold LB507A ajustado a una celda de flujo de alta presión.
El método espectrofluorométrico fue también utilizado para la determinación del propranolol y el atenolol.10 Estos medicamentos fueron disueltos en ácido clorhídrico (0,1 mol/L) y medida la fluorescencia de las soluciones a 305 nm para el atenolol y a 340 nm para propranolol. El método se aplicó para el análisis de tabletas y de soluciones inyectables.
Sin embargo, Roman y Agrawal11 plantean la utilización de un método más sencillo para la detección de microgramos en formas dosificadas de propranolol, por un método colorimétrico basado en la reacción con nitrito de sodio en presencia de ácido sulfúrico y se mide la absorbancia a 395 nm. El límite de detección de esta técnica fue de 2 a 50 mg/mL.
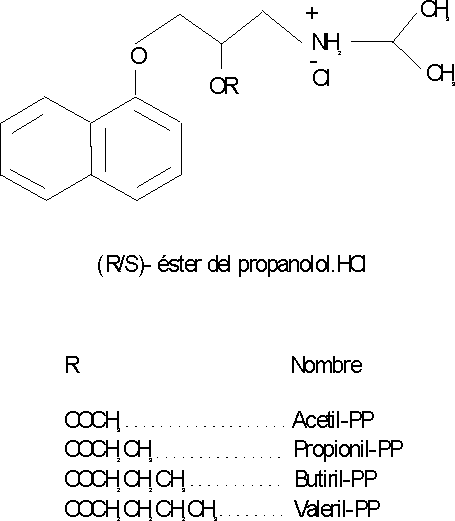
El primer método encontrado fue el empleado por Haginaka y otros14 en un estudio de enantioselectividad y orden de elución enantiomérica del racemato de propranolol y sus ésteres derivados: o-acetil, -propionil, butiril, -valeril (figura 2), sobre una columna ovomucoid (silicagel enlazada a una glicoproteína llamada ovomucoide [OVM]) de 150 x 4,6 mm de dimensión. Estos estudios se realizaron mediante la variación de pH del eluyente desde 3 hasta 7 y la utilización de diferentes modificadores orgánicos como son: 2-propanol, etanol, metanol y acetonitrilo, el flujo se mantuvo a 1 mL/min.
Se determinó que la enantioselectividad depende del pH de elución y del modificador orgánico utilizado. La inversión del orden de elución de los enantiómeros del racemato de propranolol y sus ésteres derivados ocurrió en un rango de pH entre 5 y 7 y/o por variación del modificador orgánico. Tomando en cuenta que el valor de pka del propranolol es de 9,45, este compuesto y sus ésteres son protonados a un valor de pH por encima del rango de elución estudiado; por tanto, al valor de pH entre 5-7 cuando ocurre la inversión del orden de elución de los enantiómeros, la OVM se carga negativamente por causa de su punto isoeléctrico, que se encuentra entre 3,8 y 4,3. ]]>
Este mismo método fue empleado por Ikeda y Hamasaki,15 para la separación de varios medicamentos enantioméricos, pero utilizaron como fase estacionaria quiral celulosa tris-(3,5-dimetilfenilcarbamato) en una columna Chiralcel OD (25 cm x 4,6 mm). La fase móvil empleada fue perclorato de sodio (0,05 mol/L)/ acetonitrilo (7:3), con un flujo de 1 mL/min para el caso específico del medicamento propranolol.Otro tipo de columna quiral como la quiral-AGP (10 cm x 4 mm) fue empleada para la separación de los enantiómeros del propranolol por Haupt y otros,16 quienes utilizaron como fase móvil buffer de ácido fosfórico (1 mol/L) / hidróxido de sodio (1 mol/L) y como modificadores Tween 20 y ácido heptanoico, ajustado para una fuerza iónica de 0,1 y a un valor de pH entre 4,5-6,5; el flujo empleado fue de 0,9 mL/min y detección a 250 ó 280 nm.
Una columna similar utilizaron Enquist y Hermansson,17 para la separación de los enantiómeros de agentes ß-bloqueadores, pero como fase móvil emplearon buffer fosfato que contenía diferentes concentraciones de modificadores no cargados, N,N-dimetiloctilamina (DMOA) o (-)-terodilina. La concentración de buffer fosfato fue 0,01 mol/L en esta fase móvil y 0,02 mol/L en las fases que contenían modificadores cargados. El pH se ajustó a 7,2 con NaOH y un flujo de 0,9 mL/min, y la detección entre 300 y 400 nm (excitación a 295 nm). La enantioselectividad se optimizó cuando se añadió un aditivo en la fase móvil.
Erdensson y otros18 combinaron la utilización de la columna quiral con la derivatización del analito para realizar la separación de ß-bloqueadores enantioméricos, ya que éstos son separados en una columna de silicagel enlazada a ácido a- 1-gli-coproteína (3 cm x 3,0 mm), después de ser convertidos en derivados de oxazolidinona por reacción con solución de fosgeno al 20 % en tolueno. La fase móvil utilizada fue buffer fosfato de pH=7,0/propan-2-ol (de 4 hasta 15 %), a una velocidad de flujo de 0,5 mL/min y detección a 215 nm.
El empleo de aditivos quirales en la fase móvil también aportó buenos resultados a Pettersson y otros19 cuando emplearon el contraión N-benziloxicarbonil glicil-L-prolina (ZPG), el cual fue añadido a la fase orgánica para la separación directa de los enantiómeros no derivatizados de amino-alcoholes, así como algunos agentes ß-bloqueadores adrenérgicos. La separación se realizó en una columna LiChrosorb Diol (15 cm x 3 mm) y como fase móvil utilizaron diclorometano saturado en agua con ZPG (25 mmol/L) y trietilamina (0,2 mmol/L), y detección ultravioleta. La estereoselectividad fue alta para alprenolol, metoprolol y propranolol.
Los autores plantean que el contraión contiene un grupo carboxilo que brinda energía electrostática o asociación a complejos mediante enlaces por puente de hidrógeno (pares-iónicos) con aminas en solventes orgánico. La ZPG también tiene una función carbamato y una amida que pueden dar interacciones adicionales, como por ejemplo los enlaces de hidrógeno con grupos hidroxilos en amino-alcoholes, por lo que es posible una interacción por varios puntos. Además reviste gran importancia la distancia de enlace en la selectividad quiral y ésta se pierde cuando el hidroxilo se encuentra en una posición alejada del grupo amino.
La adición de una amina a la fase móvil (por ejemplo trietilamina) provoca la competencia de ésta con los amino-alcoholes enantioméricos por la formación del par-iónico con ZPG, y además compite por la limitada capacidad de adsorción de la fase estacionaria.
Otro contraión empleado fue el ácido d-10-camforsulfónico por Gupta y otros20 para la separación de los enantiómeros del propranolol por CLAR en columna Zorbax-CN (25 cm x 9,5 mm). La fase móvil de baja polaridad contenía al contraión quiral y la ter-butilamina como base en diclorometano/ /hexano/acetonitrilo (79:20:1) y detectado a 280 nm. Los resultados de la investigación demostraron que la resolución aumenta cuando se realiza una recirculación de la fase móvil con las mezclas a separar.
La derivatización del propranolol con (+)-1-(9-fluorenyl) etilcloroformato también fue empleada para lograr la separación quiral y el mejoramiento de la detección, después se efectuó una técnica de CLAR en columna MicroPac SP C8 (15 cm x 4 mm), como fase móvil acetato de sodio / acetonitrilo (3:7) a un flujo de 2mL/min y detección fluorescente a 345 nm (excitación a 265 nm) o detección UV a 254 nm. Cuando se realizó la detección por fluorescencia se detectaron interferencias que fueron eliminadas por absorbancia UV.21
Sin embargo, Mulder y Conemans22 experimentaron la derivatización con isocianato de 2,3,4,6-tetra-O-acetil-ß-D-glucopiranosil, después de realizar una extracción en suero con diclorometano. Los derivados D y L-propranolol fueron separados por CLAR en columnas Spherisorb ODS, se utilizó dihidrogenofosfato de amonio (0,02 mol/L)/acetonitrilo (21:29) como fase móvil y detección a 230 nm. Un estudio similar fue realizado por otros autores,23 donde los enantiómeros del propranolol y 10 compuestos relacionados fueron separados por formación de derivados similares al experimento anterior o con isotiocianato de 2,3,4-tri-O-acetil-alfa-D-arabinopira-nosil. Posteriormente se les realizó una técnica por CLAR en columna Ultrasphere ODS (15 cm x 4,6 mm), con elución isocrática desde 37 hasta 75 % de acetonitrilo en fosfato de amonio (0,02 mol/L).
Este mismo método es empleado por Biermann y otros,1 pero cambiando la amina contenida en la fase móvil por 0,5 % de isopropilamina. Emplearon una columna Chiralcel OD (25 cm x 4,6 mm), la presión se mantuvo en 200 bar a temperatura de 30 oC y el flujo fue variado desde 2 hasta 4 mL/min. La detección UV se realizó a 220 nm. Se plantea que el aditivo básico en la fase móvil mejora el área del pico, pero incrementa ligeramente el tiempo de retención del último enantiómero eluido.
Una de las aplicaciones más importantes de esta técnica de reconocimiento quiral consiste en que permite evaluar la pureza enantiomérica, porque se puede determinar hasta niveles trazas de una forma enantiomérica en presencia de otra.
El reconocimiento quiral y la resolución racémica se observó con un grupo determinado de compuestos utilizados en el tratamiento clínico, dentro de los que se encuentran el grupo de los ß-bloqueadores. Estos estudios perfeccionaron el conocimiento y aplicación de las interacciones quirales con ß-ciclodextrina.
Para el reconocimiento quiral con ciclodextrina fue necesario algunos requerimientos técnicos, por ejemplo: se debe formar un complejo de inclusión, y éste debe ser de un acceso relativamente permeable entre la mitad complejada y la ß-ciclodextrina. Además, el centro quiral o un sustituyente de éste debe estar cerca e interactuar con el orificio de la cavidad de la ciclodextrina, que es donde se encuentran localizados los grupos unidireccionales 2 y 3-hidroxilo, los cuales son considerados importantes en el reconocimiento quiral.
Mediante esta técnica se observaron diferencias importantes entre los complejos de los isómeros d y 1 del propranolol con respecto a su grupo amino secundario. En el complejo d-propranolol, el nitrógeno fue localizado idealmente por el hidrógeno enlazado por ambos grupos, 2 y 3-hidroxilo de la ciclodextrina, con una distancia de enlace de 3,3 y 2,8 Å respectivamente. Mientras que la amina en el complejo 1-propranolol estuvo posicionada menos favorablemente para el enlazamiento a hidrógeno, y la distancia de enlace para encerrar los grupos 2 y 3-hidroxilo de la ciclodextrina fue de 3,8 y 4,5 Å respectivamente. Esto sugiere que el d-isómero podrá interactuar preferentemente con la ciclodextrina y de este modo ser mayormente retenido.
Por esta propiedad de la ciclodextrina de formar complejos, fue empleada en electroforesis capilar para llevar a cabo la separación de los isómeros de algunos medicamentos por Quang y Khaledi,26 quienes utilizaron un capilar de sílica (62 cm x 50 mm) a 40 oC y con un voltaje de 20 kV con detección a 240 nm. El electrólito empleado fue buffer fosfato de sodio (50 mmol/L) de pH=2,5 con ß-ciclodextrina (20 ó 30 mmol/L), y como aditivo un compuesto tetra-alquilamonio de cadena mediana para los analitos considerados como medicamentos básicos o emplearon aditivos de cadena corta como: tetrabutil y tetrametilamonio que fueron los más efectivos y pudieron ser utilizados a concentraciones máximas de 150 mmol/L. Para la resolución óptica del propranolol se utilizó 35 mmol/L de ß-ciclodextrina y 150 mmol/L de fosfato de tetrabutilamonio con una corriente de 56 mA.
Este mismo método fue empleado por Aturki y otros27 pero con ß-ciclodextrina aniónica y una técnica de carga y descarga por ajuste de pH entre 2,5-6,2. Las separaciones fueron realizadas con un capilar de sílica fusionada (40 cm x 50 mm), operó a un voltaje de 15 kV y se utilizó cualquiera de los buffer siguientes: buffer fosfato (65 mmol/L) pH=2,5;buffer fosfato (51 mmol/L) pH=3,5; buffer acetato, pH=4,5 o buffer fosfato (75 mmol/L), pH=6,2. La detección se realizó a 214 nm o barriendo longitudes de onda desde 190 hasta 360 nm.
También han sido probadas diferentes tipos de ciclodextrinas28 para lograr la separación de las soluciones racémicas de terbutalina, monosulfato de terbutalina, propranolol, efedrina y bromofenilamina (0,2 mmol/L), las cuales son inyectadas sobre capilares de sílica fusionada (57 cm x 75 mm) con __a -ciclodextrina, ß-ciclodextrina o 2-hidroxipropil-ß-ciclodextrina a 25 oC. Los buffer fosfato pH=2,5-4,5; pH=5-9 y pH=9,5-11,5 se utilizaron como electrólitos soportes con voltajes entre 5-17 kV. La detección se realizó a 214 nm. Se optimizó la resolución de los enantiómeros teniendo en cuenta la concentración del buffer, el pH y el tipo de ciclodextrina.
Matchett y otros29 realizaron un estudio similar con otros tipos de ciclodextrinas para efectuar la separación de los enantiómeros del propranolol y de 4 análogos estrechamente relacionados. La electroforesis se ejecutó sobre un revestimiento capilar (20 cm x 25 mm) a temperatura ambiente, con una corriente constante de 5 mA. El detector UV fue seteado para valores máximos de longitud de onda 254-258 nm. Los buffer de corrida contenían metanol/ /dihidrogenofosfato de potasio (50 mmol/L) (3:7) y hasta un máximo de 35 mmol/L de ciclodextrina modificada. Se comparó el efecto de 3 ciclodextrinas: metil- ß- ciclo- dextrina (Me-ß-CD), hydroxietil -ß-ciclo-dextrina (HE-ß-CD) y hepta kis (2,3-di-O-acetil)-ß-ciclodextrina (Ac-ß-CD). Los resultados indicaron que el mayor valor de resolución quiral se obtuvo con HE-ß-CD con todos los analitos y la menor resolución analizada fue con Me-ß-CD y Ac-ß-CD; esto se explicó que era por las estructuras macrocíclicas y la potencia de los enlaces de hidrógeno. Se encontró que la presencia del grupo alquil no polar en los analitos mejoró el reconocimiento quiral.
Lic. Ritsie Ruiz Caballero. Centro de Química Farmacéutica. Ave 200 y 21, Atabey, municipio Playa, Ciudad de La Habana, Apartado 16042, Cuba.
1 Licenciada en Ciencias Farmacéuticas.
2 Licenciada en Química. Investigadora Aspirante.
3 Licenciado en Química. Investigador Auxiliar. ]]>