Descriptores DeCS: QUITINA /análisis; SUPOSITORIOS; ESTABILIDAD DE MEDICAMENTOS; ALMACENAJE DE MEDICAMENTOS.
En los últimos años se ha incrementado notablemente el estudio de los biomateriales, destacándose la utilización de sustancias poliméricas naturales y sintéticas en diversas ramas de la ciencia y la técnica. La quitina es un polímero natural de potente efecto como agente acelerador de la cicatrización,1 para el cual se reportan resultados satisfactorios en el tratamiento de diversas afecciones con pérdida de la cobertura cutánea.2-4
En el presente trabajo se trata por primera vez la introducción de la quitina cubana en la forma farmacéutica supositorio, destinada al tratamiento de afecciones anorrectales; por lo que hemos dirigido nuestra investigación hacia la comprobación de la posible interacción quitina-excipiente.
En la actualidad, las exigencias a una nueva forma farmacéutica incluyen los estudios de estabilidad como requisito indispensable para el registro y venta de medicamentos.5 Los supositorios deben ser química, física y microbiológicamente estables al menos durante 2 años a temperatura de refrigeración, según recomienda la mayoría de los autores.6,7
La quitina en forma de polvo resulta extremadamente estable. Los estudios realizados por hidrólisis ácida del polímero reportados en la literatura, proponen un tiempo de vencimiento superior a los 5 a, y plantean como productos de la hidrólisis total: quitosana, N acetilglucosamina, D glucosamina y ácido acético (Nieto OM. Quitina. Su estudio y utilización como fármaco acelerador de la cicatrización. Tesis presentada en opción al título de Doctor en Ciencias Farmacéuticas. Facultad de Farmacia y Alimentos. Universidad de La Habana.1993).Considerando las propiedades físico-químicas de la quitina, especialmente su limitada solubilidad y reactividad,8 se dificulta su análisis cuantitativo.
Los métodos reportados en la bibliografía carecen de valor desde el punto de vista práctico para el control químico de este fármaco y su seguimiento, una vez introducido en una forma dosificada por constituir técnicas indirectas basadas en la estimación de alguno de los productos de hidrólisis.9-11 La gravimetría directa ha sido propuesta como una adecuada opción para realizar el control de calidad del ungüento de quitina al 5 % (Bilbao O. Evaluación de quitina en preparaciones farmacéuticas. Tesis presentada en opción al título de Doctor en Ciencias Farmacéuticas. Facultad de Farmacia y Alimentos. Universidad de La Habana. 1993). Sin embargo, esta técnica carece de la especificidad y sensibilidad exigida para su aplicación en estudios de estabilidad, por lo cual se complementa con la espectroscopia IR, según la metodología propuesta para el estudio de estabilidad de los supositorios de quitina 200 mg (Suárez Y. Supositorios de quitina, nueva opción en la terapéutica rectal. Tesis presentada en opción al título de Master en Tecnología y Control de Medicamentos. Instituto de Farmacia y Alimentos. Universidad de La Habana.1996).
Tiempo de liquefacción: se realizó el ensayo por triplicado en el equipo Erweka acoplado al baño termostatado que se ajustó a 37 ± 0,5 °C. Se determinó ![]() y DE.
y DE.
Expectroscopia IR: se determinó el espectro IR al residuo sólido seco que se obtuvo por gravimetría, se dispersó éste en fase sólida de bromuro de potasio. Estos espectros se compararon a lo largo del estudio entre sí.
Para las variables continuas: peso y contenido de quitina se aplicó análisis confirmatorio para detectar diferencias estadísticas de p < 0,05 mediante pruebas de normalidad y homogeneidad de varianzas. Para el tiempo de liquefacción que resultó ser una variable discreta, se seleccionaron las pruebas de Kruskal-Wallis para el factor temperatura y la prueba de Friedman para el efecto del tiempo de almacenamiento.
| | | ]]> Lote 5004 | ||||||||
| | | | ||||||||
| | | | | | | ]]> Peso | | | ||
| Tiempo (mes) | | | | | | | | ]]> (min) | | |
| | ||||||||||
| | | | | | | | ]]> 2,06 | | | |
| | | | | | | | ]]> 2,07 | | | |
| | | | | | | | ]]> 2,07 | | | |
| | | | | | | | ]]> 2,06 | | | |
| | ||||||||||
| | | | | | | ]]> 96,40 | | | | |
| | | | | | | ]]> 96,32 | | | | |
| | | | | | | ]]> 96,45 | | | | |
| | ||||||||||
| | | | | | ]]> 11,6 | | | | | |
| | | | | | ]]> 11,6 | | | | | |
| | | | | | ]]> 13,3 | | | | | |
Para el peso de los supositorios se detectaron por la prueba de Duncan diferencias significativas (p < 0,05) entre los 3 lotes. Sin embargo, el peso dentro de cada lote manifestó el mismo comportamiento en el tiempo y tampoco varió apreciablemente con la temperatura de almacenamiento, por lo que este parámetro resultó estable en las diferentes condiciones ensayadas durante los 24 meses de estudio.
El tiempo de liquefacción mostró para cada temperatura un comportamiento similar entre lotes, manifestando cierta tendencia al aumento. El análisis de varianza realizado por las pruebas Kruskal-Wallis, dio que las diferencias para este parámetro entre las temperaturas de almacenamiento fueron significativas. De igual forma, las diferencias resultaron estadísticamente significativas para las prueba Friedman con respecto al factor tiempo de almacenamiento (fig. 1).
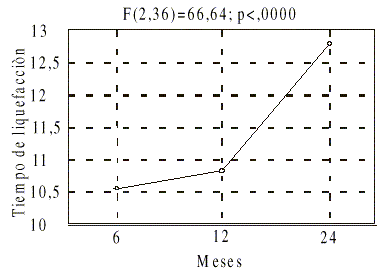
FIG.1. Efecto del tiempo de almacenamiento en el tiempo de liquefacción.
En relación con el contenido de quitina, mediante el análisis confirmatorio de los datos, se comprobó que el único factor del diseño que provocó diferencias significativas (p < 0,05) fue el lote, al conocer por la prueba de Duncan que las diferencias fueron del lote 5004 con respecto al resto (fig. 2).
Además se verificó que no existieron diferencias significativas para cada lote en el tiempo (fig. 3).
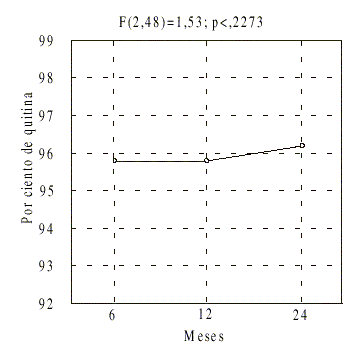
FIG.3. Efecto del tiempo de almacenamiento en el contenido de quitina.
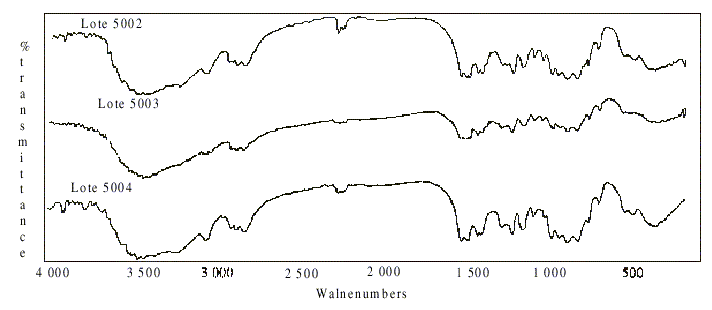
Estos resultados fueron corroborados con el análisis cualitativo por espectrofotometría IR de los residuos procesados por gravimetría. Los espectros de los 3 lotes almacenados a temperatura ambiente transcurridos 2 a desde el momento de su producción, coincidieron plenamente en cuanto a localización e intensidad de las bandas características de los grupos funcionales (fig. 4). ]]>
En la tabla 2 se presenta el conteo microbiológico aplicado a los 3 lotes almacenados a temperatura ambiente, llevados a cabo a los 6, 12 y 24 meses. Se demostró que también desde el punto de vista microbiológico el producto fue estable (tabla 2).
| Ensayo | | | | |
| Bacterias | ]]> 6 | | | |
| | | | | |
| | | ]]> 80 x g | | |
| Enterobacterias | | | | |
| | | | | |
| ]]> 24 | | | | |
| Hongos | | | | |
| | | ]]> < 10 x g | | |
| | | | | |
| Microorganismo | | | | |
| aislado | ]]> 12 | | | |
| | | | | |
| Resultados | | | ]]> Cumple | |
| | | | | |
| | | | |
La menor cantidad de fármaco en el lote 5004 pudo ser atribuida a la pesada durante la elaboración. Esta disminución no afecta significativamente la calidad del producto, pues no afectó el peso ni la liquefacción, de modo que careció de interés. De manera que el contenido de quitina osciló ligeramente dentro del rango correcto de dosificación. Es bien conocido que la gravimetría carece de la especificidad requerida para su aplicación en estudios de estabilidad, pero al determinar los espectros IR a los residuos insolubles, pudimos descartar la posibilidad de degradación química por comparación de los resultados de cada muestreo en el tiempo.
La estabilidad de la quitina en el tiempo independientemente de la temperatura de almacenamiento, constituyó un resultado valioso y a la vez esperado, teniendo en cuenta los estudios de estabilidad realizados por Nieto en 1993 al polvo de quitina y la escasa posibilidad de interacción química quitina-excipiente.
Con la combinación de la gravimetría directa con la espectroscopia IR, garantizamos que los valores obtenidos en la cuantificación fueron debidos únicamente al fármaco inalterado presente en los supositorios.
La estabilidad química de esta nueva formulación también quedó confirmada. A pesar de las diferencias observadas para el contenido de principio activo entre lotes, todos los resultados se encontraron dentro del rango aceptable de 90 a 110 %.
Las tiras de aluminio termosellable que fueron utilizadas como envase, ofrecieron adecuada protección al supositorio. Los almacenados a temperatura ambiente cumplieron las exigencias para medicamentos no estériles. Por tal motivo pudiera considerarse adecuada esta temperatura para la conservación de este nuevo producto.
Subject headings: CHITIN/analysis; SUPPOSITORIES; DRUG STABILITY; DRUG STORAGE.
1 Máster en Tecnología y Control de Medicamentos.
2 Doctor en Ciencias Farmacéuticas.
3 Licenciado en Matemáticas. ]]>