Celeste Aurora Sánchez González1 y Santa Deybis Orta Hernández2
]]>Se describió la importancia como instrumento de consulta, del compendio nacional de sustancias activas y asociaciones de uso farmacéutico industrial aceptadas y rechazadas en Cuba. Se identificó la información de seguridad para el uso racional que incorpora la clasificación terapéutica adoptada y la estructura organizativa de estas Normas Farmacológicas Cubanas (NFC). Se cuantificó su aplicación por el Centro para el Control de la Calidad de los Medicamentos (CECMED), usuarios cubanos y extranjeros durante el período 1996 al 2000, para determinar grados de novedad y caracterización terapéutica, mediante el análisis de Ensayos Clínicos Autorizados y Registros de Medicamentos otorgados. Se dimensionó el impacto en la Reglamentación Farmacéutica Nacional y la interacción con otras regulaciones. Se identificaron las perspectivas de desarrollo en su alcance y contenido. Se concluyó la utilidad de las NFC en la adecuada clasificación del grado de novedad de los productos, el ágil y preciso manejo y evaluación de trámites, así como en la caracterización del enfoque terapéutico.
]]> DeCS: FARMACOLOGIA/normas; PREPARACIONES FARMACEUTICAS; LEGISLACION DE MEDICAMENTOS; CUBA.
Las Normas Farmacológicas constituyen un esfuerzo de las Autoridades Reguladoras de Medicamentos (ARM) en el campo regulador relacionado con el uso racional de medicamentos, con las que se da respuesta por una parte, a la necesidad de brindar productos con una justificación terapéutica, basados en normas y procedimientos aprobados y por otra, a desarrollar instrumentos de consulta para las actividades relacionadas con el lanzamiento de nuevos productos al mercado. Permiten establecer de manera transparente uno de los aspectos más importantes a tomar en cuenta para determinar el grado de novedad de los medicamentos en las solicitudes de Registro, que es el uso establecido en el país y enmarcar así decisiones técnicas para su aprobación. En ellas se recopilan los fármacos y sus asociaciones aceptados y rechazados para la producción de medicamentos y la información esencial para su seguridad, como resultado del estudio y revisión permanente de los Ministerios de Salud, lo que es práctica habitual en países latinoamericanos del Pacto Andino y Centroamérica. Son varios los países con experiencia en este trabajo, entre los que se pueden citar Venezuela, Colombia, República Dominicana, Nicaragua y Bolivia.1-5
Hasta 1994, Cuba no tenía antecedentes, ni había realizado un trabajo de este tipo. A partir de esta fecha se comienzan las actividades, contemplando no solo la elaboración del documento, sino también su mecanismo de actualización permanente. Son premisas de importancia al respecto la Reunión Iberoamericana sobre Registro, Inspección y Control de la Calidad de Medicamentos celebrada en Madrid en 1991, donde se incorporó Cuba al Área de Armonización del Pacto Andino y la realizada en 1993 en Santafé de Bogotá, que acordó la elaboración de las Normas Farmacológicas Andinas mediante el proceso de armonización de las ya existentes.
Las Normas Farmacológicas Cubanas (NFC) se confeccionaron a finales de 1995 gracias a un trabajo regional desarrollado conjuntamente con las ARM de Venezuela y Colombia y con el patrocinio de la Organización Mundial de la Salud (OMS). De ello resultó un compendio con formato y características propias, de las sustancias y sus asociaciones que han sido utilizadas para la fabricación de medicamentos, tanto aceptadas como rechazadas, de acuerdo con el uso histórico de estas; así como de las advertencias, contraindicaciones y precauciones trascendentes, asociadas con la acción farmacológica, que deben aparecer obligatoriamente en los textos para impresos e información para pacientes y profesionales de la salud. Durante su elaboración se realizaron consultas a los Grupos de Especialidades Médicas, Comisión del Formulario Nacional (Actas de la Comisión del Formulario Nacional. MINSAP. Ciudad de la Habana, 1981-1995), funcionarios del Ministerio de Salud Pública, especialistas que participan en la investigación y desarrollo de productos biofarmacéuticos, Industria Farmacéutica y personal especializado. El compendio obtenido se puso a disposición de los usuarios identificados para su explotación a partir de 19966 y como objetivo del presente trabajo se propusieron:
Por tratarse de la primera edición, no se enjuició ni cuestionó el uso establecido para las sustancias, ya que el objetivo principal consistió en brindar el más fiel reflejo de la realidad, quedando para el futuro la depuración de algunas sustancias obsoletas y la reconsideración de otros aspectos que pudieran ser de utilidad. Con el mismo enfoque la clasificación se realizó atendiendo al principal uso histórico en Cuba.
Se recopilaron un total de 1 059 sustancias, de ellas 1 009 aceptadas y 50 no aceptadas, 184 asociaciones aceptadas y 136 no aceptadas y 886 normas para textos de información a pacientes y profesionales de la salud.
La estructura de la NFC se ejemplifica en el anexo. En el que se muestra la organización de las NFC,7 con un formato de 5 niveles; los cuatro primeros idénticos al ATC y como quinto la norma, a saber:
]]> Primer nivel: grupo anatómico principal (14 en total) identificado por una letra, Ej. C
Segundo nivel: grupo terapéutico principal (86 en total), identificado por dos dígitos, Ej.C01
Tercer nivel: subgrupo terapéutico (199 en total), identificado por una letra, Ej. C01A
Cuarto nivel: subgrupo químico/terapéutico (451 en total), identificado por una letra, Ej. C01AA
Quinto nivel: normas identificadas con dos dígitos, las que pueden ser normas generales, de sustancias y asociaciones aceptadas, leyendas obligatorias y sustancias y asociaciones no aceptadas (Ej. 01, 02).
Para facilitar la consulta y manejo del documento las NFC incluyeron 2 índices, uno por niveles del ATC y otro por sustancias ordenadas alfabéticamente, se anexaron las relaciones de sustancias ventajosamente sustituidas y de asociaciones aceptadas y no aceptadas.
Desde 1993 se establecieron en Cuba las Categorías de Novedad de los medicamentos para su Registro y Autorización de Ensayos Clínicos atendiendo al uso establecido en el país (Requisitos para las Solicitudes de Inscripción, en el Registro de Medicamentos de Uso Humano. República de Cuba. CECMED. Ciudad de La Habana, 1993, 1996, 1998 y 2000) y en función de estos la magnitud de la documentación requerida para la solicitud de estos trámites, sin embargo, no estaban recopiladas en ningún documento oficial publicado las sustancias con uso reconocido.
En la tabla 1 se resumen los grados de novedad para los 492 productos registrados y los 82 ensayos clínicos autorizados en este período.
TABLA 1. Productos Registrados y Ensayos Clínicos Autorizados por Grado de Novedad según NFC
| Categorías | AEC | Registro | Total |
| A | ]]> 43 | 10 | 53 |
| B | 5 | 1 | 6 |
| C | 32 | 64 | ]]> 96 |
| D | 2 | 417 | 419 |
| Total | 82 | 492 | 574 |
AEC: Autorización de Ensayos Clínicos; Registro: Productos Registrados; Categorías: establecen el grado de novedad de las sustancias; A: nuevas entidades moleculares; B: nuevas asociaciones; C: productos que circulan por primera vez en Cuba; D: productos genéricos.
]]>Resulta lógico el comportamiento numérico que se observa en la tabla 1, donde se destaca el mayor número de estudios clínicos (43) en las nuevas entidades moleculares y los productos de uso reconocido en el extranjero pero que se utilizan por primera vez en Cuba (32), mientras que la aprobación mediante el Registro para la comercialización es fundamentalmente a expensas de los productos genéricos (417). Todas las cifras que se han mencionado tienen un respaldo de aseguramiento de calidad en la NFC para el proceso de evaluación de los productos, a partir de su correcta clasificación.
En la tabla 2 se muestra la ubicación en las NFC de los productos que fueron evaluados para el Registro y Autorización de Ensayos Clínicos, este aspecto constituye un elemento importante en la caracterización terapéutica de los medicamentos, productos biológicos y naturales, lo que permite identificar el campo de la farmacología clínica a que se dirige el desarrollo de la investigación clínica y la comercialización de productos nacionales y extranjeros en Cuba.
TABLA 2. Ubicación en las NFC de los productos registrados y ensayos clínicos autorizados. CECMED. 1996-2000
| Grupo anatómico | AEC | Registro | Total |
| A (alimentario y metabólico) | ]]> 5 | 48 | 53 |
| B (sangre y derivados) | 4 | 26 | 30 |
| C (cardiovascular) | 4 | 70 | 74 |
| D ( dermatológicos) | 10 | ]]> 34 | 44 |
| G (genitourinario) | 0 | 36 | 36 |
| H (hormonas) | 0 | 12 | 12 |
| J (antiinfecciosos) | 11 | 77 | ]]> 88 |
| L (antineoplásicos e inmunomoduladores) | 41 | 24 | 65 |
| M (músculo-esquelético) | 2 | 22 | 24 |
| N (nervioso) | 1 | 68 | 71 |
| P (antiparasitarios) | ]]> 1 | 18 | 17 |
| R (respiratorio) | 1 | 27 | 28 |
| S (órganos sensoriales) | 0 | 10 | 10 |
| V (varios) | 2 | ]]> 20 | 22 |
| Total | 82 | 492 | 574 |
AEC: Autorización de Ensayos Clínicos; Registro: Productos Registrados
Se destacan los estudios clínicos en el grupo de los antineoplásicos e inmunomoduladores (41), a expensas del desarrollo de anticuerpos monoclonales y vacunas terapéuticas contra el cáncer, y el grupo de antiinfecciosos (11) con el desarrollo de las vacunas profilácticas, incluyendo las combinadas. En cuanto a la aprobación de productos para la comercialización, el mayor número de productos a estado dirigido a las enfermedades más frecuentes causadas por infecciones (77) y afecciones cardiovasculares (70).
Las NFC se encuentran interrelacionadas con los documentos normativos y reguladores inherentes a su alcance, entre los que se encuentran los requisitos para el registro como se señaló, los requisitos para los ensayos clínicos (Requisitos de Autorización y Modificación Ensayos Clínicos. CECMED. La Habana, 2000), las regulaciones para la confección de textos para impresos e información de medicamentos, y la Opción de Consulta del Sistema Automatizado para el Registro de Medicamentos de la OMS SIAMED, en su Versión Nacional (Sistema Automatizado de Medicamentos de la OMS. SIAMED. CECMED. La Habana, 1996).
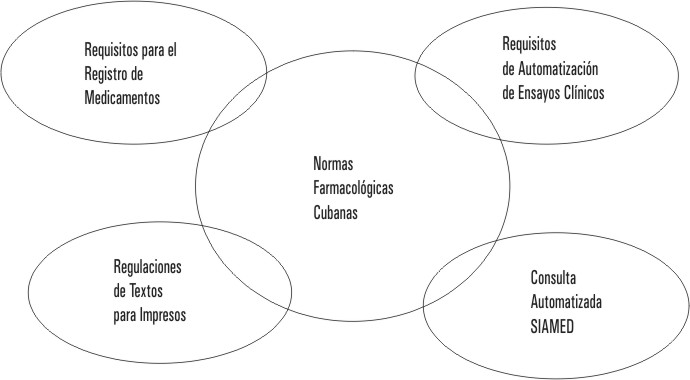
De esta forma los Requisitos de Registro y Autorización de Ensayos Clínicos establecen las Categorías de Novedad, que pueden ser identificadas solo con el empleo de las NFC, las Regulaciones para Textos e Información del Medicamento, norman la ubicación y formato de los textos obligatorios, lo que desde el punto de vista de seguridad terapéutica solo se describe de manera uniforme y precisa en las NFC, y la consulta computadorizada de las NFC se realizan mediante el SIAMED. Por todo ello resulta evidente el nivel superior alcanzado en el entorno regulador y la contribución a la continuidad y coherencia de los procesos de Autorización de Ensayos Clínicos y Registro de Medicamentos, así como al uso racional de estos, que las NFC han brindado. En la figura se muestra un esquema ilustrativo de las NFC y su impacto en el marco regulador nacional de medicamentos.
FIG. Dimensión del impacto de las NFC en el Marco Regulador.
ANEXO. Ejemplo del Formato de las NFC
| C | SISTEMA CARDIOVASCULAR |
| C01 | TERAPIA CARDíACA |
| 01 (Norma General) | En los textos de los materiales de envase impresos de los productos elaborados con sustancias de este grupo deberá aparecer en Advertencias: producto de uso delicado que debe ser administrado ]]> bajo estricta vigilancia médica |
| C01A | GLUCÓSIDOS CARDÍACOS |
| C01AA | Glucósidos digitálicos |
| 01 (Norma de Aceptación de Sustancias) | Se aceptan: Deslanósido Digitoxina Digoxina |
| C01AC | Glucósidos del estrofanto |
| 01 | Se acepta: Ouabaína |
| 02 (Norma de No Aceptación de Asociación) | No se acepta la estrofantina K por estar ventajosamente sustituida |
| C01B | ANTIARRÍTMICOS, CLASE I Y III Las sustancias que se incluyen en estos grupos son clasificadas teniendo en cuenta la clasificación de Vaughan Williams. La división de la clase I de antiarrítmicos puede variar en dependencia de la literatura que se utilice |
| 01 (Norma de No Aceptación ]]> Asociación) | No se aceptan asociaciones de antiarrítmicos con |
| C01BA | Antiarrítmicos, clase IA |
| 01 (Norma de Aceptación de Sustancia) | Se aceptan: Clorhidrato de procainamida Disopiramida (base y fosfato) Quinidina (sulfato y poligalacturonato) |
| 02 (Norma de No Aceptación de Sustancia) | No se acepta la ajmalina por estar ventajosamente sustituida |
Subject headings: PHARMACOLOGY/standars; PHARMACEUTICAL PREPARATIONS; LEGISLATION; DRUGS; CUBA
Recibido: 2 de febrero de 2003. Aprobado: 27 de febrero de 2003.
M. Celeste Aurora Sánchez González. Avenida 1era e/ 168 y 170, Edificio D-1, Apartamento 13, Reparto Flores, municipio Playa, Ciudad de La Habana, Cuba.
1 Master en Tecnología y Control de Medicamentos.
2 Especialista en Biotecnología.