Diamelva del Campo Portales,1 Mirna Fernández Cervera,2 Olga María Nieto Acosta,3 E. Gustavo Fernández Núñez4 y Loreta Delgado Díaz5
Para evaluar la capacidad como agente aglutinante de la quitosana cubana, derivada de quitina de langosta, se realizó un diseño experimental cuyas variables fueron la relación entre la masa de quitosana y granulado base, así como la concentración de ácido láctico en la solución aglutinante. Los resultados muestran que el porcentaje de ácido láctico no tiene influencia en las propiedades de los granulados elaborados con quitosana. La relación quitosana/granulado base influye sobre el tamaño de partícula promedio de los granulados estudiados. Las propiedades de los granulados elaborados con quitosana, independientemente de la relación de quitosana/granulado base y el porcentaje de ácido láctico, tienen un comportamiento intermedio entre la polivinilpirrolidona y la gelatina. Con el fármaco modelo sulfato de cloroquina, al emplear la quitosana cubana como agente aglutinante se obtuvieron tabletas con adecuadas propiedades. Adicionalmente se comparó su efectividad como aglutinante con respecto a excipientes de uso tradicional: gelatina, polivinilpirrolidona y celacol, con el clorhidrato de propranolol como fármaco modelo. Los granulados obtenidos muestran que la quitosana al 1 % tiene un comportamiento próximo al polivinilpirrolidona, celacol y gelatina, mientras que para las tabletas, independientemente del valor de la concentración de la quitosana, es similar al polivinilpirrolidona.
Palabras clave: Agente aglutinante, quitosana cubana, tabletas, vía húmeda
La quitosana, principal derivado desacetilado de la quitina, se obtiene a partir de los carapachos de los crustáceos, fundamentalmente camarones, cangrejos y langostas.1 Posee importantes propiedades biológicas que la hacen valiosa en aplicaciones biomédicas y veterinarias como su biocompatibilidad y biodegradabilidad, de especial relevancia al ser un producto natural.1,2 La quitosana es el único polisacárido catiónico natural,3 lo que le confiere características especiales y resulta útil en numerosas aplicaciones. A partir de la década de los 80 se inician los estudios para su empleo como excipiente farmacéutico. Este hecho fue motivado por la similitud estructural y de reactividad química que presenta con la celulosa.4 Entre las aplicaciones reportadas se destacan aquellas como diluente en tabletas de compresión directa,5-7 aglutinante en la granulación húmeda8-11 y desintegrante.12,13 Debido a ello, el propósito de este trabajo fue determinar las potencialidades como agente aglutinante de la quitosana cubana, derivada de quitina de langosta.
Para realizar el trabajo experimental se empleó quitosana obtenida en el Laboratorio “Mario Muñoz” (Cuba), a partir de quitina de langosta. Con vistas a evaluar la utilidad de la quitosana como agente aglutinante en la elaboración de tabletas, a partir de un granulado base (GB), se desarrolló un diseño factorial 22 con puntos adicionales (tabla 1). Los factores estudiados en este plan experimental fueron la relación entre la masa de quitosana y granulado base, en un rango de 4 x 10-3 a 12 x 10-3 g de quitosana/g de granulado base, así como la concentración de ácido láctico en la solución aglutinante (Analar®, Inglaterra) empleado como disolvente del biopolímero, en un intervalo entre 3-5 % (m/v), determinándose su influencia sobre las propiedades de los granulados obtenidos. Para todos los casos se mantuvo constante el volumen de solución aglutinante empleada. Los granulados se elaboraron por vía húmeda tradicional con el empleo de las soluciones de gelatina (Gelco, Colombia) al 10 % en medio acuoso y polivinilpirrolidona (PVP) (Basf, Alemania) al 10 % en medio alcohólico, como modelos. A partir del análisis de los resultados en el estudio con granulado base, fueron seleccionadas las condiciones del experimento V para la elaboración de tabletas de fosfato de cloroquina (Ningbo, Dahongying Pharmaceutical Co. Ltd., China), además de sustancias auxiliares de uso común en la industria farmacéutica para la fabricación de sólidos orales. Las tabletas se elaboraron en una máquina compresora rotativa de 16 estaciones Manesty D3B (Inglaterra), con la utilización de un troquel plano biselado ranurado 3/8. El peso fijado de las tabletas fue 350 mg.
Tabla 1. Matriz y resultados del diseño experimental para el estudio de la influencia de la relación de la quitosana y el ácido láctico en las propiedades físico-químicas y tecnológicas de los granulados
| Experimento | Relación | Ácido láctico | ]]> Densidad de asentamiento (g/cm3) | Densidad de vertido (g/cm3) | Velocidad de flujo (g/cm2 s) | Ángulo de reposo (°) | Tamaño de partícula (µm) |
| I | 12 | 5 | 0,62 ± 0,01 | 0,55 ± 0,05 | ]]> 19,11 ± 1,46 | 23,87 ± 0,79 | 509,5 ± 0,79 |
| II | 12 | 3 | 0,62 ± 0,01 | 0,54 ± 0,01 | 15,05 ± 0,01 | 24,83 ± 0,24 | ]]> 464,0 ± 0,55 |
| III | 4 | 5 | 0,65 ± 0,02 | 0,57 ± 0,04 | 19,11 ± 1,65 | 23,45 ± 1,10 | 499,27 ± 1,39 |
| IV | ]]> 4 | 3 | 0,65 ± 0,00 | 0,56 ± 0,00 | 12,93 ± 0,77 | 23,65 ± 0,79 | 415,58 ± 1,00 |
| V | 8 | 4 | ]]> 0,62 ± 0,01 | 0,57 ± 0,01 | 13,94 ± 0,96 | 22,96 ± 0,40 | 475,05 ± 0,74 |
| VI | 4 | 4 | 0,63 ± 0,05 | 0,55 ± 0,01 | ]]> 13,38 ± 0,02 | 23,72 ± 0,73 | 470,08 ± 0,25 |
| VII | 12 | 4 | 0,65 ± 0,01 | 0,56 ± 0,01 | 20,07 ± 0,03 | 23,33 ± 0,49 | ]]> 489,89 ± 0,69 |
| Gelatina 10 % | 0,61 ± 0,01 | 0,56 ± 0,02 | 19,11 ± 1,67 | 23,18 ± 1,38 | 474,90 ± 0,01 | ||
| PVP 10 % | 0,57 ± 0,00 | 0,47 ± 0,00 | ]]> 12,91 ± 0,76 | 27,18 ± 0,01 | 258,60 ± 0,01 | ||
Simultáneamente se llevó a cabo el estudio con el clorhidrato de propranolol (Ningbo, Dahongying Pharmaceutical Co. Ltd., China), como fármaco modelo, donde las soluciones de quitosana al 1 (Q1), 3 (Q3) y 5 % (Q5) disueltas en ácido láctico (2 %), fueron comparadas con aglutinantes clásicos de la industria farmacéutica como gelatina, PVP y metilcelulosa 450 (celacol) (Blanmer, Brasil). En todos los casos se mantuvo constante el volumen de solución aglutinante empleado. Las tabletas se elaboraron en una máquina tabletera de simple impacto de la firma Ronchi, modelo CN-4 (Italia), para lo cual se utilizó un troquel plano biselado con un diámetro de 9,25 mm y un peso por tabletas ajustado a 120 mg.
Para determinar la influencia de la quitosana en la calidad de los granulados elaborados fueron determinadas sus propiedades físico-químicas y tecnológicas, así como las propiedades físico-mecánicas y tecnológicas de las tabletas, respectivamente.14 A las tabletas obtenidas se les realizó el análisis químico con el empleo de las técnicas desarrolladas para tal efecto.15,16
El diseño de experimentos 22 con puntos adicionales, así como el procesamiento estadístico de los resultados derivados de este se realizó con la utilización del programa Design Expert Version 6.0.1. Para cada una de las variables respuestas se determinó el ajuste de los modelos estadísticos así como las ecuaciones que mejor describieran los resultados observados. Las diferencias entre los agentes aglutinantes convencionales y la quitosana en el comportamiento de los granulados o tabletas según corresponda, se analizaron con el empleo de las técnicas multivariadas de análisis de componentes principales y análisis de clusters, implementados en los programas SIMCA-P Version 11.0.0.0 y Statgraphics plus 5.0, respectivamente. Todas las determinaciones de las propiedades de los granulados y tabletas fueron realizadas por triplicado. En las tablas de resultados se muestran las medias y desviaciones estándar correspondientes a cada determinación.
Los resultados de las propiedades de los granulados se muestran en la tabla 1. Los valores de tamaño medio de partículas fueron óptimos, entre 0,4-0,5 mm, con excepción del granulado con PVP. Las propiedades de flujo en todos lo casos fueron adecuadas;17 no se mostraron diferencias apreciables entre los experimentos analizados. Los valores de las densidades aparentes por asentamiento y por vertido son similares, los que se encuentran dentro de los límites establecidos.14 Las densidades aparentes por asentamiento (ppa= 0,3524) y vertido (ppa= 0,2428), la velocidad de flujo (ppa= 0,4737) y el ángulo de reposo (ppa= 0,2029), mostraron un comportamiento independiente de la relación entre la masa de quitosana (Q) y granulado base (GB), y el porcentaje de ácido láctico en la solución aglutinante. Sin embargo, para el tamaño de partícula (Tp) se estableció un modelo matemático válido, el cual depende solamente de la relación entre la masa de quitosana/GB, que se ajusta a un modelo lineal cuya ecuación fue:
Como se observa en la figura 1, al aumentar la proporción de quitosana aumenta el tamaño de partícula de los granulados.
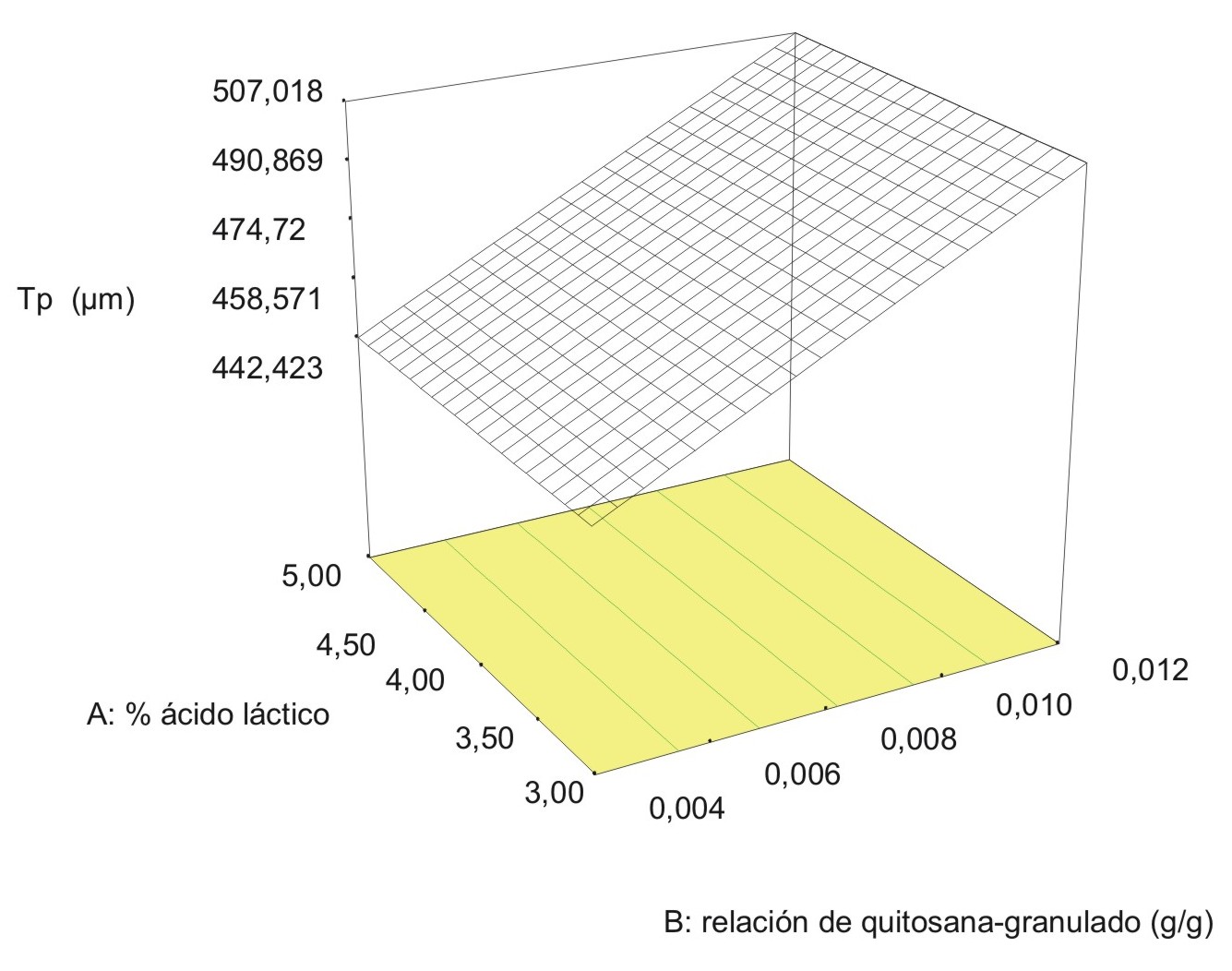
Fig. 1. Comportamiento del tamaño de partícula en los granulados elaborados con quitosana (diseño experimental).
Las diferencias y similitudes entre las propiedades físico-mecánicas y las composiciones granulométricas de los granulados, incluidos en el diseño experimental para el estudio de la quitosana, así como para el PVP y la gelatina, fueron procesadas con el empleo de un gráfico conjunto de marcas y cargas (fig. 2).

Fig. 2. Marcas y cargas para las propiedades de los granulados del plan experimental con quitosana (Q), PVP y la gelatina (G).
Tabla 2. Propiedades de los granulados y tabletas de fosfato de cloroquina
| Propiedades de granulados | Quitosana | Gelatina | Límites |
| Densidad asentamiento (g/cm3) | 0,68 ± 0,52 | 0,66 ± 0,01 | ]]> 0,6-0,7 |
| Densidad vertido (g/cm3) | 0,62 ± 0,80 | 0,58 ± 0,01 | 0,6-0,7 |
| Ángulo de reposo (°) | 23,0 ± 0,41 | 24,16 ± 0,01 | < 30,0 |
| Velocidad de flujo (g/cm2 s) | ]]> 20,06 ± 0,01 | 20,97 ± 0,01 | ≥ 7,0 |
| Tamaño de partícula (µm) | 499,87 ± 0,05 | 500,68 ± 0,01 | 0,4-0,7 |
| Propiedades de las tabletas | |||
| Peso (mg) | 355,5 ± 2,50 | ]]> 355,7 ± 1,30 | 332,5-367,55 |
| Altura (mm) | 3,90 ± 0,08 | 4,07 ± 0,01 | 3,8-4,2 |
| Dureza (Kgf/monsanto) | 6,5 ± 0,01 | 6,0 ± 0,01 | 5,0-7,0 |
| ]]> Desintegración* (min) | 4,0 ± 0,01 | 10,0 ± 0,01 | ≤ 30,0 min |
| Friabilidad (%) | 0,25 ± 0,05 | 0,38 ± 0,01 | ≤ 1,0% |
| HFR | 26,0 | ]]> 15,79 | ≥ 1,5 |
| Valoración (%) | 99,88 ± 1,34 | 101,35 ± 0,37 | 92,5-107,5 % |
| Disolución (%) | 98,48 ± 2,62 | 99,02 ± 3,58 | Q ≥ 70 % |
Las propiedades físico-químicas y tecnológicas de los granulados, al emplear el clorhidrato de propranolol (tabla 3), están acorde con los límites establecidos14 sin apreciar grandes diferencias en cuanto al comportamiento de las diversas formulaciones. No obstante, para definir la concentración de la quitosana con un comportamiento más cercano a los aglutinantes convencionales estudiados, se utilizó un gráfico de marcas en 2 componentes principales así como el análisis de clusters (fig. 3, a). Los resultados muestran una gran uniformidad en el peso y altura de las tabletas (tabla 3), lo que es indicativo de la calidad del proceso de compresión de los granulados. Se destaca además la buena resistencia mecánica de las tabletas a través de los valores de dureza, friabilidad y HFR. Al igual que para las propiedades de los granulados, se utilizó un gráfico de marcas en dos componentes principales y el análisis de clusters para definir las similitudes y diferencias entre las tabletas obtenidas con quitosana y los aglutinantes estudiados de uso frecuente en la industria farmacéutica (fig. 3, b).
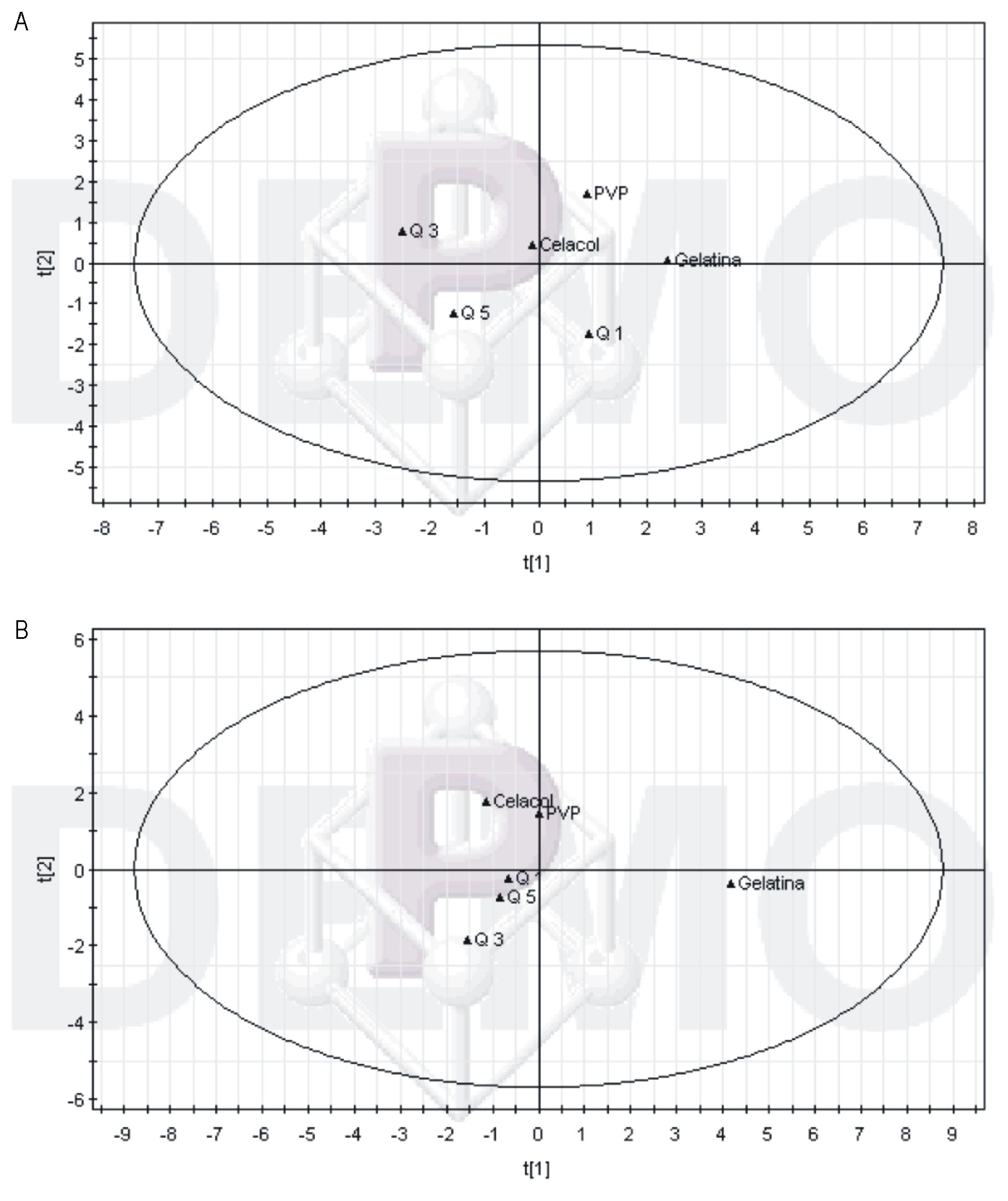
Fig. 3. Propiedades de los granulados (A) y tabletas (B) de clorhidrato de propanolol con el empleo de quitosana (Q1, Q3, Q5), gelatina,
celacol y PVP como aglutinantes.
Tabla 3. Propiedades de los granulados y tabletas de clorhidrato de propranolol
| Propiedad | Q 1 % | Q 3 % | Q 5 % | Gelatina | ]]> PVP | Celacol |
| Densidad asentamiento (g/cm3) | 0,69 ± 0,01 | 0,59 ± 0,08 | 0,63 ± 0,06 | 0,75 ± 0,01 | 0,70 ± 0,00 | 0,68 ± 0,02 |
| Densidad real (g/cm3) | ]]> 1,40 ± 0,09 | 1,43 ± 0,04 | 1,42 ± 0,10 | 1,43 ± 0,08 | 1,47 ± 0,14 | 1,45 ± 0,04 |
| Velocidad de flujo (g/cm2 s) | 10,10 ± 0,05 | 9,77 ± 0,10 | 9,30 ± 0,03 | ]]> 10,01 ± 0,07 | 9,87 ± 0,15 | 10,05 ± 0,02 |
| Porosidad (%) | 51 ± 0,00 | 59 ± 0,01 | 56 ± 0,00 | 48 ± 0,03 | 53 ± 0,01 | 54 ± 0,00 |
| ]]> Tamaño de partícula (mm) | 0,41 ± 0,01 | 0,36 ± 0,05 | 0,40 ± 0,09 | 0,39 ± 0,08 | 0,38 ± 0,08 | 0,39 ± 0,06 |
| Friabilidad granular (%) | 7,0 ± 0,46 | 7,3 ±0,38 | ]]> 7,5 ± 0,05 | 4,5 ± 0,01 | 4,5 ± 0,01 | 7,5 ± 0,00 |
| Propiedades de las tabletas | ||||||
| Peso (mg) | 120,3 ± 0,20 | 120,1 ± 0,10 | 120,2 ± 0,70 | 120,5 ± 0,30 | ]]> 120,5 ± 0,10 | 120,2 ± 0,10 |
| Altura (mm) | 2,8 ± 0,00 | 2,8 ± 0,00 | 2,8 ± 0,10 | 2,8 ± 0,10 | 2,8 ± 0,00 | 2,8 ± 0,30 |
| Dureza (kgf/monsanto) | ]]> 4,5 ±0,50 | 4,0 ± 0,20 | 5,0 ± 0,00 | 4,5 ± 0,50 | 5,5 ± 0,50 | 5,64 ± 0,10 |
| Friabilidad (%) | 0,22 ± 0,02 | 0,18 ± 0,40 | 0,24 ± 0,10 | ]]> 0,44 ± 0,00 | 0,27 ± 0,50 | 0,25 ± 0,30 |
| HFR | 20,78 | 22,33 | 20,62 | 10,21 | 20,36 | 22,56 |
| ]]> Desintegración* (min) | 5,0 ±0,50 | 5,0 ± 0,50 | 5,0 ± 0,50 | 7,0 ±0,50 | 5,0 ± 0,50 | 5,0 ± 0,50 |
| HDI** (%) | 92,0 | 98,6 | ]]> 90,7 | 32,0 | 90,7 | 100,0 |
| % disuelto 5 min | 38,9 | 29,4 | 27,1 | 37,2 | 41,7 | ]]> 51,6 |
| % disuelto 30 min | 100,0 | 100,0 | 100,0 | 100,0 | 100,0 | 100,0 |
Q (quitosana 1, 3 y 5 %)
* En agua a 37,0 ± 2 ºC
** Relación dureza-friabilidad/tiempo de desintegración (HDI= HFR/TD) x 100
El celacol produjo tabletas con los mayores valores del cociente HFR/tiempo de desintegración (TD) definido como HDI, por lo que fue seleccionado como el aglutinante estándar para calcular los valores de HDI, tomando este valor como base para comparar de modo relativo este índice en las tabletas preparadas con los aglutinantes ensayados. Basado en los valores de HDI se puede establecer el siguiente orden en cuanto a eficacia aglutinante: celacol > guitosana > PVP > gelatina. Todo esto permite plantear que la quitosana cubana puede utilizarse como agente aglutinante en tabletas de clorhidrato de propranolo; l su eficacia es comparable a la del celacol y el PVP.
To assess ability of Cuban quitosona as agglutination agent, derived from lobster quitine, we performed an experimental design of which he variable were: relationship between quitosana mass and granular base as well as lactic acid concentration in agglutination solution. Results shows that lactic acid percentage hasn’t influence on properties of granules processed using quitosana. Above mentioned relationship influences on average particle size of study granules. Properties of quitosana-processed granules, regardless of whether quitosana/granule base relationship and lactic acid percentage, have a intermediate behaviour between polyvinyl-pyrrolidone and gelatine. With model drug ,chloriquine sulfate, use of Cuban quitosana like agglutination agent, yields tablets with important properties. Also, we compared its effectiveness as agglutination agent regarding traditional excipients: gelatine, polyvinyl-pyrrolidone, and celacol, with propranolol chlorhydrate as model drug. Granules obtained shows that 1 % quitosana has a action similar to polyvinylpirrolidone, celacol, and gelatine, whereas in the case of tablets, regardless value of quitosana concentration, is similar to polyvinylpirrolidone.
Key words: Agglutination agent, Cuban quitosana, tablets, wet route.
1. Agulló E, Albertengo L, Pastor de Abram A, Rodríguez MS, Valenzuela F. Aplicaciones en alimentación y control ambiental. En: Pastor de Abram A (ed.) Quitina y quitosano: obtención, caracterización y aplicaciones. Perú: Pontificia Universidad Católica del Perú. Agosto, 2004. p. 220-2.
2. Agulló E, Mato R, Peniche C., Tapia C, Heras A, Pastor de Abram A, et al. Generalidades. En: Pastor de Abram A (ed.) Quitina y quitosano: obtención, caracterización y aplicaciones. Perú: Pontificia Universidad Católica del Perú; Agosto, 2004. p. 44-8.
3. Sandford PA, Hutchings GP. Chitosan –a natural cationic biopolymer. In: Yalpani M (ed.). Industrial Polysaccharides: Genetics Engineering, Structure/Properties relations and applications. Amsterdam: Elsevier Science B.V.; 1987. p. 363-76.
4. Machida Y, Nagai T. Chitin/chitosan as pharmaceutical excipients, Topics in Pharmaceutical Sciences. Breimer DD, Crommelin DJA, Mida KK (eds.). La Haya, 1989.
5. Sawayanagi Y, Nambu N, Nagai T. Directly compressed tablets containing chitin or chitosan in addition to lactose or potato starch. Chem Pharm Bull. 1982a;30:2935-40.
6. Sawayanagi Y, Nambu N, Nagai T. Directly compressed tablets containing chitin or chitosan in addition to mannitol. Chem Pharm Bull. 1982b;30:4216-8.
7. Kknapczyk J. Excipient ability of chitosan for direct tableting. Int J Pharm.1993; 89:1-7.
8. Henriksen I, Skaugrud O, Karlsen J. Use of chitosan malate as an excipient in wet granulation of three water soluble drugs. Int J Pharm. 1993;98:181-8.
9. Upadrashta SM, Katikaneni PR, Nuessle NO. Chitosan as a tablet binder. Drug Dev Ind Pharm. 1992;18:1701-8.
10. Ilango R, Kavimani S, Premila J, Nair DK, Jayakar B. Studies on tablets of sulfamethoxazole using chitosan. Indian J Pharm Sci. 1997;59:220-4.
11. Santos H, Veiga F, Pina M, Podczeck F, Sousa J. Physical properties of chitosan pellets produced by extrusion-spheronisation: influence of formulation variables. Int J Pharm. 2002;246:153-69.
12. Ritthidej G, Chomto P, Pummangura S, Menasveta P. Chitin and chitosan as disintegrants in paracetamol tablets. Drug Dev Ind Pharm. 1994;20:2109-34.
13. Nigalaye AG, Adusumilli P, Bolton S. Investigation of prolonged drug release from matrix formulations of chitosan. Drug Dev Ind Pharm. 1990;16:449-67.
14. Iraizoz A, Bilbao O, Barrios MA. Conferencias de Tecnología Farmacéutica II. Facultad de Farmacia y Alimentos. Departamento de Tecnología y Control de Medicamentos. Universidad de La Habana. ENPES, La Habana, 1990. p. 170-11, 237-42.
15. United Stated Pharmacopeia Convention (USP XXVI). The National Formulary Easton: Mack Printing; 2003. p. 356.
16. British Pharmacopoeia. General Notices Medicinal and Pharmaceutical Substances. Vol. II. London: The Stationary Office; 2000. p.1979.
17. Iegorava VI. Métodos de control de la calidad de los gránulos y tabletas. Industria Farmacéutica. URSS. 1964; No.1:33-5.
18. Haris Prashanth KV, Kittur FS, Tharanathan RN. Solid state structure of chitosan prepared under different N-deacetylating conditions. Carbohydr Polym. 2002;50:27-33.
19. Felt O, Buri P, Gurny R. Chitosan: a unique polysaccharide for drug delivery. Drug Dev Ind Pharm. 1998;24:979-93.
20. Georgakopoulus PP, Malamataris S. Lucust bean gum as a granulating and binding agent for tablet. Pharm Ind. 1980;42(6):642-6.
Recibido: 8 de enero de 2007. Aprobado: 9 de febrero de 2007.
Dra. C. Mirna Fernández Cervera. Instituto de Farmacia y Alimentos. Calle 23 No. 21425 entre 214 y 222, La Coronela, La Lisa, La Habana, Cuba. Correo electrónico: mirnafc@yahoo.com
1 Licenciada en Ciencias Farmacéuticas.
2 Doctora en Ciencias Farmacéuticas. Profesora Auxiliar.
3 Doctora en Ciencias Farmacéuticas. Profesora Titular.
4Ingeniero Químico. Investigador Agregado. Centro de Ingeniería e Investigaciones Químicas (CIIQ).
5 Master en Ciencias Tecnología y Control de los Medicamentos. Especialista A en Tecnología. Laboratorio “Reinaldo Gutiérrez.”