Desarrollo tecnológico de una formulación de dihidroergotoxina mesilato 0,3 mg/mL inyectable
Technological development of an injectable formulation of dihydroergotoxine mesylate 0.3 mg/mL
Anna Karelia Collado CoelloI; Lissete Martínez MirandaII; Alicia Lagarto ParraIII; Vivian Martínez EspinosaIV; Isbel Guerra SardiñasIV ]]>
I Licenciada en Ciencias Farmacéuticas. Investigadora Agregada. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). La Habana, Cuba.
RESUMEN
Los vasodilatadores cerebrales y periféricos son un conjunto de medicamentos muy heterogéneo, que tienen en común la capacidad de producir vasodilatación cerebral o periférica por mecanismos muy diferentes. Dentro de ese grupo se encuentra el fármaco que le da razón a este artículo, la dihidroergotoxina mesilato el cual estimula el ritmo del electroencefalograma e incrementa la utilización de glucosa en el cerebro. Se desarrolló una formulación inyectable estéril compuesta por dihidroergotoxina mesilato polvo, y cantidad suficiente del vehículo acuoso envasada en ampolletas de 1 mL de capacidad. Se desarrolló y validó una técnica analítica por cromatografía líquida de alta resolución para estudiar la estabilidad de la formulación y determinar la fecha de vencimiento de esta. Se comprobó la calidad microbiológica de la preparación, y se logró un producto que cumple satisfactoriamente con todas las especificaciones establecidas para preparaciones estériles. La tecnología obtenida fue fácilmente escalable.
]]>
Palabras clave: Dihidroergotoxina, dihidroergotamina mesilato, solución inyectable, estudio de estabilidad, control de la calidad.
ABSTRACT
Cerebral and peripheral vasodilators are a group of very heterogeneous drugs that have in common the capacity to produce cerebral or peripheral vasodilatation by different mechanisms. The drug that gave rise to this paper, dihydroergotoxine mesylate, is within this group. It stimulates the rhythm of the electroencephalogram and increases the utilization of glucose in the brain. A sterile injectable formulation composed of dihydroergotoxine mesylate powder and enough amount of aqueous vehicle was developed and bottled in ampoules of 1 mL. An analytical technique was developed and validated by high resolution liquid chromatography to study the stability of the formulation and to determine its expiration date. The quality of the microbiological preparation was proved, and a product that satisfactorily meets all the specifications established for sterile preparations was obtained. The technology obtained was easily scalable.
Key words: Dihydroergotoxine, dihydroergotoxine mesylate, injectable solution, stability study, quality control.
INTRODUCCIÓN ]]>
La dihidroergotamina mesilato o dihidroergotoxina mesilato como también se le llama no es más que ergotamina hidrogenada en las posiciones 9 y 10 de la sal mesilada. Es conocida químicamente como ergotaman-3,6,18-trione,9,10-dihydro-12hydroxy,2 metyl-5 phenylmethyl-5ª monomethasulfonato. Se utiliza en el tratamiento de los ataques agudos de migraña.1En cuanto a su utilidad terapéutica que se encuentra justificada en cuadros moderados de envejecimiento y demencia, con el objetivo de atenuar algunos síntomas propios (estado de alerta, memoria reciente, ansiedad, agitación), insuficiencia vasculometabólica encefálica crónica,2 secuelas de accidentes cerebrovasculares agudos, afecciones otovestibulares, oftalmopatías vasculares y la maculopatía senil.
Este fármaco es un bloqueante alfa adrenérgico, agonista parcial de los receptores dopaminérgicos D2 y de los serotoninérgicos 5HT2.2
Sus efectos secundarios son Hipotensión ortostática y/o permanente, congestión nasal, bradicardia moderada y molestias digestivas (5-10 %). Debe emplearse con precaución en caso de bradicardia sinusal o hipotensión arterial.3
Dicho esto se puede plantear que el objetivo del presente trabajo fue desarrollar una formulación inyectable de dihidroergotoxina mesilato 0,3 g/mL en ampolletas de 1 mL que sea estable física, química y microbiológicamente así como desde el punto de vista farmacológico, además del desarrollo de un método analítico para el análisis de la materia prima y del producto terminado.
MÉTODOS
Desarrollo tecnológico ]]>
En cuanto a la composición de los ensayos realizados, se emplearon agentes solubilizantes, antioxidantes, secuestrantes y preservativos antimicrobianos. Para seleccionar la mejor formulación muestras de cada ensayo, envasados en ampolletas incoloras de clase hidrolítica I, se almacenaron a 25 y 40 oC, y se evaluaron las características organolépticas, el pH y el contenido de dihidroergotamina, en las muestras recién elaboradas y transcurridos 6 meses. Para cuantificar el contenido de principio activo se utilizó el método que aparece en la monografía de la USP 27.4
Para lograr la esterilidad de la preparación se utilizaron 2 métodos, con el propósito de seleccionar el más adecuado, uno por filtración a través de membrana de nitrato de celulosa de 0,2 µm y otro por calor húmedo a 121 oC durante 20 min y filtración previa por membrana de nitrato de celulosa de 0,45 µm. Se observaron las características organolépticas, el pH, la esterilidad, la ausencia de pirógenos y el contenido de principio activo antes y después del proceso de esterilización.5
Con la fórmula y técnica seleccionada, se realizaron 3 ensayos para efectuar el estudio de estabilidad y predecir el tiempo de vida útil.
Estudio de estabilidad
Para el estudio de estabilidad se empleó la cromatografía líquida de alta resolución. Dicho estudio se realizó por el método de vida de estante, para lo cual se utilizaron muestras de 3 lotes que corresponden a la formulación que se propone. Estas se almacenaron a temperatura ambiente y fueron evaluadas periódicamente en cuanto a tanto por ciento de principio activo, pH y características organolépticas durante 1 año.6
]]> Estudio toxicológico
El estudio de la dosis letal media (DL50) se realizó mediante el método estadístico de los Probits7 y los datos fueron procesados electrónicamente.
Escalado piloto
Se realizó un escalado piloto de 10 L para evaluar aspectos del procedimiento tecnológico y el comportamiento del producto antes de su introducción industrial.
RESULTADOS
]]> Desarrollo tecnológico
En todos los casos el producto terminado cumplió con las especificaciones microbiológicas requeridas para este tipo de preparación y no mostró presencia de pirógenos. El método de esterilización seleccionado fue el de calor húmedo con filtración previa. La formulación seleccionada en el estudio de preformulación cumplió con los parámetros físicos, químicos y microbiológicos requeridos, como: características organolépticas, pH, esterilidad, contenido de principio activo, efectividad de los preservativos antimicrobianos y la ausencia de pirógenos.
Estudio de estabilidad
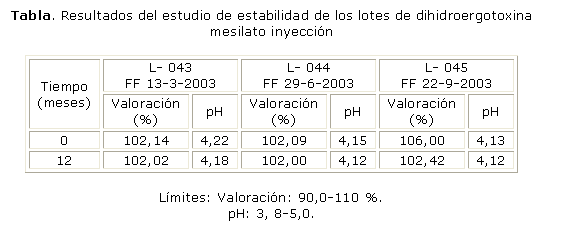
Los resultados obtenidos en el estudio de estabilidad (tabla) indican que todos los parámetros evaluados se encontraron dentro de los límites establecidos y no se observaron cambios en el aspecto organoléptico de las muestras.

Estudio toxicológico ]]>
Escalado piloto
En el escalado piloto no se presentaron dificultades con el procedimiento tecnológico y el producto obtenido cumplió satisfactoriamente con los parámetros de calidad establecidos para este tipo de formulación.
DISCUSIÓN
El método de esterilización seleccionado fue el de calor húmedo con filtración previa ya que constituyó un método más seguro para lograr la esterilidad del producto terminado y el principio activo no sufrió alteraciones.
Del estudio de estabilidad se concluye que la formulación de dihidroergotoxina mesilato inyección ampolletas unidosis es satisfactoria desde el punto de vista de su estabilidad, y se propone una fecha de vencimiento de 1 año almacenada a temperatura ambiente. ]]>
El resultado del escalado piloto indica que la fórmula y técnica desarrolladas pueden ser introducidas industrialmente. No se observó muerte de ningún animal. Los síntomas observados a la dosis administrada fue la sedación que se presentó 5 min después de la administración y se mantuvo hasta 4 h después de esta para los 3 lotes ensayados.8No se observó decremento en el peso corporal en ninguno de los grupos experimentales durante el estudio (fig.). En la autopsia realizada no se observaron alteraciones macroscópicas de órganos y tejidos.

Los 3 lotes de dihidroergotoxina mesilato no presentan toxicidad significativa tras su administración endovenosa según el ensayo de tolerancia realizado en ratones.
En conclusión, se logró una formulación inyectable de dihidroergotoxina mesilato envasada en ampolletas unidosis que cumple satisfactoriamente con los parámetros de calidad establecidos y que fue fácilmente escalable a nivel piloto. Se estableció una fecha de vencimiento del producto terminado de 1 año, mantenido a 25 ± 1 °C. El estudio toxicológico reveló que no existen diferencias significativas entre el producto nacional y el de importación.
REFERENCIAS BIBLIOGRÁFICAS
1. Iruin A. Alfaro J. Napal V. Vasodilatadores cerebrales y periféricos. Servicio de Farmacia-Hospital de Navarra. Boletín de Información Farmacoterapéutica de Navarra. 2000;4(6).
2. American Hospital Formulary Service. Drug Information. 96 ed. New York: American Society of Hospital Pharmacists; 2004. p. 870.
3. Selman-Housein E. La producción industrial de inyectables. Un enfoque según las exigencias actuales. La Habana: Ministerio de Salud Pública, Instituto Cubano del Libro; 1999. p. 20-8.
4. The United Stated Pharmacopeia (USP 27). The National Formulary (NF 19). United States Pharmacopeial Convention. Rockville: Mack Printing; 2004. p. 749-51.
5. Regulación 16-2006 Directrices sobre Buenas Prácticas de Fabricación de Productos Farmacéuticos. Anexo No. 4 (Buenas Prácticas para la fabricación de productos estériles), CECMED, La Habana, Cuba.
6. Martínez L, Técnica analítica No2004-25. CIDEM, La Habana, Cuba.
7. Diccionario de Especialidades Farmacéuticas. 26 ed. Madrid: Editorial PLM, SA; 1998. p. 327, 360, 1060.
8. Wallace Hayes A. Principles and Methods of Toxicology. 2nd ed. New York: Raven Press; 1989. p. 320-1.
Recibido: 9 de enero de 2008. ]]> Aprobado: 11 de febrero de 2008.
Lic. Anna Karelia Collado Coello. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Calle 19 de Mayo No. 21 esq. a Amézaga, municipio Plaza de la Revolución, La Habana, Cuba. Correo electrónico: cinfa@infomed.sld.cu
Centro de Investigación y Desarrollo de Medicamentos ]]>