ARTÍCULOS ORIGINALES
Características tecnológicas de mezclas de senósidos A+B con excipientes para la formulación de tabletas
Technological characteristics of mixtures of sennosides A + B with excipients for tablet formulations
Eva Arce FernándezI; Leopoldo Villafuerte RoblesII
]]>
ILicenciada en Química Farmacéutica Industrial. Departamento de Farmacia de la Escuela Nacional de Ciencias Biológicas, Instituto Politécnico Nacional de México. México, DF.
RESUMEN
Se realizó un estudio de las propiedades tecnológicas del polvo de senósidos A+B concentrados con el fin de valorar la factibilidad de su procesamiento en la forma farmacéutica de tabletas. Las características estudiadas incluyen la compactabilidad, la presión de expulsión, el tiempo de desagregación y la velocidad de flujo del polvo. Los resultados obtenidos muestran que una mezcla de celulosa microcristalina tipo 102 con sílica coloidal sería un excipiente adecuado para aumentar hasta el doble la velocidad del flujo del polvo, hasta 4 veces la resistencia a la ruptura de las tabletas y disminuir a la mitad el tiempo necesario para la desagregación de estas. Las modificaciones en la formulación antes mencionadas no afectan de manera importante las propiedades de deslizamiento de las tabletas, al ser expulsadas desde la matriz en que se fabricaron.
Palabras clave: Senósidos A+B, tecnología farmacéutica, flujo del polvo, compactabilidad, tiempo de desintegración.
ABSTRACT
]]>
The technological properties of concentrates of sennosides A+B were studied with the purpose to evaluate the feasibility of its processing to the pharmaceutical form of tablets. The studied properties include the compactibility, the ejection pressure, the disintegration time and the rate of the powder flow. The obtained results show that a mixture of microcrystalline cellulose with colloidal silica is a suitable excipient to increase to the double the powder flow rate and 4 times the tablet strength and to reduce in 40 % the time necessary to disintegrate the tablets. The above mentioned formulation modifications do not affect in an important manner the gliding properties of the tablets being ejected from the die where they were compressed.
Key words: Sennosides A+B, pharmaceutical technology, powder flow, compactibility, disintegration time.
INTRODUCCIÓN
El sen es un arbusto de la familia de las leguminosas originario de Arabia, Somalia y otros países ribereños del mar rojo que es utilizado como un laxante eficaz y seguro. Las hojas y semillas del sen contienen 2-3 % de glucósidos antraquinónicos conocidos como senósidos A+B, además de flavonoides y mucílagos que colaboran en su acción laxante y una resina irritante. Los senósidos A+B son inactivos en su estado natural, sin embargo, al llegar al colon son transformados por glicosidasas de origen bacteriano para liberar la genina, el principio activo de la molécula del senósido.1
Una de las formas farmacéuticas en que se suministra este principio activo son las tabletas. Debido a su origen vegetal y a las cantidades dosificadas (187-374 mg/tab.), las características físicas y tecnológicas del extracto de sen son determinantes para lograr las características físicas y tecnológicas adecuadas de las tabletas.2 Los extractos vegetales en forma de polvo constituyen materiales con un elevado contenido en ácidos grasos, circunstancia que hace difícil su deslizamiento a través de las tolvas de los equipos de fabricación, además de tener una pobre cohesividad para formar tabletas.
En el proceso de compresión para la formación de una tableta se consideran 3 factores: el polvo o mezcla de polvos, las herramientas de compresión y la interacción polvo-herramientas de compresión. Las características del polvo están determinadas principalmente por las propiedades del estado sólido entre las que se encuentran: a) las propiedades inherentes a la materia, como su composición química y sus características físicas; b) las propiedades que son modificables en ella, como las características cristalográficas y las mecánicas y c) las propiedades del medio ambiente en que se encuentra el polvo como la humedad relativa y las cargas electrostáticas.3
Las propiedades de los comprimidos se miden regularmente mediante propiedades que permanecen en las tabletas como su dureza o resistencia a la ruptura, la fuerza de expulsión y la cantidad disuelta del fármaco o el tiempo de desintegración de las tabletas. Sin embargo, existen otras propiedades que se miden con la finalidad de especificar las propiedades físicas de los materiales; con ellas se establecen controles que permitan asegurar la calidad y evitar desviaciones en los procesos de manufactura. Entre estas propiedades se encuentra la velocidad de flujo del polvo.4,5 ]]>
La celulosa microcristalina se ha utilizado ampliamente como un excipiente de compresión directa debido a la fluidez de este polvo, la cual es consistente y reproducible. La celulosa microcristalina tiene una buena compactabilidad y compresibilidad, acelera la desintegración y la dispersión, es un buen aglutinante para tabletas, es muy estable y tiene una buena capacidad para absorber agua.6,7 Se considera que los puentes de hidrógeno formados entre los hidrógenos de moléculas de celulosa adyacentes serían los responsables de la fuerza y cohesividad de sus compactos, además de su capacidad para deformarse plásticamente.8La sílica coloidal (Aerosil 200) se utiliza en tabletas como agente granulante y deslizante. Absorbe una gran cantidad de agua sin licuarse, por lo que se utiliza para prevenir la obstrucción del flujo de polvos higroscópicos.9 Se ha observado que el efecto promotor de la fluidez de los polvos varía en función de la estructura geométrica de los agentes deslizantes. El tamaño de partícula en diferentes marcas comerciales de sílica coloidal no porosa se encuentra en el orden Aerosil 200 < Aerosil 50 < SO-CL< SO-C5 y el tamaño de partícula de SO-C5 es casi el mismo que Adsolider 101, la cual tiene una estructura porosa.10
El objetivo de este trabajo fue estudiar las propiedades tecnológicas necesarias para formar tabletas con los senósidos A+B concentrados, en presencia de excipientes como la celulosa microcristalina (Helmcel 200), sílica coloidal (Aerosil 200) y otros excipientes.
MÉTODOS
Se evaluó un lote comercial de un concentrado de senósidos A+B en forma de polvo fino que se encuentra en el mercado mexicano, distribuido por la empresa Mundipharma e identificado con el número de lote 52959. Después de evaluar sus características tecnológicas, se realizaron diferentes formulaciones con el empleo de excipientes como la celulosa microcristalina tipo 102, lote 20535, de la empresa Helm de México; almidón de maíz, lote 123134-A de la empresa Droguería cosmopolita; sílica coloidal de la marca Aerosil, lote 1200630H, de la empresa Degussa Inc., y el glicolato de sodio y almidón conocido como Explotab, lote E2036, de la empresa JRS Pharma. El método de experimentación fue el de un factor a la vez, con la utilización de diferentes concentraciones de la celulosa microcristalina como variable independiente, y se observó su efecto sobre los senósidos puros, mezclas de los senósidos con almidón de maíz, con sílica coloidal y con Explotab.
La celulosa es un excipiente que se utiliza como aglutinante y diluente, aunque también tiene propiedades de lubricante y desintegrante, en concentraciones que van del 5 al 90 %.11,12 Dada la dosis elevada del extracto vegetal en cada tableta, se utilizaron solo concentraciones de celulosa de hasta 40 %. Los demás excipientes se utilizaron en concentraciones usuales en las formulaciones farmacéuticas. El almidón que es un desintegrante y diluente se empleó en un intervalo de hasta 30 %, la sílica coloidal al 4 % y el Explotab también al 4 %.11
No se realizó ningún tratamiento estadístico especial de los datos, fuera de lo establecido en los métodos particulares. Los resultados se registran como el promedio de las repeticiones realizadas en cada prueba, con la desviación estándar de algunos de los puntos experimentales como referencia. Para determinar la influencia de la celulosa y excipientes utilizados se determinaron las características tecnológicas de las diferentes formulaciones.
Velocidad de flujo del polvo ]]>
Compactabilidad
Se comprimieron 300 mg del polvo correspondiente durante 5 s a 6 presiones diferentes de compactación (Pc) hasta 476 MPa en una prensa hidráulica. Los punzones utilizados fueron planos y de un diámetro de 12,7 mm. Las tabletas (6) se colocaron diametralmente entre 2 superficies planas en una prensa hidráulica con un manómetro adaptado con una aguja de arrastre y se aplicó una presión creciente hasta la ruptura de la tableta. Se toma como dureza de las tabletas (D) la presión máxima ejercida. Los datos fueron tratados con la ecuación de compactabilidad siguiente:
[1] ln (-ln (1 - D/Dmáx.)) = n* ln Pc + constante
La compactabilidad de cada material se definió a través de la dureza máxima (Dmáx) obtenida, la pendiente (n) y el intercepto o constante de la curva de regresión.14
Presión de expulsión ]]>
Tiempo de desintegración
Se usó el método descrito en la FEUM 6ª edición,16 para lo cual se emplearon solo 4 tabletas para cada mezcla y se tomó como resultado el promedio de los 4 tiempos de desintegración. Con los resultados se realizó una curva de tiempo de desintegración contra presión de compactación.
RESULTADOS
El lote de materia prima 52959, del concentrado de senósidos A+B del proveedor Mundipharma, se caracterizó por ser un polvo muy fino. Entre sus partículas predominaron fuertes efectos de fricción y cohesión, lo que ocasionó que la velocidad de flujo del polvo fuera muy pobre (0,332 g/s). La dureza de las tabletas fue baja, y se obtuvo un valor máximo de 0,78 MPa a una presión de compactación de 416 MPa. El tiempo de desintegración de sus tabletas fue de más de 60 min. Por otro lado, la presión de expulsión fue baja ya que los materiales grasos funcionan como lubricantes.
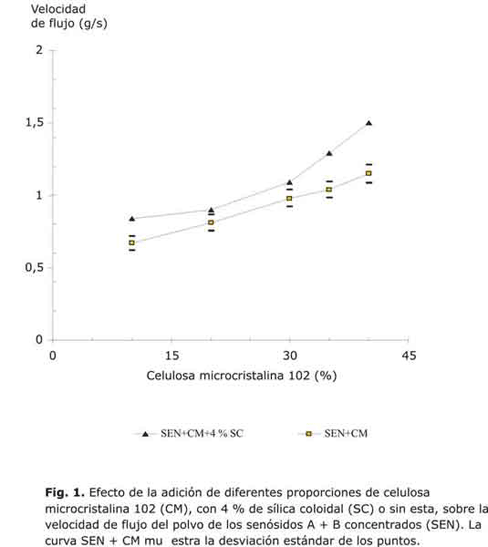
Las mezclas binarias de senósidos con celulosa microcristalina (Helm 200, lote 20535 de Helm de México) se prepararon con la adición de 10, 20, 30 y 40 % de celulosa; se observó que la celulosa aumenta considerablemente la velocidad de flujo del polvo. En el caso de las mezclas ternarias, a las mezclas anteriores se les adicionó 4 % de sílica coloidal (Aerosil 200, lote 1200630H de Degussa Inc.). El efecto observado de un aumento en la velocidad de flujo del polvo de los senósidos, por la adición de celulosa sola, se potenció con la adición de la sílica coloidal. Las mezclas ternarias presentaron mejores velocidades de flujo. La velocidad de flujo aumentó progresivamente conforme se aumentó la concentración de celulosa en la mezcla, hasta alcanzar valores por encima de los observados para la adición únicamente de la celulosa (fig. 1).

Con las mezclas binarias se fabricaron tabletas, y se observó que las propiedades de compactación de los senósidos no se vieron modificadas de manera importante. Se observó un efecto irregular. La adición de 10 % de celulosa disminuyó la dureza de las tabletas, mientras que la adición de mayores cantidades de celulosa solo permitió alcanzar una dureza máxima (0,88 MPa) algo por encima de la obtenida con los senósidos puros (0,78 MPa). ]]>
Al igual que las mezclas binarias, cada una de las mezclas ternarias fue compactada a diferentes presiones en un intervalo de 138 MPa a 416 MPa. Como muestra la figura 2, se observó un aumento gradual de la dureza de las tabletas al aumentar la presión de compactación, hasta llegar a un límite, tal como se predice con la ecuación [1]. La adición de la sílica coloidal produjo un aumento considerable de la dureza de las tabletas. Esto se puede observar en la figura 3, al tomar como referencia la dureza de las tabletas compactadas a 416 MPa.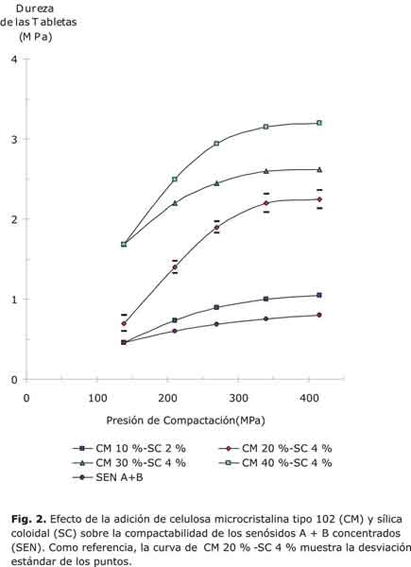

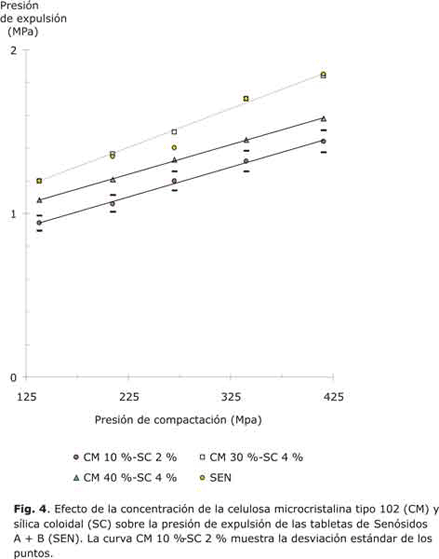
El efecto de la celulosa tipo 102 sobre la presión de expulsión de las tabletas es irregular. A una presión de compactación de 416 MPa se obtuvieron resultados que varían desde 1,5 MPa hasta 1,87, mientras que los senósidos puros presentaron una presión de expulsión de 1,85 MPa. Un efecto similar fue observado para las mezclas ternarias (fig. 4). Como era esperado, al aumentar la presión de compactación la presión residual que ejerció la tableta contra las paredes de la matriz fue mayor y por lo tanto, la presión de expulsión también fue mayor.
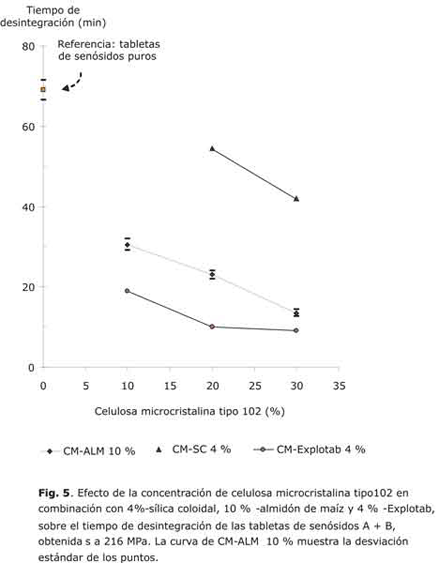
La adición de celulosa microcristalina con sílica coloidal permitió una reducción de los tiempos de desintegración a valores entre 30 y 50 min, cuando originalmente fueron mayores a 60 min. En el caso del tiempo de desintegración el efecto de la presión de compactación fue mínimo. El tiempo de desintegración se mantuvo prácticamente constante a todas las presiones de compactación utilizadas. La adición de desintegrantes más específicos como el almidón de maíz y los superdesintegrantes como el glicolato de sodio y almidón (Explotab) produjeron tiempos de desintegración menores a 30 min (fig. 5).
]]>
Otras pruebas realizadas incluyen mezclas binarias de los senósidos con 10, 20 y 30 % de almidón de maíz que deterioraron ligeramente el flujo del polvo y la compactabilidad de los senósidos; sin embargo, el tiempo de desintegración bajó casi hasta la mitad. En mezclas ternarias de senósidos-celulosa-almidón de maíz (10 %) los resultados del tiempo de desintegración (fig. 5) son prácticamente los mismos que los de las tabletas de mezclas binarias de senósidos con celulosa. El efecto del almidón sobre la velocidad de flujo de los senósidos es un aumento de esta; sin embargo, los valores observados de velocidad fueron siempre menores a los de las mezclas de los senósidos con celulosa y con celulosa y sílica. La compactabilidad de las mezclas ternarias de senósidos-almidón-celulosa, en comparación con los senósidos solos, no mostró resultados estadísticamente diferentes; sin embargo, mostraron una ligera disminución de la presión de expulsión de las tabletas.En las mezclas ternarias de senósidos-celulosa-Explotab se observó la desaparición del efecto promotor del flujo de la celulosa, que se ha observado en la figura 1; se mantuvo la velocidad de flujo prácticamente en el mismo valor de los senósidos solos. Sin embargo, la compactabilidad de la mezcla ternaria fue 5 veces mayor que la de la mezcla binaria senósidos-celulosa.
DISCUSIÓN
Los extractos secos de plantas se considera que sean generalmente de polvo muy fino, poco compresibles, higroscópicos y con tiempos de desintegración de sus tabletas muy prolongados.17 El caso de los senósidos aquí presentados no es la excepción. El carácter hidrofóbico típico del extracto de senósidos sería la causa de un tiempo elevado de desintegración de sus tabletas así como de una presión de expulsión baja. Los materiales grasos funcionarían como lubricantes y como agentes que aumentan la tensión interfacial con el agua, lo que aumentaría los tiempos de desintegración. Los materiales grasos tienen tensiones de corte bajas, lo que sería la causa de la baja resistencia a la tensión o dureza de las tabletas.
La velocidad del flujo de los polvos farmacéuticos determina propiedades importantes en las formas de dosificación. Se ha observado que los extractos vegetales comúnmente tienen partículas de tamaño pequeño que dificultan el flujo, lo cual redunda en variaciones en el peso y una pobre uniformidad de contenido en las tabletas.18 Con el propósito de mejorar el flujo de un polvo o mezcla de polvos se añaden a la formulación los agentes promotores del flujo. En nuestro caso, estos ejercerían su efecto inhibiendo o rompiendo los enlaces interparticulares y desagregando los aglomerados originales de los senósidos. La intercalación de partículas de celulosa facilitaría el flujo del polvo. El efecto de potenciación de la velocidad de flujo en las mezclas ternarias de senósidos-celulosa-sílica se puede atribuir al efecto de rodamiento que tendrían las partículas pequeñas de la sílica coloidal adsorbidas sobre partículas de mayor tamaño de celulosa y de los senósidos. En una mezcla de partículas, las que son de menor tamaño, como aquellas de los agentes deslizantes, tenderían a ocupar los lugares vacíos dejados por las partículas grandes, lo que aumentaría su empacamiento y con esto dificultaría su flujo. Sin embargo, cuando la cantidad de estas partículas finas es pequeña, podrían funcionar como rodamientos para las partículas grandes, lo que facilitaría su deslizamiento y fluidez. Los resultados obtenidos confirman los antes observados por otros autores acerca de la mejoría del flujo de polvos en presencia de la silica coloidal. Estudios anteriores sugieren que el Aerosil es un constituyente indispensable para mejorar el flujo de los polvos en las formulaciones de tabletas.19
La compactabilidad, entendida como la capacidad de un material para formar un cuerpo coherente con cierta resistencia mecánica, cuando se le aplica una presión, es el resultado de procesos de consolidación o re-arreglo de las partículas, de su deformación plástica o de su fractura. Si un material que se compacta es incapaz de deformarse plásticamente, a una velocidad suficiente para acomodar la carga aplicada, tiende a fracturarse. La fuerza de compactación es uno de los parámetros más importantes pues incrementa el área de contacto entre las partículas y por lo tanto, aumenta la fuerza del enlace entre ellas.
El poco efecto de la celulosa sobre la compactabilidad de las mezclas binarias sería debido a que las partículas de celulosa estarían totalmente rodeadas o englobadas por las de los senósidos, lo cual mantiene prácticamente la misma compactabilidad que los senósidos originales. Sin embargo, en las mezclas ternarias con la sílica coloidal es claro el aumento en la compactabilidad. Esto se puede atribuir a la localización de la sílica coloidal sobre la superficie de las partículas de celulosa y de los senósidos, lo que facilitaría su deslizamiento para consolidarse y aumentaría la atracción interpartícular. El efecto de la sílica coloidal de aumentar la dureza de las tabletas se ha observado antes en extractos de hojas de Pasiflora edulis, donde se ha utilizado una concentración de 2,0 % de Aerosil 200.20
Además de las propiedades de compactabilidad de las tabletas, existe otro tipo de propiedades de los materiales que no se desean o diseñan para mantenerse en el producto terminado. De esta manera, se habla de las propiedades de fricción de los materiales, las cuales, si son adecuadas, no serán notadas durante la obtención de las tabletas; pero si no lo son, causarán problemas como la laminación y defectos de rayado sobre los cantos de estas, así como la imposibilidad física de liberar las tabletas desde la matriz en la que se comprimen.
El efecto de la proporción de celulosa microcristalina en las mezclas binarias y de la adición de sílica coloidal en las mezclas ternarias parece no alterar de manera significativa la presión de expulsión. Este parámetro estaría determinado básicamente por el efecto lubricante de la elevada proporción de los materiales grasos que acompañan a los senósidos. ]]>
La exigencia para la disolución de los senósidos no es muy grande, la USP de 2004 exige un mínimo de disolución de 75 % a los 120, en agua. Aunque no fue parte de este estudio se considera que los tiempos de desintegración obtenidos podrían ser suficientes para obtener los límites de disolución establecidos. Desde el punto de vista de la facilidad para procesar los materiales, la fórmula de los senósidos con 40 % de celulosa microcristalina y 4 % de sílica coloidal presenta los mejores resultados. Sin embargo, si fuese necesario bajar más los tiempos de desintegración sería conveniente incluir en la formulación desintegrantes más específicos como el almidón de maíz y los superdesintegrantes como el glicolato de sodio y almidón conocido como Explotab. El Explotab tendría, además de las características desintegrantes, propiedades mecánicas que permiten mejorar la dureza de las tabletas. Esta circunstancia es una ventaja en la formulación de polvos poco compactables como los senósidos.21 Sin embargo, habría que considerar una eventual reducción en la velocidad de flujo del polvo al adicionar el Explotab.
REFERENCIAS BIBLIOGRÁFICAS
1. Grünbald J, Brendler T, Janicke C. PDR for herbal medicines. 2nd ed. Stamford: Ed. Medical Economics Company; 2000. p. 615-6.
2. Senokot y Senokot F. Tabletas de senósidos A + B. México, DF; Novartis Farmacéutica, SA [Citado 26 Jul 2007]. Disponible en: http://plm.wyeth.com.mx .
3. Jeannin C, Mangeot A, Verain A. Ingeniería farmacéutica. México, DF: Ed. El Manual Moderno; 1982. p. 20-1.
4. Shangraw RF, Pande GS, Gala P. Characterization of the tablet properties of betacyclodextrins and the effect of processing variables on inclusion complex formation , compactibility and dissolution. Drug Dev Ind Pharm. 1992;18:1831-51.
5. Schmiedt PD, Rubendörfer CJW. Evaluation of Ludipress as a multipurpose excipient for direct compression. Part I: powder characteristics and tableting properties. Drug Dev Ind Pharm. 1994;20:2899-925.
6. Shlieout G, Arnold K, Müller G. Powder and Mechanical Properties of Microcrystalline Cellulose with Different Degrees of Polymerization. AAPS PharmSciTech. 2002;3(2):article 11. Available from: http://www.aapspharmscitech.org
7. FMC Biopolymer. FMC Microcrystalline cellulose. [Cited 2007 Jul 27]. Available from: http://www.fmcbiopolymer.com/PopularProducts/FMCMicrocrystallineCellulose/Applications/tabid/813/Default.aspx ]]>
8. Shangraw RF. Direct compression tableting. In: Swarbirck J, Boylan JC. editores. Encyclopedia of pharmaceutical technology. Vol. 4, New York: Marcel Dekker; 2002. p. 97-8.
9. Martindale. The Extra Pharmacopoeia. Coloidal silicon dioxide. 26 ed. London: Pharmaceutical Press; 1975. p. 1087-8.
10. Ohta KM, Fuji M, Chikazawa M. Effect of Geometric Structure of Flow Promoting Agents on the Flow Properties of Pharmaceutical Powder Mixture. Pharmaceutical Res. 2003;20(5):804-9.
11. Handbook of pharmaceutical excipients. Bulk and tap density or volume. Washington, DC: American Pharmaceutical Association; 1986. p. 362-3.
12. Reus Medina ML, Kumar V. Evaluation of cellulose II powders as a potential multifunctional excipient in tablet formulation. Int J Pharm. 2006;322:31-5.
13. Martínez López MT, Ibarra Trejo A, Villafuerte Robles L. Propiedades reológicas de los polvos farmacéuticos: un nuevo equipo. Rev Mex Cienc Farmceut. 2001;32(1):11-5.
14. Castillo S, Villafuerte L. Compactibility of binary mixtures of pharmaceutical powders. Eur J Pharm Biopharm. 1995;41(5):309-14.
15. Villafuerte Robles L. Propiedades de fricción de tabletas de mezclas de celulosa microcristalina tipo 102 y fosfato de calcio dihidratado. Rev Mex Cienc Farmaceut. 1995;26(2):14-9.
16. Farmacopea de los Estados Unidos Mexicanos. 6a ed. México, DF: Desintegración. Secretaria de Salud; 1994. p. 113-7.
17. Lira Soares LS, González Ortega G, Petrovick PR, Schmidt PC. Optimization of tablets containing a high dose of spray-dried plant extract: a technical note. AAPS PharmSciTech. 2005;6(3):article 46. Available from: http://www.aapspharmscitech.org
18. Pereira de Souza T, Martínez-Pacheco R, Gómez-Amoza JL, Petrovick PR. Eudragit E as excipient for production of granules and tablets from Phyllanthus niruri L spray-dried extract. AAPS PharmSciTech. 2007;8(2):article 34. Available from: http://www.aapspharmscitech.org
19. Martinello T, Kaneko TM, Robles Velasco MV, Santos Takeda ME. Consiglieri VO. Optimization of poor compactable drug tablets manufactured by direct compression using the mixture experimental design. Int J Pharm. 2006;322:87-95.
20. Linden R, Ortega GG, Petrovik PR. Basan VL. Response surface analysis applied to the preparation of tablets containing a high concentration of vegetable spray-dryed extract. Drug Dev Ind Pharm. 2000;6(4):441-6.
21. Edge S, Steele DF, Staniforth JN, Chen A, Woodcock PM. Powder compaction properties of sodium starch glycolate disintegrants. Drug Dev Ind Pharm. 2002;28(8):989-99.
Recibido: 25 de abril de 2008.
Aprobado: 2 de junio de 2008. ]]>
Lic. Eva Arce Fernández. Instituto Politécnico Nacional de México. Carpio y Plan de Ayala s/n, Col. Santo Tomás, Código Postal 11 340, Distrito Federal, México. Correo electrónico: lvillaro@encb.ipn.mx ]]>