ARTÍCULOS ORIGINALES
Caracterización de eventos adversos asociados a vacunas que inmunizan contra enfermedades infecciosas. Años 2006-2007
Characterization of adverse events associated with vaccines immunizing against infectious diseases. 2006-2007
Ivette Díaz MatoI; Ashley Lázaro Chao CardesoII; Giset Jiménez LópezIII; Yanet López ValdésIV
]]>
IEspecialista de I Grado en Farmacología. Máster en Enfermedades Infecciosas. Asistente. Facultad de Medicina "Dr. Salvador Allende". La Habana, Cuba.
IIEspecialista de I Grado en Farmacología. Instructor. Unidad Coordinadora Nacional de Farmacovigilancia. Centro para el Desarrollo de la Farmacoepidemiología (CDF). La Habana, Cuba.
IIIEspecialista de II Grado en Farmacología. Máster en Economía de la Salud. Profesora Auxiliar. Unidad Coordinadora Nacional de Farmacovigilancia. CDF. La Habana, Cuba.
IVEspecialista de I Grado en Farmacología. Instructora. Hospital Pediátrico San Miguel del Padrón. La Habana, Cuba.
RESUMEN
Se realizó un estudio descriptivo, transversal y retrospectivo para caracterizar los eventos adversos temporalmente asociados con las vacunas que se emplean en la prevención y el control de las enfermedades infecciosas, y que fueron notificados a la Unidad Coordinadora Nacional de Farmacovigilancia entre los años 2006-2007. Se determinó su comportamiento de acuerdo con la edad, sexo, procedencia de la notificación, personal que reporta, localización y severidad. Se identificaron además los principales eventos reportados y las vacunas implicadas en su aparición. La fiebre constituyó el 60 % del total de eventos notificados. Estos últimos se distribuyeron de igual forma entre uno y otro sexos, en tanto los lactantes resultaron ser los más afectados (46,8 %). Se destacó en el reporte la Atención Primaria de Salud con 812 notificaciones. Los médicos fueron los profesionales que más reportaron (36 %). El comportamiento en cuanto a severidad no se diferenció de lo reportado en la literatura, pues afortunadamente predominaron los eventos leves (66,4 %). Sin embargo, contrario a lo que se esperaba, los eventos sistémicos fueron los de mayor cuantía (80,2 %). La vacuna pentavalente estuvo implicada en el 29,6 % de los eventos adversos temporalmente asociados a vacunación.
Palabras clave: Evento adverso, vacunas, enfermedades infecciosas, farmacovigilancia.
A descriptive, transversal and retrospective study was conducted to characterize the adverse events temporarily associated with vaccines used in prevention and control of infectious diseases and that were notified to National Coordinator Unit of Pharmacosurveillance between the 2006-2007 years. Its behavior was determined according to the age, sex, notification origin, reporting staff, location and severity. Also, it was possible to identify the leading events reported and the vaccines involved in its appearance. Fever accounted for the 60 % of total of reported events. These latter were distributed equally between both sexes where the infants were the most affected (46.8 %).Report from Health Primary Care report was the more significant with 812 notifications. The most reports came from physicians (36 %). The behavior as regards severity was not different from that reported in literature, since fortunately there was predominance of slight events (66.4 %). However, contrary to expected, the systemic events had the greatest amount (80.2 %). pentavalent vaccine was related to 29.6 % of adverse events temporarily associated with vaccination.
Key words: Adverse event, vaccines, infectious diseases, Pharmacosurveillance.
INTRODUCCIÓN
Hace un cuarto de siglo, expertos en enfermedades infecciosas aseguraron que la lucha contra las infecciones había sido ganada. Sin embargo, la aparición de nuevas enfermedades, muchas de las cuales permanecen 20 años después sin tratamiento específico para combatirlas, la reaparición y alza de un grupo de enfermedades infecciosas ya casi en extinción, y el hecho de que una de cada 2 muertes sea provocada por alguna enfermedad infecciosa en países subdesarrollados, contradicen tal afirmación.1 Razones que además han motivado entre otras cosas, la aplicación y el perfeccionamiento de los distintos programas de vacunación. Hoy por hoy la inmunización es, sin lugar a duda, la intervención más efectiva y de mejor balance costo-beneficio con que se cuenta para enfrentar el embate de numerosas enfermedades infecciosas.2 Ahora bien, ningún producto con actividad farmacológica, incluyendo a las vacunas, es 100 % seguro.
En este sentido, la Organización Mundial de la Salud ha definido como evento adverso temporalmente asociado a la vacunación (ETAV), a cualquier accidente médico que ocurre después de administrar una vacuna y que puede o no estar relacionado con la aplicación de esta, además de otros eventos inusuales que ocurran antes de que hayan transcurrido más de cuatro semanas de la vacunación, incluyendo los eventos mortales cuyo agente causal no esté bien precisado.3
En nuestro país, la vigilancia de eventos adversos supuestamente atribuibles a la vacunación es efectuada por la Dirección de Higiene y Epidemiología del Ministerio de Salud Pública. Nuestra Unidad Coordinadora Nacional de Farmacovigilancia (UCNFv) se integra activamente a esta actividad y, envía informes ejecutivos a diferentes entidades: centros productores, reguladores, industria químico farmacéutica, entre otros.
Teniendo en cuenta la carencia de información al respecto, y considerando que es un tema de mucha importancia, se realizó este estudio, para caracterizar los eventos adversos temporalmente asociados a las vacunas que se emplean en Cuba, para la prevención y el control de las enfermedades infecciosas, y que fueron notificados a la UCNFv durante los años 2006-2007. Específicamente se determinó su comportamiento de acuerdo con la edad, el sexo, la procedencia de la notificación, el personal que reporta, localización y severidad. Se identificaron además las principales vacunas implicadas en su aparición. ]]>
MÉTODOS
Se diseñó un estudio descriptivo, transversal y retrospectivo, para caracterizar los eventos adversos temporalmente asociados con las vacunas que se emplean en la prevención y control de enfermedades infecciosas y que fueron notificados a la UCNFv entre los años 2006-2007, para determinar su comportamiento de acuerdo a la edad, sexo, procedencia de la notificación, personal que reporta, localización y severidad. Además de identificar los principales eventos reportados y las vacunas implicadas en su aparición.
La información necesaria para cumplimentar los objetivos propuestos, se obtuvo de la Base de Datos Nacional de Farmacovigilancia relacionada con vacunas.
Se determinó su frecuencia de aparición en términos porcentuales según sexo, edad, tipo de vacuna, procedencia de la notificación, personal que reporta, localización y severidad.
Se aplicaron técnicas de estadística descriptiva para cada variable. Los principales resultados se presentaron en tablas de distribución de frecuencias y de clasificación cruzada, para facilitar una mejor comprensión de los mismos.
RESULTADOS
Desde enero de 2006 hasta diciembre del 2007, se recibieron en la UCNFv, 28 338 reportes de reacciones adversas medicamentosas. De ellas, hubo 852 reacciones relacionadas con las vacunas que inmunizan contra las enfermedades infecciosas, lo que en términos de vacunas se refiere a 852 ETAV.
Según puede apreciarse en la tabla 1, el ETAV notificado más frecuentemente fue la fiebre (60,0 %). La inflamación y el dolor en el sitio de inyección, también estuvieron dentro de los más reportados. ]]>
En la tabla 2 se muestra la distribución de los ETAV por sexo y grupos de edades. Obsérvese un predominio de ETAV en el sexo masculino y en los lactantes, respectivamente.La tabla 3 presenta la distribución de los ETAV por tipo de vacuna. Sin duda, la pentavalente se asoció a un mayor número de eventos indeseables (252). Nada despreciable fue el número de ETAV relacionados con las vacunas antidiftérica-antitetánica y tetravalente.
Como se aprecia en la tabla 4, el 95,3 % de los ETAV fueron notificados por la Atención Primaria de Salud (APS). Véase además que los médicos, fueron los profesionales que más reportaron (36,0 %)
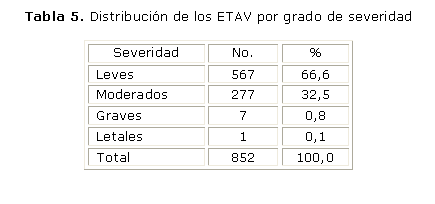
La tabla 5 expone la distribución de los ETAV por grado de severidad. En este caso la supremacía fue para los eventos leves, con 567 de los 852 que conformaron el total.
Tal y como se representa en la tabla 6, predominaron los ETAV sistémicos (683). La fiebre, la erupción cutánea, la irritabilidad y los vómitos fueron los máximos responsables.
DISCUSION
En Cuba desde 1959, se aplica un programa de inmunización orgánicamente planificado, gratuito y accesible a toda la población. Con su cumplimiento, se ha logrado la eliminación de 5 enfermedades infecciosas: poliomielitis, difteria, sarampión, tos ferina y rubéola.4 Para que se tenga una idea de la magnitud de este gran logro de la medicina cubana, baste mencionar que en la actualidad, la tasa de letalidad en los casos de poliomielitis con compromiso bulbar o respiratorio es cercana al 40 %.5 Si este ejemplo fuese insuficiente, valdría la pena entonces resaltar, que el sarampión cobra anualmente 875 000 vidas en todo el mundo, el cual es responsable de casi la mitad de los 1,7 millones de muertes anuales por enfermedades que pueden prevenirse por vacunación.5 Pero no solo se ha logrado eliminar estas cinco enfermedades, sino que también se han eliminado 2 formas clínicas severas y 2 complicaciones graves. Dentro de las primeras se incluyen la meningitis tuberculosa en menores de 1 año y el tétanos neonatal.4 Este último, responsable de 500 000 defunciones anuales en todo el mundo.5 En cuanto a las complicaciones, se eliminó el síndrome de la rubéola congénita y la meningoencefalitis posparotiditis.4 ]]>
Si aun quedaran dudas acerca del impacto del Programa de Inmunización en nuestro país, se puede decir, que por primera vez en 102 años de registro de tétanos, no se notificaron casos en los años 2004 y 2005.6 Se mantiene además la reducción de la incidencia de meningoencefalitis por Haemophilus influenzae tipo B. La vacuna cubana contra este microorganismo se introduce en el esquema oficial de vacunación en el año 1999, justificando de esta forma que en el 2005 se notificaran, 33 casos menos que en el año 2000.6 Otra de las enfermedades que ha dejado afortunadamente de constituir un problema de salud en Cuba, por mostrar tasas de incidencia inferiores a 0,1 x 100 000 habitantes, es la fiebre tifoidea.6 La enfermedad meningocócica, la hepatitis B, y la parotiditis, que antaño constituían verdaderos problemas epidemiológicos, también han reducido considerablemente su morbilidad mortalidad.6Con todos estos elementos podríamos catalogar de extraordinario el impacto que ha tenido el programa ampliado de inmunización en nuestro país. Ahora bien, sin querer opacar los beneficios de las vacunas preventivas, que por demás superan ampliamente los riesgos, todavía se siguen observando eventos adversos relacionados con su uso. Tal es así que 852 reacciones adversas de las 28 338 que se notificaron a la UCNFv entre los años 2006 y 2007, estuvieron relacionadas con las vacunas que se emplean en nuestro país para la prevención y el control de las enfermedades infecciosas.7
Según la tabla 1 el evento adverso notificado más frecuentemente fue la fiebre (60,0 %). Considerado el prototipo de los eventos sistémicos en lo que a vacunas se refiere, se comportó como un evento común para prácticamente todas las vacunas incluidas en nuestra investigación (tabla 6).
La inflamación, el dolor y el enrojecimiento en el sitio de inyección, son eventos locales comunes, que suelen presentarse también con una elevada frecuencia de aparición.8.9 Atribuidos generalmente a los adyuvantes del antígeno vacunal, ocuparon el segundo, tercer y quinto puesto, respectivamente (tabla 1). Mucho se ha avanzado en el conocimiento de la naturaleza y el mecanismo de acción de los adyuvantes, sustancias que mejoran la inmunogenicidad y por lo tanto, la efectividad del antígeno vacunal. Sin embargo, todavía el grado de toxicidad y la pirogenicidad los limitan con respecto a su uso.10
Los errores técnicos o programáticos, que incluyen la inapropiada esterilización de agujas y/o jeringuillas, la incorrecta preparación de la vacuna, la inmunización en el lugar errado, entre otros, si bien no están relacionados directamente con la composición de las vacunas, pueden causar también eventos locales en el sitio de inyección,3 y aunque se confía en que sean los menos dado la profesionalidad de nuestro personal de salud, no debe descuidarse en este sentido.
La edad es un factor intrínseco, que se tiene en cuenta a la hora de elaborar y programar el calendario de vacunaciones o inmunizaciones de cada país. Generalmente, se desea la administración precoz de vacunas a los lactantes, para protegerlos antes de que se expongan a los agentes patógenos bacterianos o víricos.11 Cabe esperar entonces que si este es el grupo expuesto a más productos vacunales, presente entonces mayor número de eventos adversos (46,8 %). En cuanto a la distribución por sexo no hubo diferencias significativas (tabla 2).
Otro de los resultados obtenidos estuvo relacionado con las vacunas asociadas a un mayor número de eventos adversos, destacándose la pentavalente con 252 de las 852 que conformaron el total (tabla 3). Esta nueva vacuna combinada, cuyo nombre comercial es Heberpenta, y de la que se dispone desde el 2006, ofrece una gran cobertura vacunal. Protege contra 5 enfermedades infecciosas que causan miles de defunciones anuales en todo el mundo: la difteria, el tétanos, la tos ferina, la hepatitis B y el Haemophilus Influenzae tipo B.12 Asimismo, reduce en gran medida la cantidad de inyecciones que los más pequeños de casa deben recibir como parte del Programa Nacional de Inmunización. Claro está, no sería descabellado pensar que independientemente de los beneficios que sin lugar a duda reportan las vacunas combinadas, también podría aumentar la frecuencia de aparición de eventos adversos. Ténganse en cuenta los eventos individuales de cada vacuna. Sin embargo, hay estudios que plantean, que con la combinación de antígenos, lo que sucede más bien es que se complejiza la valoración de la reactogenicidad, por cuanto se hace más difícil atribuir los eventos adversos a cada uno de sus componentes.13 Tener presente además que desde su salida al mercado (menos de 5 años), este producto se encuentra en vigilancia intensiva, lo cual favorece que se reporte un número de ETAV superior al resto de las vacunas que no se encuentran sometidas a este método activo de farmacovigilancia.
La eficacia del toxoide tetánico está dada fundamentalmente por la capacidad que tiene el individuo inmunizado de evitar la enfermedad. En contraste, la eficacia de los programas de vacunación contra la difteria está relacionada con la inmunidad poblacional y la interrupción de la cadena de transmisión. La prevención de estas enfermedades se apoya en esquemas de vacunación con vacunas polivalentes que incluyen ambos toxoides.14 Dentro de ese grupo se encuentra la vacuna antidiftérica-antitetánica, de nombre comercial VA-DIFTET, segunda dentro de las más implicadas en la aparición de eventos adversos (tabla 3). Su reactogenicidad está relacionada esencialmente, con la presencia del adyuvante hidróxido de aluminio en su composición, predominando así las reacciones locales.14 Resultado similar a otro estudio de farmacovigilancia.15
Cuando aun no se contaba con la pentavalente en el Esquema Nacional de Inmunización, la DPT solía encabezar las listas de vacunas causantes de eventos adversos en nuestro país.16-18 La literatura plantea que la reactogenicidad de dicha vacuna obedece a la presencia del componente antitosferinoso de células enteras, una suspensión de microorganismos inactivos de Bordetella pertussis.19 De cualquier forma, se mantiene dentro de las primeras 6 vacunas asociadas a un mayor número de eventos adversos (tabla 3).
Si se analiza que el grueso de vacunas se administra en la APS, será fácil entender porque la mayoría de las notificaciones provienen justamente de ese nivel de atención médica (95,3 %) (tabla 4). ]]>
En la tabla 4 puede verse también que no fue el personal de enfermería, sino los médicos, los profesionales que más reportaron (36 %). La explicación quizás esté, en que muchas de los eventos adversos notificados, como la fiebre, el dolor, el edema, entre otros, no suelen ser reacciones inmediatas. Por lo general aparecen tiempo después de la vacunación, y son motivo frecuente de consulta médica, amén de la motivación personal que se tenga para notificar.La tabla 5 por su parte, presenta la distribución de los eventos por grado de severidad. Tal y como se esperaba predominaron los leves (66,4 %), signos y síntomas que generalmente aparecen en las primeras 48 h tras la vacunación y que ceden espontáneamente.
Siete eventos fueron clasificados como graves, y solo uno ocupó el sitio de las reacciones mortales (tabla 5). Ahora bien, es válido aclarar que cuando se aplica el algoritmo de causalidad la mayoría de estos eventos graves, incluyendo el evento mortal, no tenían una asociación estrecha de causalidad con la vacuna aparentemente implicada, lo que demuestra una vez más que en términos de vacunas los beneficios superan ampliamente los riesgos.
A diferencia de lo que se recoge en la literatura,20 los eventos sistémicos fueron los de mayor cuantía (tabla 6). Sin duda, los 511 casos con fiebre que se mencionaron al inicio de la discusión hipertrofiaron esta categoría. No obstante se debe tener en cuenta que muchas de las manifestaciones reportadas incluidas en el saco de los eventos sistémicos como la irritabilidad, los vómitos, la ansiedad, la lipotimia, entre otros, pudieron estar relacionados con el mismo acto de la inyección, y no con las propiedades inherentes de las vacunas. Si a esto se le suma la posibilidad de que los eventos adversos hayan sido coincidentales con cualquiera de las enfermedades que afectan a los niños, será más fácil entender por qué este resultado se convierte en solo un estimado.
Se concluye que los principales ETAV relacionados con las vacunas que inmunizan contra las enfermedades infecciosas fueron la fiebre, la inflamación y el dolor en el sitio de inyección. Tal y como se esperaba los ETAV predominaron en lactantes. La afectación fue prácticamente igual en uno y otro sexos. La APS se destacó en la notificación. Los médicos fueron los profesionales que más reportaron. El comportamiento en cuanto a severidad coincidió con lo reportado en la literatura. En cambio, hubo diferencias en cuanto a la distribución de los ETAV según su localización. La pentavalente se asoció a un mayor número de eventos.
REFERENCIAS BIBLIOGRÁFICAS
1. Morejón M. Actualización en antimicrobianos sistémicos. Cuba: ECIMED; 2005
2. Berdasquera D, Cruz G, Suárez CL. La vacunación, antecedentes históricos en el mundo. Rev Cubana Med Gen Integr. 2000;16(4):375-8.
3. Berdasquera D, Suárez CL, Jiménez L. Vigilancia de eventos adversos a vacunas Un problema de salud en la comunidad. Rev Cubana Med Gen Integr. 2000;16(4):379-83.
4. Organización Panamericana de la Salud. Salud en las Américas. Washington, DC: OPS; 2007 (Publicación Científica y Técnica No. 622).
5. Organización Panamericana de la Salud. Curso de gerencia para el manejo efectivo del Programa Ampliado de Inmunización (PAI). Modulo I: Enfermedades del PAI. Washington, DC: OPS; 2006.
6. Ministerio de Salud Pública. Anuario Estadístico de Salud. La Habana: Dirección Nacional de Estadística; 2006
7. Centro para el Desarrollo de la Farmacoepidemiología. Informe Anual. La Habana: UCNFv; 2007
8. Corretger JM, Aristegui J, Hernández-Sampelayo T. Las recientes imputaciones a las vacunas: interpretación actual. Revista Vacunas. Investigación y Práctica. 2004;5:87-91.
9. Calvo DM, Cires M, Cruz MA, Delgado I, Furones JA. Formulario Nacional de Medicamentos. La Habana: ECIMED; 2006.
10. Aguilar Rubido JC, Leal Angulo MJ. Adyuvantes vacunales: estado actual y nuevas tendencias Biotecnología Aplicada. 2000;17(3):147-160.
11. Vaughan N. Tratado de Pediatría. 15 ed. New York: Editorial Mc Graw- Hill; 1998
12. Grupo de análisis de Información de Finlay Ediciones. Nueva vacuna cubana combinada (DPT-hepatitis B-Hib). Vacci Monitor. 2006;15(2):30
13. Elliman D, Bedford H. Safety and efficacy of combination vaccines. Combinations reduce distress and efficacious. BJM 2003;326-46.
14. Ochoa RF, Morelia I, Menéndez J. Reactogenicidad e inmunogenicidad de una nueva vacuna de toxoide tetánico y diftérico con concentración reducida en adolescentes cubanos. Vacci Monitor. 2006;15(2):13-7.
15. Chao A. Caracterización de eventos adversos temporalmente asociados a vacunación. Cuba 2003-2005. Trabajo para optar por el título de Especialista de Primer Grado en Farmacología. La Habana: Hospital Calixto García; 2007.
16. Centro para el Desarrollo de la Farmacoepidemiología. Informe Anual. La Habana: UCNFv; 2003.
17. Centro para el Desarrollo de la Farmacoepidemiología. Informe Anual. La Habana: UCNFv; 2004.
18. Centro para el Desarrollo de la Farmacoepidemiología. Informe Anual. La Habana: UCNFv; 2005.
19. Peña MA, Triana RTM, Menéndez HJ, Mirabal SM, Armesto del Río M, Baró SM. Seguimiento de la reactogenicidad de la vacuna DTP cubana utilizando dos métodos paralelos. Vacci Monitor. 2005;14(1):10-20.
20. Collet JP, MacDonald N, Cashman N, Ples R. Vigilancia de la seguridad de las vacunas: evaluación de las notificaciones de episodios adversos por un comité consultivo de expertos. Boletín de la OMS 2003. Recopilación de artículos No 3:51-7.
Recibido: 8 de abril de 2010. ]]> Aprobado: 17 de mayo de 2010.
Dra. Ivette Díaz Mato. Facultad de Medicina "Dr. Salvador Allende". Czda. del Cerro No. 1 551, Cerro, Ciudad de La Habana. Cuba. Correo electrónico: ivettediaz@infomed.sld.cu ]]>