ARTÍCULOS ORIGINALES
Estudio de la fotodegradación de ácido fólico encapsulado en microesferas de goma arábiga y maltodextrina
Study of photodegradation of folic acid encapsulated in microspheres of gum arabic and maltdextrin ]]>
Seneida Lopera CardonaI; Cecilia Gallardo CabreraII
IProfesional en Ciencia y Tecnología de Alimentos. Magister en Ciencias Farmacéuticas. Investigadora. Grupo de Estabilidad de Medicamentos Cosméticos y Alimentos. Facultad de Química Farmacéutica. Universidad de Antioquia. Medellín, Colombia.
IIDoctora en Ciencias Químicas. Química Farmacéutica. Asistente. Grupo de Estudios de Estabilidad de Medicamentos, Cosméticos y Alimentos. Facultad de Química Farmacéutica. Universidad de Antioquia. Medellín, Colombia.
]]>
RESUMEN
En este estudio se adaptó un método HPLC de par iónico que permitió medir de forma selectiva el ácido fólico y sus 2 productos de degradación formados en las condiciones de irradiación usadas (lámpara de xenón a 250 Wm-2). Los tiempos de retención fueron: ácido fólico 10,2 min, formilpterina 4,4 min y p-aminobenzoil-L-ácido glutámico 6,1 min. El método se aplicó para determinar la longitud de onda responsable de la fotodegradación y para cuantificar el porcentaje de degradación que sufre el ácido fólico incorporado en microesferas obtenidas por secado por aspersión y con proporciones diferentes de goma arábiga-maltodextrina: 100-0, 80-20, 70-30 y 50-50, como materiales de cubierta. Se encontró como responsable de la fotodegradación la radiación de 350 nm, y las microesferas con mayor contenido de goma arábiga fueron las que presentaron mayor capacidad de proteger el ácido fólico, en estas el porcentaje de degradación fue de 20,1 % mientras que en el control fue de 49,2 %.
Palabras clave: Ácido fólico, fotoestabilidad, método HPLC indicador de estabilidad.
ABSTRACT
In present paper a par ionic HPLC method was adapted to measure in a selective way the folic acid and its two degradation products formed under the irradiation conditions used (250 Wm2). The retention times were: folic acid (10.2 min; formylpterin (4,4 min) and p-aminobenzoil-glutamic acid (6,1 min). Method was applied to determine the wavelength accounting for photodegradation and also to quantify the degradation percentage suffering ty the folic acid added in microspheres obtained by aspersion driying and with different ratios of gum arabic and maltodextrin: 100-0, 80-20, 70-30 and 50-50 as covering materials. The responsible of photodegradation was the 350 nm radiacion and the microspheres with a great content of gum arabic had the greater ability to protect the folic acid, in these ones el degradation percentage was of 20.1 % whereas in the control it was of 49.2 %.
Key words: Folic acid, photostability, HPLC method as stability indicator.
]]>
]]>
INTRODUCCIÓNEl ácido fólico (AF), N-4 [{(2-amino-1,4-dihydro-4-oxo-6-pteridinyl)-methyl}amino]benzoyl, pertenece a la familia de los folatos, los cuales actúan como un cofactor en reacciones de transferencia de carbono (formilo, hidroximetilo y metilo) en la biosíntesis de nucleótidos (bases purinas y pirimidinas), metabolismo de aminoácidos (metionina, histidina), metabolismo de neurotransmisores (serina, colina).1
La deficiencia de AF en la dieta está relacionada con defectos del tubo neural, enfermedades coronarias y anemia megaloblástica, y dado que los animales y humanos no pueden sintetizar folatos, es necesario incorporarlos dentro de la dieta a partir de fuentes vegetales o mediante la fortificación de alimentos usando el AF.2
Además el AF es un agente potencial para la prevención del cáncer, en el atrapamiento de radicales libres porque tiene actividad antioxidante.3
Los folatos naturales, son altamente inestables, siendo el AF el más estable. El AF es lábil a la luz.4-7 perdiendo su actividad biológica.4 En la fotodegradación se da una ruptura del enlace amino C9-N10, dando lugar a compuestos como 6-formilpterin(FPT), 6-carboxipterin (CPT) y p-aminobenzoil-L-ácido glutámico (PGA).5
Para el seguimiento de la fotodegradación de AF se han propuesto métodos como la cromatografía líquida de alta resolución (HPLC en inglés)6,7 y espectroscopia de fluorescencia.3,8 A pesar de ser bien reconocida la relevancia del AF para el ser humano y de tener evidencias de su fotoinestabilidad, hasta el momento se han reportado muy pocos estudios sobre la fotoestabilización, a saber: estabilización a través de la microcapsulación con polímeros de alginato y pectina,9 vehiculización del AF en micelas poliméricas de alcohol polivinílico sustituido con ácido oleico,10 y adición de ácido ascórbico.11,12
El objetivo de este artículo fue reportar la adaptación de un método indicador de estabilidad validado para monitorear la fotodegradación del AF, identificar la longitud de onda responsable de la fotodegradación y evaluar el efecto protector que puede ejercer la microencapsulación del AF en microesferas de maltodextrina y goma arábiga.
MÉTODOS
]]>
Materiales
Se utilizó AF calidad materia prima farmacéutica certificada (Laboratorio Sintofarm SPA) para la preparación de microesferas y AF estándar secundario para los ensayos cuantitativos por HPLC. La enzima dextrozima GA (270 UGA/ mL), los reactivos hidróxido de tetrabutilamonio (20 % acuoso), hidróxido de sodio, ácido cítrico, fosfato disódico anhídrido, dihidrógeno fosfato de potasio, metanol grado HPLC correspondieron a la marca Merck. Para todos los ensayos se usó agua purificada. Los 4 tipos de microcápsulas, M1, M2, M3 y M4 de AF fueron obtenidos como se reporta previamente por Gallardo, Lopera, Guzmán y Cataño.13
Método de cuantificación del ácido fólico
El método de cuantificación fue adaptado y estandarizado a partir del método HPLC de apareamiento iónico reportado por Khan y otros.6 Se utilizó un cromatógrafo Perkin Elmer con detector UV con arreglo de diodos serie 200 EP y una columna LC SORBAX SB-C18 (150 x 3 mm x 3,5 µm), a una temperatura de 30 ± 2 ºC, la longitud de onda del detector fue 254 nm y la fase móvil consistió en una mezcla de solución amortiguadora de pH 6,97 ± 0,1 que contenía dihidrógeno fosfato de potasio 0,017 M y el modificador hidróxido de tetrabutilamonio (0,22 %) y metanol, en relación de 66:34, respectivamente, con un pH final de la mezcla de 7,7 ± 0,1.
Para la estandarización del método se usaron soluciones de AF en una concentración de 264 µg/mL, en solución amortiguadora citrato-fosfato pH 7,5 ± 0,1, algunas de las cuales fueron sometidas a irradiación como se especifica, para observar el comportamiento cromatográfico de los productos de degradación.
La validación del método consistió en evaluar los parámetros: linealidad, exactitud y precisión en la señal cromatográfica correspondiente al AF, siguiendo las directrices de la guía ICH.14 Para ello se prepararon soluciones de AF en 6 valores de concentración: 290, 264, 204, 150, 92 y 60 µg/mL, en solución amortiguadora citrato-fosfato pH 7,5 ± 0, 1, filtradas a través de membranas Millipore 0,45 µm. Cada concentración se preparó 5 veces de manera independiente.
]]>
Condiciones de irradiación de muestras
Para los ensayos de fotoestabilización se utilizó una cámara Solarbox, (ERICHSEN), equipada con lámpara de xenón de 1 500 W de acuerdo con la guía de fotoestabilidad para evaluación de medicamentos de la Conferencia Internacional de Armonización (ICH en inglés),14 ajustada a una irradianza integral (300 y 800 nm) de 250 W/m2, y con un tiempo de irradiación hasta 30 min las muestras para ser sometidas a la radiación se envasaron en balones volumétricos de 50 mL.
Para efectos de visualizar el efecto fototoprotector de las microesferas se irradiaron conjuntamente soluciones y suspensiones de AF, y suspensiones de microesferas de AF, en concentraciones equivalentes a 264 µg/mL, preparadas en solución amortiguadora citrato-fosfato pH 7,5.
Las suspensiones no presentaron sedimentación durante el tiempo del ensayo (20 min). Se prepararon 6 suspensiones en cada caso, 3 muestras fueron protegidas de la luz y las otras tres se llevaron a la cámara de irradiación. Inmediatamente después de la irradiación, las muestras fueron sometidas al proceso de extracción de AF y cuantificadas por HPLC.
Determinación de la longitud de onda responsable de la fotodegradación del ácido fólico
Se usaron filtros ópticos de vidrio: magenta y Azul (Edmund Industrial Optics), los cuales fueron caracterizados con un espectrofotómetro UV-Visible 1601 Shimadzu, registrando el espectro entre 190-800 nm. Muestras de la solución de AF (264 µg/mL) fueron envasadas en recipientes de vidrio con un diámetro superior de 4 cm, el filtro óptico se ubicó en la parte superior del envase; los lados laterales y el fondo del envase se cubrieron completamente con papel negro y papel aluminio, de manera que solo llegara a la muestra la luz que atravesó el filtro. La solución así dispuesta se sometió a irradiación en la cámara ajustada a 250 W/m2 durante 20 min, tomando alícuotas cada 5 min, para ser analizadas por el método HPLC.
]]>
Método de extracción del ácido fólico
Cada muestra de suspensiones de AF como de microesferas se sometió al siguiente procedimiento: se le adicionó 0,2 mL de solución de ácido cítrico al 50% hasta un pH de 4,3, pH óptimo de la actividad de la enzima que genera el rompimiento de la maltodextrina. Se adicionó 70 mL de enzima dextrozima GA y se llevó a 60 °C en baño María durante 10 min. Se adicionó a cada suspensión y para facilitar la solubilidad del AF, 5 mL de solución amortiguadora citrato-fosfato pH 7,5 ± 0,1, ajustando el pH con NaOH al 10 %. Se agitó por 5 min en baño ultrasónico (Transsonic TP 690- Elma), y finalmente se tomó una alícuota de 2 mL, se filtró y se procedió al análisis por HPLC.
Métodos estadísticos
Se usó el paquete estadístico Statgrafics 5.1, Se aplicó análisis de regresión, determinación de coeficiente de correlación, de variación y de determinación, prueba de la t de Student, análisis de varianza y ensayo de Cochran.
RESULTADOS ]]>
Adaptación y validación del método indicador de estabilidad
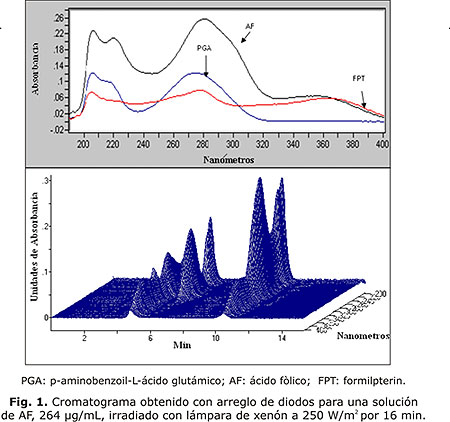
Dado que el método reportado por Khan y otros, que consiste en el empleo de una fase móvil compuesta por una mezcla de solución amortiguadora dihidrògeno fosfato de potasio 0,017 M, hidróxido de tetrabutilamonio (20 % acuoso), y metanol, en relación 870:15:250 v/v, respectivamente, con una columna C18 (300 x 3,9 mm), no se especifica temperatura, flujo de 1,0 mL/min, longitud de onda de 254 nm, con tiempos de análisis altos (30 min), se realizó una optimización del método usando una columna C18 de menor longitud (150 x 3 mm) y con tamaño de partícula de relleno de 3,5 mm, controlando la temperatura y usando la misma fase móvil, buscando reducir el tiempo de análisis; por tanto, se procedió a evaluar diferentes relaciones de fase metanólica y acuosa (solución amortiguadora dihidrógeno fosfato de potasio 0,017 M y hidróxido de tetrabutilamonio 0,22 %), manteniendo constante las siguientes condiciones cromatográficas: longitud de onda del detector 254 nm, temperatura de trabajo: 30 °C, flujo de 0,4 mL min-1. Las mejores condiciones cromatográficas obtenidas, teniendo en cuenta el tiempo de análisis y la resolución, fueron logradas con una fase móvil fase acuosa:metanólica 66:34, respectivamente, con pH final de la mezcla de 7,7 ± 0,1, donde el AF eluyó a 10,2 min (lmax a 205, 280 nm y 350 nm) y los productos de degradación a 6,1 y 4,4 min (lmax a 205, 278 y 365 nm), se obtuvieron los siguientes parámetros cromatográficos: factor de capacidad, K: 3,27; platos teóricos N: 2 420; factor de simetría para la señal correspondiente al AF: 1,4 y resolución 6,6. En la figura 1 se puede observar un cromatograma tridimensional que muestra los espectros de absorción del AF y los fotoproductos formados en las condiciones del estudio.
Para la evaluación de la linealidad del método se elaboró una curva de calibración de soluciones de AF con 5 replicas, la cual fue lineal en el intervalo de concentraciones entre 60 y 264 µg/mL; en estudios preliminares se consideró un valor de concentración de 0,010 mg/mL pero se observó que el método ya no es lineal en estas concentraciones, dado que el pico cromatográfico correspondiente al AF pierde simetría. El modelo lineal fue descrito por la ecuación Area= 93,7734 *Concentración -281,27, con un coeficiente de correlación (r) de 0,9997 y un coeficiente de determinación (r2) de 0,9995.
Como se muestra en la tabla 1, al evaluar los parámetros del modelo, intercepto y pendiente, se encontró que la pendiente es diferente de cero (p< 0,05), ya que el valor p crítico hallado fue 0,0000 y el intercepto es igual a cero (p> 0,05), ya que el valor p crítico hallado fue 0,1100. La independencia del modelo cumplió, al ser evaluada con el ensayo gráfico de residuales donde no se encontraron tendencias en la distribución de los puntos. Al aplicar el ensayo de homogeneidad en varianza con p> 0,05, al aplicar el ensayo de Cochran's, se confirmó que el factor concentración no influyó en la variabilidad de los datos. De acuerdo con el análisis de varianza, los datos obtenidos en la curva lineal, se ajustaron al modelo matemático, ya que la hipótesis nula no fue rechazada con p= 0, 4888, indicando que la falta de ajuste no es significativa en el modelo de regresión.
La precisión y exactitud del método fueron evaluadas conjuntamente, la precisión se evaluó a través de los coeficientes de variación de los datos obtenidos en 3 valores de concentraciones (60, 150 y 264 µg/mL), durante 3 días, como se muestra en la tabla 2. Los CV obtenidos para precisión fueron menores del 1 %, y los porcentajes de recuperación para el ensayo de exactitud fueron cercanos a 100 %.
]]>
Determinación de la longitud de onda responsable de la fotodegradación del ácido fólico
En los estudios anteriores sobre la fotodegradación del AF se reporta el uso de diferentes tipos de lámparas, y no se precisa cuál es la longitud de onda que produce la fotólisis del AF. Dado que conocer esta longitud de onda es importante para el estudio de su fotoestabilización, se realizaron ensayos usando filtros adicionales para separar rangos de longitud de onda específicos considerando que el AF presenta 3 lmax de absorción a 205, 280 y 350 nm; la degradación en condiciones naturales sería comprensible si la longitud de onda de 350 nm está implicada. Los resultados de la descomposición del AF usando estos filtros se observa en la figura 2, donde se comparan con la cinética de descomposición de una solución de AF sin usar filtros, en esta última se observó que la descomposición del AF sigue una cinética de orden cero, con una velocidad de -9,75 µg mL-1min-1;mientras que con el filtro magenta que bloquea la luz a 350nm, la velocidad de descomposición se reduce a -1,806 µg mL-1 min-1, y con el filtro azul que deja pasar la luz a 350 nm la velocidad de degradación fue de -4,556 µg mL-1 min-1 (este filtro presenta cierto grado de bloqueo a 350 nm, por lo que se esperaba que la velocidad de filtración fuera menor que la cinética donde no se usó filtro).
Evaluación de la fotoestabilización del ácido fólico microencapsulado
Las microesferas de AF fueron obtenidas usando como agente encapsulante mezclas de goma arábiga y maltodextrina en 4 proporciones diferentes 100-0, 80-20, 70-30 y 50-50, respectivamente, y se sometieron a secado por aspersión (fig. 3). El tamaño de partícula de los 4 tipos de microesferas, fue determinado en un intervalo de 0,2-4,0 µm, la eficiencia de encapsulación se determinó en un intervalo de 88,00-97,34 %; los detalles de la preparación y caracterización fueron los reportados previamente por Gallardo, Lopera, Guzmán y Cataño.13
Para los ensayos de irradiación se prepararon suspensiones acuosas de microesferas y el grado de degradación se comparó con la irradiación de suspensiones de AF, como también de soluciones acuosas, en igual concentración.
DISCUSIÓN
Adaptación y validación del método indicador de estabilidad
De acuerdo a los espectros de absorción reportados en la literatura para el AF y sus principales fotoproductos, cuyas longitudes de onda de máxima absorción corresponden a: (1) AF 280 nm y 350 nm, (2) p-aminobenzoil-L-àcido glutámico (PABG) 275 nm y (3) formilpterina (6-FPT) 278 nm, 365 nm, no es posible seguir la degradación del AF por método espectrofotométrico, resultado también reportado por Capparelli y otros y Krisrtian y otros, pero con esta información es posible acercarse a la identificación de los fotoproductos. El espectro que corresponde a la señal cromatográfica con TR de 10,2 min, corresponde al AF, donde la absorbancia 280 nm asociada a las transiciones electrónicas que sufre el grupo p-aminobenzoíco y la lmax de 350 nm corresponde al grupo pteridina.
Adicionalmente, el pico cromatográfico correspondiente al AF es un pico puro, no se observan señales de absorbancia que muestren la elusión concomitante de otro compuesto. El espectro que corresponde al pico cromatográfico con TR de 4,4 min, siendo reportado como característicos de fotoproducto 6-FPT y el espectro que corresponde al pico cromatográfico con TR de 6,1 min, presenta una lmax a 205 y 275 nm, el cual resulta característico de PABG. De acuerdo con estos resultados la reacción que se está llevando a cabo en la solución de AF en las condiciones y en el tiempo de irradiación observado, corresponde a la primera fase de la reacción de degradación, donde no ha comenzado la oxidación del 6-FTP.
De acuerdo con los resultados de la tabla 1, se considera que el método cumple con la linealidad en las condiciones del ensayo y se puede concluir que la hipótesis de linealidad de la relación entre la respuesta del detector y la concentración del AF, es válida. Según el análisis de varianza, los datos de la curva lineal, se ajustan al modelo matemático, ya que la hipótesis nula no fue rechazada con P 0,4888, validando así la regresión lineal significativa.
En los resultados de la tabla 2 se presentan los datos de la evaluación de la exactitud y la precisión del método, que fueron menores de 2,0 % se puede concluir que el método es preciso y exacto y los porcentajes de recuperación se consideran aceptados para las condiciones del método, ya que están en el intervalo de 99 y 101 %. Al aplicar el ensayo de Cochran se obtuvo un valor de p= 0,50> 0,05, por lo tanto los datos cumplían con la homogeneidad en varianza; al aplicar la prueba de la t de Student, se obtuvo un t experimental de 1,8075 menor que el valor de t critico de 2,021, por lo tanto se confirmó que no existían diferencia significativa entre la recuperación media global obtenida de 100,34 y el 100 %, por lo que el método cumplió el ensayo de exactitud.
En la determinación de la longitud de onda responsable de la fotodegradación del AF, los resultados permitieron concluir que la lmax de 350 nm del AF fue la responsable de su fotodegradación. Este resultado muestra que el AF es susceptible a la degradación en condiciones naturales porque la radiación de 350 nm se encuentra en la región UVA que alcanza la superficie terrestre ya que no es débilmente absorbida en la atmósfera; por otra parte, este resultado también indica que la fotodegradación se debe a transiciones electrónicas que sufre el anillo de pteridina. ]]>
En la evaluación de la fotoestabilización del AF microencapsulado, en la preparación de soluciones se consideró el ajuste del pH, ya que este es un factor fundamental para la solubilidad y estabilidad del AF. Siendo el AF una molécula anfótera, con valores de pKa de 3,5 (a-COOH), 4,8 (b-COOH) y 8,38 (amina del grupo pteridina);15 experimentalmente se encontró que a valores de pH de 7,5 y con solución amortiguadora citrato-fosfato el AF presentó una buena solubilidad para concentraciones de 264 µg/mL. En reportes anteriores también se encontró que la estabilidad del AF era mayor en el intervalo de pH 5,0 a 7,0.16 El cálculo de los porcentajes de degradación encontrados para las soluciones y suspensiones de AF y microesferas sin irradiar e irradiadas (fig. 3), fueron determinados por el método HPLC, siguiendo el proceso de extracción descrito. La cuantificación del porcentaje de recuperación del AF desde las microesferas no fue posible evaluarla al no disponer de un sistema de secado por aspersión a escala laboratorio que permitiera obtener una muestra de microesferas en forma analítica, luego el método se evaluó a través del coeficiente de variación del contenido de AF encontrado en las microcàpsulas antes de irradiarlas, cuyos coeficientes de variación estuvieron en el intervalo de 0,4-2,2, que indican una buenaLos resultados mostraron que en la suspensión de AF se encontró un 47,83 ± 2,37 % de fotodegradación a los 30 min, mientras que el AF en solución a pH 7,5 sufre fotodegradación de un 58,7 ± 3,0 % en 16 min y a los 20 min esta degradación alcanza cerca del 80 %, lo cual es de esperarse puesto que las reacciones de degradación química, son más rápidas cuando el principio activo está en solución y adicionalmente en una suspensión se da lugar a reflexión de la luz con las mismas partículas sólidas suspendidas. En algunas matrices alimentarias, como jugos, cervezas, agua, el AF puede encontrarse en solución y en estos casos, la fotodegradación sería más drástica. Los resultados muestran que tanto en solución como en suspensión se presenta fotodegradación del AF libre, en proporciones importantes.
Los resultados con las microesferas muestran que la microencapsulación del AF disminuye la degradación del AF promovida por la luz, siendo las microesferas preparadas en relación goma arábiga:maltodextrina 100:0 y 80:20, las que presentan el mayor porcentaje de protección de los 4 tipos de microesferas, es decir, las que mayor proporción de goma arábiga presentan. Esto se puede explicar tomando en consideración la morfología de las microesferas, donde se observó que microesferas con mayor contenido de goma arábiga se caracterizan por presentar una cubierta rugosa pero continua, mientras que la maltodextrina forma microesferas mas esféricas pero con fracturas en su cubierta según los resultados obtenidos por Sem, vistos en previa publicación por Gallardo, Lopera, Guzmán y Cataño,13 lo que permite inferir que la goma arábiga presenta un papel importante en la fotoprotección del AF. Este efecto protector de la goma arábiga frente a reacciones de fotólisis ha sido observado anteriormente con otro tipo de sustancias activas como la bixina,17 aceites esenciales de cumina18 y riboflavina;19 se ha mencionado que la goma arábiga puede proveer fotoestabilidad por su limitada permeabilidad al oxígeno porque puede desempeñar una función más activa desde el punto de vista fotoquímico por desactivación de estados excitados.
En conclusión, el método adaptado, permite la separación del AF y sus fotoproductos dentro de un tiempo razonable de análisis (13 min), y cumple con la linealidad, repetibilidad y exactitud, requeridas para la cuantificación de AF en soluciones con concentración en el intervalo de 60 a 264 µg/mL.
La fotólisis del AF es promovida fundamentalmente por la luz absorbida por el grupo pteridina y que compromete al máximo de absorción a 350 nm.
El AF al estar en forma de suspensión, presenta un menor porcentaje de fotodegradación que en solución, y este porcentaje es aún menor, si este está recubierto en forma de microesferas. Las microesferas del AF con goma arábiga y maltodextrina elaboradas por el método de secado por aspersión representan una alternativa para la protección del AF, en el cumplimiento de estabilidad para lograr su función nutricional.
Las microesferas que permiten mayor fotoprotección al AF, son las que tienen en su composición mayor porcentaje de goma arábiga, probablemente debido a las características morfológicas que confiere la goma arábiga.
]]>
AGRADECIMIENTOS
Este trabajo fue desarrollado gracias al apoyo financiero del Comité para el Desarrollo de Investigación CODI-Universidad de Antioquia. Se declara que no existe conflicto de intereses de los investigadores con este Comité.
REFERENCIAS BIBLIOGRÁFICAS
1. Bekaert S, Storozhenko S, Mehrshahi P, Bennett MJ, Lambert W, Gregory JF et al. Folate bioforti?cation in food plants. Trends Plant Sci. 2002;13(1):28-35.
2. Avendaño López MC. Introducción a la Química Farmacéutica. Madrid: McGraw Hill; 1993.
3. Tyagi Y, Penzkofer A. Fluorescence Spectroscopic Behaviour of Folic Acid. Chem Phys.2009; 236(2-3):83-92.
4. Herschel K, Folic Acid. III. Chemical and Physiological Properties. J. Am. Chem. Soc. 1944; 66 (2):271-4.
5. Christopher B. Density functional theory study of possible mechanisms of folic acid Photodecomposition. J Photoch Photobio A Chemistry. 2009;208(1):1-6.
6. Khan A, Ahmad I, Akhtar JM. High performance liquid chromatographic determination of folic acid and its photodegradation products in the presence of riboflavin. J Pharmaceut Biomed. 1997;16(1):95-9.
7. Capparelli AL, Franco GS, Cabrerizo M, Lorent C, Thomas A. Study of the photolysis of folic acid and 6-formylpterin in acid aqueous solutions. J Photoch Photobio A Chemistry. 2000;135(2-3):147-54.
8. Kristian M, Steidal AE, Porojnicu AC, Juzeniene A, Vorobey A, Johnsson A, et al. Ultraviolet photodegradation of folic acid. J Photoch Photobio B. 2005;80(1):47-50.
9. Madziva H, Kailasaphaty K, Phillips M. Evaluation of alginatepectin capsules in cheddar cheese as s food carrier for the delivery of folic acid. Food Sci Technol-LEB. 2006;39(2):146-1.
10. Andrisano V, Bartolini M, Bertucci C, Cavrini V, Luppi B y Cerchiara T. Analytical methods for the determination de folic acid in a polymeric micellar carrier. J Pharmaceut Biomed, 2003;32(4-5):983-9.
11. Arcot J, Shrestha A. Folate: methods of analysis. Trends Food Sci Tech. 2005;16 (6-7):253-66.
12. Hendrickx ME Indrawati I, Ludikhuyze LR, Van Loey AM. Comparative study on presure and temperature stability of 5-methyltetrahydrofolic acid in model systems and food products. J Agr Food Chem. 2004;52(3):485-92.
13. Gallardo C, Lopera SM, Guzmán C, Cataño C. Desarrollo y caracterización de micropartículas de AF formadas por secado por aspersión, utilizando goma arábiga y maltodextrina como materiales de pared. Vitae. 2009;16(1):55-65.
14. International Conference on Harmonization (ICH), Guidelines for the photostability testing of new drug sustances and products. Federal Register. 1997;62:27115-22.
15. Bryant CN, Sharpless KE, Sander LC. Quantitative determination of folic acid in multivitamin/multielement tablets using liquid chromatography/tandem mass spectrometry. J Chromatographic A. 2006;1135 (2):203-11.
16. Ahmad I, Khan MA, Akhtar JM. Photodegradation of folic acid in aqueous solution. J Pharm Biomed Anal. 1999;19(3-4):269-5.
17. Barbosa MIMJ, Borsarelli CD, Mercadante AZ. Light stability of spray-dried bixin encapsulated with different edible polysaccharide preparations. Food Res Int. 2005;38(8-9):989-94.
18. Dattanand Kanakdande, Rajesh Bhosale, Rekha S. Singhal. Stability of cumin oleoresin microencapsulated in diVerent combination of gum arabic, maltodextrin and modiWed starch. Carbohyd Polym. 2007;67(4):536-41.
19. Montenegro M, Nunes L, Mercadante A, Borsarelli C. Photoprotection of vitamins in skimmed milk by an aqueous soluble lycopene-gum arabic microcapsule. J Agr Food Chem. 2007;55(2):323-9.
Recibido: 8 de junio de 2010.
Aprobado: 17 de julio de 2010.
]]>
MSc. Seneida Lopera Cardona. Facultad de Química Farmacéutica. Universidad de Antioquia. Calle 50A No. 63-85, Medellín, Colombia. Correo electrónico: gallardoqf@gmail.com; cgallardo@farmacia.udea.edu.co ]]>