ARTÍCULO ORIGINAL
Desarrollo y validación de un método por cromatografía en capa delgada para los estudios de estabilidad del naproxeno
Development and validation of a thin-layer chromatography method for stability studies of naproxen
Yaslenis Rodríguez Hernández,I Yania Suárez Pérez,II Oscar García Pulpeiro,III Tania Rodríguez BorgesIV
]]>
I Licenciada en Ciencias Farmacéuticas. Máster en Ciencias Tecnología y Control de Medicamentos. Instructor. Instituto de Farmacia y Alimentos. Universidad de La Habana. La Habana, Cuba.
RESUMEN
Se realizó la validación de un método analítico con vistas a su aplicación en los estudios de estabilidad de las futuras formulaciones de supositorios de naproxeno para uso infantil y adulto. Se determinaron los factores que más influyeron en la estabilidad del naproxeno; la mayor degradación ocurrió en el medio ácido, oxidante y por acción de la luz. Se determinó la posibilidad de formación de ésteres entre el grupo carboxilo libre presente en el naproxeno y el monoestearato de glicerilo presente en la base como una de las vías de degradación en la nueva formulación; se obuvieron resultados satisfactorios. Se desarrolló un método por cromatografía en capa delgada y se seleccionaron las mejores condiciones cromatográficas. Se emplearon placas de sílica gel GF254 y revelador ultravioleta a 254 nm. Se evaluaron 3 sistemas de disolventes entre los cuales el A, compuesto por: acético glacial:tetrahidrofurano:tolueno (3:9:90 v/v/v), permitió una adecuada resolución entre el analito y los posibles productos de degradación, con un límite de detección de 1 µg. La aplicación del método propuesto se limitó a la identificación de los posibles productos de degradación solo con fines cualitativos y no como prueba límite. El método fue suficientemente sensible y selectivo para aplicarlo con el objetivo para el cual fue diseñado, según los resultados obtenidos en la validación.
Palabras clave: naproxeno, estabilidad, cromatografía en capa delgada (CCD), validación, supositorios.
]]>
ABSTRACTThe validation of an analytical method was carried out to be applied to the stability studies of the future formulations of naproxen suppositories for infant and adult use. The factors which mostly influenced in the naproxen stability were determined, the major degradation occurred in oxidizing acid medium and by action of light. The possible formation of esters between the free carboxyl group present in naproxen and the glyceryl monoestereate present in the base was identified as one of the degradation paths in the new formulation. The results were satisfactory. A thin-layer chromatography-based method was developed as well as the best chromatographic conditions were selected. GF254 silica gel plates and ultraviolet developer at 254 nm were employed. Three solvent systems were evaluated of which A made up of glacial acetic: tetrahydrofurane:toluene (3:9:90 v/v/v)allowed adequate resolution between the analyte and the possible degradation products, with detection limit of 1 µg. The use of the suggested method was restricted to the identification of possible degradation products just for qualitative purposes and not as final test. The method proved to be sensitive and selective enough to be applied for the stated objective, according to the validation results.
Key words: naproxen, stability, thin-layer chromatography, validation, suppositories.
INTRODUCCIÓN
El naproxeno se considera desde el punto de vista químico, un derivado del ácido propiónico: ácido (S)-6-metoxi-a-metil-2-naftalenacético.1,2
Los factores que afectan la estabilidad del naproxeno son: la hidrólisis catalizada por ácidos y luz, así como la presencia de oxígeno.1
Otros autores plantean que la estabilidad del naproxeno como materia prima o en una forma farmacéutica se puede afectar bajo diferentes condiciones de estrés como: la temperatura, luz, humedad y el pH, los cuales pueden producir diferentes tipos de productos de degradación como el 2-metoxi-6-etil naftaleno (MEN). Además, se ha reportado el 2-acetil-6-metoxi naftaleno (AMN) como una de las principales impurezas derivadas del procedimiento de síntesis.3 ]]>
También se ha estudiado la descarboxilación oxidativa del naproxeno como un método alternativo de degradación del fármaco.4Las técnicas de elección para el seguimiento de la estabilidad química son las cromatográficas, siendo la cromatografía líquida de alta resolución (CLAR) un método muy ventajoso. El empleo de métodos por cromatografía en capa delgada (CCD) para estudios de estabilidad constituye una variante aceptada para llevar a cabo evaluaciones en la etapa de desarrollo del producto, es por esta razón que se propone para los estudios de estabilidad del naproxeno en supositorios para uso infantil y adulto.
MÉTODOS
Desarrollo del método por cromatografía en capa delgada para estudios de estabilidad de naproxeno en supositorios. Validación
Selección de las condiciones cromatográficas
Se utilizaron 3 sistemas de disolventes con el objetivo de evaluar el comportamiento cromatográfico del analito y sus posibles productos de degradación. Los sistemas de disolventes empleados fueron:
Sistema A: ácido acético glacial:tetrahidrofurano:tolueno (3:9:90 v/v/v) reportado para sustancias relacionadas en la suspensión oral de naproxeno.2 ]]>
Sistema B: ácido acético glacial:acetonitrilo:2-propanol:n-hexano (5:50:100:845 v/v/v/v) reportado como fase móvil para la determinación de la pureza enantiomérica del naproxeno por HPLC.2Sistema C: cloroformo en presencia de vapores de amoníaco.
En los 3 casos se utilizaron como fases estacionarias placas de sílica gel GF254 y como revelador luz UV suministrada por una lámpara UV HANAU a 254 nm.
Tratamiento de la muestra
Se sometió el naproxeno, ingrediente farmacéutico activo (IFA), y la sustancia auxiliar (Rosupol) de la futura formulación de supositorios, a condiciones de estrés con el objetivo de obtener los posibles productos de degradación.
Las condiciones degradativas fueron las siguientes:
1. Pirólisis: naproxeno (materia prima) sometido a una temperatura de 200 ± 5 °C.
2. Medio ácido: 1 parte de HCl 1 mol/L más 2 partes de agua más 7 partes de disolución de naproxeno en etanol al 2 % (m/v).
3. Medio básico: 1 parte de NaOH 1 mol/L más 2 partes de agua más 7 partes de disolución de naproxeno en etanol al 2 % (m/v). ]]>
4. Medio oxidante: 3 partes de H2O2 al 30 % (v/v) más 7 partes de disolución de naproxeno en etanol al 2 % (m/v).5. Luz natural: se preparó de 2 formas:
-7 partes de disolución de naproxeno en etanol al 2 % (m/v) más 3 partes de agua.
-10 mL de disolución de naproxeno al 2 % en etanol (m/v).
Ambas muestras fueron expuestas a la luz durante 60 días.
Las muestras expuestas a los medios: ácido, básico y oxidante se sometieron a reflujo por 16 h al igual que una disolución de naproxeno al 2 % en etanol (m/v).
Se preparó un patrón de naproxeno materia prima y se disolvió en etanol para lograr una concentración final de 5 % (m/v).
La muestra sometida a pirólisis se disolvió en etanol para lograr una disolución de igual concentración que el patrón de naproxeno (5 % m/v).
También se prepararon muestras con la grasa que es el excipiente del supositorio de la siguiente forma: ]]>
1. Grasa dura pura (20 g).2. Naproxeno (0,5g) más grasa dura (20 g).
3. Glicerina.
4. Naproxeno (0,5 g) más glicerina (20 g).
5. Grasa dura (18 g) más monoestearato de glicerilo al 10 % (2 g).
6. Grasa dura (16 g) más monoestearato de glicerilo al 20 % (4 g).
7. Grasa dura (18 g) más monoestearato de glicerilo al 10 % (2 g) más naproxeno (0,5 g).
8. Grasa dura (16 g) más monoestearato de glicerilo al 20 % (4 g) más naproxeno (0,5 g).
Todas las muestras que contenían grasa se colocaron en la estufa a 105 ± 5 °C durante 7 días. Transcurrido este tiempo se pesó de cada muestra 0,5 g; se trasvasaron a volumétricos de 10 mL y se completó a volumen con etanol.
]]>
Procesamiento extractivo aplicado a muestras de supositorios previo a la aplicación del método por cromatografía en capa delgada
Se consideró la necesidad de aplicar un procesamiento extractivo previo a la aplicación de la CCD teniendo en cuenta la composición de la forma terminada, a partir del tratamiento de muestra reportado para naproxeno supositorios sustancias relacionadas,2 realizando algunos cambios. El procedimiento se describe en la figura 1.
Metodología recomendada para la toma de muestra a partir de supositorios
Teniendo en cuenta la forma farmacéutica en estudio para la cual se propone el método, se estableció un procedimiento para la toma de la muestra previo al análisis que se describe a continuación:
1. Pesar individualmente en balanza analítica 10 supositorios
2. Calcular el peso promedio.
3. Fundir los supositorios hasta obtener una masa homogénea. ]]>
4. Agitar homogenizando hasta enfriar la masa.5. Pesar una masa equivalente al contenido de naproxeno que se desea analizar (100 %), según composición de la formulación.
Validación del método por cromatografía en capa delgada
Para poder aplicar el método en el estudio de estabilidad del naproxeno en supositorios, se realizó la validación de este teniendo en cuenta los parámetros mínimos exigidos para la categoría II cualitativa.5
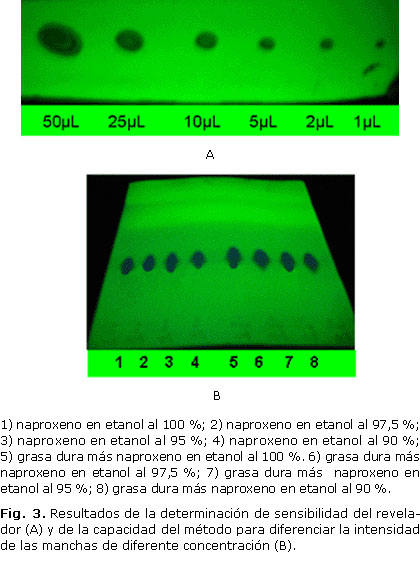
]]> Se probó la sensibilidad del revelador preparando una disolución de naproxeno en etanol 1 mg/mL. Se puntearon sobre una placa los siguientes volúmenes: 1, 2, 5, 10, 25 y 50 µL los cuales equivalen a 1, 2, 5, 10, 25 y 50 µg respectivamente. Posteriormente se dejaron secar las manchas y se revelaron bajo la luz UV.
Límite de detección
Criterio de aceptación: Se estableció como límite de detección la menor concentración de analito detectada con suficiente nitidez.
Selectividad
Se aplicaron en una placa 10 µL de las disoluciones alcohólicas resultantes de procesar todas las muestras preparadas según se describió anteriormente, así como los patrones de naproxeno en etanol equivalentes al 100 %.
Se determinó en cada caso el valor del factor de retardo (Rf). Se verificó visualmente la separación del fármaco respecto a los posibles productos de degradación, sustancias relacionadas y excipientes.
Criterio de aceptación: El método se consideró selectivo si se obtiene adecuada resolución expresada por los valores diferentes de Rf.
Experimento complementario para selectividad del método por cromatografía en capa delgada ]]>
Se prepararon las siguientes muestras:
1. Patrón (solución de naproxeno en cloroformo al 0,25 % m/v).
2. 4 mL de la solución de naproxeno en cloroformo al 0,25 % m/v más 250 mg de monoestearato de glicerilo no autoemulsionable.
3. 0,5 g de monoestearato de glicerilo no autoemulsionable en 8 mL de cloroformo.
4. Naproxeno más monoestearato de glicerilo no autoemulsionable al 5 % sometido a calentamiento en estufa a 170 °C por 8 h.
Posteriormente se preparó una disolución de la muestra 4, pesando 0,5 g en 8 mL de cloroformo. Se puntearon 10 µL de cada muestra en placas de sílica gel GF 254, se utilizó como fase móvil cloroformo, con simple corrimiento y como detector luz UV a 254 nm.
Una vez analizados los resultados y confirmada la formación de ésteres, se pesó 1,5 g de la muestra 4, se le añadió 25 mL de KOH alcohólico y se reflujó durante 45 min (muestra 5). Simultáneamente se puntearon iguales volúmenes (10 µL) de las muestras 1, 3, 4, 5 y 2 descritas anteriormente, en este mismo orden.
Evaluación de la capacidad del método para diferenciar la intensidad de las manchas en correspondencia con la diferencia de concentración ]]>
Se analizaron por triplicado muestras de placebo cargado con naproxeno en cantidades equivalentes al 2.5, 5 y 10 % de degradación respectivamente, procesadas según se describe en la figura 1 y se comparó la intensidad de las manchas con las resultantes de aplicar 10 µL de los patrones de iguales concentraciones de naproxeno en etanol. Adicionalmente se punteó 10 µL del patrón de naproxeno en etanol al 5 % (0 % de degradación).
Se analizó la intensidad y tamaño en las manchas correspondientes a los diferentes niveles evaluados entre placebos cargados y soluciones de referencia. Además, se compararon los valores de Rf obtenidos después de realizar los corrimientos cromatográficos correspondientes.
RESULTADOS
Desarrollo del método por cromatografía en capa delgada
Se utilizaron los 3 sistemas de disolventes mencionados con anterioridad con el objetivo de evaluar el comportamiento cromatográfico del analito y sus posibles productos de degradación. En la figura 2 se representan esquemáticamente, los resultados obtenidos al ensayar los 3 sistemas de disolventes. Teniendo en cuenta los resultados obtenidos, se seleccionó el sistema A: ácido acético glacial: tetrahidrofurano: tolueno (3:9:90 v/v/v) como el de mayor resolución. En él se lograron manchas bien separadas, que no quedaron en el punto de aplicación, es decir, con un corrimiento adecuado expresado por los valores de Rf (Fig. 2) (A1 y A2), mientras que en el sistema de disolvente B: ácido acético glacial:acetonitrilo:2-propanol:n-hexano (5:50:100:845 v/v/v/v), las manchas no quedaron bien resueltas y se observaron colas. En el sistema C: cloroformo en presencia de vapores de amoníaco, las manchas no migraron del punto de aplicación, excepto para las condiciones de estrés por medio de la luz en las que tampoco existió una buena separación, pues se observó también la presencia de colas. ]]>
Sensibilidad del revelador
Para la evaluación de la sensibilidad se realizó la determinación del límite de detección (Ld), cuyos resultados se muestran en la figura 3 (A). Se detectaron todas las manchas desde 1 hasta 50 µg, por lo que se pudo establecer 1 µg como Ld.
Selectividad
Con respecto a la selectividad los resultados fueron positivos para el sistema seleccionado (sistema A). Se obtuvo una mancha principal de adecuada nitidez a un valor de Rf = 0,381 correspondiente al naproxeno en las aplicaciones 1 y 6 (patrones), las cuales aparecieron también en las restantes muestras sometidas a condiciones de degradación, y fueron mucho menos intensa en la muestra 10 que contenía naproxeno disuelto en etanol, sometido a reflujo por 16 h (Fig. 2) (A1). Este comportamiento sugiere la posible degradación en estas condiciones que se comprobó con el experimento complementario, lo cual avaló el comportamiento observado para la muestra 10. Sin embargo, los componentes del supositorio, solo incluyen al Rosupol. Esta grasa dura no sufrió degradación alguna detectable en las condiciones estudiadas. ]]>
Acompañando a la mancha principal, para los patrones se obtuvo una mancha secundaria de mayor Rf (Rf= 0,724) correspondiente a la sustancia relacionada. Esta mancha secundaria igualmente se presentó en todas las muestras con excepción de la 10 y se intensificó considerablemente en las muestras sometidas a medio ácido (Ver 4 y 8). En estas mismas muestras apareció adicionalmente una mancha en el punto de aplicación (Rf= 0), la cual pudiera relacionarse a posibles productos de degradación. En la muestra sometida a oxidación con H2O2 (Ver 9) se percibió igualmente esta mancha pero con una menor intensidad, mientras que en la expuesta a la luz (Ver 5), se observó similar comportamiento pero con menor nitidez. Estos resultados concordaron con lo reportado por otros autores.1De forma similar se presentaron manchas de diferente tonalidad atribuibles a la degradación del naproxeno presentes en valores de Rf= 0,592, en las muestras sometidas a pirólisis (2), medio ácido (4 y 8), medio alcalino (7) y muy tenuemente en la 10 (reflujo en medio alcohólico).
A pesar de que en estas condiciones se mostró la degradación del naproxeno debido a la aparición de manchas secundarias, fue la acción de la luz la que generó la mayor degradación. Este comportamiento se corresponde con las recomendaciones de la BP del 2009 para el manejo del IFA. En este caso fueron detectadas 5 manchas a los siguientes valores de Rf: 0; 0,079; 0,224; 0,381 y 0,724.
Todas las manchas fueron perfectamente separadas de los componentes de la formulación y del principio activo. Los excipientes oleosos apolares no interfirieron, ni apareció ningún producto de degradación de estos (Fig. 2). (A2).
Experimento complementario para selectividad del método por cromatografía en capa delgada
Los resultados de este estudio complementario se representan en la figura 4 y demostraron que ocurrió la reacción de formación de ésteres, entre el naproxeno y el monoestearato de glicerilo, en las nuevas condiciones. En la muestra 4 se observaron 2 manchas adicionales a valores de Rf de 0,274 y 0,414 respectivamente, las cuales fueron atribuidas a la formación de ésteres con los monoglicéridos (mancha de menor Rf) y con los diglicéridos (mancha de mayor Rf) del monoestearoto de glicerilo no autoemulsionable, catalizado por el calentamiento en la estufa. La muestra 3 que corresponde al monoestearato de glicerilo no autoemulsionable en cloroformo, no mostró mancha alguna, lo cual evidencia la participación del grupo -COOH libre del naproxeno en la formación de ésteres.
Como se observa, en el corrimiento correspondiente a la muestra 5 desaparecieron las manchas correspondientes a la formación del éster debido a la saponificación de los ésteres en presencia de KOH y etanol.
El conjunto de estos resultados confirma la formación de éster como posible producto de degradación a partir del -COOH libre del naproxeno y de los -OH del monoestearto de glicerilo. ]]>
Se evaluó la capacidad del método para diferenciar niveles de concentración equivalentes a 2,5; 5 y 10 % de degradación.
Según se aprecia en los resultados de la figura 3 (B), no fue posible establecer las diferencias en intensidad y coloración de las manchas, para el patrón de naproxeno y las muestras. No se apreciaron modificaciones en los corrimientos de los placebos cargados, lo cual corroboró la posibilidad de aplicación del método.
DISCUSIÓN
Desarrollo del método por cromatografía en capa delgada
La estabilidad se puede monitorear por la disminución del fármaco o por el aumento del producto de degradación en el tiempo. Esta última variante sólo es válida en el caso que la degradación sea conocida y rinda siempre el mismo producto. La degradación del naproxeno rinde más de un producto de degradación,3,4,6 por lo que se recomienda monitorear la disminución en el tiempo de su contenido. ]]>
El empleo de métodos semicuantitativos para estudios de estabilidad constituye una variante aceptada para llevar a cabo evaluaciones en la etapa de desarrollo del producto, fundamentalmente para estudios de estrés cuando no se tiene información en la bibliografía del comportamiento del producto desde el punto de vista de su estabilidad química. La información que de ellos se deriva, permite establecer los niveles de degradación que tienen lugar por comparación con patrones de concentración conocida en términos de rango. Uno de los métodos semicuantitativos de mayor aplicación es la CCD. Mediante esta técnica se logra establecer el rango de degradación por comparación del tamaño y la intensidad de las manchas obtenidas en la cromatoplaca. Además estos métodos sirven como técnicas complementarias para el seguimiento de la estabilidad en estudios definitivos, comparando sus resultados con los obtenidos por técnicas selectivas cuantitativas. En su defecto completan los métodos cuantitativos, como herramientas para la identificación de los posibles productos de degradación durante los estudios de estabilidad.Para poder desarrollar el método por CCD fue necesario en primer lugar, seleccionar las condiciones cromatográficas que garanticen una elevada resolución del sistema cromatográfico. Se escogió como soporte las placas de sílica gel GF 254 considerando las características estructurales del naproxeno, ya que este presenta grupos cromóforos en su estructura que se pueden detectar bajo la luz UV, por lo que este soporte fue el más apropiado. El revelado bajo luz UV ofrece como ventajas que es más sencillo y rápido, se evita la atomización de la cromatoplaca con un revelador químico, lo cual en muchas ocasiones retarda la operación y limita en cuanto a sensibilidad del método.
La selección del sistema de disolvente se llevó a cabo frente a patrón de principio activo (naproxeno); disoluciones de naproxeno en etanol sometidas a las diferentes condiciones degradativas explicadas anteriormente y de una mezcla de naproxeno con grasa dura (Rosupol) presente en la formulación, así como con glicerina y monoestearato de glicerilo al 10 y al 20 % también sometidos a condiciones de estrés. El objetivo de someter estas muestras a condiciones de estrés fue conocer los posibles productos de degradación tanto del naproxeno como de la grasa dura, que es el único excipiente que estará presente en la futura formulación y que pudiera afectar también la estabilidad y la calidad del supositorio.
Se utilizó la glicerina y el monoestearato de glicerilo (compuestos con -OH libres) para facilitar la ocurrencia de reacciones de esterificación entre el grupo carboxilo libre presente en el naproxeno y los grupos -OH. De esta forma, por analogía, estos -OH pudieran estar presentes eventualmente en la grasa dura, la cual es una mezcla de triglicéridos, diglicéridos y monoglicéridos. Es decir, la base del supositorio no es más que glicerina esterificada con ácidos grasos; los cuales pudieran provocar en presencia de calor, una transacetilación o lo que es lo mismo, la esterificación del grupo carboxilo del naproxeno.
Se utilizaron los 3 sistemas de disolventes mencionados con anterioridad con el objetivo de evaluar el comportamiento cromatográfico del analito y sus posibles productos de degradación.
Los métodos de la categoría II que se aplican como análisis cualitativo requieren solamente de la validación de 2 parámetros: selectividad y límite de detección.5
Selectividad
Los resultados obtenidos están en perfecta correspondencia con los obtenidos por varios autores.1,3
Trifonova y otros,1 en 1997, en su estudio corroboraron la mayor degradación de naproxeno en medio ácido, así como en muestras expuestas a la luz en presencia de oxígeno (fotoxidación). ]]>
Adhoum y otros,3 en el 2003, demostraron la afectación del naproxeno en condiciones de estrés como pirólisis, medio ácido y medio alcalino, y reportaron como uno de los principales productos de degradación al 2-metoxi-6-etil naftaleno, el cual por sus características estructurales, pudiera tener un corrimiento similar al observado.
Capacidad del método para diferenciar la intensidad de las manchas en correspondencia con la diferencia de concentración
La selección de estas cantidades se realizó teniendo en cuenta la necesidad de distinguir la intensidad en la coloración de las manchas, aspecto fundamental para que el método pueda ser usado con fines semicuantitativos. Generalmente se recomienda que las concentraciones sean al menos el doble respecto a la de referencia, para que por observación visual se perciba sin dificultad la diferencia entre ellas.
La aplicación de la CCD se limitó a la identificación de los posibles productos de degradación solo con fines cualitativos y no como prueba límite. Teniendo en cuenta el conjunto de resultados obtenidos en la validación, se puede afirmar que el método fue suficientemente sensible y selectivo para aplicarlo con el objetivo para el cual fue diseñado.
REFERENCIAS BIBLIOGRÁFICAS
1. Trifonova E, Vistel M, Lemus MZ, Nápoles R. Naproxeno tabletas. Un nuevo producto de la industria farmacéutica nacional. MEDISAN. 1997:1;31-6. ]]>
2. British Pharmacopoeia Volume I & II Monographs: Medicinal and Pharmaceutical Substances Naproxen. London: The Stationery Office; 2009. [Monographic in CD-ROM].
3. Adhoum N, Monser L, Toumi M, Boujlel K. Determination of naproxen in pharmaceuticals by differential pulse voltammetry at a platinum electrode. Anal Chim Acta. 2003:495;69-75.
4. Boscá F, Martínez-Máñez R, Miranda MA, Primo J, Soto J, Vaño L. Oxidative Decarboxylation of Naproxen. J Pharm Sci. 1992:81;479-82.
5. United States Pharmacopoeial Convention and National Formulary 25st. USP XXX. United States Pharmacopoeia Convention. Rockville: Staff Liaison; 2007. [Monographic in CD-ROM].
6. Monser L, Darghouth F. Simultaneous determination of naproxen and related compounds by HPLC using porous graphitic carbon column. J Pharm Biomed Anal. 2003:32;1087-92. ]]>
Recibido: 25 de mayo de 2011.
Aprobado: 30 de junio de 2011.
Dra. C. Yania Suárez Pérez. Instituto de Farmacia y Alimentos (IFAL). Universidad de La Habana. Ave 23 No. 21 425 e/ 214 y 222. La Coronela, La Lisa. La Habana, Cuba. Correo electrónico: yaniasp@ifal.uh.cu, yania_as@yahoo.es ]]>