
Validación de un método cromatográfico para la cuantificación de latanoprost 50 µg/mL en el colirio de producción nacional
Validation of a chromatographic method for quantitation of 50 µg/mL Latanoprost in a Cuban eye drops
MSc. Caridad Margarita García Peña, Téc. Vivian Martínez Espinosa, MSc. Ania González Cortezón
]]>
Centro de Investigación y Desarrollo de Medicamentos. La Habana, Cuba.
RESUMEN
Introducción: el latanoprost está indicado para el tratamiento de la presión intraocular elevada en pacientes con hipertensión ocular o glaucoma de ángulo abierto.
Objetivo: desarrollar y validar un método analítico por cromatografía líquida de alta resolución, aplicable al control de la calidad del latanoprost 50 µg/mL, colirio.
Métodos: para cuantificar el principio activo en el producto terminado, la separación se realizó a través de una columna cromatográfica Altima C-18 (10 µm) (250 × 4 mm), con detección ultravioleta a 205 nm, empleando una fase móvil compuesta por acetonitrilo-buffer fosfato pH 4,5 (650:350) y la cuantificación de este frente a una muestra de referencia con el método del estándar externo.
Resultados: los resultados de los parámetros evaluados en la validación del método se encontraron dentro de los límites establecidos.
Conclusiones: el método analítico desarrollado y validado por cromatografía líquida de alta resolución para el control de la calidad del colirio de latanoprost 50 µg/mL, resultó específico, lineal, exacto y preciso en el rango de concentraciones estudiadas, por lo que puede emplearse de manera confiable y segura. ]]>
ABSTRACT
Introduction: Latanoprost is indicated to treat high intraocular pressure in patients suffering from ocular hypertension or from open angle glaucoma.
Objective: to develop and to validate a high performance liquid chromatography-based analytical method for quality control of 50 µg/mL Latanoprost eye drops.
Methods: to quantify the active principle of the final product, the separation was performed through Altima C-18 chromatographic column (10 µm) (250 × 4 mm), with ultraviolet detection at 205 nm, and a mobile phase made up of acetonitryle-phosphate buffer of pH= 4.5 (650:350). The quantification of the principle against a reference sample was carried out with the external standard method.
Results: the results of the evaluated parameters in the validation of the method were found to be within the set limits.
Conclusions: the developed and validated high performance liquid chromatography-based analytical method for the quality control of 50 µg/mL Latanoprost eye drops proved to be specific, linear, exact and precise within the range of the studied concentrations; therefore, it may be safely and reliably used.
Key words: latanoprost, high performance liquid chromatography, eye drops, quality control.
]]>
INTRODUCCIÓN
El latanoprost está indicado para el tratamiento de la presión intraocular elevada, por un incremento del flujo de humor acuoso, en pacientes con hipertensión ocular o glaucoma de ángulo abierto. Su nombre químico es: Acido [1R-[1a (Z), 2b (R*), 3a, 5a]]-7-[3,5 dihidroxi-2-(3-hidroxi-5-fenilpentil) ciclopentil]-5-heptenoico-1-metil ester. Su peso molecular es 432,58, con una fórmula global de C26H40O5.
No existen métodos informados en la literatura para la cuantificación del latanoprost en el colirio, por lo que el objetivo de este trabajo es desarrollar y validar un método de análisis para realizar el control de la calidad del producto terminado de producción nacional. Siempre que se realiza el desarrollo de un método analítico se debe realizar el estudio de validación a fin de obtener pruebas documentales de que el método propuesto es confiable y seguro.1,2 Estos incluyen los métodos destinados a cuantificar el fármaco en el colirio recién elaborado, es decir, al control de calidad. Dichos estudios son de vital importancia y deben realizarse según las exigencias actuales.
MÉTODOS
La sustancia de referencia química de Latanoprost se suministró por el grupo de sustancias de referencia del Centro de Investigación y Desarrollo de Medicamentos (CIDEM, La Habana, Cuba), la cual se analizó por el método cromatográfico establecido para realizar el control de la calidad de la materia prima, con una pureza de 99,8 %. El producto terminado en forma de colirio, se elaboró en la Empresa Farmacéutica "Julio Trigo", identificado como el lote 9001, fabricado en marzo de 2009, el cual cumplió con las especificaciones de calidad establecidas para el control de la calidad de los colirios.
Todos los reactivos utilizados fueron de calidad analítica. En el ensayo se empleó un cromatógrafo (KNAUER) con detector UV variable Kanuer acoplado a una computadora para la adquisición de los cromatogramas mediante el software CHROMGATE (versión 3.1) ajustado a 205 nm, un inyector con un rulo de 200 µL. La separación se realizó isocráticamente para lo que se empleó una columna Altima C-18 (10 µm) (250 × 4 mm) y un flujo de 1,0 mL/min. La fase móvil consistió en una mezcla desgasificada de acetonitrilo-solución amortiguadora fosfato pH 4,5 (650:350). Como diluente se empleó una mezcla de acetonitrilo:agua en una proporción de 70:30.
Preparación de la muestra: se tomaron 2 mL de muestra, se trasvasó a volumétrico de 10 mL adicionándose diluente, se aplicó ultrasonido por 3 min y se completó volumen con diluente. ]]>
Preparación de la sustancia de referencia química: se pesaron 10 mg de sustancia de referencia química de latanoprost y se trasvasó a un volumétrico de 100 mL adicionándose acetonitrilo, se aplicó ultrasonido por 5 min y se completó volumen con acetinitrilo. Se tomó una alícuota de 1 mL y se trasvasó a un volumétrico de 10 mL adicionándose diluente y se completó volumen con diluente.
Validación del método analítico
La validación fue realizada según la Regulación 41-2007 del Centro Estatal para el Control de los Medicamentos (CECMED) y la Farmacopea de los Estados Unidos (USP 32); se evaluaron los parámetros que a continuación se describen:1,2
Linealidad: se realizaron los modelos de tres determinaciones para cinco concentraciones diferentes: 60, 80, 100,120, y 140 % del principio activo a cuantificar. Se determinó la ecuación de la recta, el coeficiente de correlación, la prueba de significación estadística de la pendiente Sb rel (%) y el coeficiente de variación de los factores de respuesta.
Exactitud: se realizaron los modelos de tres réplicas para tres concentraciones diferentes: 80, 100, 120 %; se determinó el % de recuperación, la desviación estándar y el coeficiente de variación. Se determinó además la prueba de Cochram con vistas a comprobar si la variación de la concentración produce diferencias significativas en los resultados y la prueba de la t de Student para la determinación de las diferencias significativas entre la recuperación media y el 100 %.
Precisión: se sugieren los modelos de repetibilidad seis réplicas. Con ellas se determinaron los valores medios, la desviación estándar y el coeficiente de variación.
De igual manera para el ensayo de la precisión intermedia se utilizaron dos analistas y dos días diferentes. Se aplicaron las pruebas de Fisher y de la t de Student para determinar si existían diferencias significativas entre los resultados al variar las condiciones de análisis.
Especificidad: se analizaron la sustancia de referencia de Latanoprost, el placebo y las muestras de producto terminado. ]]>
Criterio de aceptación: no debe obtenerse señales del placebo en la zona de elusión del principio activo. Las áreas bajo las curvas del patrón y del Latanoprost en el producto terminado deben ser similares.
RESULTADOS
La figura muestra los resultados obtenidos en el estudio de especificidad del método. Como se observa en el cromatograma correspondiente a la muestra placebo, no se obtuvo ninguna señal en la zona de interés (5,0-8,5 min), al ser comparado con la señal obtenida para las soluciones estándar de referencias y de la muestra de colirio, lo cual indica que los excipientes o sustancias auxiliares de la solución no interfieren en la determinación del principio activo.
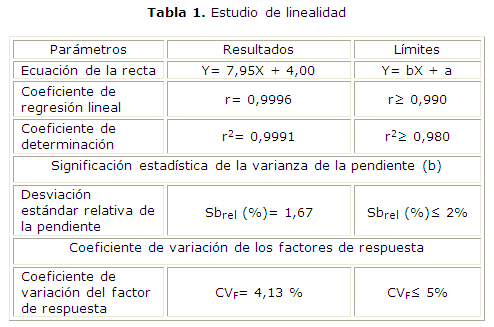
En la tabla 1 se reportan los resultados del estudio de la linealidad del sistema; el coeficiente de regresión lineal fue de 0,9996 y el coeficiente de variación de los factores de respuesta resultaron igual a 4,13.
El resultado del estudio de precisión del método desarrollado se presenta en el cuadro y la tabla 2. En el estudio de repetibilidad, la media obtenida fue de 99,7 % y el coeficiente de variación fue de 0,43 %, mientras que los valores de F y t calculadas resultaron menores que los valores tabulados para cada uno de los niveles estudiados; los valores tabulados para la prueba de Fischer fueron por analistas 1,00 y por días 2,51; mientras que para la prueba de la t de Student fueron por analistas 1,39 y por días 0,82 para un 95 % de confianza.
En la tabla 3 aparecen informados los resultados del estudio de exactitud. La recuperación media fue de 100,04 % y el valor de t calculada (1,740) y de G calculada (0,385) resultaron menores que los valores tabulados, t tabulada 2,306 para un 95 % de confianza y G tabulada 0,797 para un 95 % de confianza, k= 3 y n= 3. ]]>
DISCUSIÓN ]]>
Los resultados del estudio de especificidad del método (Fig.), demuestran la especificidad del método al no presentarse interferencias de picos adicionales en la determinación del principio activo, no se evidencian interferencias de los excipientes,3,4 por lo que puede aplicarse en el control de la calidad del producto terminado.Los resultados de los estudios de linealidad muestran coeficiente de regresión y de determinación superiores a los exigidos, 0,99 y 0,98, lo que demuestra con el valor del coeficiente de correlación obtenido, cercano a la unidad, la existencia de correlación con una probabilidad elevada, así como el grado de relación entre las variables concentración y respuesta detectada por el equipo empleado. También el coeficiente de variación de los factores de respuesta y la desviación estándar relativa de la pendiente fueron inferiores al normado como máximo para estos indicadores: 5 y 2 %; ambos son considerados estimadores puntuales que permiten caracterizar la variabilidad. El valor obtenido de los coeficientes de variación de los factores de respuesta, permite demostrar que existe variabilidad en la relación respuesta y concentración para cada nivel evaluado. El intervalo de confianza del intercepto incluye al cero, lo que permite excluir la significación del error del intercepto. Se demuestra con los resultados la linealidad del método propuesto.
En los estudios de la repetibilidad (cuadro) realizado a una misma muestra, por el mismo analista, el mismo día, a través de 6 réplicas, se alcanzó un coeficiente de variación adecuado, lo que demuestra la buena precisión del método; se observa una variabilidad de los resultados dentro de los límites establecidos para los métodos cromatográficos: CV £ 2,0 %.1,2
Los valores que se obtienen en los estudios de precisión intermedia, de las pruebas de Fischer y t de Student, para el estudio de la precisión intermedia demuestran que no existen diferencias significativas entre las precisiones alcanzadas por los analistas en diferentes días para un 95 % de confianza, ya que el valor de F calculado fue menor que la F tabulada, estos resultados permiten establecer que las precisiones son similares (tabla 2). Al realizar las pruebas de la t de Student, el valor calculado resultó menor que el tabulado, para un 95 % de confianza, lo cual demuestra que no existen diferencias significativas entre las medias alcanzadas, con un nivel de significación de un 5 %.
El valor de porcentaje de recobro estuvo dentro de los límites establecidos para los métodos cromatográficos (98-102 %) y el valor del coeficiente de variación para cada uno de los niveles de concentración estudiados resultó ser menor que el 2 %. En la influencia del factor concentración sobre la variabilidad de los resultados de la exactitud al aplicar la prueba de Cochran, se obtuvo que la G calculada fuer menor que la G tabulada para un 95 % de confianza, k= 3 y n= 3; por lo tanto, las varianzas de las concentraciones empleadas son equivalentes, lo que indica que la concentración no influye en la variabilidad de estos. Al realizar la prueba de significación entre la recuperación media y el 100,0 % de recuperación, el coeficiente de variación fue adecuado, el valor de t calculada resultó menor que la t tabulada. En el rango seleccionado en el estudio de exactitud, los valores de porcentaje de recobro están dentro de los límites establecidos para los métodos cromatográficos (98-102 %) y los valores del coeficiente de variación, para cada uno de los niveles de concentración estudiados, fueron menores que el 2 %.1,2
El método analítico desarrollado y validado por CLAR para el control de la calidad del colirio de latanoprost 50 µg/mL, resultó específico, lineal, exacto y preciso en el rango de concentraciones estudiadas, por lo que puede emplearse de manera confiable y segura.
REFERENCIAS BIBLIOGRÁFICAS
1. Regulación 41/07. Validación de métodos analíticos. Centro Estatal para el Control de Medicamentos (CECMED). La Habana, 2007. Disponible en http://www.cecmed.sld.cu/Pages/Reg_EvalEL.htm
2. The Unites Satated Pharmacopeial, USP 32. 30 ed. Rockville: Mack Printing; 2009. [Versión electrónica].
3. Quattrocchi OA, Laba RF. Introducción al HPLC en aplicación y práctica. Buenos Aires: Ed. Artes Gráficas Farro SA; 1992. p. 106-22; 284; 302-28.
4. Dierksneier G. Métodos cromatográficos. La Habana. Ed. Científico-Técnica; 2005. p. 1-4; 256-12.
Recibido: 3 de abril de 2012. ]]> Aprobado: 24 de junio de 2012.
Caridad Margarita García Peña. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave. 26 No. 1605 entre Boyeros y Puentes Grandes. CP 10600. Plaza de la Revolución, La Habana, Cuba. Correo electrónico: caridadgp@infomed.sld.cu ]]>