 ]]>
]]>
Estabilidad de una formulación cubana de albendazol tabletas
Stability study of a Cuban formulation of Albendazole tablets
Dr. Cs. Jorge Enrique Rodríguez Chanfrau, MSc. Iverlys Díaz Polanco, Téc. José. Manuel Gil Apan, Viviana Fuste Moreno
]]>
Centro de Investigación y Desarrollo de Medicamentos (CIDEM). La Habana, Cuba.
RESUMEN
Introducción: el albendazol es un medicamento cuya acción farmacológica lo define como un antihelmíntico de amplio espectro. Como parte del proceso de desarrollo de la industria farmacéutica cubana, se ha investigado e introducido una tecnología para la producción de tabletas de 200 mg de albendazol.
Objetivo: evaluar la estabilidad química y microbiológica del medicamento.
Métodos: tres lotes de 5 kg cada uno fueron preparados acorde con el proceso tecnológico desarrollado previamente. Los lotes elaborados se dividieron a la mitad; una parte se envasó en frascos plásticos de polietileno de alta densidad (formato No. 8), con tetina, tapa de rosca y sello de inviolabilidad por 10 tabletas, y la otra parte, en sobres termoconformados de PVC y aluminio por 10 tabletas. Estudios de estabilidad acelerada y de vida de estante se realizaron, aplicándose un método de análisis por cromatografía líquida de alta resolución descrito en la farmacopea americana, al cual previamente se le evaluó su especificidad. Las muestras se colectaron a tiempo 0, 1, 2, 3 y 6 meses para el estudio de estabilidad acelerado y a tiempo 0, 6, 12, 18 y 24 meses para la estabilidad por vida de estante.
Resultados: se comprobó que los lotes al inicio cumplieron con los parámetros de calidad establecidos para el producto según la técnica de análisis. Los estudios de estabilidad acelerada a la temperatura de 40 ºC, del comportamiento del producto frente a la luz y del comportamiento frente a la humedad mostraron que el medicamento no sufrió variaciones apreciables en estas condiciones.
Conclusiones: los estudios de estabilidad realizados demostraron que la tecnología cubana desarrollada para la elaboración de tabletas de albendazol es idónea, lo que garantiza que el medicamento mantenga sus parámetros de calidad química y microbiológica durante 24 meses. ]]>
ABSTRACT
Introduction: Albendazole is a medication whose pharmacological action defines it as wide-spectrum anti-helminthic. As part of the process of the Cuban pharmaceutical industry development, a new technology for the production of 200 mg Albendazole tablets was researched and implemented.
Objective: to evaluate the chemical and microbiological stability of the drug.
Methods: three batches of 5 kg each were prepared according to the previously developed technological process. They were divided into two parts. One half was packed in high density plastic polyethylene reservoirs (format number 8) containing 10 tablets, with threaded cap and tamper-proof seal, whereas the other half was placed in 10-tablet thermoformed PVC and aluminum packets. Chemical stability and shelf-life studies were conducted on the basis of the high performance liquid chromatography method described in the US Pharmacopea, the specificity of which was previously determined. The samples were collected at 0, 1, 2, 3 and 6 months for the accelerated stability study whereas they were gathered at 0, 6, 12, 18 and 24 months for the shelf-life stability study.
Results: it was confirmed that the batches met at the beginning the set quality parameters for the product as per the analysis technique. The studies of accelerated stability at 40° and of the product's behavior on light and on humidity showed that Albendazole did not suffer sizeable variations under these conditions.
Conclusions: the stability studies proved that the technology developed in Cuba for Albendazole tablet manufacture is optimal, which assures the chemical and microbiological quality of the drug for 24 months.
Key words: albendazole, stability, tablets, high performance liquid chromatography.
]]>
INTRODUCCIÓN
El albendazol es un medicamento cuya acción farmacológica lo define como un antihelmíntico, de amplio espectro, con efecto adulticida, hervicida y ovicida, sobre nemátodos gastrointestinales (Haemonchus, Ostertagias, Trichostrongylus, Nematodirus, Cooperia, Bonustomun, Strongyloides, Anpillaria, Chavertias, Neoascaris vitailorum, Teuchuris y Oesophagostomum), nemátodos pulmonares (Dictyocaulus viviparus) y céstodos (Fasciola hepática). Los enfermos de sida, deben combatir la criptosporidiosis producida por un protozoo del género Eimeria, el cual se encuentra asociado generalmente a esta enfermedad y para lo cual este medicamento es eficiente.1-3
Como parte del proceso de desarrollo de la Industria Farmacéutica cubana, se ha investigado e introducido una tecnología para la producción de tabletas de 200 mg de albendazol. El objetivo de este trabajo fue evaluar la estabilidad química y microbiológica del medicamento envasado en frascos plásticos y en sobres termoconformados, con vistas a definir su fecha de vencimiento y las condiciones de almacenamiento.
MÉTODOS
Se elaboraron tres lotes a escala piloto según la tecnología desarrollada en la UCTB Tecnologías Básicas del Centro de Investigaciones y Desarrollo de Medicamentos (CIDEM). Se empleó como materia prima activa albendazol, suministrada por la firma SIGMA, la cual cumplía con los parámetros de calidad establecidos en la USP.4
Los lotes elaborados fueron divididos a la mitad y una parte fue envasada en frascos plásticos de polietileno de alta densidad (formato No. 8), con tetina, tapa de rosca y sello de inviolabilidad por 10 tabletas (identificados como lotes 04001F, 04002F y 04003F) y la otra parte en sobres termoconformados de PVC y aluminio por 10 tabletas (identificados como lotes 04001B, 04002B y 04003B).
Para la evaluación de la materia prima activa se empleó el método de análisis descrito en la USP,4 con relación a los parámetros de descripción, disolución y valoración del principio activo, utilizándose un equipo HPLC (KNAUER) con detector UV y columna Lichrospher® 100, RP 18 (25 cm de longitud y 4 mm de diámetro y 5 µ). El flujo de la fase móvil fue de 1 mL/min y el volumen de inyección fue de 10 µL. ]]>
Previamente se realizó un análisis de la especificidad del método de valoración descrito en la USP para este producto. Para ello se degradó materia prima y tabletas a las siguientes condiciones de trabajo:a) 70 ºC durante 72 h.
b) Medio básico (NaOH 1 mol/L) y 70 ºC durante 72 h.
c) Medio ácido (HCl 1 mol/L) y 70 ºC durante 72 h.
d) Medio oxidante (peróxido de hidrógeno al 30 %) por 24 h.
Al finalizar se evaluaron las muestras aplicando el método descrito, y se determinó la presencia o no de productos de degradación en las condiciones de trabajo establecidas.
Se realizaron los estudios de estabilidad acelerada para valorar el comportamiento del producto frente a condiciones de temperatura, de humedad y la luz natural. Para ello se tomaron muestras correspondientes a los tres lotes, en cada uno de los envases estudiados y se colocaron a temperatura de 40 ºC durante 180 días; se realizaron mediciones al inicio, 1, 2, 3 y 6 meses. Igualmente se colocaron muestras en condiciones de humedad a 84, 92 y 98 % de HR y a la luz natural en frascos transparentes durante 180 días, y en todos los casos se realizaron determinaciones al inicio y al finalizar el estudio. Paralelamente se valoró el comportamiento de las características organolépticas;5 y también se realizaron estudios para conocer el comportamiento microbiológico de las muestras, y se realizaron determinaciones al inicio, 12 y 24 meses, según lo descrito en la USP.4
Para el estudio de estabilidad por vida de estante las muestras almacenadas a la temperatura de 30 ± 2 ºC y 70 % de HR, fueron valoradas al inicio, a los 6, 12, 18 y 24 meses de fabricados los lotes.5
]]>
RESULTADOSEl cromatograma de las muestras de principio activo y tabletas sin degradar presentan un pico a un tiempo de retención de 11 min, mientras que el cromatograma de la muestra placebo no presenta ningún pico en las condiciones de trabajo establecidas.
El estudio de degradación para comprobar la especificidad del método empleado, mostró que para el caso del tratamiento en medio oxidante, se observa en el cromatograma de las tabletas un pico a un tiempo retención de 3,1 min, que coincide con un pico que aparece a igual tiempo en la muestra placebo tratada en igualdad de condiciones. En el caso de la muestra de principio activo no se observa la aparición de este pico (Fig.).
Por otro lado, al evaluar los resultados del tratamiento en medio básico y 70 ºC durante 72 h, se observó la aparición de un pico de degradación a un tiempo de retención de 8,5 min, el cual también es observado en el principio activo tratado en igualdad de condiciones (Fig.), pero que no se observa en el cromatograma de la muestra placebo.
En ambos casos los picos fueron separados del pico correspondiente al principio activo (tr= 11 min) en las condiciones de trabajo propuesta.
En el caso de los otros tratamientos realizados (70 ºC durante 72 h y medio ácido (HCl 1 mol/L) y 70 ºC durante 72 h) no hubo aparición de ningún pico en los cromatogramas correspondientes; solo se observó en el cromatograma del principio activo y de las tabletas el pico correspondiente al albendazol, el cual aparece a un tiempo de retención de 11 min.
Los resultados del análisis inicial de los lotes demostraron que estos cumplen con los parámetros de calidad establecidos para el producto según la técnica de análisis.4
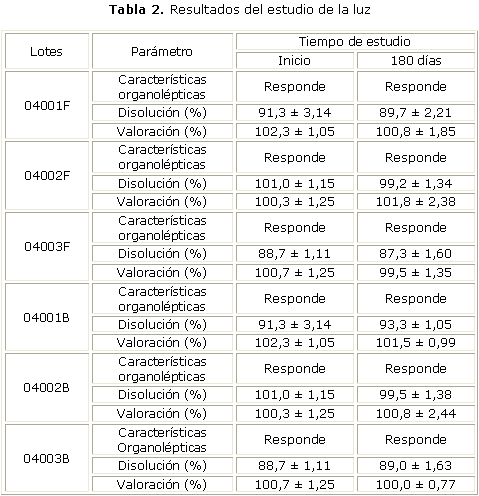
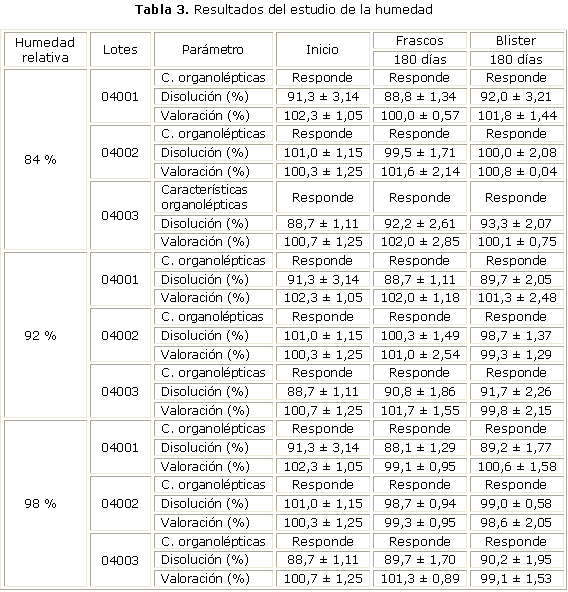
Los estudios de estabilidad acelerada a la temperatura de 40 ºC (tabla 1), del comportamiento del producto frente a la luz (tabla 2) y del comportamiento frente a la humedad (tabla 3), mostraron que el medicamento no sufre variaciones apreciables en estas condiciones.
Los resultados del estudio de estabilidad por vida de estante se presentan en la tabla 4, los que demostraron que el medicamento mantiene sus parámetros de calidad durante 24 meses.
DISCUSIÓN
Los resultados de los estudios de especificidad del método de análisis comprueban que en el medio básico el principio activo sufre degradación, con la aparición de un pico a un tiempo de retención diferente al pico del principio activo, los cuales son separados sin dificultad por el método de análisis propuesto.
En el caso de las muestras tratadas en un medio oxidante se observa la aparición de un pico de degradación, el cual puede ser provocado por la degradación de algunos de los componentes de la formulación, pues este solamente aparece en las muestras placebo y en la muestra tableta, pero no se observa en la muestra de principio activo.
En todos los casos los picos de degradación son separados del pico correspondiente al principio activo, por lo que se puede afirmar que el método de análisis es específico para la determinación del principio activo y sus productos de degradación, el cual puede ser empleado para realizar los estudios de estabilidad.6
Se confirma que la formulación es estable en condiciones extremas de humedad, luz y calor, así como en condiciones de vida de estante (30 ± 2 ºC y 70 % HR). En esta última mostró que a los 24 meses de elaborada cumplía con los parámetros de calidad establecidos por la farmacopea americana, en ambos envases estudiados.4
Los estudios microbianos realizados en el tiempo, también demostraron que el medicamento estudiado cumple con los requisitos de calidad microbiológica.4
Por todo lo anterior, se puede concluir que la tecnología cubana desarrollada para la elaboración de tabletas de albendazol es idónea, lo que garantiza que el medicamento mantenga sus parámetros de calidad química y microbiológica durante 24 meses, envasados en frascos plásticos de polietileno de alta densidad (formato No. 8), con tetina, tapa de rosca y sello de inviolabilidad por 10 tabletas y sobres termoconformados de PVC y aluminio por 10 tabletas. ]]>
REFERENCIAS BIBLIOGRÁFICAS
1. Popa G. Clinical study of the efficacy of albendazole treatment in human hydatidosis. Chirurgia. 1997;92(5):331-5.
2. Labanchi J, Herrero E, Cantoni G, Pérez A, Odruzola M. Ultrasorographic diagnosis and medical treatment of human cystic echinococcosis in asymptomatic school age carrier: 5 years of follow-up. Acta Trop. 2004;91(1):5-13.
3. Paral J, Plodr M, Ferko A, Zvak J. Echinococcal cysts in liver and lungs. Rozhl Chir. 2003;82(7):349-52.
4. United States Pharmacopeia USP 32. National Formulary 27. Rockville: Marck Printing; (2009). p. 1436.
5. Regulación No 23. Requerimientos de los estudios de estabilidad para el registro de nuevos ingredientes farmacéuticos activos. Centro Estatal para el Control de Medicamentos (CECMED). La Habana, 2000.
6. Regulación No. 41/07. Validación de métodos analíticos. Centro Estatal para el Control de Medicamentos (CECMED). La Habana, 2007. Disponible en: http://www.cecmed.sld.cu/Pages/Reg_EvalEL.htm
Recibido: 10 de abril de 2012.
Aprobado: 25 de mayo de 2012.
Jorge Enrique Rodríguez Chanfrau. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave. 26 No. 1605 entre Boyeros y Puentes Grandes. CP 10600. Plaza de la Revolución, La Habana, Cuba. Correo electrónico: jorge.rodriguez@infomed.sld.cu ]]>