Efecto sobre la viabilidad celular de una nueva serie de espirosteroides sintéticos en células PC12
Effect of a new series of synthetic spiroteroids on the PC12 cell line viability
Lic. Laura García-Pupo; MSc. Yanier Nuñez Figueredo; DrC. Juan Enrique Tacoronte Morales; DrC. René Delgado Hernández
Centro de Investigacion y Desarrollo de Medicamentos. La Habana, Cuba. ]]>
RESUMEN
Introducción: la diosgenina y sus derivados se han descrito como potentes inhibidores de la proliferación en varias líneas tumorales. Sin embargo otras moléculas relacionadas estructuralmente con dichos derivados, se han reportado como candidatos terapéuticos y otras de ellas se incluyen en alimentos de consumo humano.
Objetivo: el presente trabajo evalúa el efecto sobre la viabilidad celular de una nueva serie de espiroesteroides sintéticos derivados de la diosgenina, en células tipo neurales PC12.
Métodos: la viabilidad de los cultivos de PC12 se determinó mediante el ensayo de MTT y se calcularon descriptores moleculares teóricos como la lipofilicidad (logP virtual) y la superficie de área polar (SAP), con el objetivo de establecer relaciones estructura-actividad.
Resultados: nuestros resultados demuestran que solo el acido taurodesoxicólico disminuye de manera significativa la viabilidad celular. Más aun, dicha molécula presenta valores menores y mayores de logP virtual y SAP, respectivamente, respecto al resto de los esteroides de la serie.
Conclusiones: los resultados anteriores avalan el estudio del acido taurodesoxicólico como potencial inhibidor de la proliferación celular y al resto de las moléculas de la serie como candidatos neuroprotectores a evaluar en esta misma línea celular y dosis de tratamiento.
Palabras clave: espirosteroides, citotoxicidad, acido taurodesoxicólico, relación estructura-actividad.
Introduction: diosgenin and its derivatives have been described as potent anti-proliferative compounds in several tumor cell lines. However, other structurally-related compounds are reported to exert neuroprotective activity and are also included in food for human consumption.
Objective: to evaluate the effect of a novel series of diogesin-derived synthetic spirosteroids on cellular viability of neuron-like PC12 cell line.
Methods: cellular viability was determined by the MTT assay along with some theorical molecular descriptors, such as lipophilicity and polar surface area, in order to establish the structure-activity relationships.
Results: the results demonstrated that only taurodeoxycholic acid significantly decrease PC12 cell culture viability. Moreover, this molecule presents lower virtual logP values and higher polar surface area values than the rest of spirosteroid series.
Conclusions: those results endorse future studies of taurodeoxycholic acid as a potential anti-tumor candidate and of the rest of the molecules in this series as potential neuroprotective agents to be evaluated in this PC12 cell line and similar therapeutic dose.
Keywords: spirosteroids, cytotoxicity, taurodeoxycholic acid, structure-activity relationship.
]]>
INTRODUCCIÓN
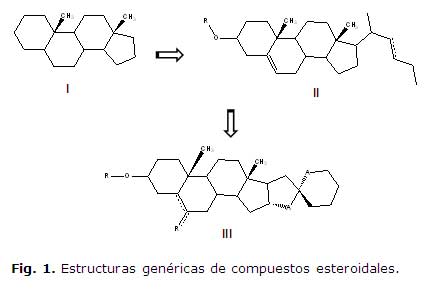
El núcleo ciclopentanoperhidrofenantreno (fig. 1, I) constituye la base de las moléculas esteroidales, las cuales durante su evolución química han derivado en esteroles (fig. 1, II) de amplia distribución en los reinos animal y vegetal. Dichos esteroles continuaron el curso quimioevolutivo hasta convertirse en compuestos esteroidales policíclicos y polisustituidos con una gran variedad de actividades biológicas1 (fig.1, III).La diosgenina constituye una sapogenina esteroidal de origen natural (fig. 1, III), presente en una amplia variedad de especies vegetales.2 En cuanto a su actividad biológica, existen numerosos resultados que demuestran su efecto inhibidor de la proliferación e inductor de la apoptosis, en varias líneas tumorales de colon humano,3 osteosarcoma,4 leucemia,5 eritroleucemia,6 mama7 y hepáticas.8 Sin embargo, la diosgenina se incluye actualmente en alimentos enriquecidos en fitosteroles para consumo humano, ya que se ha demostrado su efecto estimulador de la secreción biliar de colesterol y por tanto su utilidad en el mantenimiento de los niveles de colesterol.9; 10
Por otro lado, a partir de ésta molécula natural se han diseñado y sintetizado numerosos derivados que presentan efectos citotóxicos y antitumorales.11 No obstante, otros fitoesteroles derivados de la dehidroepiandosterona, y relacionados estructuralmente, tienen efectos neuroprotectores sobre células de feocromocitoma de rata (PC12) sometidas a privación de glucosa y oxígeno.12 El presente trabajo investigó el efecto de una nueva serie de espiroesteroides derivados de la diosgenina, sobre la viabilidad de células PC12 y las relaciones estructura-actividad preliminares entre ellos, así como estableció una concentración no citotóxica a la cual dichas moléculas puedan ser candidatos neuroprotectores.
MÉTODOS
Para dar cumplimiento al objetivo trazado, las células PC12 se cultivaron rutinariamente en medio de crecimiento RPMI-1640 suplementado con 10 % de suero equino inactivado por calor y 5 % de suero fetal bovino, según se describe en la literatura.13 Al inicio de los experimentos, se realizó la siembra celular en placas de 96 pocillos recubiertas con Poli-D-lisina, a una densidad de 150,000 células/mL y se mantuvieron durante 24h en atmósfera de 37°C y 5 % de CO2. Posteriormente se aplicaron los esteroides a su respectivo grupo de tratamiento a 10 µM de concentración, disueltos en dimetilsulfóxido (DMSO) 0.01 %, y se incubaron nuevamente las células durante 24 horas en iguales condiciones atmosféricas. Se seleccionó la concentración de 10µM para cada esteroide, debido a que la mayoría de los esteroles ejercen su actividad anti-inflamatoria y neuroprotectora in vitro por debajo de esta concentración9; 11; 12. Transcurrido dicho intervalo de tiempo, se realizó la medición de viabilidad celular mediante el ensayo del bromuro de 3-(4,5- dimetiltiazol-2-ilo)-2,5-difeniltetrazol (MTT), el cual se basa en la degradación mitocondrial de dicho compuesto por las células vivas y la formación de cristales de formazán como producto, que pueden ser cuantificados espectrofotométricamente a una longitud de onda de 540nm. Las células PC12 se trataron con 0.5mg/mL de MTT durante 4h, luego los cristales de formazán se disolvieron con una mezcla de dodecilsulfato de sodio 3 % en isopropanol/HCl y se midió la absorbancia a 540nm.14
RESULTADOS ]]>
Como se puede observar en la fig.1, dentro de la serie sintética de 18 esteroides y derivados espirostánicos, solo el acido taurodesoxicólico (YT2-020) afectó significativamente la viabilidad de las células PC12, respecto a aquellos cultivos celulares que no fueron sometidos a tratamientos (fig. 2). El resultado anterior motivó la búsqueda de características estructurales propias de dicha molécula, que pudieran ser las responsables de su efecto citotóxico distintivo. El ácido taurodesoxicólico presenta un grupo polar en posición 21 del núcleo ciclopentanoperhidrofenantreno, constituido por un grupo sulfónico y átomos de oxigeno y nitrógeno (fig. 3), el cual no está presente en ninguna otra molécula de la serie sintética. Con el objetivo de evaluar si este gran grupo polar en el acido taurodesoxicólico influía en su efecto citotóxico, mediante mecanismos que afectaran la estabilidad y el empaquetamiento de la membrana citoplasmática, se estimaron parámetros moleculares teóricos relacionados a la difusión a través de membranas lipídicas.
Las células se sembraron en placas de 96 pocillos a una densidad de 150,000 células/mL y se incubaron durante. Posteriormente se aplicaron los espirosteroides a su respectivo grupo de tratamiento a una concentración de 10 µM disueltos en dimetilsulfóxido (DMSO) 0.01%, y se incubaron por otras 24 horas. Se incluyó un grupo de células control que no recibieron tratamientos. Finalmente se determinó la viabilidad celular mediante el ensayo con MTT. Los resultados se muestran como porcientos de viabilidad celular respecto al control no tratado. **p<0.0005 ANOVA, Dunnet´s Test GraphPad Prism 5.
]]>
Primeramente se estimaron los valores teóricos de lipofilicidad (logPv), mediante el paquete ChemOffice v8.0 y la obtención de estructuras 3D empleando algoritmos MOPAC. Todos los esteroides, excepto el YT2-003, que no afectaron de manera significativa la viabilidad de las células PC12 e indujeron valores significativamente mayores respecto al acido taurodesoxicólico (Fig.1), presentan valores de logPv entre 3-5 (tabla 1), los cuales son mayores que el valor para el acido taurodesoxicólico (2.7254). Sin embargo, el esteroide YT2-003, que no se mostró citotóxico, presentó un logPv de 2.9546, el cual es muy similar al observado para el acido taurodesoxicólico (tabla 1). Esto puede deberse a limitaciones propias en el cálculo de dicho parámetro, como por ejemplo la desestimación del solvente y el pH de disolución real en que se encuentran las moléculas.Posteriormente y con el objetivo de establecer una correlación más fina entre los efectos sobre la viabilidad celular y los parámetros moleculares, se realizó el calculo de la superficie de área polar (SAP), mediante el paquete SurfArea v1.1. Dicho descriptor molecular se ha demostrado como uno de los más fieles en el establecimiento de predicciones para el transporte y absorción de fármacos orales en humanos15. En este sentido, los valores de SAP para los esteroides no significativamente citotóxicos, excepto la molécula YT2-003, oscilaron entre 2.5 y 14 %, mientras que el acido taurodesoxicólico mostró un valor notablemente mayor (21.9 %) (tabla 1).
DISCUSIÓN
Nuestros resultados demuestran que ninguno de los espiroesteroides estudiados disminuye significativamente la viabilidad de las células PC12, en las condiciones experimentales empleadas. En este sentido, otros espiroesteroides obtenidos recientemente por vía sintética ejercen su actividad neuroprotectora12 y promotora de la diferenciación neuronal16 in vitro en concentraciones y condiciones experimentales similares a las aplicadas en nuestro estudio. Sin embargo, no puede afirmarse que nuestros espiroesteroides carecen de potencial citotóxico, ya que la concentración de tratamiento empleada (10µM) se encuentra por debajo de la concentración inhibitoria media determinada para la actividad citotóxica de moléculas esteroidales y espirostanicas similares.17 18 19
Por otro lado, solo el acido taurodesoxicólico disminuye de manera significativa la viabilidad celular. Más aun, dicha molécula presenta valores menores y mayores de logP virtual y SAP, respectivamente, respecto al resto de los esteroides de la serie. Contrariamente, la similitud entre los valores de SAP del esteroide YT2-003 y el acido taurodesoxicólico (tabla 1), y las diferencias en cuanto a sus efectos en la viabilidad celular podrían deberse a sus diferentes distribuciones espaciales de los átomos y grupos electronegativos, donde el YT2-003 presenta dichos átomos electronegativos dispersos mas homogéneamente respecto al acido taurodesoxicólico, el cual sí presenta una gran cabeza polar definida. En relación a esto, se ha demostrado que los ácidos biliares y dentro de ellos el acido taurodesoxicólico, provocan muerte celular necrótica en células T de leucemia humana.20 En el caso del desoxicolato, el cual presenta una cabeza polar de menor tamaño respecto a la del acido taurodesoxicólico, se ha postulado recientemente un modelo de interacción con la bicapa lipídica en presencia de indometacina que podría explicar su efecto citotóxico.21 En dicho modelo, la indometacina se estabiliza en la bicapa mediante su interacción con los grupos polares del desoxicolato y la formación de complejos multiméricos que desestabilizan la membrana y causan la muerte celular.21 En nuestro caso, la mayor cabeza polar del acido taurodesoxicólico respecto al desoxicolato podría comportarse como la indometacina en el modelo teórico descrito por Zhou y colaboradores, de manera que se formaran complejos multiméricos similares, se afectara el empaquetamiento de la membrana citoplasmática y por tanto se indujera la muerte celular.
Dentro de esta nueva serie de esteroides sintéticos derivados de la diosgenina, solo el acido taurodesoxicólico mostró efecto citotóxico sobre las células PC12. Estas evidencias avalan estudios futuros de este compuesto como inhibidor de proliferación de otras líneas tumorales, así como la evaluación del resto de las moléculas de la serie como candidatos neuroprotectores en esta misma línea celular y en dosis hasta 10µM, teniendo en cuenta los resultados publicados sobre otras moléculas estructuralmente afines en modelos de neuroprotección in vitro.
Agradecimientos
Los autores agradecen la valiosa colaboración del Lic. Yasser Almeida (Centro de Inmunología Molecular), en el empleo de los paquetes computacionales reportados. ]]>
REFERENCIAS BIBLIOGRÁFICAS
1. Mackenzie AS, Brassell SC, Eglinton G, Maxwell JR . Chemical fossils: the geological fates of steroids. Science. 1982; 217: 490-504.
2. Raju J, Mehta R. Cancer chemopreventive and therapeutic effects of diosgenin, a food saponin. Nutr Cancer. 2009; 61(1): 27-35.
]]>
3. Raju J, Patlolla J M. Diosgenin, a steroid saponin of Trigonella foenum graecum (Fenugreek), inhibits azoxymethane-induced aberrant crypt foci formation in F344 rats and induces apoptosis in HT-29 human colon cancer cells. Cancer Epidemiol Biomarkers Prev. 2004; 13(8): 1392-1398.
4. Corbiere C, Liagre B. Different contribution of apoptosis to the antiproliferative effects of diosgenin and other plant steroids, hecogenin and tigogenin, on human 1547 osteosarcoma cells. Int J Oncol. 2003; 22(4): 899-905.
5. Liu M J, Wang Z. Diosgenin induces cell cycle arrest and apoptosis in human leukemia K562 cells with the disruption of Ca2+ homeostasis. Cancer Chemother Pharmacol. 2005; 55(1): 79-90.
6. Leger D Y, Liagre B. Diosgenin dose-dependent apoptosis and differentiation induction in human erythroleukemia cell line and sedimentation field-flow fractionation monitoring. Anal Biochem. 2004; 335(2): 267-278.
7. Srinivasan S, Koduru S. Diosgenin targets Akt-mediated prosurvival signaling in human breast cancer cells. Int J Cancer. 2009; 125(4): 961-967.
8. Li F, Fernandez PP. Diosgenin, a steroidal saponin, inhibits STAT3 signaling pathway leading to suppression of proliferation and chemosensitization of human hepatocellular carcinoma cells. Cancer Lett. 2010; 292(2): 197-207.
9. Moghadasian MH. Pharmacological properties of plant sterols in vivo and in vitro observations. Life Sci. 2000; 67(6): 605-615. ]]>
10. Wester I. Cholesterol-lowering effect of plant sterols. Eur. I Lipid Sci Tech. 2000; 102: 37-44.
11. Melo PS, De Azevedo MB. Cytotoxicity of the phytosterol diosgenin and its derivatives in rat cultured hepatocytes and V79 fibroblasts. Hum Exp Toxicol. 2004; 23(10): 487-493.
12. Calogeropoulou T, Avlonitis N. Novel dehydroepiandrosterone derivatives with antiapoptotic, neuroprotective activity. J Med Chem. 2009; 52(21): 6569-6587.
]]>
13. Greene L A, Tischler AS. Establishment of a noradrenergic clonal line of rat adrenal pheochromocytoma cells which respond to nerve growth factor. Proc Natl Acad Sci U S A. 1976; 73(7): 2424-2428.
14. van Meerloo J, Kaspers GJ. Cell sensitivity assays: the MTT assay. Methods in molecular biology. 2011; 731: 237-245.
15. Linnankoski J, Makela JM. Computational prediction of oral drug absorption based on absorption rate constants in humans. J Med Chem. 2006; 49(12): 3674-3681.
16. Hur J, Lee P. Neurite outgrowth induced by spicatoside A, a steroidal saponin, via the tyrosine kinase A receptor pathway. European Journal of Pharmacology. 2009; 620: 9-15.
17. Huang Y, Cui J. Synthesis and cytotoxicity of 17a-aza-D-homo-androster-17-one derivatives. Bioorganic & Medicinal Chemistry Letters. 2011; 21: 3641-3643.
18. He Z, Tian Y. Anti-tumour and immunomodulating activities of diosgenin, a naturally occurring steroidal saponin. Natural Product Research: Formerly Natural Product Letters. 2012: 1-4.
19. Kongkathip B, Hasakunpaisarn A. Synthesis of cytotoxic novel 9,11-secosterol analogs: Structure/activity studies. Steroids. 2010; 75: 834-847. ]]>
20. Fimognari C, Lenzi M. Apoptosis and modulation of cell cycle control by bile acids in human leukemia T cells. Ann N Y Acad Sci. 2009; 1171: 264-269.
21. Zhou Y, Dial E J. Effect of indomethacin on bile acid-phospholipid interactions: implication for small intestinal injury induced by nonsteroidal anti-inflammatory drugs. Am J Physiol Gastrointest Liver Physiol. 298(5): G722-731.
Recibido: 5 de agosto de 2012.
Aprobado: 13 de septiembre de 2012. ]]>
Laura García-Pupo
Calle Mercado #14511 e/ 3era y Final, Barrio Obrero, SMP, La Habana. Tel.: (07) 6980631.Correo electrónico: laura.garcia@cidem.sld.cu ]]>