ARTÍCULO ORIGINAL
Microagujas y Transcutol® como promotores de la penetración transdérmica de sibutramina formulada en parche transdérmico
Microneedles and Transcutol® as transdermal penetration enhancers of sibutramine formulated in a transdermal patch
Lic. Pablo Serrano Castañeda, Dr. José Juan Escobar Chávez, MSc. Elvia Adriana Morales Hipólito, Dra. Clara Luisa Domínguez Delgado, Dr. Víctor Hugo Abrego Reyes ]]>
Facultad de Estudios Superiores Cuautitlán-Universidad Nacional Autónoma de México. Estado de México, México.
RESUMEN
Introducción: la principal barrera de permeación que tenemos es la piel. A pesar de ser una barrera casi impermeable para la mayoría de sustancias, se han buscado maneras para mejorar su permeabilidad utilizando nuevas tecnologías como es el uso de microagujas o promotores químicos como el Transcutol®.
Objetivo: desarrollar y caracterizar un parche transdérmico a base de clorhidrato de sibutramina como fármaco modelo, usando Transcutol® y microagujas como agentes promotores de la penetración transdérmica.
Métodos: se realizó la caracterización fisicoquímica de los parches mediante estudios de microscopia con luz polarizada, estudios de bioadhesión y resistencia a la ruptura. Los estudios de difusión se efectuaron en celdas de difusión verticales tipo Franz, utilizando piel abdominal humana como membrana entre ambos compartimentos. La cuantificación del principio activo se realizó mediante electroforesis capilar.
Resultados: se obtuvieron parches bioadhesivos, con una adecuada estabilidad del activo en la matriz polimérica de quitosán al no precipitarse. El uso de Transcutol® y microagujas incrementó el paso de clorhidrato de sibutramina a través de piel humana con respecto al parche control. Se obtuvieron valores de flujo de 0,0649 mg.cm-2.h-1 y 0,0816 mg.cm-2.h-1 en el parche con agente promotor y microagujas de 1 y 2 mm respectivamente, en comparación con los valores de flujo de 0,0527 mg.cm-2.h-1 y 0,0554 mg.cm-2.h-1 para el parche sin agente promotor (control) utilizando microagujas de 1 y 2 mm respectivamente.
Conclusiones: los resultados ponen de manifiesto la posibilidad de usar Transcutol® y microagujas para incrementar el paso de fármacos potentes y con estructura similar a la sibutramina por vía transdérmica, lo que genera de esta manera nuevas alternativas a las formas farmacéuticas orales para el tratamiento de padecimientos y enfermedades. ]]>
ABSTRACT
Introduction: the main permeation barrier is the skin. Although it is almost an impermeable barrier to most substances, new ways have been examined to improve its permeability by using new technologies such as microneedles and chemical enhancers like Transcutol®.
Objective: to develop and to characterize a transdermal patch containing sibutramine hydrochloride as model drug and using microneedles and Transcutol® as transdermal drug delivery enhancers.
Methods: Physicochemical characterization of sibutramine hydrochloride patches using polarized light microscopy, bioadhesion, tensile strength studies. The diffusion studies were performed in Franz-type diffusion cells with human abdominal skin as a sort of membrane between both compartments. The active ingredient was quantified through capillary electrophoresis.
Results: bioadhesive patches were obtained, with adequate stability of sibutramine hydrochloride in the polymer matrix of chitosan. The use of microneedles and Transcutol® increased sibutramine hydrochloride delivery through the human skin when compared with the control patch. The flow rates were 0.0649 mg.cm-2.h-1 and 0,0816 mg.cm-2.h-1 in the enhanced patch by using 1 and 2 mm microneedles respectively, in comparison with flow rates of 0,0527 mg.cm-2.h-1 and 0.0554 mg.cm-2.h-1 for the control patch having no enhancing agent with 1 and 2 mm microneedles respectively.
Conclusions: the results show that it is possible to use Transcutol® and microneedles to increase the delivery of potent drugs having a structure similar to that of sibutramine through transdermal administration. All this generates new alternatives to oral pharmaceuticals in order to treat ailments and diseases.
Key words: microneedles, Transcutol®, physical and chemical enhancers, transdermal patch, skin.
]]>
INTRODUCCIÓN
Los fármacos administrados por vía oral presentan desventajas como son el efecto de primer paso e irritabilidad gastrointestinal entre otras, en comparación con la vía transdérmica, que posee ventajas tales como: liberación controlada, se evita el efecto metabólico de primer paso, duración de acción prolongada, aumento del intervalo de actividad, comodidad de administración, de gran interés en aquellos fármacos con una corta semivida de eliminación, posibilidad de retiro del parche transdérmico rápidamente, así como la eliminación de la variabilidad asociada a la vía oral.1-3
Por las ventajas que ofrecen las formas de administración transdérmica y la posibilidad de incluir agentes promotores de penetración, tanto químicos (Transcutol®)4-8 como la utilización de agentes promotores de penetración físicos (microagujas) para favorecer el paso de fármacos hacia y a través de la piel,9,10 es posible realizar una formulación farmacéutica que permita aprovechar dichas ventajas que ofrece la vía transdérmica.4,5
Por lo que este estudio consiste en la elaboración de parches transdérmicos de una matriz polimérica de quitosán, así como la utilización de promotores físicos y químicos de penetración (Transcutol® y microagujas) para hacer más eficiente el paso de clorhidrato de sibutramina a través de piel abdominal humana.4
]]>
MÉTODOS
Preparación del parche transdérmico
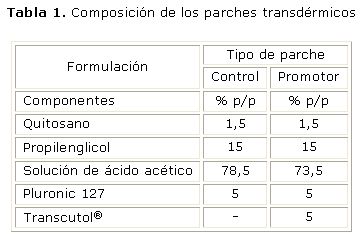
Las láminas adhesivas se prepararon utilizando el quitosano, un biopolímero natural atóxico.11-14 La composición de cada sistema matricial elaborado se muestra en la tabla 1.
El procedimiento de elaboración de los parches se realizó según la metodología descrita por Escobar-Chávez y otros.15
]]>
Se examinaron muestras circulares de cada uno de los parches con un diámetro de 3,6 cm mediante microscopia con luz polarizada usando el microscopio (Motic PM-2805, Wetzlar, Germany) para verificar la presencia de cristales de fármaco que pudieran modificar considerablemente la absorción de los activos a través de la piel. Dichas determinaciones se les realizaron a los parches transdérmicos a los 30, 60 y 90 días de haber sido preparados.
Estudios de bioadhesión
Se realizaron estudios por sextuplicado en el antebrazo de seis voluntarios sanos sin tratamiento farmacológico o cosmético previo de al menos 12 h. Se cortaron parches circulares con un área de 1 pulgada de diámetro y se colocaron en la sonda cilíndrica del texturómetro TA.XT2 (Texture Technologies Corp., Scarsdale, NY, USA). Los voluntarios colocaron el antebrazo en la parte baja del texturómetro, y en ese momento se inicio el descenso de la sonda cilíndrica (cilindro perplex) a una velocidad de 2 mm/s hasta entrar en contacto el parche adherido a la sonda cilíndrica con el antebrazo de los voluntarios, aplicando una fuerza de compresión de 200 g/10 s. Finalmente el parche se removió a una velocidad de 10 mm/s hasta obtener una distancia de separación de 15 cm, midiéndose la fuerza necesaria que se requiere para remover el parche de la piel.
Resistencia a la ruptura
Se usó el texturómetro TA.XT2 para estudios de bioadhesión. Se realizó de igual manera por sextuplicado para cada parche transdérmico la prueba de resistencia a la ruptura. Para ello, se colocaron parches con un área de 20 cm2 fijados en la base del texturómetro y atados a la sonda cilíndrica; se utilizó una fuerza de tensión de 1 cm y una distancia máxima de separación de 50 cm, determinándose la fuerza a la cual el parche se rompe. ]]>
Estudios in vitro de absorción percutánea
Los estudios de permeación in vitro se realizaron usando celdas de difusión tipo Franz con su respectivo compartimento receptor. Se utilizó como membrana entre ambos compartimentos piel abdominal humana completa obtenida de lipectomías. Los parches formulados se colocaron sobre la piel. El compartimento receptor se llenó con una solución amortiguadora HEPES de pH 7,4. Todo el montaje de las celdas se colocó en un agitador magnético multiplaza con control de temperatura. La solución del compartimento receptor se mantuvo en agitación continua usando una barra magnética a 50 rpm; la temperatura se fijó a 37 ºC. La toma de muestras se realizó a diferentes intervalos durante 36 h y el contenido de fármaco se determinó mediante electroforesis capilar. Las cantidades acumuladas de fármaco por centímetro cuadrado de los parches se graficaron en función del tiempo para obtener los perfiles y los parámetros correspondientes de los estudios de difusión.
RESULTADOS
Microscopia de luz polarizada
Se observó cada parche formulado a los 30, 60 y 90 días de haber sido elaborados. No hubo presencia de cristales de clorhidrato se sibutramina (Fig. 1). ]]>

Estudios de bioadhesión
La bioadhesión es un parámetro importante para la seguridad, eficacia y efecto terapéutico de los parches transdérmicos. En la tabla 2 y la figura 2 (A) se muestran los resultados de la prueba de bioadhesión del parche control y con agente promotor así como la prueba de resistencia a la ruptura.
Para el parche control se obtuvo una fuerza de bioadhesión promedio de 86,59 g, con una distancia de separación media de 1,182 mm mientras, que para el parche con agente promotor la fuerza de bioadhesión fue de 112,66 g y la distancia media de separación de 1,70 mm.
Resistencia a la ruptura
La prueba de resistencia a la ruptura, solo se realizó en los parches control debido a que los parches con agente promotor eran sumamente frágiles, por lo que no resultó posible someterlos a esta prueba. El estiramiento de los parches control fue de 312,243 %, tomando en cuenta la distancia de estiramiento promedio (31,22 mm) así como el tamaño original del parche (10 cm de largo y de ancho de 4 cm), lo cual dio como resultado parches muy elásticos. Los datos se presentan en la tabla 2 así como en la figura 2 (B).
Estudios in vitro de absorción percutánea
Se evaluaron los perfiles de penetración promedio del clorhidrato de sibutramina en función del tiempo para cada uno de los parches formulados (control y con Transcutol® como agente promotor) (Fig. 3) (A), así como las microagujas evaluadas de diferentes longitudes (1 mm y 2 mm), en la tabla 2 se muestra el resumen de los parámetros obtenidos (tiempo de latencia, Kp y flujo).
Sobre la base de los perfiles obtenidos se puede observar que los parches transdérmicos con agente promotor (Transcutol®) mostraron una mayor concentración de clorhidrato de sibutramina que penetra a través de la piel en comparación con los parches transdérmicos control (al ser comparados con las microagujas de la misma longitud). Al observar el parche transdérmico control con microagujas de 2 mm y el parche transdérmico con agente promotor con microagujas de 1 mm, hubo una mayor concentración de clorhidrato de sibutramina en el parche transdérmico control a comparación del parche transdérmico con agente promotor permitiendo las microagujas de 2 mm, una mayor penetración del principio activo. En la figura 3 (B), se muestra la cantidad acumulada de clorhidrato de sibutramina por área expuesta teniendo mayor cantidad acumulada los parches que contenían agente promotor (Transcutol®) que los parches control que no lo contenían.
DISCUSIÓN
Los estudios de microscopia con luz polarizada son útiles para evaluar la estabilidad física del parche transdérmico debido a que un parche transdérmico debe de mantenerse estable durante su vida útil.16 El cambio de color puede ser indicio de incompatibilidad entre los componentes, tales como la matriz del polímero, principio activo u otros componentes. Es común en matrices que los componentes del parche transdérmico presenten cristalización dentro de la matriz, esto se observa durante el envejecimiento del parche transdérmico.16 En base a las micrografías obtenidas de los parches transdérmicos tanto control como con agente promotor mostraron una buena estabilidad física ya que no se observó una cristalización dentro de la matriz así mismo se mantuvo la misma coloración de los parches a lo largo del tiempo siendo también la coloración de los parches, un indicador de estabilidad física de los mismos.
Para el parche control se obtuvo una fuerza de bioadhesión en promedio de 86,59 g, con una distancia de separación media de 1,182 mm mientras que para el parche con agente promotor se obtuvo una fuerza de bioadhesión de 112,66 g y la distancia media de separación de 1,70 mm. Siendo más bioadhesivos y teniendo mayor distancia de separación los parches con agente promotor, en base a estos resultados se obtuvieron unos parches bioadhesivos La bioadhesión es un factor crítico en la seguridad, eficacia y calidad del producto, ya que se encuentra ligada con el efecto terapéutico del parche transdérmico.17
La resistencia a la ruptura en los parches control fue buena de 52,364 g a excepción del parche con agente promotor el cual fueron sumamente frágiles. Este parámetro tiene relación con la seguridad, eficacia así como la calidad del producto y el efecto terapéutico.
Se obtuvieron parches bioadhesivos, con una adecuada estabilidad del activo en la matriz polimérica de quitosán al no precipitarse. El uso de Transcutol® y microagujas incrementa el paso de clorhidrato de sibutramina a través de piel humana.
Se observó un importante efecto sinérgico al evaluar el parche transdérmico que contenía Transcutol® (promotor químico) en combinación con el uso de microagujas (promotor físico) para el clorhidrato de sibutramina, incrementándose la penetración de este activo a través de piel humana de un 5 % a un 33 %, respectivamente con respecto al parche control (sin Transcutol®), además se observó otro efecto en las microagujas ya que al incrementar su longitud se incrementa la penetración del fármaco en un 26 %. Con estos resultado se pone de manifiesto la posibilidad de usar Transcutol® y microagujas para incrementar el paso de fármacos potentes y con estructura similar a la sibutramina por vía transdérmica, lo que genera de esta manera nuevas alternativas a las formas farmacéuticas orales para el tratamiento de padecimientos y enfermedades.
Agradecimientos ]]>
El agradecimiento a los PAPIIT TA 200-312 y PAPIIT IN 209709-3, al PAPIME 203612 y a la Cátedra NCONS-17.
REFERENCIAS BIBLIOGRÁFICAS
1. Soler Ranzani L. Desarrollo y evaluación biofarmacéutica de un sistema de administración transdérmica de alprazolam [tesis doctoral]. Barcelona: Universidad de Barcelona, Facultad de Farmacia; 2006.
2. Escobar Chávez JJ. Estudio de la penetración a través de la piel de naproxeno sódico utilizando agentes promotores de penetración (azona y trancutol), y de dicluconato de clorhexidina mediante iontoforesis [tesis doctoral]. Estado de México: FESC UNAM; 2006.
3. Ávila Avalos M. Métodos convencionales actualmente empleados para estudios de penetración percutánea [tesis]. Estado de México: FESC UNAM; 2010. ]]>
4. Serrano Castañeda P. Uso de microagujas para hacer más eficiente el paso de clorhidrato de sibutramina a través de piel humana formulado en parches transdérmicos de una matriz polimérica de quitosán con Transcutol [tesis]. Estado de México: FESC UNAM; 2011.
5. Escobar Chávez JJ, Bonilla Martínez D, Villegas González MA, Molina Trinidad E, Casas Alancaster N, Revilla Vázquez AL. Microneedles: A valuable physical enhancer to increase transdermal drug delivery. J Clin Pharmacol. 2011;51(7):964-77.
6. Escobar Chávez JJ, Rodríguez Cruz IM, Domínguez Delgado CL. Chemical and Physical enhancers for transdermal drug delivery. In: Gallelli L, editor. Pharmacology. Rijeka: InTech; 2012. p. 397-433.
7. Escobar-Chávez JJ, Merino V, editors. Current Technologies to increase the Transdermal Delivery of Drugs. The Netherlands: Bentham Science Publishers; 2010.
8. Domínguez-Delgado CL, Rodríguez-Cruz IM, López-Cervantes M. The skin a valuable route for administration of drugs. In: Escobar-Chávez JJ, Merino V, editors. Current Technologies To Increase The Transdermal Delivery Of Drugs. The Netherlands: Bentham Science Publishers Ltd; 2010. p. 1-22. ]]>
9. Escobar-Chávez JJ, Merino V, Díez Sales O, Nácher Alonso A, Ganem Quintanar A, Herráez M, Merino Sanjuán M. Transdermal nortriptyline hydrochloride patch formulated within a chitosan matrix intended to be used for smoking cessation. Pharm Develop Technol. 2011;16(2):162-9.
10. Escobar-Chavez JJ, Quintanar-Guerrero D, Ganem-Quintanar A. In vivo skin permeation of sodium naproxen formulated in PF-127 gels: Effect of AzoneR and Transcutol®. Drug Develop Industr Pharm. 2005;31(4-5):447-54.
11. Ammar HO, Salama HA, El-Nahhas SA, Elmotasem H. Design and evaluation of chitosan films for transdermal delivery of glimepiride. Curr Drug Delivery. 2008;5(4):290-8.
12. Albasarah YY, Somavarapu S, Stapleton P, Taylor KM. Chitosan-coated antifungal formulations for nebulisation. J Pharm Pharmacol. 2010;62(7):821-8.
13. Harris R, Lecumberri E, Heras A. Chitosan-genipin microspheres for the controlled release of drugs: clarithromycin, tramadol and heparin. Marine Drugs. 2010;8(6):1750-62. ]]>
14. Jintapattanakit A, Peungvicha P, Sailasuta A, Kissel T, Junyaprasert VB. Nasal absorption and local tissue reaction of insulin nanocomplexes of trimethyl chitosan derivatives in rats. J Pharm Pharmacol. 2010;62(5):583-91.
15. Escobar Chávez JJ, Merino Sanjuán V, López Cervantes M, Urban Morlan Z, Piñon Segundo E, Quintanar Guerrero D, Ganem Quintanar FA. Tape-Stripping Technique as a Method for Drug Quantification in Skin. J Pharm Pharmaceut Sci. 2008;11(1):104-30.
16. Hsieh Dean S. Drug permeation enhancement theory and applications. Indiana: Marcel Dekker Inc.; 1994. p. 3-24, 95-104.
17. Wokovich MA, Prodduturi S, Doub HW, Hussain SA. Transdermal drug delivery system (TDDS) adhesion as a critical safety, efficacy and quality attribute. Eur J Pharm Biopharm. 2006;64:1-8.
]]>
Recibido: 23 de marzo de 2013.
Aprobado: 29 de mayo de 2013.
José Juan Escobar Chávez. Facultad de Estudios Superiores Cuautitlán-Universidad Nacional Autónoma de México. Carretera Cuautitlán-Teoloyucan, Km 2.5, San Sebastián Xhala, 54700, Cuautitlán Izcalli, Estado de México, México. Correo electrónico: josejuanescobarchavez@gmail.com ]]>