Detección de reacciones adversas a medicamentos metabolizados por el Citocromo P4502C9
Detection of adverse reactions to Cytochrome P4502C9-metabolized drugs
MSc. Mayra Álvarez Corredera I, Dr. Yeset Cervelo Fernández II, Dr. C. Bárbaro Pérez Hernández III , MSc. Obdulio Juan González Hernández IV
I Facultad de Ciencias Médicas-General Calixto García, Metodóloga Departamento de Innovación y Evaluación de Tecnologías Sanitarias. La Habana, Cuba.
II Policlínico Joaquín Albarrán. La Habana, Cuba. ]]>
III Facultad de Ciencias Médicas “General Calixto García, Universidad de Ciencias Médicas de La Habana. Cuba.
IV Consejo Nacional de Sociedades Científicas de la Salud. MINSAP. La Habana, Cuba.
RESUMEN
Introducción: la existencia de variaciones interindividuales en la respuesta a los medicamentos es multifactorial e incluye la genética y el medio ambiente por tanto, en la práctica clínica es importante considerar los efectos de los medicamentos biotransformados por enzimas polimórficas como el citocromo P4502C9 (CYP2C9), que metaboliza aproximadamente el 16 % de los fármacos de uso habitual, de forma tal, que la asociación entre los estudios de farmacovigilancia y farmacogenética permitirían relacionar algunos fármacos con riesgo de reacciones adversas y por tanto, racionalizar la farmacoterapéutica.
Objetivo: describir la aparición de las reacciones adversas a fármacos metabolizados por el CYP2C9, en pacientes de un consultorio médico.
Métodos: se realizó un estudio observacional, descriptivo, transversal en los 143 pacientes de un Consultorio Médico del Policlínico Joaquín Albarrán, que en el periodo de estudio consumían fármacos metabolizados por el CYP2C9.
Resultados: se detectaron 43 reacciones adversas, el 88.4 % vinculadas a antiinflamatorios no esteroideos, entre ellos al ibuprofeno correspondió el 65.1 % de las mismas. La edad y el sexo no influyeron en la aparición de las reacciones. El 55.8 % de las reacciones clasificaron como leves.
Conclusiones: la quinta parte de los pacientes que presentaron reacciones adversas consumieron fármacos metabolizados por el CYP2C9, resultando insuficientes para predecir la respuesta a los medicamentos; variables tradicionalmente aceptadas, así como la edad y el sexo; deben ser considerados los factores que influyen sobre la capacidad de biotransformación de las enzimas metabolizadoras de fármacos, durante el proceso de prescripción.
ABSTRACT
Introduction: the existence of variations in the drug response among individuals is multifactoral and includes genetics and environment; so it is important for clinical practice to consider the effects of drugs that are biologically transformed by polymorphic enzymes such as cytochrome P4502C9 (CYP2C9), which roughly metabolizes 16% of regularly used drugs so that the association of pharmacovigilance and pharmacogenetic studies would allow relating some drugs with possibilities of adverse reactions, and therefore, being more rational in drug therapy.
Objective: to describe the occurrence of adverse reactions to drugs metabolized by CYP2C9 in patients from a physician's office.
Methods: observational, descriptive and cross-sectional study conducted in 143 patients from a physician's office of "Joaquin Albarran" polyclinics, who took CYP2C9-metabolized drugs in the study period.
Results: there were detected 43 adverse reactions, being 88.4% of them linked to non-steroidal anti-inflammatory drugs; Ibuprofen accounted for 65.1% of them. Age and sex did not influence the occurrence of reactions. In the group;, 55.8% of reactions were rated as mild.
Conclusions: the fifth part of patients who showed adverse reactions had taken cytochrome CYP2C9-metabolized drugs, they were not sufficient to predict response to traditionally accepted variable drugs as well as age and sex. The factors having an impact on the capacity of biotransformation of drug-metabolizing enzymes should be taken into consideration at the time of prescription of a drug.
Keywords: adverse drug reactions, cytochrome P4502C9.
]]>
INTRODUCCIÓN
El estudio de las reacciones adversas a medicamentos (RAM) constituye un tema de vital importancia en la actualidad, ya que éstas se asocian a una elevada morbilidad y mortalidad y originan importantes gastos a los sistemas de salud.1-7
Estudios realizados en diferentes países muestran que estas son las responsables de hasta el 7 % de las hospitalizaciones, número que se incrementa hasta el 30 % en personas mayores de 70 años. Mundialmente se estima que el costo de las RAM es aproximadamente el mismo que el del tratamiento medicamentoso, pero desafortunadamente, en los últimos años, se ha incrementado su número en comparación con la prescripción de fármacos; una gran parte de las mismas son de causa metabólica o inmunológica; el aumento del costo por una RAM se ha estimado en un 19,86 %.1-7
En un estudio de caracterización epidemiológica del consumo de medicamentos por la población adulta de Cuba (2007-2010), se determinó que se producen 43,7 reacciones adversas por cada 100 habitantes consumidores, lo que significa que casi la mitad de la población consumidora de medicamentos puede experimentar una reacción adversa.8
Un estudio preliminar en un número reducido de voluntarios sanos de la población cubana, reportó una baja frecuencia de metabolizadores lentos para el CYP2C9, aunque el estudio recomienda ampliar la muestra para corroborar estos resultados.9
Se conoce que la influencia de factores genéticos, a los cuales se atribuye entre el 60-80 % de la variabilidad de la respuesta a los fármacos, así como ambientales (tratamiento concomitante, tabaco, alcohol, etc.), pueden modificar la actividad de las enzimas metabolizadoras de medicamentos como por ejemplo la enzima citocromo P4502C9 (CYP2C9), que constituye una parte importante del contenido del citocromo en el hígado humano y metaboliza aproximadamente el 16 % de los fármacos de uso habitual en la clínica diaria, tales como, numerosos antiinflamatorios no esteroideos (AINEs) y algunos medicamentos como los anticoagulantes, sulfonilureas, anticonvulsivantes e inhibidores del receptor de la angiotensina II.1-4,10-11
Existen reportes de la frecuencia de los polimorfismos del CYP2C9 en diferentes poblaciones, su relación con la eficacia o fracaso terapéutico de los medicamentos biotransformados por esta isoenzima, así como la influencia de este polimorfismo y otros factores en la aparición de reacciones adversas.2-4,10
Desde el punto de vista clínico, en aquellas personas consideradas como metabolizadoras lentas, el polimorfismo puede determinar la acumulación del fármaco, la acentuación y prolongación de sus efectos, y la aparición de reacciones adversas dependientes de la concentración de esta.11
Entre los reportes relacionados a fármacos biotransformados por el CYP2C9 incluidos en la base de datos cubana de la Unidad Coordinadora Nacional de Farmacovigilancia (UCNFV), se localizan los analgésicos no opioides con 1 071 reacciones adversas en el 2009, de las cuales el 0,4 % fueron clasificadas como graves, el 32,3 % como moderadas y el resto leves.12 Durante el año 2010 fueron reportadas 1 386 reacciones adversas para este grupo de fármacos, de ellas el 0,4 % fueron graves, el 42,8 % moderadas y el 2,6 % leves, sin que ocurrieran reacciones mortales asociadas al uso de este grupo farmacológico.13 En relación a la distribución por sexo, fue el femenino el más relacionado con sospechas de efectos adversos con un comportamiento similar en ambos años.12-13
]]> Se estima que aproximadamente cada año 4,5 millones de visitas médicas están relacionadas con la ocurrencia de RAM, la mayoría a pacientes no hospitalizados. Es de destacar que en Cuba, el 85 % de estas reacciones adversas ocurrieron en la Atención Primaria de Salud (APS), primer nivel de asistencia médica y donde habitualmente reciben asistencia médica mayor volumen de personas.12-14En consideración con la aparente contradicción entre la frecuencia de metabolizadores lentos encontrada en la población cubana y los reportes de RAM de la UCNFV para medicamentos de amplio uso en la APS metabolizados por el CYP2C9, se decide describir la aparición de las reacciones adversas a medicamentos metabolizados por esta enzima en un consultorio médico, como un estudio inicial que permita posteriormente establecer una metodología para evaluar la relación entre las RAM a estos fármacos y los factores genético-ambientales.
MÉTODOS
Se realizó un estudio observacional, descriptivo, transversal, en el universo de pacientes que pertenecen al Consultorio Médico de la Familia # 5 del Policlínico Joaquín Albarrán, que acudieron a consulta en el periodo comprendido desde el 1ro de febrero al 31 de agosto de 2009 y consumían fármacos metabolizados por el CYP2C9. Todos los pacientes fueron informados de los objetivos del estudio y firmaron el acta de consentimiento para participar en la investigación. Se utilizó como fuente de información un modelo de recogida de datos diseñado para este estudio donde la fuente primaria de información fue la entrevista con cada paciente. Se tomaron como variables el sexo, la edad (0-14, 15-30, 31-60 y mayor de 60) y la intensidad o gravedad clasificadas según las normas de trabajo del sistema cubano de farmacovigilancia (leve: se presentan signos y síntomas bien tolerados, no requieren tratamiento, no prolongan la hospitalización y pueden no requerir la suspensión del tratamiento; moderada: interfiere con las actividades habituales, no amenaza la vida del paciente, requiere tratamiento farmacológico, la suspensión del medicamento que provocó la reacción no es siempre necesaria; grave: pone en peligro la vida del paciente o le ocasiona la muerte, requiere hospitalización o prolongación de la hospitalización, es causa de invalidez o incapacidad persistente o significativa, es causa de malformaciones o alteraciones en el recién nacido; letal: contribuye directa o indirectamente a la muerte del paciente).
Los resultados se expresaron en sus respectivas medidas de resumen: números relativos y absolutos. Se utilizó el Test de comparación de proporciones en las variables cuantitativas.
RESULTADOS
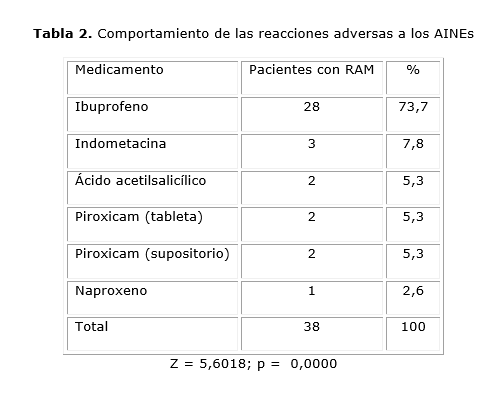
Durante los seis meses que conformaron el período de estudio fueron incluidos 143 pacientes que consumían fármacos metabolizados por el CYP2C9, de los cuales 34 presentaron reacciones adversas a estos medicamentos, lo que representa el 23.8 % de pacientes con RAM. El total de RAM presentadas en los 34 pacientes fue de 43. El grupo farmacológico que presentó más RAM fue los AINEs (88,4 %; p<0.05), entre ellos, al ibuprofeno correspondió el 65.1 % (p<0.05) de las RAM que aparecieron en este grupo (tablas 1 y 2).
]]> El estudio de la relación entre las reacciones adversas y las variables sexo y edad, arrojó que no hubo diferencias significativas entre hombres y mujeres, así como entre grupos de edades, aunque hubo un predominio de RAM en el sexo femenino (23.8 % del total de RAM) y en pacientes mayores de 60 años (16.8 % de pacientes con RAM).Más del 50 % de las RAM presentadas fueron leves (p<0.05), como por ejemplo, gastropatías por AINEs; no se detectaron reacciones graves, letales, ni interacciones medicamentosas asociadas a las RAM encontradas durante el período de estudio (tabla 3).
DISCUSIÓN
La variabilidad de los individuos para responder a los fármacos constituye un importante problema en la práctica clínica, por lo que identificar a los pacientes de riesgo evitaría no sólo la ineficacia de los medicamentos, sino que también minimizaría la aparición de efectos colaterales.1,4,10
Aproximadamente 1 500 pacientes han estado en contacto con un medicamento, al momento de ser aprobado un medicamento para entrar al mercado, lo que constituye una limitante para detectar RAM. Estas son consideradas una de las mayores causas de enfermedad iatrogénica en medicina. Muchas reacciones adversas son prevenibles y, aunque idealmente no debieran ocurrir, se debe decir que muchas otras son imposibles de evitar, ya que no se conoce la causa ni como ocurren.5,6,8,15
La frecuencia de RAM a fármacos metabolizados por el CYP2C9 encontradas en estos pacientes, es semejante a la de estudios realizados en Cuba por Dorado P y Pardo Cabello en España.7,9,15-17
El hecho de que los AINEs constituyeran el grupo de fármacos que aportó el mayor número de RAM, coincide con los resultados de estudios de FV realizados en Cuba e internacionalmente,6-7,8-12,18 donde este grupo de medicamentos estuvo entre los más reportados y en este caso fue el que más se relacionó con múltiples reacciones para un individuo. Un estudio realizado en España7 estima la tasa de RAM por AINEs en 71 por millón de dosis diarias, así como se asocia una muerte por cada 1 200 pacientes que consumen AINEs o ácido acetil salicílico durante más de dos meses.
Múltiples investigaciones asocian al sexo femenino con mayor frecuencia de reacciones adversas; en este estudio, aunque no se demostró una influencia significativa del sexo en la aparición de RAM a fármacos metabolizados por el CYP2C9, hubo un predominio del sexo femenino.6-12,15,17,19
Se reconoce que la edad es un factor que predispone a la aparición de RAM, además de las interacciones farmacológicas, enfermedades concomitantes, entre otros; precisamente, el paciente geriátrico, generalmente tiene asociadas otras enfermedades y consume diferentes medicamentos,5,8,11,14 sin embargo, de manera similar al reporte de un estudio realizado en un hospital de Colombia,20 en este caso tampoco se evidenció la influencia de la edad ni las interacciones medicamentosas sobre la aparición de RAM, aunque éstas aparecieron con mayor frecuencia en los individuos mayores de 60 años. Estos resultados son semejantes a los dos estudios realizados en México19 y España,7 así como un estudio de costo de RAM desarrollado en dos hospitales de la capital cubana.17
]]> En relación a la severidad, a diferencia de otros estudios donde la mayoría de las RAM eran clasificadas como moderadas, en este caso y en el estudio realizado por Milian AJ en el año 2010,8 predominaron las catalogadas como leves. Las diferencias halladas en la gravedad de las RAM entre estudios se puede explicar por los disímiles escenarios en que las investigaciones se efectuaron, el tipo de pacientes incluidos y los fármacos considerados ya que, aunque la mayoría de los fármacos son prescritos en la APS, los estudios que se publican por lo general son hospitalarios, además que el objetivo de este estudio solo fue analizar fármacos metabolizados por el CYP2C9, por lo que se excluyen otros medicamentos como vacunas y antimicrobianos, que no se metabolizan por esta vía y son causas muy frecuentes de RAM en la APS.8,17,19,20La información sobre el impacto de la farmacogenética en la APS, aún es insuficiente. El primer intento por describir el rol de la farmacogenética en la APS fue publicado en el año 2006 por Grise GR y colaboradores11 con el objetivo de determinar la frecuencia de reacciones adversas a dieciséis medicamentos sometidos a polimorfismo genético. En el estudio se encontró que los analgésicos, antidepresivos y antihipertensivos, muchos de los cuales son biotransformados por el CYP2C9, fueron los que más frecuentemente se asociaron a RAM.11
Se considera la asimilación de la información farmacogenética en la práctica clínica y sobre el impacto de la farmacogenética en la APS, aún es lenta; sin embargo, la ciencia ha demostrado la relación entre los polimorfismos genéticos y el metabolismo de fármacos, por lo que el hecho de que en este estudio, más de la quinta parte de los pacientes que consumieron fármacos metabolizados por el CYP2C9 presentaron RAM, permite inducir que la edad, el sexo, y otras variables tradicionalmente aceptadas, son insuficientes para predecir la respuesta a los medicamentos; por lo que deben ser considerados los factores que influyen sobre la capacidad de biotransformación de las enzimas metabolizadoras de fármacos, durante el proceso de prescripción.
REFERENCIAS BIBLIOGRÁFICAS
1. Cavallari LH. Tailoring Drug Therapy Based on Genotype. J Pharm Pract. 2012;25(4):413-6.
2. Kudzi W, Adjei GO, Ofori-Adjei D, Dodoo AN. Pharmacogenetics in Ghana: reviewing the evidence. Ghana Med J. 2011;45(2):73-80.
3. Wang D, Jiang Z, Shen Z, Wang H, Wang B, Shou W, et al. Functional evaluation of genetic and environmental regulators of p450 mRNA levels. PLoS One. 2011;6(10):e24900. Epub. 2011; Oct 5.
]]>4. Josansson I, Ingelman-Sundberg M. Genetic Polymorphism and Toxicology—With Emphasis on Cytochrome P450. [on line]. 2011 [citado 31 agosto 2012]; [aprox 13p]. Disponible en: http://toxsci.oxfordjournals.org/content/120/1/1.long
5. Chile Orellana R. Pharmacological surveillance system in the Hospital of the University of Chile. Medwave. 2011;11(08):e5111 DOI: 10.5867/medwave.2011.08.5111.
6. Calderón CA, Urbina AP. La Farmacovigilancia en los últimos 10 años: actualización de conceptos y clasificaciones. Logros y retos para el futuro en Colombia. MéD.UIS. 2010;24:57-73.
7. Pardo Cabello AJ. Reacciones adversas medicamentosas fatales en pacientes hospitalizados [tesis doctoral]. Granada: Universidad de Granada, Facultad de Medicina; 2008.
8. Milián García AJ. Caracterización epidemiológica del consumo de medicamentos por la población adulta de Cuba. 2007-2010 [tesis doctoral]. La Habana: Escuela Nacional de Salud Pública; 2010.
9. Dorado P, Álvarez M, Pérez B, Llerena A. Comportamiento de la relación genotipo-fenotipo del citocromo CYP2C9 en una muestra de cubanos. Rev Cub Farm 2007; 41(Supl Esp 2):259-260.
10. Twardowschy CA, Werneck LC, Scola RH, De Paola L, Silvado CE. CYP2C9 polymorphism in patients with epilepsy: genotypic frequency analyzes and phenytoin adverse reactions correlation. Arq Neuropsiquiatr. 2011;69(2A):153-8.
11. Grice GR, Seaton TL, Woodland AM, McLeod HL. Defining the opportunity for pharmacogenetic intervention in primary care. Pharmacogenomics. 2006; 7(1):61-5.
12. Centro para el Desarrollo de la Farmacoepidemiologia. Unidad Coordinadora Nacional de Farmacovigilancia Informe Anual 2009 [citado 18 Mayo 2011]; Disponible en: http://files.sld.cu/cdfc/files/2010/02/informe-anual-2009.pdf.
13. Centro para el Desarrollo de la Farmacoepidemiologia. Unidad Coordinadora Nacional de Farmacovigilancia. Informe Anual 2010 [citado 18 Mayo 2011]. Disponible en: http://files.sld.cu/cdfc/files/2010/02/informe-anual-2010.pdf.
14. Sarkar U, López A, Maselli JH, González R. Adverse drug events in U.S. adult ambulatory medical care. Health Serv Res. 2011;46(5):1517-33.
15. Pirmohamed M, Park K. Adverse drug reactions: back to the future. Br J Clin Pharmacol. 2003;55(5):486–492.
16. Rascón-Sabido R, Sabido-Siglher AS, Márquez-Celedonio FG, Soler-Huerta E. Programa de Farmacovigilancia en atención primaria: experiencia en una clínica de Veracruz, México. Archivos en Medicina Familiar [Revista on-line]. 2007 [citado 12 Julio 2011]; 9(2): [aprox 10p.]. Disponible en: http://redalyc.uaemex.mx/src/inicio/ArtPdfRed.jsp?iCve=50711454005.
17. Jiménez G, Lara M, Bayarre H, Rego J, García B. Costo de los efectos adversos que causan ingreso en hospitales seleccionados de Ciudad de La Habana. Año 2006. Boletín Fármacos [Revista on-line]. 2009 [citado 20 Mayo 2011]; 12(2): [aprox 6p.]. Disponible en:
www.boletinfarmacos.org/.../advertencias_sobre_medicamentos_Investigaciones.asp .
18. Chao A, Díaz I, Jiménez G, López Y, Fernández X. Análisis de las sospechas de reacciones adversas producidas por analgésicos no opioide. Boletín Fármacos [Revista on-line]. 2009 [citado 20 Mayo 2011]; 12(2): [aprox 8p.]. Disponible en: http://www.boletinfarmacos.org/042009/advertencias_sobre_medicamentos_Investigaciones.asp .
19. Zavaleta M, Rosete A. Reacciones adversas a medicamentos (RAM) en el Hospital Médica Sur. Avances y dirección de nuestros logros. Rev Médica Sur, México [Revista on-line]. 2007 [citado 12 diciembre 2010]; 14(4): [aprox 8p.]. Disponible en:
]]> http://www.medigraphic.com/pdfs/medsur/ms-2007/ms074b.pdf .20. Tribiño G, Maldonado C, Segura O, Díaz J. Costos directos y aspectos clínicos de las reacciones adversas a medicamentos en pacientes hospitalizados en el servicio de medicina interna de una institución de tercer nivel en Bogotá. Biomédica [Revista on-line]. 2006 [citado 28 Mayo 2011]; 26 (001): [aprox 11p.]. Disponible en: http://redalyc.uaemex.mx/redalyc/src/inicio/ArtPdfRed.jsp?iCve.
Recibido: 1 de febrero de 2014
Aprobado: 23 de mayo 2014
Mayra Silvia Álvarez Corredera. Dirección de Ciencia y Técnica. Ministerio de Salud Pública. 23 y N, Plaza, La Habana, Cuba. Teléfono: 8396345 Correo electrónico: farmacol@infomed.sld.cu
]]>