Estabilidad de una formulación de adrenalina 1 mg/mL inyectable, para uso veterinario
Stability of a formulation of 1mg/ml adrenaline injectable product for veterinary use
MSc. David Alexis Mora Atiés,I MCs. Caridad Margarita García Peña,II Ing. Yanet Montes de Oca Porto,II MSc. Lisandra García Borges,II Téc. Vivian Martínez Espinosa,II Lic. Marlen Milanés Fernández,I Lic. Yanaisa Gordo García,I Lic. Yarelys Álvarez HernándezI
]]> I Grupo Empresarial LABIOFAM. La Habana, Cuba.
RESUMEN
Introducción: el inyectable de adrenalina 1 mg/mL se emplea en bovinos, equinos, caprinos, ovinos, porcinos, perros y gatos como estimulante directo del miocardio, en el shock anafiláctico, el espasmo bronquial por su acción broncodilatadora, en anestesia local para prolongar su acción, como hemostático local en hemorragias superficiales, en urticaria y descongestivo conjuntival.
Objetivo: evaluar el desempeño del método analítico por cromatografía líquida de alta resolución, aplicable al control de la calidad y al estudio de estabilidad del inyectable y su estabilidad en el tiempo.
Métodos: la separación para cuantificar el principio activo en el producto terminado se realizó a través de una columna cromatográfica Lichrosorb RP- 18(5 µm) (250 x 4 mm), con detección ultravioleta a 280 nm, empleando una fase móvil compuesta por metanol‒solución de fosfato de sodio monobásico 0,05 M, 1‒octanosulfonato de sodio y edetato de sodio a pH 3,58 (3:17) y la cuantificación de este frente a una muestra de referencia con el método del estándar externo. El estudio de vida de estante se desarrolló por un periodo de doce meses a temperatura ambiente y el de estabilidad acelerada a 40 0 C durante seis meses.
Resultados: los resultados obtenidos de los parámetros analizados en la evaluación del desempeño del método se encontraron dentro de los límites establecidos. Los resultados del estudio de estabilidad por vida de estante después de transcurridos los doce meses indicaron que el producto mantiene los parámetros que determinan su calidad durante ese tiempo y no se observó degradación significativa del producto en los estudios acelerados.
Conclusiones: la evaluación del desempeño del método analítico desarrollado demostró la confiabilidad del mismo. Se estableció un año como fecha de vencimiento en las condiciones señaladas.
Palabras clave: adrenalina, cromatografía líquida de alta eficiencia, inyectable, control de calidad, estudio de estabilidad.
Introduction: one mig/ml adrenaline injectable product is used in bovines, horses, caprine, ovines, swines, dogs and cats as direct myocardial stimulant in the anaphylactic shock, bronchial spasm because of its bronchodilating action, in local anesthesia to extend its action, local hemostatic agent in superficial hemorrhages, in urticaria and as conjunctival decongestive agent.
Objective: to evaluate the high performance liquid chromatography analytical method applicable to the quality control and the stability study of the injectable and its time stability.
Methods: for quantification of the active principle in the final product, the separation was performed with a chromatographic columm Lichosorb RP-18(5 µm) (250 x 4mm)and ultraviolect detection at 280nm, using a mobile phase of methanol-monobasic sodium phosphate 0.05 M, 1-sodium octanosulphonate and sodium edentate solution at pH 3.58 (3:17) and the quantification against a reference sample was made with the external standard method. The shelf life study was conducted for 12 months at room temperature and that of accelerated stability at 40°C for six months.
Results: the achieved results in the parameters analyzed in the evaluation of the method performance were within the set limits. The results of the shelf life stability study after 12 months indicated that the product keep the parameters that determine its quality during that time and no significant degradation of the product was observed in the accelerated studies.
Conclusions: the evaluation of the analytical method performance showed the reliability of the method. The expiry date was then set as one year under the stated conditions.
Keywords: adrenaline, high performance liquid chromatography, injectable, quality control, stability study.
]]> INTRODUCCIÓN
La adrenalina incrementa la fuerza y la velocidad de la contracción cardiaca; es hipertensor y vasoconstrictor periférico; tiene acción midriática, inhibe la actividad gastrointestinal y relaja el espasmo bronquial. Inhibe el vaciamiento de la vejiga urinaria e incrementa el metabolismo. También reduce el flujo sanguíneo en la piel, la mucosa y el riñón.1,2
En los vasos esplécnicos produce vasoconstricción, y en el pulmón y el cerebro su acción vasoconstrictora es escasa, sin embargo a nivel de los músculos esqueléticos produce vasodilatación. En los bronquios ocasiona la dilatación de su musculatura lisa, acción que se ve más acentuada cuando se encuentra contraída. La acción estimulante directa de la adrenalina sobre el miocardio se usa para combatir el colapso cardiaco en el individuo antes sano y normal. Se aplica en el tratamiento de los ahogados, en la hipoxia del recién nacido y en algunos accidentes anestésicos. Para que la acción estimulante sea eficaz, debe inyectarse inmediatamente de producirse el colapso cardiaco.1,2
La inyección intravenosa inhibe los movimientos en el estómago y los intestinos, las paredes intestinales se relajan pero se produce constricción en el esfínter pilórico, ileocólico y anal interno. Retarda el movimiento de la ingesta. Relaja la vesícula biliar pero contrae el conducto biliar. Produce constricción en los vasos sanguíneos mesentéricos. Se emplea en anestesia local agregándose a soluciones anestésicas locales para prolongar su acción.1,2
En la Farmacopea de los Estados Unidos (USP 32, 2009)3 aparece reportado un método analítico por Cromatografía Líquida de Alta Resolución (CLAR) para el control de la calidad del inyectable de adrenalina, por lo que se realizó la evaluación del desempeño del método analítico reportado para nuestro producto y en nuestras condiciones, con el objetivo de obtener pruebas documentales de que el método a emplear en el control de la calidad y el estudio de estabilidad del producto terminado es confiable y seguro.4,5
La Cromatografía Líquida de Alta Resolución le brinda la posibilidad al analista de emplear esta herramienta para solucionar los inconvenientes de los métodos espectrofotométricos en los estudios de estabilidad, pues además de presentar una alta sensibilidad y exactitud, es en esencia un método separativo; lo que permite medir con gran selectividad el compuesto deseado, siempre y cuando se encuentre un sistema cromatográfico que asegure una adecuada separación.5
La validación es el proceso establecido para la obtención de pruebas documentadas de que el método es lo suficientemente fiable para producir el resultado esperado.
Los parámetros analíticos que pueden ser considerados en la evaluación del desempeño de un método analítico son exactitud, precisión, especificidad y linealidad.4,5
La estabilidad de los productos farmacéuticos representa un importante eslabón en el desarrollo y formulación de toda forma terminada. De esta manera se puede definir las condiciones de almacenamiento en el envase propuesto y establecer la vida útil del producto farmacéutico. Estos estudios contemplan la conservación de la potencia, pureza, características organolépticas y su efectividad. Es una exigencia del Instituto de Medicina Veterinaria (IMV) para registrar un nuevo medicamento que se realicen los estudios de estabilidad.6 Con el objetivo de evaluar el desempeño del método analítico por cromatografía líquida de alta resolución (CLAR), aplicable al control de la calidad y al estudio de estabilidad de la adrenalina 1 mg/mL del inyectable y su estabilidad en el tiempo.
]]> MÉTODOS
EVALUACIÓN DEL DESEMPEÑO DEL MÉTODO
La sustancia de referencia química de trabajo de epinefrina se suministró por el grupo de sustancias de referencia del Centro de Investigación y Desarrollo de Medicamentos (CIDEM, La Habana, Cuba), la cual se analizó por el método cromatográfico establecido para realizar el control de la calidad de la materia prima, con una pureza de 99,7 %. El producto terminado en forma de inyectable, se elaboró en el Grupo empresarial LABIOFAM identificado como el lote 001 (piloto), el cual cumplió con las especificaciones de calidad establecidas para el control de la calidad del inyectable.
Todos los reactivos utilizados fueron de calidad analítica. En el ensayo se empleó un cromatógrafo (KNAUER) con detector UV variable Kanuer acoplado a una computadora para la adquisición de los cromatogramas mediante el software CHROMGATE (versión 3,1) ajustado a 280 nm, un inyector con un rulo de 20 µL. La separación se realizó isocráticamente para lo que se empleó una columna Lichrosorb RP‒18 (5 µm) (250 x 4 mm Altima C‒18 (10 µm) (250 x 4 mm) y un flujo de 1,0 mL/min. La fase móvil, consistió en una mezcla binaria desgasificada de metanol‒ solución compuesta por un litro de solución de fosfato de sodio monobásico 0,05 mol/L, 519 mg de 1‒octanosulfonato de sodio y 45 mg de edetato de sodio, ajustando el pH 3,58 con ácido fosfórico (3:17)
Preparación de la muestra: se tomó un 1 mL de muestra, se trasvasó a volumétrico de 10 mL adicionándose fase móvil, se aplicó ultrasonido por 3 min y se completó volumen con fase móvil.
Preparación de la sustancia de referencia química: se pesaron 10 mg de sustancia de referencia química de epinefrina y se trasvasó a un volumétrico de 100 mL adicionándose fase móvil, se aplicó ultrasonido por cinco minutos y se completó volumen con fase móvil.
EVALUACIÓN DEL DESEMPEÑO DEL MÉTODO
La evaluación del desempeño fue realizada según la Regulación 41-2007 (CECMED) y la Farmacopea de los Estados Unidos (USP 32); se evaluaron los parámetros que a continuación se describen:3,4
Linealidad: se realizaron tres determinaciones para cinco concentraciones diferentes, correspondientes al 50, 75, 100, 125, y 150 % de epinefrina materia prima a cuantificar. Se determinó la ecuación de la recta, el coeficiente de correlación, la prueba de significación estadística de significación de la pendiente Sb rel (%) y los coeficiente de variación de los factores de respuesta.
Exactitud: se realizaron tres réplicas para tres concentraciones diferentes equivalentes al 80, 100, 120 % de epinefrina en el producto terminado, empleando el método de recuperación (muestras placebos cargadas con epinefrina materia prima) se determinó el % de recuperación, la desviación estándar y el coeficiente de variación. Se determinó además la prueba de Cochram con vistas a comprobar si la variación de la concentración produce diferencias significativas en los resultados y la prueba de la t de Student para la determinación de las diferencias significativas entre la recuperación media y el 100 %.
]]> Precisión: el estudio de repetibilidad se realizó por un mismo analista, el mismo día a través de seis réplicas de la muestra de adrenalina inyectable 1 mg/mL. Con ellas se determinaron los valores medios, la desviación estándar y el coeficiente de variación.De igual manera para el ensayo de la Precisión Intermedia se utilizaron tres niveles de concentración que corresponden al 80, 100 y 120 % para dos analistas y tres días diferentes. Se aplicó la prueba de Fisher y de t de Student para determinar si existen diferencias significativas entre los resultados al variar las condiciones de análisis.
Especificidad: para el estudio de Especificidad se analizaron: la sustancia de referencia, el placebo y la muestra de adrenalina inyectable 1 mg/mL; las muestras de producto terminado y muestras sometidas a condiciones drásticas tales como: hidrólisis ácida con 15 mL de HCL 3 mol/L, hidrólisis básica con 15 mL de NaOH 3 mol/L; luz las muestras fueron expuestas a la luz solar; se almacenaron las muestras colocadas en una estufa a temperatura controlada de 40±2 OC y oxidación con peróxido de hidrógeno (5 mL de reactivo) todas las muestras sometidas a condiciones extremas fueron almacenadas durante 7 días.
No debe observarse señales del placebo y de los productos de degradación en la zona de elusión del principio activo. Las áreas bajo las curvas del patrón y en el producto terminado deben ser similares.
ESTUDIO DE ESTABILIDAD
Para el desarrollo de la formulación se empleó como materia prima epinefrina, la cual fue analizada siguiendo las especificaciones de calidad descritas en la monografía de la USP 32.
Este estudio se realizó por los métodos de vida de estante y estabilidad acelerada. Se emplearon muestras de los lotes pilotos 001, 002 y 003, producidos en el Grupo Empresarial LABIOFAM envasados en bulbos de color ámbar.
Estabilidad acelerada: en los estudios de estabilidad acelerada, se almacenaron las muestras de los lotes estudiados en un horno a temperatura controlada de 40 ± 2 ºC y 75 ± 5 % de humedad relativa (HR); se evaluaron al inicio, 1, 2, 3 y 6 meses, se evaluaron las características organolépticas, pH y valoración en cada uno de los tiempos.
Estabilidad por vida de estante: en el estudio de estabilidad por vida de estante, los lotes estudiados se almacenaron a temperatura ambiente (30 ± 2 ºC y 70 ± 5 % de HR; se valoraron al inicio y a 6, 9 y 12 meses de fabricados, evaluándose las características organolépticas, pH, valoración y esterilidad en cada uno de los tiempos.
]]> RESULTADOS
EVALUACIÓN DEL DESEMPEÑO DEL MÉTODO
Las figuras 1 y 2 muestran los resultados obtenidos en el estudio de especificidad del método. Como se observa en los cromatogramas no se obtiene ninguna señal, en el placebo, en la zona de interés, al ser comparado con la señal obtenida para la solución de referencia química y la muestra, lo que indica que los excipientes o sustancias auxiliares no interfieren en la determinación del principio activo. En cuanto a las muestras sometidas a condiciones drásticas se observa una disminución del área del pico de la epinefrina y la aparición de picos secundarios, atribuibles a un posible producto de degradación, el cual no interfiere en la determinación del principio activo.
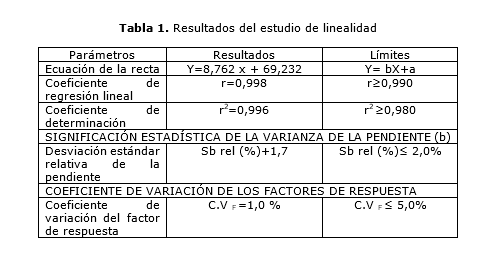
En la tabla 1 se reportan los resultados del estudio de la linealidad del sistema; el coeficiente de regresión lineal fue de 0,996 y el coeficiente de variación de los factores de respuesta resultó igual a 1,00.
El resultado del estudio de precisión del método desarrollado aparece reportados en las tablas 2 y 3. En el estudio de repetibilidad, la media obtenida fue de 99,8 % y el coeficiente de variación fue de 0,36 %, mientras que los valores de F y t calculadas resultaron menores que los valores tabulados para cada uno de los niveles estudiados, para un 95 % de confianza.
En la tabla 4, aparecen reportados los resultados del estudio de exactitud. La recuperación media fue de 99,98 % y el valor de t calculada (1,580) y de G calculada (0,613) resultaron menores que los valores tabulados, t tabulada 2,306 para un 95 % de confianza y G tabulada 0,797 para un 95 % de confianza, k=3 y n=3.
ESTUDIO DE ESTABILIDAD
]]> Los resultados del estudio de estabilidad acelerada a 40 ± 2 ºC y 75 ± 5 % HR, correspondiente a los lotes 001, 002 y 003, se reportan en la tabla 5, se demostró que el producto terminado no presenta cambios significativos.Los resultados del estudio de vida de estante, al inicio, 6, 9 y 12 meses, se muestran en la tabla 6; se observó que el producto terminado cumple con las especificaciones de calidad durante el estudio.
DISCUSIÓN
EVALUACIÓN DEL DESEMPEÑO DEL MÉTODO
Los resultados obtenidos en el estudio de especificidad del método (figura 1), demuestran la especificidad del método al no presentarse interferencias de picos adicionales en la determinación del principio activo, que presenta un tiempo de retención (tr) de aproximadamente 3 minutos. En el cromatograma A correspondiente al placebo no se observan señales en el tr de la epinefrina, evidenciándose que no existen interferencias de los excipientes. Los cromatogramas B y C correspondientes a la sustancia de referencia química y el producto terminado, respectivamente, permiten demostrar que las áreas bajo la curva y los tiempos de retención son similares. Los cromatogramas de las muestras de producto terminado (figura 2) sometidas a condiciones drásticas (D, E, F, G, H) demuestran que los productos de degradación no interfieren en la determinación del principio activo porque no eluyen al mismo tiempo de retención de la epinefrina, se observa la disminución de la señal correspondiente a la epinefrina y la aparición de picos secundarios a otros tr. Los resultados obtenidos demuestran la especificidad del método y factibilidad de su aplicación en el control de la calidad y estudio de estabilidad del producto terminado.4,5
Los resultados de los estudios de linealidad mostraron valores superiores a los exigidos para los coeficientes de regresión y de determinación; se demostró con el valor del coeficiente de correlación obtenido, cercano a la unidad, la existencia de correlación con una probabilidad elevada, así como el grado de relación entre las variables concentración y respuesta detectada por el equipo empleado. También el coeficiente de variación de los factores de respuesta y la desviación estándar relativa de la pendiente fueron inferiores al normado como máximo para estos indicadores: 5 y 2 %, respectivamente, considerados estimadores puntuales que permiten caracterizar la variabilidad. El valor obtenido del coeficiente de variación del factor de respuesta demostró que existe variabilidad en la relación respuesta y concentración para cada nivel evaluado. Se demuestra con los resultados obtenidos la linealidad del método propuesto.4,5
En los estudios de la repetibilidad (tabla 2) realizado a una misma muestra, por el mismo analista, el mismo día, a través de seis réplicas, se alcanzó un coeficiente de variación adecuado, lo que demuestra la buena precisión del método; se observa una variabilidad de los resultados dentro de los límites establecidos para los métodos cromatográficos: CV ≤2,0 %.4,5
Los valores que se obtienen en los estudios de precisión intermedia, de las pruebas de Fischer y t de Student, para el estudio de la precisión intermedia demuestran que no existen diferencias significativas entre las precisiones alcanzadas por los analistas en diferentes días para un 95 % de confianza, ya que el valor de F calculado fue menor que la F tabulada, estos resultados permiten establecer que las precisiones son similares (tabla 3). Al realizar las pruebas de la t de Student, el valor calculado resultó menor que el tabulado, para un 95 % de confianza, lo cual demuestra que no existen diferencias significativas entre las medias alcanzadas, con un nivel de significación de un 5 %.
]]> El valor de porcentaje de recobro estuvo dentro de los límites establecidos para los métodos cromatográficos (98‒102 %) y el valor del coeficiente de variación para cada uno de los niveles de concentración estudiados resultó ser menor que el 2 %. En la influencia del factor concentración sobre la variabilidad de los resultados de la exactitud al aplicar la prueba de Cochran se obtuvo que la G calculada fuer menor que la G tabulada para un 95 % de confianza, k=3 y n=3; por lo tanto, las varianzas de las concentraciones empleadas son equivalentes, lo que indica que la concentración no influye en la variabilidad de estos. Al realizar la prueba de significación entre la recuperación media y el 100,0 % de recuperación, el coeficiente de variación fue adecuado, el valor de t calculada resultó menor que la t tabulada. En el rango seleccionado en el estudio de exactitud, los valores de porcentaje de recobro están dentro de los límites establecidos para los métodos cromatográficos (98,0‒102,0 %) y los valores del coeficiente de variación, para cada uno de los niveles de concentración estudiados, fueron menores que el 2 %.4,5ESTUDIO DE ESTABILIDAD
El conjunto de los resultados obtenidos en el estudio de estabilidad acelerada a 40±2 ºC y 75±5 % de HR, demostraron la estabilidad del producto. Los valores de pH y las características organolépticas se encuentran dentro de los límites establecidos. Sin embargo, se evidencia una disminución de más de un 8 % en la determinación del contenido de principio activo, la disminución es inferior al límite establecido (10 %) para productos de uso veterinario. Se demostró la estabilidad térmica del producto ya que después de transcurridos seis meses se mantuvo la concentración conforme con los límites establecidos en las especificaciones de calidad del producto terminado.
En el estudio de vida de estante realizado, no se observaron cambios en los aspectos organolépticos, ni en el pH y se evidencia una disminución de más de un 7 % en la determinación del contenido de principio activo, valor que se encuentra dentro de los límites establecidos para el registro de medicamentos de uso veterinario, se demostró que el producto cumple con las evaluaciones microbiológicas realizadas al inicio y a los 12 meses, por lo que se evidenció la estabilidad del producto terminado por un periodo de un año, ya que el producto se mantuvo estable en el tiempo de duración del estudio.
La evaluación del desempeño del método analítico desarrollado demostró la confiabilidad del mismo. Se estableció un año como fecha de vencimiento en las condiciones señaladas.
REFERENCIAS BIBLIOGRÁFICAS
1. Martindale The Complete Drug Reference. 36th Edition. London: Pharmaceutical Press; 2009. p. 1203–1206.
2. Donald C. Veterinary drug handbook 4ta edition. Minneapolis, Minnesota: Plumb; 2004. p. 531 – 534.
3. The United States Pharmacopoeia Convention. USP32. [CD-ROM]; Rockville: Mack Printing; 2009.
4. Centro Estatal para el Control de Medicamentos. Regulación 41/07. Validación de Métodos de analíticos. La Habana, Cuba: CECMED; 2007. [citado 26 agosto 2014] Disponible en http://www.cecmed.sld.cu/Pages/Reg_EvalEL.htm
5. Dierksneier G. Métodos Cromatográficos. La Habana: Ed. Científico – Técnica; 2005. p. 1- 4, 256-412.
6. Guía para el registro de uso veterinario en el Instituto de medicina veterinaria. La Habana, Cuba: Instituto de Medicina Veterinaria; 2012.
]]> Recibido: 26 de agosto de 2014.
MSc. Caridad Margarita García Peña. Centro de Investigación y Desarrollo de Medicamentos (CIDEM). Ave. 26 No. 1 605 entre Boyeros y Puentes Grandes. CP 10 600. Plaza de la Revolución, La Habana, Cuba. Correo electrónico: caridadgp@infomed.sld.cu
]]>