Evaluación del uso del esquema de paclitaxel con carboplatino en pacientes con cáncer de mama metastásico
Paclitaxel-carboplatine scheme assessment applied in patients presenting with metastatic breast cancer
Jorge L. Soriano GarcíaI; Mayté Lima PérezII; Noyde Batista AlbuerneII; Joaquín González GonzálezII; Salvador Manuel PanguiIII
]]>
I Especialista de II Grado en Oncología. Hospital Clinicoquirúrgico "Hermanos Ameijeiras", La Habana, Cuba.
II Especialista de I Grado en Oncología. Hospital Clinicoquirúrgico "Hermanos Ameijeiras", La Habana, Cuba.
III Especialista de I Grado en Oncología. Hospital Central de Luanda, Angola.
RESUMEN
Introducción: La quimioterapia con paclitaxel es fundamental en el cáncer de mama metastásico (CMM). Se evaluó la eficacia y seguridad del uso del paclitaxel combinado con carboplatino. Métodos: Se realizó un estudio retrospectivo y descriptivo de 63 pacientes tratadas en el Servicio de Oncología del Hospital "Hermanos Ameijeiras", desde enero de 2001 hasta diciembre de 2005, con confirmación histológica de cáncer de mama y enfermedad metastásica, tratadas previamente con antraciclinas (en la adyuvancia). Resultados: Hubo predominio de éstas en etapa premenopáusica; la mediana de edad fue de 44,2 años. Predominaron los receptores hormonales negativos y la presencia de un solo sitio metastásico, El hueso y el pulmón fueron las localizaciones metastásicas más comunes, 26,4 y 21,8 %, respectivamente. El índice de respuesta global fue 33,3 %. No hubo diferencias significativas en los índices de respuestas según las variables pronósticas. La supervivencia a 1, 2 y 3 años fue de 60, 46,4 y 28,2 %, respectivamente. La mediana de supervivencia fue de 16,2 meses. Las variables asociadas a mejor pronóstico fueron índice de Karnofsky ³ 60 %, receptores hormonales positivos y presencia de un solo sitio metastásico. La enfermedad diseminada en hueso, partes blandas y piel tiene mejor pronóstico. Las principales toxicidades fueron: hematológicas, neurológicas y digestivas. El promedio de procesos adversos por paciente fue de 2,6 y 20 % de estos fueron grado 3-4. El incremento de las enzimas hepáticas provocó mayor cantidad de suspensiones de tratamiento. Conclusiones: Los esquemas de combinación con paclitaxel tienen buen perfil de seguridad y eficacia aceptable.
]]>
Palabras clave: Cáncer de mama metastásico, quimioterapia, taxanos.ABSTRACT
Introduction: Paclitex chemotherapy is essential in metastatic breast cancer (MBC). We assessed effectiveness and safety of combined use of carboplatine. Methods: We made a descriptive and retrospective study of 63 patients treated in Oncology Service of "Hermanos Ameijeiras" Surgical Clinical Hospital from January, 2001 to December, 2005 with a histological confirmation of breast cancer, and metastatic disease, previously treated with anthracyclins (in adjuvant therapy). Results: There was a predominance of negative hormonal receptors, and presence of an only metastatic site. Bone and lungs were the more common metastatic locations, 26.4 % and 21.8 %, respectively. Global response rate was of 33.3 %. There were not significant differences in response rate by prognostic variables. Survival at 1, 2, ant 3 years was of 60, 46.4 and 28.2 %, respectively. Survival average was of 16,2 months. Variables associated with a better prognosis were a Karnofsky rate ³ 60 %, positive hormonal receptors and presence of an only metastatic site. Disease disseminated in bone, soft tissues, and skin had a better prognosis. Main toxicities were: hematologic, neurologic, and digestives. The adverse processes average by patient was of 2.6 and the 20 % of these ones were 3-4 degrees. Increment in hepatic enzymes caused a higher level of treatment suspension. Conclusions: Combined schemes with Paclitaxel have a good and acceptable profile of safety and effectiveness.
Key words: Metastatic breast cancer, chemotherapy, taxanes.
INTRODUCCIÓN ]]>
El cáncer de mama en Cuba ocupa el primer lugar dentro de las causas de incidencia y el segundo en mortalidad, entre las neoplasias malignas del sexo femenino, con una tasa de incidencia en el 2005 de 33,9 por 100 000 mujeres, mientras que la tasa de mortalidad en el 2007 fue de 15,1 y en ese año representó el 17 % de las defunciones por cáncer en este sexo. En los países latinoamericanos y africanos ocupa el segundo lugar, después del cáncer de cuello uterino, y en el continente asiático es también el segundo después del cáncer gástrico. El número de casos nuevos al nivel mundial es de 720 000 por año.1-3El carcinoma de mama metastásico continúa siendo en estos momentos una de las principales causas de muerte por cáncer en la mujer, pese a los grandes avances alcanzados gracias al pesquizaje, que ha incrementado de forma notable el diagnóstico en etapas tempranas de la enfermedad, y el desarrollo de terapéuticas adyuvantes. Al menos 30 % de las pacientes sin afectación ganglionar inicial y entre 50 y 60 % de las pacientes con ganglios positivos presentarán a lo largo de su vida una recaída de la enfermedad.1 A este grupo de pacientes, hay que añadir el 7-10 % de los casos de cáncer de mama que presentan metástasis al momento del diagnóstico (estadio IV de la clasificación UICC).4
Los objetivos principales de la terapéutica en esta situación de enfermedad son la óptima paliación y la prolongación de la supervivencia global. Es importante el uso de todos los tratamientos posibles para conseguir el máximo control de síntomas y prevenir complicaciones, alterando lo mínimo posible, la calidad de vida de la paciente. Una de las principales armas con las que contamos en el tratamiento de la enfermedad metastásica es la quimioterapia. Múltiples agentes citotóxicos han demostrado su actividad en el tratamiento del carcinoma de mama metastásico, con índices de respuesta muy variables.5
Dentro de los nuevos fármacos incorporados al tratamiento del cáncer de mama están los taxanos (paclitaxel y docetaxel). El paclitaxel es derivado de la Taxus brevifolia. Este medicamento promueve la polimerización y estabilización de la tubulina, forma microtúbulos e inhibe su normal disociación, interfiere con la formación del huso mitótico, se trastorna la reorganización de los microtúbulos, los cuales participan en actividades vitales de las células.6
El objetivo del presente trabajo es evaluar la eficacia y la seguridad del uso del paclitaxel en combinación con carboplatino en pacientes con cáncer de mama metastásico evolutivo, luego de haber utilizado algún régimen de antraciclinas en la quimioterapia adyuvante a la cirugía del tumor primario.
MÉTODOS
Se realizó un estudio retrospectivo y descriptivo desde enero de 2001 hasta diciembre de 2005, de pacientes tratadas en el Servicio de Oncología del Hospital Clinicoquirúrgico "Hermanos Ameijeiras", seleccionadas según criterios de elegibilidad. ]]>
Criterios de inclusión
- Pacientes del sexo femenino.
- Confirmación histológica de cáncer de mama.
- Enfermedad metastásica evolutiva.
- Tratamiento previo con antraciclinas en la adyuvancia.
- Edad ³ 18 años y £ 80 años.
- Estado general clasificados en la escala Eastern Cooperative Oncology Group (ECOG) £ 2 (índice de Karnofsky ³ 60 %).
- Expectativa de vida mayor de 6 meses. ]]>
- Funcionamiento normal de los órganos y de la médula ósea, definidos por: leucocitos ³ 3 000/mL; conteo absoluto de neutrófilos ³ 1 500/mL; plaquetas ³ 100 000/mL; bilirrubina total y ALAT/ASAT £ 2,5 LSN; aclaramiento de creatinina ³ 60 mL/min/1,73 m2.
Se incluyeron en el estudio 63 pacientes que reunieron los requisitos antes mencionados. El resto de las pacientes (21) fueron excluidas del trabajo por las siguientes razones: 17 habían recibido algún tratamiento previo a los taxanos en el estado metastásico y 4 tenían un índice ECOG > 2.
Plan de tratamiento
El tratamiento consistió en: paclitaxel a dosis de 175 mg/m² (en infusión de 3 h) con premedicación de: difenhidramina, ranitidina y dexametasona; más carboplatino a dosis de 350 mg/m² en infusión de 1 h, cada 3 sem. La profilaxis antiemética se realizó con anti-serotoninérgicos y esteroides del tipo del ondansetron y dexametasona. Las dosis utilizadas fueron las que convencionalmente se utilizan para prevenir la emesis aguda y retardada, contempladas en los documentos de trabajo del servicio.
]]> Evaluación
La evaluación basal consistió en: examen radiográfico simple de tórax, ecografía abdominal, gammagrafía ósea y examen radiográfico selectivo y/o TAC y/o RMN (en dependencia de cada caso), ecografía mamaria y mamografía (en caso de requerirlo). La evaluación de seguimiento fue la siguiente: exámenes imagenológicos en dependencia de la evolución de cada paciente. El examen físico, los exámenes hematológicos y hemoquímicos se realizaron cada 21 d, previo a cada tratamiento, y luego de finalizado, cada 28 d. Los exámenes imagenológicos fueron realizados según los síntomas y en caso de no presentar ninguno, cada 3 meses.
La evaluación de respuesta se realizó según los criterios de respuesta del sistema RECIST (JNCI. 2000;92:205-16).], que se basa en la suma de los diámetros más largos (unidimensional), en lugar de la suma de los productos, a partir de las 4 sem de comenzar el tratamiento, mientras que para evaluar la toxicidad, se utilizó la clasificación de toxicidad del NCI-CTC [Cancer Therapy Evaluation Program, Common Terminology Criteria for Adverse Events, Version 3.0, (http://ctep.cancer.gov), Publish Date: June 10, 2003]. En la valoración de toxicidad sólo se recogió el mayor grado de toxicidad y complicación registrado por cada paciente.
Análisis estadístico
Se utilizaron métodos de estadística descriptiva para el análisis de las características demográficas y médicas de los pacientes. La supervivencia global fue estimada mediante el método de Kaplan-Meier y la distribución de supervivencia fue comparada usando el método de log-rank.
RESULTADOS ]]>
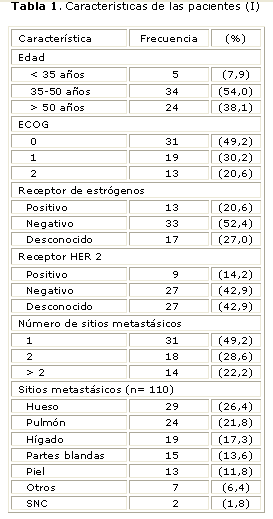
Se observó predominio de la etapa premenopáusica entre las 63 pacientes estudiadas, el grupo de edad más representado fue el de 35-50 años, que representa más del 50 % de la muestra (tabla 1). La mediana de edad es de 44,2 años. Aproximadamente, el 80 % de las pacientes presentaron un estado general muy bueno (ECOG 0-1).
Predominaron los receptores hormonales negativos, mientras que en el de HER 2, hubo igual distribución de los negativos con respecto a los que no se les determinó este receptor. Aproximadamente, en la mitad de las pacientes se encontró un solo sitio metastásico, mientras que el hueso y el pulmón fueron las localizaciones metastásicas más frecuentemente halladas en el 26,4 y el 21,8 %, respectivamente.
En la tabla 2 se pueden apreciar las características generales de las pacientes incluidas en el estudio en relación con los antecedentes de la enfermedad maligna mamaria. Predominó la histología ductal infiltrante y un pobre grado de diferenciación, así como los tumores mayores de 2 cm y la presencia de ganglios positivos, en casi el 90 % de las pacientes. Por etapas clínicas, al 80 % de las pacientes se les diagnosticó la enfermedad en una etapa III, y de éstas, la gran mayoría en etapa IIIb. A más del 60 % de las pacientes se les diagnosticó la enfermedad metastásica con un intervalo libre de enfermedad corto (menos de 24 meses).
El índice de respuestas completas más el de la parcial fue de 33,3 % (fig.). En cuanto al análisis de la respuesta al tratamiento en relación con las variables pronósticas, solo hubo diferencias, aunque no estadísticamente significativas, en la localización de las metástasis (tablas 3 y 4).
]]>

La mediana de supervivencia fue 16,2 meses, mientras que la supervivencia a 1, 2 y 3 años, fue de 60; 46,4 y 28,2 %, respectivamente. En la tabla 5 se exponen los resultados de la supervivencia a 1 y 3 años en relación con determinadas características, las más significativas (asociada a un mejor pronóstico) fueron el buen estado general, los receptores hormonales positivos y el reducido número de sitios metastásicos. Cuando se hace este mismo análisis para las localizaciones y el tipo de metástasis, la presencia de enfermedad diseminada en hueso, partes blandas y piel le confiere un mejor pronóstico que las localizaciones viscerales (tabla 6).
La toxicidad de la quimioterapia con paclitaxel combinado con carboplatino está representada en la tabla 7, donde se observa que las principales toxicidades están relacionadas con la esfera hematológica, neurológica y digestiva. El promedio de procesos adversos por paciente fue de 2,6. El 20 % de los procesos adversos fueron clasificados como grado 3-4 y, dentro de éstos, la anemia y el incremento de las enzimas hepáticas fueron las más frecuentes. Esta última toxicidad provocó el mayor número de suspensiones al tratamiento.
DISCUSIÓN
En este estudio, el mayor número de mujeres se presentó entre 35 y 50 años de edad y no hubo diferencias significativas en cuanto al color de la piel. En relación con el resto de las características de nuestras pacientes, no hay mucha diferencia en comparación con las de otros estudios.7,8 Los diferentes ensayos clínicos en CMM según el pronóstico, cuando se han utilizado antraciclinas como tratamiento adyuvante, han sido contradictorios. Se ha postulado que el uso de antraciclinas en la adyuvancia puede causar emergencia de clones celulares resistentes a estos fármacos y, por tanto, limitar el claro beneficio de su uso.9,10 Actualmente, es más extendido su uso como adyuvante, por lo que constituye una "barrera" a vencer en el diseño de nuevos ensayos clínicos, o en la interpretación de éstos, cuando se evalúan nuevos fármacos en el CMM.
Lamentablemente, no se les pudieron determinar los receptores hormonales ni el HER 2, a un mayor número de pacientes, por no disponerse de los bloques de las biopsias de los tumores primarios de mama, fundamentalmente de casos remitidos al servicio, procedentes de otros hospitales. Estos marcadores biológicos son considerados marcadores predictivos de respuesta11-14 y la determinación de ellos se ha convertido en uno de los elementos más importantes en la decisión terapéutica. Debemos enfatizar en la posibilidad de centralizar estos recursos, pues la variabilidad que existe en la determinación de estos receptores y su alto costo, hacen que esta medida organizativa cobre mayor fuerza en países con recursos limitados, como el nuestro.
El 80 % de los tumores de mama son carcinomas ductales infiltrantes,14 lo cual se corresponde con lo hallado en este estudio. Cuando se analizan las características de la enfermedad al momento del diagnóstico del tumor primario, se puede observar que la mayoría de las pacientes tienen factores de muy alto riesgo de recaída y metástasis a distancia. Al tener en cuenta el factor pronóstico más importante (el compromiso ganglionar), se halló que la mayoría (más del 65 %) tenía compromiso de más de 3 ganglios axilares. El riesgo global de recaída es del 20 al 30 % a 10 años después de la cirugía en las pacientes sin compromiso axilar (N0), mientras que es del 50 al 60 % en las pacientes con ganglios positivos (N+). En el presente estudio, este porcentaje es mucho mayor, dado que casi el 50 % de las pacientes tenían un pobre grado de diferenciación y más del 80 % se hallaban inicialmente en etapa III, lo que habla de un grado de avance considerable de la enfermedad, peor comportamiento de las variables biológicas y mayor "agresividad" clínica de la enfermedad. De ahí que el intervalo libre de enfermedad (ILE) sea tan corto y que más del 60 % evolucione hacia enfermedad metastásica en menos de 2 años.
Los factores que tienen valor pronóstico independiente en relación con la supervivencia son: número de sitios metastásicos, ILE corto y uso de antraciclinas en el tratamiento adyuvante. Los 2 primeros han sido relacionados clínicamente con mayor capacidad para causar metástasis y mayor proliferación celular. Estos factores mantienen su valor, a pesar del uso de tratamientos adyuvantes.15,16
Para determinar los posibles sitios metastásicos, es necesario el cumplimiento estricto de protocolos de actuación,17 pues de lo contrario, podría sub-estadiarse el caso y no valorar exactamente la carga tumoral real y, por tanto, no poder seleccionar la terapéutica más racional. Deben seleccionarse los métodos diagnósticos más fiables, racionales y factibles en la detección de los probables sitios metastásicos, una vez que se sospeche la presencia de CMM.
El índice global de respuestas es bajo, en comparación con el de otros estudios, pero esto se justifica, en parte, por las características generales de la muestra, en la que puede observarse mayor número de factores de mal pronóstico que en la de los otros estudios de referencia.18,19 En el CMM existe una relación significativa demostrada entre respuesta al tratamiento y supervivencia.20 El índice de respuesta completa (RC) fue de 14,3 % (IC 95 %: 12,5-16,3 %) y el de respuesta parcial (RP), de tan solo 19,1 % (IC 95 %: 16,9-21,5 %), mientras que la supervivencia global (SV) fue 39,8 y 21,6 meses, respectivamente. La SV global de las pacientes que progresaron (n= 20) fue tan solo 3,6 meses. Estos resultados demuestran lo anteriormente planteado e indican que la expectativa de vida de las pacientes con CMM puede ser incrementada significativamente si es instaurado un régimen de tratamiento efectivo y administrado precozmente, dado que más del 60 % de las pacientes iniciaron el tratamiento para su CMM, luego de 2 meses del diagnóstico de su enfermedad metastásica. ]]>
En el presente estudio se empleó la SV global como variable principal de respuesta (end point), y de eficacia, que es considerada aún como la más objetiva e incuestionablemente más importante en las pacientes con CMM. Una limitación del estudio fue no evaluar la supervivencia libre de progresión (SLP) y el tiempo para progresión (TPP). Estas variables, si bien en los últimos años se están empleando cada vez más en los diferentes estudios de CMM,21,22 tienen un gran inconveniente en los estudios retrospectivos como el nuestro, pues la ausencia de puntos de evaluación de la respuesta muy bien definidos como sucede en los estudios prospectivos, entre los que se incluyen los ensayos clínicos, hace que no exista uniformidad y exactitud para determinar el momento específico de progresión de la enfermedad.La posible influencia del tipo de tratamiento adyuvante inicial en el patrón de recaída fue abordada por el Grupo Internacional de Estudio del Cáncer de Mama (IBCSG),23 el cual realizó una serie de estudios con quimioterapia adyuvante realizados en la década de los 80, y en la que concluyeron que, al parecer, con la quimioterapia adyuvante empleada en esa época se puede modificar el patrón de recaídas locales, pero no así, las viscerales u óseas. La localización de la recaída tiene una notable influencia en la supervivencia global de las pacientes, así las mujeres que presentan únicamente enfermedad ósea24 tienen una mediana de supervivencia de 28 meses, comparada con los 13 meses de las que presentan enfermedad visceral. Dentro de la afectación visceral, no todas tienen un comportamiento homogéneo y las pacientes con recaídas en hígado, sistema nervioso central, pericardio y peritoneo sobreviven significativamente menos que las que lo hacen en pleura o pulmón. Por otra parte, la expresión hormonal del tumor primario parece predefinir otro patrón de recaídas: aquellas con tumores que no expresan receptores hormonales (no endocrino respondedoras) presentan peor pronóstico y tienen mayor índice de recaídas al nivel visceral y con mayor precocidad, mientras que las pacientes con receptores hormonales positivos (endocrino respondedoras) tienen un índice de recaída menor y, fundamentalmente, en hueso y partes blandas.25
En una revisión sistemática, en la que se incluyeron 21 estudios al azar en CMM, compararon protocolos de tratamiento con taxanos versus no taxanos y se puso en evidencia el beneficio de la utilización de este fármaco en esos casos. No obstante, cuando se limitó su utilización a la primera línea del CMM, los resultados no fueron altamente significativos.26
Verma7 señala en su estudio que el paclitaxel es considerado como la primera opción de tratamiento en pacientes con CMM que han recibido tratamiento con antraciclinas o refractarios a éstas. Antes del uso de los taxanos, el grado de respuesta en pacientes con tumor resistente a antraciclinas era menos del 10 % y la SV global, inferior a 6 meses.
En un estudio retrospectivo27 donde compararon paclitaxel y carboplatino con el paclitaxel y epirubicina (como tratamiento de primera línea en CMM), se demostró que no hubo diferencias en la SV global, pero el TPP fue mejor en el brazo que contenía platino y con un perfil de seguridad y calidad de vida superior. En otros estudios fase II y III, Pérez28 observó que las combinaciones de taxanos con carboplatino tenían mejor eficacia en el CMM, que la utilización del carboplatino solo, o alguno de los taxanos por separado. Ambos reportes admiten la utilización de estas combinaciones particularmente cuando existe contraindicación al uso de las antraciclinas o cuando ésta se ha usado en tratamientos adyuvantes previos.
El primer ensayo fase III de comparación directa entre paclitaxel y docetaxel en CMM se realizó entre 1994 y el 2002.29 Los principales resultados demostraron que no existían diferencias significativas entre ambos fármacos en cuanto a índices de respuestas, pero en SV y TPP, los resultados favorecieron al brazo de docetaxel, aunque con mayor número de toxicidades (fundamentalmente grados 3 y 4), con mayor incidencia de neutropenias febriles y muertes relacionadas, y con un costo económico directo e indirecto superior. Las combinaciones de taxanos con las sales de platino son generalmente mejor toleradas que las combinaciones de taxanos con antraciclinas, además que los perfiles de toxicidad de estos fármacos no se solapan.28
La dosis de administración del paclitaxel en el tratamiento de primera línea del CMM o como tratamiento de rescate se ha ensayado en un rango de 135-250 mg/m2 y en diferentes tiempos de infusión (3-96 h) administrada cada 21 d. El incremento de la dosis produce mayor toxicidad y no eleva el índice de respuestas. Por consenso general se ha aceptado que el paclitaxel en el CMM debe ser administrado a dosis de 175 mg/m2 y con un tiempo de infusión de 3 h. No obstante, se ha podido observar que la administración semanal de paclitaxel, a una dosis de 80 mg/m2, es generalmente muy bien tolerada, con toxicidad hematológica limitada, neurotoxicidad manejable y rara neutropenia febril.30,31
A estas ventajas anteriormente mencionadas para la administración semanal de paclitaxel, hay que añadir los estudios realizados en el caso neo-adyuvante, en los que se ha visto la eficacia superior de este régimen. Múltiples factores pueden contribuir a esto: mayor exposición de células tumorales en división a los efectos citotóxicos del paclitaxel con frecuencia semanal; mayor inhibición del recrecimiento tumoral entre los ciclos (densidad de la dosis); incremento del índice terapéutico del paclitaxel; disminución de la probabilidad de emergencia de subpoblaciones celulares malignas resistentes e incremento de los efectos apoptóticos y antiangiogénicos del paclitaxel.32-34
El perfil de seguridad del uso de paclitaxel en combinación con el carboplatino en nuestro estudio fue muy similar al reportado en otras publicaciones.18,26,27,35,36 No obstante, la disponibilidad y el uso precoz de los factores estimulantes granulocíticos y eritropoyéticos en aquellos casos que lo requirieron (según los protocolos de su uso), determinaron una toxicidad de anemia y neutropenia mucho menor que en el resto de los estudios de referencia. No se produjeron toxicidades cardíacas, ni reacciones de hipersensibilidad.
La decisión para el tiempo de iniciación y continuación del tratamiento con quimioterapia, hormonoterapia o de agentes biológicos, en el caso de metastásis, debe ser individualizada. Esta selección de tratamiento debe ser guiada por:32-34,37 el estado de los receptores hormonales, el estado del receptor HER-2/neu, la duración del intervalo libre de enfermedad (< 2 años vs. > 2 años), el tipo y localización de las metástasis (visceral vs. no-visceral), los tratamientos previos y sus efectos y tolerancia, los síntomas y las comorbilidades asociadas, las preferencias de la paciente, la disponibilidad y el acceso al tratamiento. ]]>
En conclusión, este trabajo, a pesar de las limitaciones propias de los estudios retrospectivos, demostró que la combinación del paclitaxel con carboplatino es un esquema de quimioterapia eficaz y seguro en las pacientes con CMM. El incremento en número y diversidad de agentes citotóxicos ha abierto las puertas al tratamiento más efectivo en este tipo de pacientes y los taxanos constituyen una de las piedras angulares en el tratamiento. Su uso más eficaz en el futuro dependerá de los resultados de las investigaciones en el área de la genómica, que determinarán qué subgrupos de pacientes se pueden beneficiar mucho más de la acción de éstos en combinación (como el presente estudio), en monoterapia o administrado de forma secuencial a otros citotóxicos. Hoy día, no existe "la mejor quimioterapia estándar", por lo que la selección de tratamiento debe ir encaminada a optimizar la eficacia, incrementar la calidad de vida y reducir la toxicidad y los costos sanitarios. De ahí que el CMM constituya un desafío y un reto terapéutico para el oncólogo médico.
REFERENCIAS BIBLIOGRÁFICAS
1. González M, Isla M. Afecciones mamarias más frecuentes. En: Álvarez Sintes, editor. Temas de Medicina General Integral. Vol. 2. La Habana: Editorial Ciencias Médicas;2001. p. 786.
2. Instituto Nacional de Oncología y Radiobiología. Registro Nacional de Cáncer 2004-2005. Ciudad de La Habana, 2007.
3. Viladiú P, López JJ. Aspectos generales del cáncer de mama. Oncología Médica. 2000;(2):877.
4. Singletary SE, Connolly JL. Breast cancer staging: working with the sixth edition of the AJCC cancer staging manual. CA Cancer J Clin. 2006;56:37-47.
5. Lluch A, Paz L, Solá C. Quimioterapia en cáncer de mama. Oncología Médica. 2000;(2):918.
6. Morris PG, Fornier MN. Novel anti-tubulin cytotoxic agents for breast cancer. Expert Rev Anticancer Ther. 2009;9:175-85.
7. Verma S, Trudean S, Pritchard K, Oliver T. The role of the taxanes in the management of metastatic breast cancer. Practice Guideline Report # 1-3, April 2003.
8. Hortobagyi G. Treatment of Breast Cancer. New Engl J Med. 2007;14:980.
9. Venturini M, Bruzzi P, Del Mastro L, Garrone O, Bertelli G, Guelfi M, et al. Effect of adjuvant chemotherapy with or without anthracyclines on the activity and efficacy of first-line cyclophosphamide, epidoxorrubicin and fluoruracil in patients with metastatic breast cancer. J Clin Oncol. 1996;14:764-73.
10. Alba E, Ribelles N, Sevilla I, Rueda A, Alonso L, Márquez A, et al. Adjuvant anthracycline therapy as a prognostic factor in metastatic breast cancer. Breast Cancer Res Treat. 2001;66:33-9.
11. Diaz LK, Sneige N. Estrogen receptor analysis for breast cancer: current issues and keys to increasing testing accuracy. Adv Anat Pathol. 2005;12:10-9.
12. Wells CA, Sloane JP, Coleman D. Consistency of staining and reporting of oestrogen receptor immunocytochemistry within the European Union —an inter-laboratory study. Virchows Arch. 2004;445:119-28.
13. Hauser-Kronberger C, Dandachi N. Comparison of chromogenic in situ hybridization with other methodologies for HER2 status assessment in breast cancer. J Mol Histol. 2004;35:647-53.
14. Wilkinson NW, Shahryarinejad A, Winston JS. Concordance with breast cancer pathology reporting practice guidelines. J Am Coll Surg. 2003;196:38-43.
15. Fukuda H, Takue Y, Narabayashi M, Adachi I, Takashima S. Construction and validation of a practical prognostic index for patients with metastatic breast cancer. J Clin Oncol. 1998;16:2401-8.
16. Porter GJR, Evans AJ, Pinder SE, James JJ, Cornford EC, Burrell HC, et al. Patterns of metastatic breast carcinoma: influence of tumour histological grade. Clin Radiol. 2004;59:1094-8.
17. Soriano J. Protocolo de actuación asistencial en cáncer de mama. En: Manual de Prácticas Médicas del Hospital Hermanos Ameijeiras. 2 ed. ISBN 978-959-212-392-2. La Habana, 2008. Disponible en: http://www.hospitalameijeiras.sld.cu/hha/mpm/documentos/ONCOLOGIA/PA/CANCER%20DE%20MAMA.pdf (Fecha de acceso: 15 de enero del 2009).
18. Carrick S, Parker S, Thornton CE, Ghersi D, Simes J, Wilcken N. Single agent versus combination chemotherapy for metastatic breast cancer. Cochrane Database of Systematic Reviews 2009, Issue 2. Art. No.: CD003372. DOI: 10.1002/14651858.CD003372.pub3.
19. Tubiana-Hulin M. How to maximize the efficacy of taxanes in breast cancer. Cancer Treat Rev. 2005;31 (Suppl 4):S3-S9.
20. Smith I. Goals of treatment for patients with metastatic breast cancer. Sem Oncol. 2006;33:S2-S5.
21. Di Leo A, Bleiberg H, Buyse M. Overall survival is not a realistic end point for clinical trials of new drugs in advanced solid tumors: a critical assessment based on recently reported phase III trials in colorectal and breast cancer. J Clin Oncol. 2003;21:2045-7.
22. Saad ED, Katz A. Progression-free survival and time to progression as primary end points in advanced breast cancer: often used, sometimes loosely defined. Ann Oncol. 2009;20:460-4.
23. Goldhirsch A, Gelber RD, Price KN. Effect of systemic adjuvant treatment on first sites of breast cancer relapse. Lancet. 1994;343:377.
24. Pérez JE, Machiavelli M, Leone BA. Bone-only versus visceral-only metastatic pattern in breast cancer: analysis of 150 patients. Am J Clin Oncol. 1990;13:294.
25. Bezwoda W, Esser J, Dansey R. The value of estrogen and progesterone receptor determinations in advanced breast cancer. Cancer. 1991;68:867.
26. Ghersi D, Wilcken N, Simes J, Donoghue E. Taxane containing regimens for metastatic breast cancer (Cochrane Review). The Cochrane Library, Issue 2. 2005. Chichester UK: John Wiley and Sons Ltd, 2005.
27. Fountzilas G, Kalofonos HP, Dafni U. Paclitaxel and epirubicin versus paclitaxel and carboplatin as first-line chemotherapy in patients with advanced breast cancer: a phase III study conducted by the Hellenic Cooperative Oncology Group. Ann Oncol. 2004;15:1517-26.
28. Pérez EA. Carboplatin in combination therapy for metastatic breast cancer. Oncologist. 2004;9:518-27.
29. Jones SE, Erban J, Overmoyer B. Randomized phase III study of docetaxel compared with paclitaxel in metastatic breast cancer. J Clin Oncol. 2005;23:5542-51.
30. Winer EP, Berry DA, Woolf S. Failure of higher-dose paclitaxel to improve outcome in patients with metastatic breast cancer: cancer and leukemia group B trial 9342. J Clin Oncol. 2004;22:2061-8.
31. Pérez EA, Vogel CL, Irwin DH. Multicenter phase II trial of weekly paclitaxel in women with metastatic breast cancer. J Clin Oncol. 2001;19:4216-23.
32. Bernard-Marty C, Cardoso F, Piccart MJ. Facts and controversies in systemic treatment of metastatic breast cancer. Oncologist. 2004;9;617-32.
33. Beslija S, Bonneterre J, Burstein H, Cocquyt V, Gnant M, Goodwin P, et al. Second consensus on medical treatment of metastatic breast cancer. Ann Oncol. 2007;18:215-25.
34. Schwartzberg LS. Taxanes: a cornerstone of treatment for metastatic breast cancer. Comm Oncol. 2008;5 Suppl. 8:S3-S8.
35. Leyland-Jones B, Semiglazov V, Pawlicki M, Pienkowski T, Tjulandin S, Manikhas G. Maintaining normal hemoglobin levels with epoetin alfa in mainly nonanemic patients with metastatic breast cancer receiving first-line chemotherapy: a survival study. J Clin Oncol. 2005;23:5960-72.
36. Di Constanzo F, Manzione L, Gasperoni S, Bilancia D. Paclitaxel and mitoxantrone in metastatic breast cancer: a phase II trial of the Italian Oncology Group for Cancer Research. Cancer Invest. 2004;22(3):331-7.
37. Smith IE. Which tools can I use in daily clinical practice to improve tailoring of treatment for breast cancer? Treatment decision-making in advanced disease. Ann Oncol. 2008;19 Suppl. 7:VII51-VII57.
Recibido: 2 de marzo de 2009.
Aprobado: 2 de mayo de 2009.
]]>
Dr. Jorge L. Soriano García. Hospital Clinicoquirúrgico "Hermanos Ameijeiras". Servicio de Oncología. San Lázaro No. 701 entre Belascoaín y Marqués González, Centro Habana, Ciudad de La Habana, Cuba. Correo electrónico: soriano@infomed.sld.cu ]]>