Interferón alfa 2b recombinante más ribavirina en el tratamiento de la hepatitis crónica C
Recombinant Interferon alfa-2b plus Ribavirin in treatment of chronic hepatitis C
]]>
Yoan Antonio Sánchez RodríguezI; Enrique Arús SolerII; Bienvenido Grá OramasIII; Pedro López SauraIV; Hugo Nodarse CuníV
IEspecialista de I Grado en Gastroenterología. Instituto de Gastroenterología. La Habana, Cuba.
IIDoctor en Ciencias Médicas. Especialista de II Grado en Gastroenterología. Instituto de Gastroenterología. La Habana, Cuba.
IIIDoctor en Ciencias Médicas. Especialista de II Grado en Anatomía Patológica. Investigador Auxiliar. Profesor Auxiliar. Instituto Nacional de Gastroenterología. La Habana, Cuba.
IVDoctor en Ciencias Biológicas. Investigador Titular. Profesor Titular. Centro de Ingeniería Genética y Biotecnología. La Habana, Cuba. ]]>
VMáster en Ciencias Farmacéuticas. Investigador Agregado. Centro de Ingeniería Genética y Biotecnología. La Habana, Cuba.
RESUMEN
]]>
El virus de la hepatitis C se ha convertido en la causa principal de hepatitis crónica, cirrosis hepática, hepatocarcinoma, y trasplante de hígado a nivel mundial.
Palabras clave: Hepatitis crónica C, interferón a 2b, ribavirina, respuesta virológica sostenida.
ABSTRACT
The hepatitis C virus becomes in leading cause of chronic hepatitis, hepatic cirrhosis, hepatocarcinoma and liver transplant at world level.
OBJECTIVE: The aim of present study is to determine the virological, biochemical and histological course of patients presenting with Chronic hepatitis C under a combination of recombinant Interferon alfa-2b plus Ribavirin and to identify the main factors associated with the rates obtained of virological response. ]]>
METHODS: A non-controlled and multicenter phase IV clinical-therapeutical trial was sponsored by the Institute of Gastroenterology and the Genetics and Biotechnology Engineering Center from May, 2002 to May, 2006. Sample included 122 patients diagnosed with chronic hepatitis C fulfilling the predetermined inclusion and exclusion criteria. Recombinant Interferon alfa-2b (3 millions of t.i.d units) was used plus Ribavirin (1000 or 1200 mg daily depending on the body weight) during 48 weeks.
RESULTS: We achieved a sustained biochemical and virological response rate of 32.8 and 50.8 %, respectively at week 72. A 41.3,% from the total of patients had a histological improvement at the expense of reduction of fibrosis and a few changes in inflammation level.
CONCLUSIONS: Raking into account the global response rate achieved this combined treatment was considered effectiveness for chronic hepatitis C and we recommended to deepen in the knowledge of infection in Cuba, as well as in more efficient treatment options for this disease.
Key words: Chronic hepatitis C, Interferon a 2b, Ribavirin, sustained virological response.
INTRODUCCIÓN
]]>
El virus de la hepatitis C (VHC) desde su primera descripción en 19891 ha sido motivo de múltiples investigaciones.2,3 Es el mayor agente causal de hepatitis crónica, cirrosis hepática y carcinoma hepatocelular y se estima que ha infectado aproximadamente entre 170 y 200 millones de personas en el mundo.3,4Cuba, país en desarrollo, con una prevalencia de VHC de 0,7 %, mantiene una incidencia anual de 12 casos por 100 000 habitantes.5
El tratamiento actual contra este virus va encaminado a la obtención de la respuesta virológica sostenida (RVS), definida como la no detección del ARN-VHC en suero, 6 meses después de finalizada la terapia antiviral.
El empleo de los interferones en las hepatitis virales se justifica por su efecto antiviral, antiinflamatorio, antifibrótico y anticarcinogenético.6 Sin embargo, los resultados de la monoterapia con interferón (IFN) en pacientes naive (sin antecedentes de tratamiento antiviral o paciente virgen) con hepatitis crónica C (HCC), comprobaron que el régimen terapéutico de monoterapia con IFN solo permitía alcanzar hasta 17 % de RVS.7
En un ensayo clínico cubano controlado, aleatorizado, con IFN monoterapia durante 9 meses, se logró una tasa de respuesta bioquímica sostenida de 33,3 % en el grupo en tratamiento y 0 % para el grupo control, pero este ensayo tuvo la limitante de no contar con estudios virológicos.8
La combinación de la ribavirina con el IFN permite desarrollar una respuesta frente a varias proteínas virales de predominio CD 4 tipo 1, que podría justificar la RVS.9
En un ensayo clínico con terapia combinada, IFN más ribavirina, donde se estudiaron 912 pacientes con HCC, se obtuvo en el grupo que usó la combinación durante 48 sem, 38 % de RVS contra 13 % en el grupo que usó monoterapia con IFN por igual tiempo.10 Otros investigadores obtuvieron similares resultados con igual periodo de tratamiento.11,12
En otro estudio cubano, aleatorizado, a doble ciegas y controlado con 47 pacientes afectos de HCC y tratados con terapia combinada, se obtuvo un 65 % de negativización del ARN viral, 73 % de mejoría histológica y 72 % de normalización de las transaminasas. La evaluación global de los pacientes en este estudio mostró un 46 % de respuesta completa.13
Con el surgimiento del interferón pegilado se abre una nueva brecha en el tratamiento de la HCC.14 Se han realizado varios estudios con este medicamento, pero la investigación que devino pauta en el tratamiento de esta enfermedad fue la del griego Hadziyannes, et al.15 en la que con una serie de 1 311 casos, concluyó que el tratamiento con peginterferón a 2ª más ribavirina es efectivo y debe ser individualizado según el genotipo.
Con vistas a generalizar en nuestro país el uso de la terapia combinada IFN a 2b recombinante más ribavirina se realizó este estudio, encaminado a determinar la evolución virológica, bioquímica e histológica de pacientes crónicamente infectados por el virus de la hepatitis C, bajo tratamiento combinado con interferón a 2b recombinante más ribavirina durante 48 sem. Se procedió, además, a identificar los principales factores asociados a las tasas de respuesta virológica sostenida obtenidas al final del ensayo. ]]>
MÉTODOS
Se realizó un ensayo clínico fase IV, abierto, no controlado y multicéntrico, que rectoraron el Instituto de Gastroenterología y el Centro de Ingeniería Genética y Biotecnología, en el período de mayo de 2001 a mayo de 2006. Se estudiaron 122 pacientes con HCC y cifras de alanin aminotransferasas (ALAT), al menos, 2 veces por encima del valor normal, anticuerpos contra el VHC y ARN-VHC en suero, así como un daño hepático característico de hepatitis crónica según los resultados de una biopsia realizada en los 12 meses previos a su inclusión. Los pacientes reclutados fueron mayores de 18 años de edad y ofrecieron su consentimiento por escrito para participar en el estudio. Se excluyeron mujeres en edad fértil que no utilicen algún anticonceptivo no hormonal, embarazadas o que lacten, pacientes con cualquier enfermedad crónica descompensada, cifras bajas de hemoglobina o con historia de hipersensibilidad a alguno de los componentes de la terapia.
Se realizó un análisis por intención de tratar.
El interferón se indicó a una dosis de 3 millones de unidades, por vía intramuscular, 3 veces por sem y la ribavirina 2 veces al día por vía oral hasta cumplir con la dosis total de 1 000 o 1 200 mg/día según correspondiera de acuerdo al peso corporal, ambos durante 48 sem.
La terapia fue llevada a cabo de manera ambulatoria por lo que fue solicitada la colaboración del nivel primario de salud.
La eficacia primaria se evaluó por la respuesta virológica sostenida, definida por la negativización del PCR-ARN-VHC 24 sem después de finalizado el tratamiento, mientras que la eficacia secundaria estuvo dada por las cifras de ALAT y el resultado de la biopsia hepática a la sem 72. Las muestras de tejido hepático fueron evaluadas por un solo patólogo de acuerdo al Índice de actividad histológica de Knodell.
Para estudiar el comportamiento de las variables involucradas se estimaron las medidas de tendencia central y dispersión, así como la distribución de frecuencias. Se realizaron los análisis univariado y multivariado final (regresión logística múltiple) pertinentes, teniendo en consideración la naturaleza de cada variable y su distribución. ]]>
Para el procesamiento de los datos nos auxiliamos del Software Estadístico Profesional SPSS Versión 15.0.
RESULTADOS
La baja incidencia de pacientes con fibrosis hepática severa o cirrosis constituida 17(13,9 %), así como el puntaje de Knodell presente al inicio de la terapia, en nuestra serie, fueron similares a los reportados en otros estudios.10,11 El antecedente de patología hepática más frecuente fue la esteatosis y los porcentajes de presentación de pacientes naive y no respondedores fueron 59 y 41 % respectivamente.
El valor de la media para el índice de masa corporal (IMC) se encontró por encima del rango normal (18,5-24,9) lo que nos permitió conocer sobre la tendencia al sobrepeso y la obesidad presente en nuestros casos.
Los niveles de ARN-VHC fueron indetectables solo en 40 (32,8 %) pacientes al final del período de seguimiento, a pesar de haber obtenido una cifra mayor al final del tratamiento (Fig. 1).
La hemoglobina y las transaminasas, al contrario de lo que ocurrió con las plaquetas, experimentaron un rápido descenso con el inicio de la terapia, pero después se recuperaron y alcanzaron valores cercanos a aquellos pretratamiento. Al final de la terapia obtuvimos 105 (86,1 %) pacientes con cifras de ALAT normales, de los cuales solo 62 (50,8 %) continuaron con igual condición de manera sostenida, coincidiendo con lo reportado incluso, en relación con el empleo del interferón pegilado.14,15 (Fig. 2)
]]>
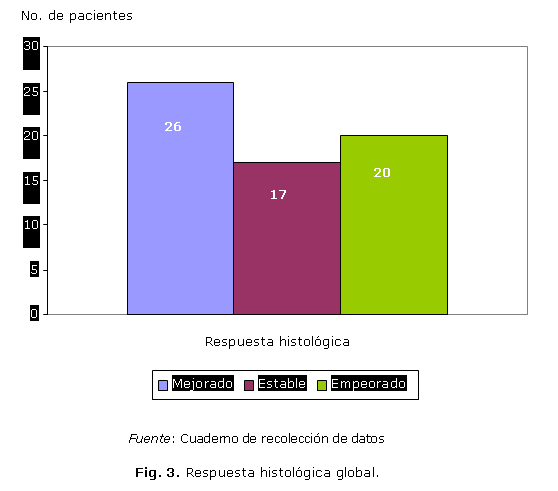
De los 63 casos en los que fue posible disponer de una segunda biopsia hepática, en 26 (41,3 %) pacientes se observó mejoría (Fig. 3). Dicho resultado se encuentra incluido dentro del rango de respuesta histológica que reportan la mayoría de los estudios sobre terapéutica en HCC, el cual oscila entre 30-63 %.10-12
El índice de masa corporal (IMC) elevado y la obesidad guardaron relación significativa con los valores de RVS (P=0,03). Se obtuvo una asociación importante entre el tipo de paciente (naive o no respondedor) y la RVS, lo que coincide ampliamente con lo reportado en otras casuísticas.10-12
Se demostró que la reducción de la dosis de ribavirina guardaba relación con la respuesta virológica a la semana 72, y al evaluar la asociación entre las variables obtenidas del análisis univariado y las tasas de RVS, la evaluación virológica a la sem 24 resultó la variable de mayor significación clínica y estadística (tabla).
DISCUSIÓN
La importancia de alcanzar la RVS se ha demostrado en diferentes estudios al mejorar la calidad de vida de los pacientes,16 mejorar la actividad histológica, e incluso el riesgo de desarrollar un hepatocarcinoma.17 Actualmente, continúan las investigaciones sobre los factores implicados en la selección de pacientes con mayores posibilidades de aclarar el virus, aunque un reciente estudio publicado demuestra la persistencia de pequeñas cantidades de ARN viral en macrófagos y linfocitos 9 años después de que se alcanzara una RVS.18 ]]>
Clínicamente, cuando evaluamos las tasas de RVS con el empleo de terapias modernas, es fácil comprender que aún falta mucho para llegar al tratamiento ideal que podamos considerar como efectivo sostenido en HCC. Por tal motivo, en nuestra opinión debe considerarse exitoso el haber obtenido un porcentaje no desestimable de pacientes en los que se logró, al menos, frenar la actividad necroinflamatoria y la fibrosis, como es el caso de los pacientes con histología estable tras cumplir el tratamiento.La categoría respuesta global depende directa y proporcionalmente de la RVS a la semana 72.19 A su vez, esta depende de una serie de factores claramente definidos como los relacionados con el propio paciente, los relacionados con el virus o con el tratamiento impuesto.14 De estos tres grupos, mención especial merecen los factores virológicos, pues se ha sugerido que una carga viral basal baja permite obtener tasas de RVS mayores que en los pacientes con carga viral pretratamiento más alta. Por otra parte, los pacientes con genotipos 2 y 3 son los mejores respondedores dentro de los 6 genotipos que se han descrito hasta el presente.15
En nuestro estudio no fue posible incluir estas dos variables (genotipo y carga viral) con vistas a esclarecer las causas del porcentaje menor de RVS obtenido (32,9 %) en comparación con otras series.9-12 No obstante, en trabajos muy recientes como el de Wright M et al.20 este autor obtiene una tasa de RVS muy similar a la nuestra (33 %) que, incluso, fue menor en los pacientes con genotipo 1. Los escasos estudios cubanos publicados sobre genotipaje de VHC realizados hasta la fecha resaltan la prevalencia del genotipo 1 en Cuba21 y esto, de cierta forma, acentúa la desventaja en la obtención de mayores tasas de RVS.
El mecanismo fisiopatológico que ha intentado explicar la relación inversa IMC-RVS, se apoya en la relación que existe entre el síndrome metabólico de obesidad-hígado graso y la resistencia a la insulina e hiperinsulinemia. La hiperinsulinemia tiene la capacidad de bloquear el efecto terapéutico del IFN, al disminuir su capacidad de producir PKR (proteína kinasa dependiente de ARN de doble cadena) e IRF-1 (enzima esencial en la síntesis endógena de IFN) y de potenciar la replicación viral.22-24
Se ha observado que en pacientes no respondedores a IFN existe un descenso en la expresión de los receptores para IFN alfa y en los niveles de ARNm que induce la síntesis de estos receptores. Las proteínas virales NS5A y E2 bloquean la inducción de ISG (grupo de genes sensibles al IFN) mediante la actuación sobre PKR y al inhibir la activación óptima de las proteínas STAT.25
Un factor fundamental para conseguir una RVS es la adherencia al tratamiento, y se ha postulado que el haber consumido, al menos, el 80 % de las dosis recomendada de IFN-ribavirina durante, al menos, el 80 % del tiempo recomendado, incrementa las posibilidades de respuesta frente a los menos cumplidores.16 En nuestra serie, demostramos que la adherencia al tratamiento fue una variable asociada significativamente a la RVS y ello pudiera contribuir a la interpretación de nuestros resultados.
Con la obtención de un valor de OR igual a 7,015 en relación con la variable evaluación virológica a la sem 24 se interpreta que es 7 veces más probable que un paciente que sea respondedor virológico a la sem 24, también lo sea a la sem 72, y desde el punto de vista práctico, este dato representa una herramienta de incalculable valor, incluso costo-efectivo, en la conducta a asumir frente a estos pacientes.
Finalmente, la administración de esta terapia combinada a pacientes afectos de HCC nos ha permitido obtener tasas de respuesta virológica y bioquímica sostenidas similares a las observadas en otros estudios. Un número no despreciable de pacientes presentó mejoría histológica dada por un descenso en la fibrosis sin modificación importante de la inflamación y, en muchos de ellos se logró, al menos, detener la actividad de la enfermedad. Aunque se identificaron una serie de variables asociadas con las tasas finales de RVS, la evaluación virológica y bioquímica a la sem 24 y el tipo de paciente previo a la terapia resultaron ser las más significativas.
]]>
REFERENCIAS BIBLIOGRÁFICAS
1. Choo QL, Kuo G, Weiner AJ. Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science. 1989;244:359-61.
2. Rodés J, Arroyo V, Bruguera M. Gastroenterología y Hepatología. 2006;92:101-49.
3. Penin F, Dubuisson J, Rey FA. Structural biology of hepatitis C virus. Hepatology. 2004;39:519.
4. Shepard CW, Finelli L, Alter MJ. Global epidemiology of hepatitis C virus infection. Lancet Infect Dis. 2005;5:558-67.
5. Dirección Nacional de Higiene y Epidemiología. Informe Anual 2008. La Habana: Ministerio de Salud Pública; 2008.
6. Neumann AU, Lam NP, Dahari H. Hepatitis C viral dynamics in vivo and the antiviral efficacy of interferon-alpha therapy. Science. 1998;282:103-7.
7. Myers RP, Poynard T, Regimbeau C. Interferon for interferon naïve patients with chronic hepatitis C. Cochrane Database Syst Rev. 2002;(2):CD000370.
8. Arús SE, Infante VM, Padrón GJ. Interferón alfa-2b Recombinante en Hepatitis C Crónica: Resultados del Tratamiento y Determinación de Anticuerpos Anti-interferón. Biotecnología Aplicada. 1997;14(4):242-7.
9. Kamal SM, Fehr J, Roesle B. Peginterferon alone or with ribavirin enhances HCV-specific CD4+ T-helper 1 responses in patients with chronic hepatitis C. Gastroenterology. 2002;123:1070-83.
10. McHutchison JG, Gordon SC, Schiff ER, Shiffman ML, Lee WM, Rustgi VK, et al. Interferon a 2b alone or in combination with Ribavirin as initial treatment for chronic hepatitis C. N Engl J Med. 1998;339:1485-92.
11. Davis GL, Esteban-Mur R, Rustgi V, Hoefs J, Gordon ST, Trepo C, et al. Interferon a 2b alone or in combination with Ribavirin for the treatment of relapse of chronic hepatitis C. N Engl J Med. 1998;339:1493-9.
12. Poynard T, Marcellin P, Lee SS, Niederau C, Minuk GS, Ideo G, et al. Randomized trials of interferon alfa 2b plus ribavirin for 48 weeks or for 24 weeks versus interferon alfa 2b plus placebo for 48 weeks for treatment of chronic infection with hepatitis C virus. International Hepatitis Interventional Therapy Group (IHIT). Lancet. 1998;352:1426-32.
13. Galbán E, Vega H. Interferón alfa-2b en hepatitis crónica C. Combinación con Ribavirina. Gen. 2000;54(3):169-86.
14. Moreno-Otero R. Therapeutic modalities in hepatitis C: challenges and development. J Viral Hepat. 2005;12(1):10-9.
15. Hadziyannis SJ, Sette H Jr, Morgan TR, Balan V, Diago M, Marcellin P, et al. Peginterferón-a 2ª and Ribavirin combination therapy in chronic hepatitis C. Ann Intern Med. 2004;140:346-55.
16. Diago M, Pérez C. Paciente con genotipo 1 y carga viral alta. En: Diago M, Moreno-Otero R. Situaciones clínicas en hepatitis virales. España: Editorial Grupo Acción Médica, 2005. p. 3-15.
17. Ikeda K, Saitoh, Arase Y. Effect of interferon therapy on hepatocellular carcinogenesis in patients with chronic hepatitis type C:a long-term observation study of 1, 643 patients using statistical bias correction with proportional hazard analysis. Hepatology. 1999;29:1124-30.
18. Radkowski M, Jablonska J, Wilkinson J. Persistence of hepatitis C virus in patients successfully treated for chronic hepatitis C [abstract]. Hepatology. 2004;40(Suppl1):180 A.
19. Pawlotsky JM. Therapy of hepatitis C: from empiricism to eradication. Hepatology. 2006;43(Suppl1):S207-20.
20. Wright M, Forton D, Main J. Treatment of histologically mild hepatitis C virus infection with interferon and ribavirin: a multicenter randomized controlled trial. J Viral Hepat. 2005;12(1):58-66.
21. Roca J, Massot A, Padrón G. Hepatitis C virus genotyping in developing countries: Results from Cuba, India and Turkey. Biotecnología Aplicada. 1999;16:88-92.
22. Sanyal AJ, Chand N, Comar K. Hyperinsulinism blocks the inhbition of hepatitis C virus (HCV) replication by interferon: a potential mechanism for failure of interferon therapy in subjects with HCV and non alcoholic fatty liver disease [abstract]. Hepatology. 2004;40(Suppl1):179A.
23. Ratziu V, Heurtier A, Bonyhay L. Review article: an unexpected virus-host interaction-the hepatitis C virus-diabetes link. Aliment Pharmacol Ther. 2005 Nov;22 Suppl 2:56-60.
24. Ratziu V, Trabut JB, Poynard T. Fat, diabetes, and liver injury in chronic hepatitis C. Curr Gastroenterol Rep. 2004 Feb;6(1):22-9.
25. Katze MG, He Y, Gale M, Jr. Viruses and interferon: a fight for supremacy. Nat Rev Inmunol. 2002;2:675-87.
]]>
Recibido: 2 de noviembre de 2009.
Aprobado: 10 de noviembre de 2009.
Dr. Yoan Antonio Sánchez Rodríguez. Instituto de Gastroenterología. Calle 25 # 503 entre H e I, Vedado, CP 10 400. La Habana, Cuba. Correo electrónico: yoan.sanchez@infomed.sld.cu ]]>