
Identificación de tumor primario en pacientes con metástasis como forma de presentación de cáncer
Identification of the primary tumor in patients with metastases presenting as cancer
Dr. Luis Alfonso Senra Armas, Dr. Rayner Menéndez Pérez
Hospital Clinicoquirúrgico "Hermanos Ameijeiras". La Habana, Cuba.
]]>
RESUMEN
Introducción: hoy día el cáncer compite con la cardiopatía isquémica como primera causa de muerte en Cuba, muy por encima incluso de la enfermedad cerebrovascular, los accidentes y la neumonía. En muchos casos, el cáncer se presenta con metástasis y solo se logra identificar el tumor primario en una parte de ellos, mientras que en el resto, se mantiene "oculto" tras una investigación considerada "óptima".
Objetivo: determinar la frecuencia con que se identifica en nuestro medio un tumor primario cuando el cáncer se ha presentado con metástasis, la distribución topográfica de los sitios de metástasis y las variantes histológicas en casos de tumor primario "oculto".
Métodos: estudio transversal, prospectivo y descriptivo realizado en el Servicio de Medicina Interna del Hospital Clinicoquirúrgico "Hermanos Ameijeiras" en el período comprendido de enero 2010 a enero 2013. El universo de trabajo estuvo constituido por 100 pacientes con metástasis sin primario identificado como diagnóstico de hospitalización, que cumplían los criterios de inclusión. Se utilizaron las variables: localización de tumor primario, sitios de metástasis y variedades histológicas. Se emplearon principalmente métodos de estadística descriptiva, especialmente los aplicables a variables cualitativas (incidencia).
Resultados: se logró identificar tumor primario en 50 pacientes. Las localizaciones más frecuentes fueron pulmón (11 %), colon, ovario y próstata (5 % en cada caso). En 50 % de los casos no se identificó tumor primario. El sitio más común de metástasis fue el hígado (56,0 %), seguido por los ganglios (41,0 %) y la pleura pulmón (19,0). En el caso de los pacientes en los que no se logró identificar el tumor primario, la variedad más frecuente fue adenocarcinoma bien diferenciado (42 %) seguida del carcinoma poco diferenciado (34 %) y el carcinoma neuroendocrino (20 %).
Conclusiones: en nuestro medio, se logra identificar tumor primario en la mitad de los pacientes que se presentan con metástasis . Ello es independiente del número de metástasis al momento de la presentación. El sitio de afectación metastásica más frecuente es el hígado. La variante histológica predominante entre pacientes con tumor primario "oculto" fue adenocarcinoma.
Palabras clave: tumor primario, metástasis, cáncer de primario oculto (CPO).
ABSTRACT
]]>
Introduction: today cancer competes with ischemic heart disease as the leading cause of death in Cuba, even far above cerebrovascular disease, accidents, and pneumonia. In many cases, cancer has metastasized and only the primary tumor is only identified in a part of them, while in the rest, the tumor remains "hidden" behind a research considered as "optimal".
Objective: to determine, in our context, how often a primary tumor is identified when the cancer has metastasized, the topographical distribution of metastasis sites and histological variants in cases of "hidden" primary.
Methods: A cross-sectional, prospective and descriptive study was conducted in the Department of Internal Medicine, at Hermanos Ameijeiras Clinical Hospital from January 2010 to January 2013. The working universe consisted of 100 patients with metastasis with no primary tumor identified as diagnosis of hospitalization, who met the inclusion criteria. Location of primary tumor, metastatic sites and histological types were variables used. Descriptive statistics were mainly used, especially those applicable to qualitative variables (incidence).
Results: primary tumor was identified in 50 patients. The most common sites were lung (11 %), colon, ovarian and prostate (5 % each). no primary tumor was identified in 50 % of cases. The most common site of metastasis was liver (56.0 %), followed by lymph (41.0 %) lung and pleura (19.0). the most common strain was well-differentiated adenocarcinoma (42 %) in those patients whose primary tumor failed to be identified; followed by the poorly differentiated carcinoma (34 %) and neuroendocrine carcinoma (20 %).
Conclusions: In our context, identifying the primary tumor is achieved in half of the patients with metastases. This is independent of the number of metastases at presentation. Liver is the most common site of metastasis. The predominant histological variant among patients with "hidden" primary was adenocarcinoma.
Key words: primary tumor, metastasis, hidden primary cancer (HPC).
INTRODUCCIÓN
Cuando una célula del cuerpo se vuelve atípica, comienza a crecer y se multiplica rápidamente de modo desorganizado, provoca la aparición de lo que se conoce como tumor maligno o cáncer. Esta formación anómala tiene la capacidad de dar origen a metástasis.1
]]> Se reconocen 3 vías principales de diseminación de las células tumorales: linfógena, hematógena y transcelómica. Dentro de ellas la linfógena es la más frecuente.2 Por ende, de la localización topográfica de las metástasis puede inferirse la posible localización del sitio primario.3-6Hoy el cáncer compite con la cardiopatía isquémica como primera causa de muerte en Cuba, muy por encima incluso de la enfermedad cerebrovascular, los accidentes y la neumonía. Estadísticas recientes de Estados Unidos evidencian que aproximadamente 15 % de los pacientes con cáncer se presentan con metástasis y solo se logra identificar el tumor primario en dos tercios de ellos, mientras que en el tercio restante el tumor se mantiene "oculto".7,8
El cáncer de primario oculto (CPO) se define como enfermedad maligna diseminada, demostrada mediante el estudio anatomopatológico de una de sus metástasis, sin que se consiga identificar el origen del tumor primario, a pesar de una evaluación clínica considerada óptima.9,10 La mayoría de los grupos de trabajo consideran como investigaciones indispensables una analítica de sangre que comprenda: hemograma completo, bioquímica sanguínea que mida función hepática y renal; sedimento urinario, test de sangre oculta en heces, una radiografía de tórax posteroanterior y lateral, ecografía y tomografía axial computarizada (TAC) abdominal y, de modo particular, antígeno específico de la próstata (en varones) y mamografía (en mujeres).
En algunos países, el CPO supone de 4-10 % de todos los cánceres que se diagnostican, la edad media de presentación es 60 años.11 El pronóstico es generalmente malo, con una mediana de supervivencia de 3-4 meses y una supervivencia al año, inferior al 20 %, lo cual lo ubica en Estados Unidos como la cuarta causa de muerte por cáncer.8,12,13 Estudios realizados sobre reportes de necropsia indican incapacidad para identificar el tumor primario en 15-25 % de los casos.14-16
Al momento de la presentación, 60 % de los pacientes tienen metástasis al menos en 2 órganos y 30 % en más de 3.17-22 Las localizaciones más comunes de tumor primario “oculto” son pulmón (20 %) y páncreas (25 %),21 otras posibles localizaciones a tener en cuenta son tracto gastrointestinal (estómago, colon y recto), tracto hepatobiliar y riñón. De modo global, los sitios de metástasis más frecuentes son ganglios, hígado, pulmón, hueso y pleura.22
En los últimos años, las vías clínicas sugieren que en ausencia de pistas clínicas evidentes por su valor orientativo y pronóstico parece razonable comenzar por el estudio histopatológico de la metástasis.23,24
Según la clasificación histopatológica de Hainsworth y Greco, las metástasis se pueden agrupar en 4 grandes categorías:9
- Adenocarcinoma bien o moderadamente diferenciado: representa la variante histológica más frecuente de CPO, constituye aproximadamente el 50-60 %.22,25 La forma más característica de aparición es en pacientes mayores, con metástasis en diferentes órganos. Las localizaciones más frecuentes del tumor primario (TP) son el pulmón y el páncreas.22,26 El pronóstico es malo, con una supervivencia media de unos 3-4 meses.22,27
- Carcinoma escamoso o epidermoide: constituye el 2-5 % de los CPO.22 Suele presentarse en pacientes con hábito tabáquico y/o enólico; el lugar más frecuente de metástasis es los ganglios cervicales, seguido de los inguinales.1,22 Localizaciones frecuentes de TP son nasofaringe, piel, tercio proximal del esófago, pulmón, ano, vulva y pene.
- Carcinoma indiferenciado, con rasgos de adenocarcinoma pobremente diferenciado o sin estos: representa de 30-40 % de los CPO, 22,27 generalmente aparecen en pacientes más jóvenes y con frecuencia presentan una rápida progresión de los síntomas, con rápido crecimiento tumoral. Las localizaciones más frecuentes de diseminación son los ganglios linfáticos, espacio retroperitoneal y mediastino. Este grupo, incluye los tumores de células germinales atípicas, timomas malignos, melanomas y otros.28
]]> - Carcinoma neuroendocrino: representa el 5 % de los CPO, las metástasis pueden incluir ganglios linfáticos y órganos sólidos. En general se consideran como un grupo de pronóstico favorable y de ahí lo importante de su reconocimiento.22,23,29El examen histológico basado en las técnicas de tinción convencional (hematoxilina-eosina) permite agrupar los diagnósticos en “específicos” (linfomas, sarcomas, melanomas o adenocarcinomas) e “inespecíficos”. Un grupo de tumores continúan siendo tan indiferenciados que se limita la posibilidad de subclasificarlos y se requiere de técnicas de inmunohistoquímica. No obstante, el término CPO vincula por lo general pacientes con adenocarcinomas.9,12,18,30,31
El pronóstico general de los pacientes con CPO es precario, con baja supervivencia media. Solo 25 % de los pacientes están vivos al año y el 10 %, a los 5 años. No obstante, existe al menos un 30 % de pacientes que, dependiendo de la localización primaria, tipo histológico o formas de presentación metastásica, se pueden beneficiar de un tratamiento específico con aceptables niveles de respuesta y supervivencia (subgrupos de buen pronóstico).17,20
Conocer la frecuencia con que se identifica en nuestro medio un tumor primario en pacientes que se presentan con metástasis, la topografía de las metástasis y las variantes histológicas dentro del grupo CPO fue lo que nos motivó a realizar esta investigación.
MÉTODOS
Estudio transversal, prospectivo y descriptivo realizado en el Servicio de Medicina Interna del Hospital Clinicoquirúrgico “Hermanos Ameijeiras” en el período comprendido de enero 2010 a enero 2013.
El universo de trabajo estuvo constituido por los pacientes con metástasis sin tumor primario identificado como diagnóstico de hospitalización, mientras que la muestra quedó conformada por los pacientes que cumplieron los criterios de inclusión.
Criterios de inclusión
Criterios de exclusión
Pacientes en los que no se demostró, por estudio histológico, el diagnóstico de cáncer, independientemente de si existía o no evidencia clínico-radiológica de malignidad.
Sistemática de estudio
En la definición de caso se asumió la establecida en la literatura científica: “Neoplasia maligna histológicamente demostrada cuyo tumor primario no se evidencia tras historia clínica, exploración física completa, estudios básicos de laboratorio (hemograma, bioquímica de sangre, ecografía y TAC abdominal, radiografía de tórax PA y lateral, así como PSA, en hombres y mamografía, en mujeres.9
A todos los pacientes incluidos (ver “criterios de inclusión”) se les hizo evaluación clínica y fueron seguidos hasta demostrar, desde el punto de vista histológico, el origen maligno de la lesión metastásica y su clasificación. Posteriormente se procedió a detectar la localización del tumor primario basado en el contexto clínico, topografía de las metástasis y variedad histológica. Para ello se emplearon estudios imaginológicos (contrastados de vías digestivas, tomografía axial computarizada), exploraciones endoscópicas (digestiva superior, colonoscopia, broncoscopia) o la toma de biopsias por punción con aguja fina (PAF), trucut con control de ecografía o TAC, o cirugía mínimamente invasiva.
Operacionalización de variables
Se consideró presencia del tumor primario en: pulmón, páncreas, colon, ovario, hígado, mama, estómago, próstata, intestino delgado, corazón, vejiga, pleura, pericardio, recto, testículo, tiroides, útero, vesícula o no identificado (cáncer primario oculto). Variable cualitativa nominal politómica.
Sitios de metástasis
Región corporal donde hubo demostración histológica o por imágenes (en casos con, al menos, una demostrada por histología) de metástasis (ganglios linfáticos, hígado, pulmón, glándulas suprarrenales, huesos, peritoneo, cerebro, pleura, riñón, páncreas, pericardio y otras). Variable cualitativa nominal politómica.
Variedad histológica
Se consideró según lo descrito en el reporte de biopsia: adenocarcinoma bien o moderadamente diferenciado, carcinoma escamoso o epidermoide, carcinoma pobremente diferenciado y carcinoma neuroendocrino. Variable cualitativa nominal politómica.
Análisis estadístico
Dado el diseño descriptivo del estudio, se emplearon principalmente métodos de estadística descriptiva, especialmente los aplicables a variables cualitativas (incidencia), porque todas las variables del estudio son de este tipo. Mediante un análisis gráfico, los resultados se muestran en discos, histogramas o tablas.
]]> De acuerdo al número de metástasis, se crearon 2 grupos (uno de tumor primario identificado y otro de primario oculto) que fueron comparados de según la presencia de 1, 2 o más metástasis, para ello se aplicó el test de chi cuadrado y el resultado se consideró estadísticamente significativo cuando el valor de p ≤ 0,05. El análisis estadístico se hizo utilizando el programa SPSSv.20 (IBMr).
Consideraciones éticas
La investigación fue aprobada por el Comité Científico y el Comité de Ética del hospital. Se solicitó consentimiento a pacientes y familiares. Los resultados de esta investigación solo serán empleados con fines científicos y en ningún caso se mostrará la identidad de los pacientes.
RESULTADOS
De 145 casos evaluados, 100 pacientes cumplieron los criterios de inclusión. Los excluidos se debieron, en su mayoría, a que su estado clínico no aconsejaba la realización de una toma histológica, a negativa personal o familiar.
Exactamente en la mitad de los casos no se pudo precisar el origen del tumor primario; en los que sí fue posible, el identificado con más frecuencia fue pulmonar (11 %). Otros tumores primarios identificados, en orden descendente de frecuencia, fueron de colon, ovario, próstata y mama (tabla 1).
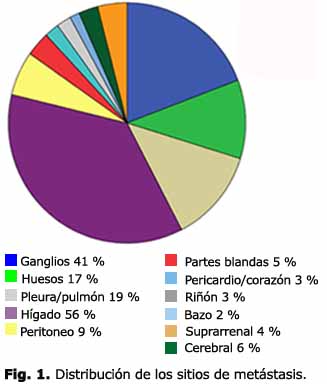
El sitio más común de metástasis fue hígado (56,0 %), seguido por ganglios (41,0 %) y pleuro/pulmonar (19,0 %). La figura 1 muestra la distribución de los sitios de metástasis.
]]>
En relación con la topografía de la afectación ganglionar, las más frecuentes correspondieron a cervicales bajas (10 %), seguidas de las retroperitoneales (8 %), las cervicales altas y las supraclaviculares (ambas 7 %).
Del total de pacientes, 60 tenían una lesión metastásica única, mientras 40 presentaban 2 o más. En pacientes con lesión única se logró identificar tumor primario en 32 de ellos, mientras 28 se clasificaron como CPO. En aquellos que presentaron 2 o más metástasis se logró identificar tumor primario en 18, mientras 22 engrosaron el grupo de CPO (tabla 2).
En el caso de los pacientes en los que no se logró identificar el tumor primario, la variedad más frecuente fue adenocarcinoma bien diferenciado (42 %) como se observa en la figura 2.
La figura 3 correlaciona los sitios de metástasis con las variedades histológicas en el grupo CPO. En las variedades de carcinoma bien y poco diferenciado, los sitios más frecuentes fueron hígado (67 y 59 %, respectivamente) seguido de ganglios (24 y 35 %, respectivamente) y pulmón (28 y 10 %, respectivamente).
DISCUSIÓN
]]>Las estadísticas de EUA evidencian que en pacientes que tienen metástasis como forma de presentación del cáncer se logra identificar el tumor primario en las 2/3 partes de los casos manteniéndose oculto en el 1/3 restante.7 En nuestra serie, la identificación del tumor primario fue menor (50 %), el cáncer de pulmón fue la localización evidenciable más frecuente (11 %). Esta menor eficacia en la identificación de sitios primarios probablemente se deba a algunas características particulares de la muestra de investigación que se comentarán más adelante y, sobre todo, a limitaciones en recursos de apoyo al diagnóstico en las áreas de imágenes y anatomía patológica.
Entre los estudios imaginológicos recomendados que no disponemos en el momento actual, está la tomografía con emisión de positrones (PET, por sus siglas en inglés) con 18 F- fluorodeoxyglucosa (FDG),32,33 aunque su utilidad es controversial, se emplea en la localización del tumor primario y sitios adicionales de metástasis sobre la base de su facultad para identificar el incremento del consumo metabólico de oxígeno por el tejido afectado; según un reciente meta-análisis,34 la predicción de la localización del tumor primario con esta técnica es del 37 %, con una sensibilidad y especificidad del 84 %.Otra investigación, que incluyó 221 pacientes, sugiere que en el 41 % de los casos el tumor primario pudo identificarse con este estudio después que los exámenes convencionales fueron infructuosos, reportaron como principal localización el pulmón, en el 59 % de los casos y hallaron sitios de metástasis adicionales en 37 %.35 Para algunos, la PET/TAC ha cambiado de forma significativa el manejo clínico de los pacientes con carcinoma de primario oculto, no obstante, se reporta un elevado porcentaje de falsos positivos (58 %) para tumores del tracto digestivo inferior y su mayor utilidad parece corresponder a la identificación de tumores de la cabeza y cuello.33 Todo ello sin considerar su utilidad para evaluar la respuesta biológica al tratamiento con quimioterapia.36
Otro recurso que gana en popularidad es la mamografía por IRM. Algunos estudios reportan identificación de tumores mamarios en 37 % de las pacientes en que dichos tumores habían sido omitidos por ecografía y mamografía.32
Resulta llamativo en nuestra serie que la localización más frecuente de metástasis sea hepática superando a la ganglionar, probablemente como consecuencia de que un número no despreciable de pacientes con lesiones cervicales son enviados directamente a consulta especializada de tumores de cabeza y cuello, lo que pudiese contribuir a un sesgo en la muestra.
En nuestra serie solo fue posible emplear técnicas anatomopatológicas de inmunohistoquímica en 32 de los casos y en este grupo se logró identificar tumor primario en 68,75 %, superior sin dudas al de la muestra global. Recientemente, Fizazi y otros37 han sugerido que la batería de estudios inmunohistoquímicos, debe incluir al menos citoqueratinas (CK-7, CK-20), LCA, S100, TTF-1, marcadores ováricos y de mama, HEPAR-1, fosfatasa alcalina placentaria/OCT-4, WT-1/PAX8, sinaptofisina y cromogranina. Algunos reportes aseveran que tan solo con los estudios inmunohistoquímicos, se puede precisar hasta el 35-40 % de la localización primaria de los tumores.38
Sin embargo, según otros autores, que centran la pesquisa en el empleo de algoritmos de diagnóstico basados en estudios de inmunohistoquímica, sitúan la predicción en la localización del tumor primario hasta en un 80 %.39 Otro estudio similar mostró una sensibilidad y especificidad en la predicción de la localización del tumor primario, del 80,3 % y el 97,6 %, respectivamente.40
Adicionalmente,40 de los pacientes que finalmente se incluyeron en el grupo en los que no fue posible identificar el tumor primario, tenían notable deterioro del estado general con perfomance score, con puntajes entre 3 y 4 al emplear la escala evaluativa del Grupo Oncológico Cooperativo Europeo (ECOG, por sus siglas en inglés) lo que limitó la realización de algunas instrumentaciones diagnósticas, más cuando correspondían con variedades histológicas de pronóstico desfavorable, a lo que se añadió en algunos casos la negativa del paciente o sus familiares a que se les realizaran.
Se han reportado metástasis múltiples en 30 % de los pacientes con CPO.41 No obstante, en nuestra serie se hallaron lesiones múltiples en 44 % de aquellos en los que no se identificó tumor primario. El número de metástasis al momento de presentación (únicas o múltiples) no influyó en la identificación del tumor primario.
]]>Se encontró alta incidencia de metástasis hepática (56 %), seguida por las metástasis ganglionares (41 %) y pleuropulmonares (19 %). El hígado recibe toda la sangre venosa que proviene de los órganos del aparato digestivo y además, gran parte del drenaje linfático de la región inferior del cuerpo se relaciona con el hígado, todo lo que hace a este órgano un receptor frecuente de metástasis. Una proporción importante de los tumores primarios identificados, se localizaron en la región intrabdominal, por lo que no es de extrañar la alta incidencia de metástasis en el hígado. Si recordamos que el cáncer con primario oculto con mayor frecuencia suele ser de origen pancreático y pulmonar,25 es muy probable que una gran cantidad de los tumores primarios no identificados en nuestros pacientes sean emisores potenciales de metástasis hepáticas, óseas y pulmonares.
Cincuenta y seis de nuestros pacientes tenían metástasis hepáticas y entre ellos se logró identificar tumor primario solo en 24, es decir que 58 % de los casos con metástasis hepáticas engrosaron el grupo de CPO.
Según otros estudios, las metástasis hepáticas no son las más frecuentes y solo aparecen en alrededor del 9 % de los casos con tumor primario no identificado, detrás de las metástasis en ganglios linfáticos (25 %) y las óseas (18 %).41 El segmento colon recto tal vez sea el primer emisor de lesiones secundarias al hígado, incluso es de empleo habitual la clasificación en metástasis de origen colorrectal o de otro. La carencia de recursos como colonoscopia virtual por TAC (de uso creciente) o convencional, no siempre técnicamente óptima, explica en parte esta disparidad en los resultados.
Pentheroudakis y otros,17 en una serie de 884 pacientes con CPO, diagnosticados entre 1994 y 2000, los sitios principales de diseminación fueron pulmón (46 %), ganglios linfáticos (35 %), hígado (23 %), hueso (17 %) y cerebro (16 %), los cuales son similares en localizaciones, pero no frecuencia, a los encontrados en el presente estudio.
En relación con la topografía de las metástasis ganglionares encontramos como más frecuentes las cervicales bajas que aunque aparecen principalmente en tumores de la cabeza y el cuello, también pueden originarse en localizaciones como mama y pulmón, frecuentes en nuestro estudio. Vale recordar que muchos pacientes con lesiones cervicales altas son asistidos por otros especialistas. Le siguieron en frecuencia las del espacio retroperitoneal justificadas por localizaciones primarias intrabdominales como colon, ovario y próstata. En región supraclavicular coincidentes con la frecuencia de tumores digestivos, de mama y pulmón. Los casos que presentaron metástasis cervicales altas se relacionaron con primarios al nivel de faringe, amígdala y tiroides.
Principales variedades histológicas en paciente con CPO
Las variedades histológicas identificadas con mayor frecuencia fueron adenocarcinoma bien diferenciado (42 %) y carcinoma poco diferenciado (34 %). Estudios previos reportan la siguiente frecuencia: adenocarcinoma (50-70 %), carcinoma poco diferenciado (20-30 %), carcinoma de células escamosas (5-8 %) y tumores neuroendocrinos (2-3 %).35,40 Distintivo en nuestra serie es la variedad carcinomas neuroendocrinos (representó 20 % de los casos), probablemente vinculado a la carencia de recursos diagnósticos como cápsula endoscópica para exploración de intestino delgado o ecografía endoscópica para exploración de lesiones pancreáticas entre otros.
]]> Al igual que en nuestro trabajo, la variedad histológica identificada en mayor proporción en el estudio realizado por Al-Brahim y otros fue el adenocarcinoma (69,9 %) coincidente con los resultados de trabajos realizados por Maiche, en 1993, donde la frecuencia fue de 53 %.13,15 Esto ha llevado a que algunos grupos utilicen el adenocarcinoma de primario oculto o desconocido como sinónimo al referirse al CPO.
Asociación entre variedades histológicas y sitios de metástasis en pacientes con CPO
Según la asociación entre variedades histológicas y sitios de metástasis, encontramos que en las variedades de adenocarcinoma bien y poco diferenciado las metástasis se localizaron con mayor frecuencia en hígado, ganglios y pulmón. En la variedad de carcinoma escamoso, la totalidad de las metástasis asentaron en ganglios y en el grupo de carcinoma neuroendocrino al nivel de hígado, pulmón y pleura. Estos resultados coinciden con los reportados en la literatura en el caso de las variedades de adenocarcinoma bien diferenciado, poco diferenciado y carcinoma escamoso40,42 y no así en el caso de los tumores neuroendocrinos donde, según estudio realizado por Hainsworth y otros,43 los sitios de metástasis más frecuentes identificados son las estructuras retroperitoneales (20 %), ganglios periféricos (14 %), mediastino (12 %), hígado (12 %) y huesos (11 %). Estas diferencias pudiesen ser dependientes del número de casos (10) con variedad neuroendocrina presentes en nuestra serie.
Una limitante de esta investigación es que a pesar de ser un estudio prospectivo, es esencialmente descriptivo, por lo que no se puede establecer una relación causa-efecto entre las variables estudiadas. No obstante, aporta información clara acerca de las posibilidades de detección en nuestro medio de tumores primarios en pacientes que se presentan con metástasis, frecuencia de afectación por órganos y variantes histológicas en la presentación del cáncer con primario oculto.
REFERENCIAS BIBLIOGRÁFICAS
1.Oncología y Hematología. Cap. 95. En: HarrisonꞋs. Principios de Medicina Interna. 17a ed. Parte VI. Sección 1. Philadelphia: The McGraw-Hill Companies; 2008. p. 614-6.
2. Hammar S. Metastatic adenocarcinoma of unknown primary origin. Hum Pathol. 2008;29:1393-402.
3. Abbott NJ, Ronnback L, Hansson E: Astrocyteendothelial interactions at the blood-brain barrier. Nat Rev Neurosci. 2006;7:41–53.
4. Yu Q, Stamenkovic I. Transforming growth factor beta facilitates breast carcinoma metastasis by promoting tumor cell survival. Clin Exp Metastasis. 2004;21:235-42.
5. Kozlow W, Guise TA. Breast cancer metastasis to bone: mechanisms of osteolysis and implications for therapy. J Mammary Gland Biol Neoplasia. 2005;10:169-80.
6. Chambers AF, Groom AC, MacDonald IC. Dissemination and growth of cancer cells in metastatic sites. Nat Rev Cancer. 2002;2:563–72.
7. Muir C. Cancer of unknown primary site. Cancer. 2005;75:353.
8. Perry Michael. Citing a hypothesis advanced by Larry Norton of the Memorial-Sloan Kettering Cancer Center. The Lancet Oncology. 2010.
9. Greco F, Hainsworth J. Cancer of unknown primary site. En: De Vita VT, Hellman S, Rosenberg SA, editors. Cancer: Principles and practice of Oncology. 7a ed. Philadelphia: J.B. Lippincott; 2005. p. 2213-34.
10. Abbruzzese J, Abbruzzese M, Hess K, Raber M, Lenzi R, Frost P. Unknown primary carcinoma: natural history and prognostic factors in 657 consecutive patients. J Clin Oncol. 2004;12:1272-80.
11. Altman E, Cadman E. An analysis of 1539 patients with cancer of unknown primary site. Cancer. 2006;57:120.
12. Greco F, Vaughan W, Hainsworth J. Advanced poorly differentiated carcinoma of unknown primary site: recognition of a treatable syndrome. Ann Intern Med. 1986;104:547-53.
13. Maiche AG. Cancer of unknown primary. A retrospective study based on 109 patients. Am J Clin Oncol. 1993;16:26-9.
14. Senra L, Hernández E, Álvarez R, Rodríguez H, Cand C, Roca V. Valor del examen post mortem en pacientes con cáncer de tumor primario oculto. Rev Cubana Med. 2011;50(4):376-89.
15. Al-Brahim N, Ross C, Carter B, Chorneyko K. The value of postmortem examination in cases of metastasis of unknown origin-20 year retrospective data from a tertiary care censer. Ann Diagnos Pathol. 2005;9:77-80.
16. Blaszyk H, Hartmann A, Bjornsson J. Cancer of unknown primary: clinicopathologic correlations. APMIS. 2003;111:1089-94.
17. Pentheroudakis G, Briasoulis E, Pavdilis N. Cancer of unknown primary site: missing primary or missing biology? The Oncologist. 2007;12:418-25.
18. Ayoub J, Hubbard P, Lenzi. Unknown primary carcinomas: diagnosis and management. En: Pazdur R, editor. Medical oncology. A comprehensive review. 2nd ed. New York: PRR Inc.; 1996. p. 559-66.
19. ESMO. Minimum clinical recommendations for diagnosis, treatment and follow-up of. Ann Oncol. 2013;12:1057-8.
20. NCCN. Practice guidelines in oncology. Occult primary. Version 1. National Comprehensive Cancer Network. Inc.; 2013.
21. Hillen HFP: Unknown primary tumours. Postgrad Med J. 2006;76:690-3.
22. Van der Wouw AJ, Jansen RLH. The Unknown biology of the unknown pimary tumour. Annals of Oncology. 2003;14:191-6.
23. Varadhachary GR, Greco A. Overview of management and future directions in unknown primary carcinoma. Seminars in Oncology. 2009;36(1):75-80.
24. Losa Gaspà F, Germà JR, Llucha L, Camacho Cuarterob L, Niubó Danielc R, Albareda Boledac JM, et al. Planteamiento diagnóstico y terapéutico frente al cáncer de presentación metastásica y origen desconocido; Rev Clin Esp. 2002;202(11):604-14.
25. Khosravi P, Rueda A, Álvarez J. Neoplasias de origen desconocido. An Med Inter. 2004;21(10):501-6.
26. Bishop JF, Tracey E, Glass P, Jelfs , Roder D. Prognosis of sub-types of cancer of unknown primary (CUP) compared to metastasic cancer. J Clin Oncol. 2007;25(18S):abstr 21010.
27. Chorost MI, Lee C, Yeoh C, Molina M, Ghosh BC. Unknown primary. Journal of Surgical Oncology. 2004;87:191-203.
28. Leong SP, Cady B, Jablons DM. Clinical patterns of metastasis. Cancer Metast Rev. 2006;25:221-32.
29. Erlander MG, Moore MW, Cottem P. Molecular classification of carcinoma of unknown primary by gene tissues. J Clin Oncol. 2004;22(14S):abstr 9545.
30. Mackay B, Ordóñez N. Pathological evaluation of neoplasms with unknown primary tumor site. Semin Oncol. 2003;20:206-28.
31. Gown A, Vogel A. Monoclonal antibodies to human intermediate filament proteins. Analysis of tumors. Am J Clin Pathol. 1995;84:413-24.
32. Park JS, Yim JJ, Kang WJ, Chung JK, Yoo ChG, Kim YW. Detection of primary sites in unknown primary tumors using FDG-PET or FDG-PET/CT. BMC Research Notes. 2011;4:56.
33. Karapolat I, Kumanlioğlu K. Impact of FDG-PET/CT for the detection of unknown primary tumours in patients with cervical lymph node metastases. Mol Imag Radionucl Ther. 2012;21:63-8.
34. Kwee TC, Kwee RM. Combined FDG-PET/CT for the detection of unknown primary tumors: systematic review and metaanalysis. EurRadiol. 2009;19:731-44.
35. Krämer A, Hübner G, Schneeweiss A, Folprecht G, Nebene K. Carcinoma of unknown primary – an orphan disease? Breast Care.2008;3:164-70.
36. Hwang JE, Yoon JY, Bae WK, Shim HJ, Chung IJ. Complete biologic response to taxane based chemotherapy confirmed by [18F] FDG PET/CT and surgery in a cancer of unknown primary site. J Gynecol Oncol. 2011;23:65-8.
37. Fizazi K, Greco FA, Pavlidis N, Pentheroudakis G, on behalf of the ESMO Guidelines Working Group. Cancers of unknown primary site: ESMO Clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2011;22(Supplement 6): vi64-vi68.
38. Hashimoto K, Sasajima Y, Ando M, Yonemori K, Hirakawa A, Furuta K, et al. Immunohistochemical profile for unknown primary adenocarcinoma. PloS ONE. 2012;7:e31181.
39. Dennis JL, Hvidsten TR, Wit EC, Komorowski J, Bell AK, Downie I, et al. Markers of adenocarcinoma characteristic of the site of origin: development of diagnostic algorithm. Clin Cancer Res. 2005;11:3766-72.
40. Briasoulis E, Pavlidis N. Cancer of unknown primary origin. The Oncologist. 2007;2:142-52.
41. Abbruzzese JL, Abbruzzese MC, Hess KR, Raber AN, Lenzi R, Frost P. Unknown primary carcinoma: natural history and prognostic factors in 657 consecutive patients. J Clin Oncol. 2004;12:1272-80.
42. Khosravi Shahi P, Del Castillo Rueda A, De Portugal Álvarez J. Neoplasias de origen desconocido. Anales de medicina Interna. 2004;21:501-6.
43. Hainsworth JD, Spigel DR, Litchy S, Greco FA. Phase II trial of paclitaxel, carboplatin, and etoposide in advanced poorly differentiated neuroendocrine carcinoma: a Minnie Pearl Cancer Research Network Study. J Clin Oncol. 2006;24:3548-54.
Recibido: 15 de abril de 2014.
Aprobado: 10 de junio de 2014.
Dr. Luis Alfonso Senra Armas. Hospital Clinicoquirúrgico "Hermanos Ameijeiras", San Lázaro No. 701 entre Belascoaín y Marqués González, Centro Habana, La Habana, Cuba. CP 10 300. luis.senra@gmail.com
]]>