± 3,6 %) en relación con el adulto (25,5 ± 4,2 %) cuando se utilizó suero humano inactivado como fuente de opsoninas, y no se hallaron diferencias significativas al utilizar suero fresco de ratón o suero adulto activo. Se destaca además el incremento de la capacidad reductora del leucocito PMN del recién nacido (58 y 95 %) de incremento al utilizar suero de adulto activo o ratón respectivamente contra el adulto (7,8 y 39,2 %) en iguales condiciones.]]>
± 3,6 %) compared with the adult (25.5 ± 4,2 %) when inactivated human serum was used as a source of opsonins. No significant differences were found on utilizing mouse's fresh serum or active adult serum. It is also stressed the reducing capacity of the PMN leucocyte in the newborn (58 and 95 %) on using active adult serum or the mouse's fresh serum, respectively, against the adult (7.8 and 39.2 %) under equal conditions.]]>
Descriptores DeCS: NITROAZUL DE TETRAZOLIO; NEUTRÓFILOS; RECIÉN NACIDO; SANGRE FETAL; FAGOCITOCIS; COMPLEMENTO.
Las defensas del neonato humano son inmunológicamente inmaduras, lo que contribuye sustancialmente a la alta incidencia de sepsis en el recién nacido (RN) a término.1 Uno de los trastornos que parece incrementar el riesgo de infecciones bacterianas son los cambios cuantitativos y cualitativos en el sistema fagocitario, que pudieran llevar a una deficiencia en la habilidad de los leucocitos PMN de fagocitar y matar microorganismos,2 pues las investigaciones sobre la capacidad del suero de RN de servir como fuente de opsoninas han mostrado ser menor en relación con el adulto,3 y en particular el estudio del sistema complemento resulta elemento de especial interés en el RN, pues la actividad del complemento hemolítico total (mide la integridad de la vía clásica) constituye el 50 % de la del adulto, y la actividad de la vía alternativa (que tiene entre sus activadores las paredes celulares de la levadura,4 está aún más dañada;1 lo que nos indujo a valorar los efectos de diferentes niveles de complemento sobre la actividad fagocitaria de los leucocitos PMN del RN ante la levadura, manteniendo niveles aceptables de IgM e IgG.
El grupo control lo conformaron 80 adultos sanos con edades comprendidas entre 17 y 25 años, de uno y otro sexos, donantes voluntarios de banco de sangre o estudiantes del ISCM-VC, a quienes se les extrajo sangre venosa en tubos heparinizados.
En todos los casos se realizó conteo de leucocitos y determinación del porcentaje y número absoluto de granulocitos neutrófilos mediante coloración de Giemsa.
Aislamiento de granulocitos neutrófilos: La obtención de granulocitos se hizo según la técnica descrita por Hudson5 ligeramente modificada: 10 mL de sangre total se mezclaron con 2,5 mL de Dextran T-500 (Pharmacia Fine Chemicals) a una concentración de 30-10-3 en solución salina. Se incubó en posición vertical a 37 oC por espacio de 1 hora; posteriormente se eliminó el sobrenadante, y el precipitado se centrifugó a 1 000 g para eliminar totalmente el plasma. Las células fueron lavadas con solución de buffer fosfato (PBS), 3 veces durante 10 mi-nutos a 1 000 g. Se realizó el conteo de granulocitos y se ajustó a una concentración final de 5.106 células/mL.
Prueba de reducción de NBT: La levadura (Saccharonyces cerevisiae) como partícula, fue utilizada para inducir la fagocitosis. La solución salina que contenía un fragmento de levadura se llevó a temperatura de ebullición durante 30 min. Se filtró por gasa varias veces y se ajustó a una concentración de 4.106 células/mL; posteriormente se distribuyó en pequeños volúmenes y almacenó a -20 oC.
La técnica de reducción del NBT se hizo de acuerdo con la descripción de Stelzner.6 La solución de NBT se preparó en PBS a una concentración de 2.10.-3 Posteriormente se mezclaron 100 m L de suspensión de células, 50 m L de la suspensión de levaduras, 100 m L de NBT y 20 m L de suero como fuente de opsoninas, y se incubaron 30 minutos a 37 oC. Se realizó la determinación microscópica del porcentaje y número absoluto de células formazán positivas; fueron consideradas como tal aquéllas en cuyo citoplasma se observó un precipitado azul, por presentar inclusiones de azul de formazán.
Fuente de opsoninas: Para valorar los efectos de diferentes niveles de complemento sobre la actividad fagocitaria del leucocito PMN del neonato, se utilizó, en 16 muestras de recién nacidos y 30 de adultos, suero humano AB inactivado por calentamiento durante 30 minutos y a 56 oC, método que es capaz de abolir o reducir severamente la actividad opsónica dependiente del complemento, no así el efecto de IgM e IgG, termoestables en estas condiciones.7 En un segundo grupo (30 recién nacidos y 50 adultos) se utilizó suero de ratón, rico en componentes del complemento, y en el último, suero AB humano sin decomplementar.
Cálculos estadísticos: Los resultados correspondientes a RN y controles fueron obtenidos al calcular la media aritmética y el error estándar de la media. La comparación entre los valores de ambos grupos se realizó con la aplicación de la prueba de la "t" de Student de diferencia de medias y proporciones para un límite de confianza de p = 0,05.
| | | |||
| Muestra | | | | |
| Recién nacidos | | | ]]> 4 487±120 | |
| Adultos | | | | |
En la tabla 2 se dan a conocer los valores (![]() ± s
± s![]() ) de la prueba del NBT en el grupo de recién nacidos y el de adultos, ante diferentes fuentes de complemento. El porcentaje de leucocitos PMN reductores del NBT fue significativamente inferior en el recién nacido (p < 0,01) con respecto al del adulto, cuando se utilizó suero humano inactivado como fuente de opsoninas, por lo que no se encontraron diferencias significativas al utilizar suero de adulto activo o suero fresco de ratón.
) de la prueba del NBT en el grupo de recién nacidos y el de adultos, ante diferentes fuentes de complemento. El porcentaje de leucocitos PMN reductores del NBT fue significativamente inferior en el recién nacido (p < 0,01) con respecto al del adulto, cuando se utilizó suero humano inactivado como fuente de opsoninas, por lo que no se encontraron diferencias significativas al utilizar suero de adulto activo o suero fresco de ratón.
TABLA 2. Resultados de la prueba del nitroazul de tetrazolio en recién nacidos y adultos con la utilización de diferentes fuentes de complemento (![]() ± s
± s![]() )
)
| ]]> % PMN reductores del NBT | ||||
| Muestra | | | | |
| Recién nacidos | | | | |
| Adultos | | ]]> 25,5±0,46 | | |
En la figura se describe cómo el incremento en el porcentaje de leucocitos PMN que reducen al NBT en sangre de cordón umbilical de recién nacidos, es superior al mostrado entre los adultos cuando se eleva la disponibilidad de componentes del sistema complemento, con crecimientos del 58 y 95 % al utilizar suero activo o suero fresco de ratón respectivamente, muy superiores al 7,8 % y 39,2 % en adultos en iguales condiciones.
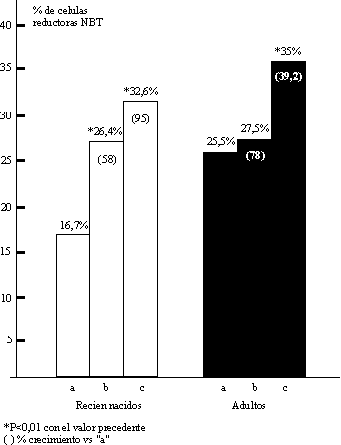
Se destaca el hecho de que entre los adultos sólo se encontró un incremento de significación estadística con el uso de suero de ratón como fuente de opsoninas.
componentes del sistema complemento y los anticuerpos de la clase IgM para una marcada actividad opsónica, se puede comprender entonces, la necesidad de un sistema íntegro para la opsonificación de este microorganismo. La activación del sistema complemento lleva a la generación de componentes tales como C3b y C3bi, que actúan como opsoninas por unión con las partículas a que se fagocitarán y las hace susceptibles a la ingestión por una variedad de células que llevan receptores específicos para el complemento (CR),9 de los cuales CR1 y CR3 han sido descritos en detalle, y es CR1 específico para C3b y CR3 para C3bi.10
Una vez estimulada la membrana del leucocito por la adhesión a sus receptores de sustancias particuladas, se activan una serie de procesos bioquímicos que desempeñan una importante función en la activación bactericida.11 La magnitud de este proceso, conocido por explosión respiratoria, puede valorarse al determinar la capacidad de los leucocitos PMN de reducir al NBT, el que entonces origina un precipitado citoplasmático de formazán como consecuencia de una reacción redox, donde intervienen enzimas oxidasas dependientes del nicotín-adenín dinucleotidofosfato (NADPH), que bajo activación adecuada catalizan la transferencia de electrones, vía una flavoproteína y el citocromo b-245 al oxígeno,11 y se genera el anión superóxido. ]]>
En nuestros experimentos, si analizamos el efecto de los niveles crecientes de complemento sobre los resultados de la prueba de NBT, observamos un incremento esperado tanto en los recién nacidos como en los adultos del porcentaje de células reductoras. Sin embargo, fue inesperado el marcado incremento del recién nacido, especialmente cuando se deja de utilizar suero inactivado, que refleja una dependencia mucho más estrecha que en el adulto, para la fagocitosis de la levadura, de un adecuado nivel de complemento, y que pone de manifiesto factores intrínsecos, dependientes del leucocito PMN del neonato, y no sólo extrínsecos, dependientes de los niveles de opsoninas séricas, como había sido señalado por otros.12 Nuestros resultados concuerdan con los estudios sobre receptores para complemento leucocitario, donde se ha comprobado que la estimulación de neutrófilos aislados induce una rápida movilización de los receptores para complemento de un gran pool citoplasmático, e incrementa su expresión sobre la superficie celular.13 Debido a que la mayor parte del C3 fijado sobre la levadura consiste en C3bi7,14 la fagocitosis de levadura opsonizada requiere de poca unión a CR1, pero depende de CR3. Se ha comprobado además, que la unión de C3b a CR1 contribuye poco a la explosión respiratoria inducida por levaduras. En contraste con esto, anticuerpos monoclonales contra CR3 inhiben sustancialmente la producción de superóxido en iguales condiciones.15La justificación a los requerimientos incrementados de componentes del sistema complemento del leucocito PMN neonatal, para promover un nivel dado de unión, ingestión y activación del metabolismo oxidativo en relación con el adulto, cuando se parte de los niveles bajos proporcionados por el suero neonatal, podría estar relacionada directamente con la observación de que la expresión máxima de CR3 en neutrófilos neonatales estimulados es del 75 % del valor del adulto16 no así CR1, donde el incremento es superior en el recién nacido,13,16 lo que puede ser una de las causas de la respuesta del neonato a la infección, donde la limitada concentración de opsoninas en el sitio de ataque puede dañar la fagocitosis. La estabilidad alcanzada en la reducción del NBT en condiciones de un aporte de elementos del sistema de complemento apropiados, reflejan un metabolismo oxidativo del leucocito PMN del neonato intacto, hasta donde es capaz de hacerlo la prueba de reducción del NBT, prueba informada por otros autores3 con resultados elevados en el período neonatal en otras condiciones experimentales. El patrón aquí encontrado sería válido para aquellos microorganismos que siguen un modelo de opsonificación similar a la levadura, con estrecha dependencia de C3bi y CR3.
Subject headings: NITROBLUE TETRAZOLIUM; NEUTROPHILS; INFANT NEWBORN; FETAL BLOOD; PHAGOCYTOSIS; COMPLEMENT.
1 Especialista de II Grado en Bioquímica Clínica. Asistente. Instituto Superior de Ciencias Médicas de Villa Clara (ISCM-VC).
2 Doctora en Ciencias Médicas. Especialista de I Grado en Inmunología. Profesora Titular. ISCM-VC. ]]>