Rev Cubana Pediatr. 2017;89(2)
ARTÍCULO ORIGINAL
Estudio aleatorizado abierto de niños con exacerbación aguda del asma tratados con esteroides inhalados
Open randomized study of children with acute exacerbation of asthma and treated with inhaled steroids
Elías Kassisse,I Linair Prada,II Ixora Salazar,II Hecmary García,II Jorge KassisseIII
]]> IHospital "Dr. Santos Aníbal Dominicci". Carúpano, Estado Sucre, Venezuela.
RESUMEN
Introducción: la terapia primaria en la crisis de asma aguda, incluye administración de oxígeno, uso de β2-agonistas por vía inhalada y la administración de esteroides sistémicos. Las ventajas que se citan sobre el uso de los esteroides inhalados serían, su rápido inicio de acción y su buen perfil de seguridad, en contraposición a los esteroides sistémicos.
Objetivo: evaluar la utilidad de los corticoides inhalados en el tratamiento de la crisis de asma aguda en niños mayores de 2 años.
Métodos: se realizó un estudio prospectivo, transversal, experimental, aleatorizado, de eficacia clínica; la selección se realizó por medio de una tabla de números aleatorios, y se incluyeron tres grupos: el I recibió terapia estándar, el II la sustitución del esteroide sistémico por el inhalado y el III combinó a la terapia estándar el esteroide inhalado. El análisis estadístico se realizó por medio de ANOVA y chi cuadrado con una p< 0,05 como significativa.
Resultados: se estudiaron 165 pacientes, los tres grupos de tratamiento mejoraron la escala de severidad inicial. Los pacientes que recibieron esteroides inhalados adicionados a la terapia estándar, tuvieron 73 % de posibilidades de no ser hospitalizados, 27 % de posibilidades de reducir el riesgo de hospitalizaciones y de cada 100 pacientes tratados con la combinación, se pudieran prevenir 8 hospitalizaciones.
Conclusiones: los esteroides inhalados muestran equivalencia terapéutica a los esteroides sistémicos.
Palabras clave: asma aguda; corticosteroide inhalado; budesonida; corticosteroide sistémico.
ABSTRACT
Introduction: primary therapy for acute asthma attacks includes administration of oxygen, use of inhaled β2-agonists and of systemic steroids. The advantages of the use of inhaled steroids will be rapid onset of action and good safety profile in comparison with the systemic steroids.
Objective: to evaluate the usefulness of inhaled corticoids in treating acute asthma attacks in children older than 2 years.
Methods: prospective, cross-sectional, experimental, randomized study of clinical effectiveness was conducted; the selection of patients was based on a random number table and included three groups: the first received standard treatment, the second one replaced systemic steroid by the inhaled one and the third combined standard treatment and inhaled steroid. The statistical analysis included ANOVA and Chi-square with p< 0.05 as significant value. ]]>
Results: one hundred and sixty five patients were studied and the three treatment groups improved their initial severity scale. The patients who received inhaled steroids added to the standard therapy showed 73 % possibilities of non hospitalization, 27 % possibilities of reduced risk of hospitalization and 8 hospitalizations were prevented per every 100 patients treated with the combination.
Conclusions: inhaled steroids were therapeutically equivalent to systemic steroids.
Keywords: acute asthma; inhaled corticosteroid; budesonide; systemic corticosteroid.
INTRODUCCIÓN
El asma es un problema de salud a nivel mundial. La prevalencia es variable, y genera una alta proporción de gastos directos e indirectos.1,2
Los esteroides sistémicos forman parte integral del tratamiento de la exacerbación y deben ser iniciados de forma inmediata. Su uso se ha asociado a bajas tasas de admisiones;3-5 mientras que para estos se ha logrado establecer su uso y beneficios, no ha ocurrido así con los inhalados, y las conclusiones no han sido consistentes.6-8
]]> Los inhalados han mostrado ser seguros y efectivos en un evento agudo, poseen un inicio de acción y efecto mucho más rápido. Existen estudios que han mostrado su beneficio.9,10Comparten los mismos mecanismos de acción que los sistémicos, pero a los inhalados se les atribuye una propiedad adicional no genómica, y que actuarían a los pocos minutos de haber sido administrados. Esta respuesta está condicionada por la inhibición de la recaptura de la norepinefrina, y por lo tanto, se origina vasoconstricción con disminución del flujo sanguíneo epitelial y mejoría del edema. Este efecto es dosis dependiente y transitorio.11,12
Para la budesonida se ha determinado que la mejoría de la función pulmonar puede hacerse entre la primera y cuarta hora de haber sido inhalada, tanto en pacientes con asma estable como en asma aguda, y que esto puede ser acompañado de disminución de los marcadores inflamatorios entre la cuarta y sexta hora.13-15
El objetivo del presente estudio fue el evaluar la utilidad de usar esteroides inhalados durante el desarrollo de la exacerbación asmática en niños mayores de 2 años.
MÉTODOS
Se realizó un estudio prospectivo, transversal, aleatorizado, de eficacia clínica, en la sala de emergencia pediátrica del Hospital "Antonio Patricio De Alcalá", del Estado Sucre, en Venezuela, entre enero y diciembre de 2015. De manera secuencial fueron evaluados aquellos pacientes > de 2 años y < de 12 años que consultaron por exacerbación asmática.
Se consideraron como individuos asmáticos aquellos en quienes se había realizado el diagnóstico médico previo, o en aquellos que habían experimentado, al menos, más de tres exacerbaciones y que habían mejorado con el uso de broncodilatadores. Fueron excluidos aquellos con enfermedades cardiacas, renales, inmunológicas o hematológicas concomitantes. Igualmente fueron excluidos si habían sido hospitalizados en las últimas 4 semanas por cualquier causa, o si se encontraban recibiendo para el momento del estudio esteroides sistémicos o inhalados.
El estudio fue evaluado y aprobado por la Comisión de Estudio de Postgrado del hospital, quien reconoció los aspectos éticos ajustados a la Declaración de Helsinki. De todos los pacientes fue obtenido consentimiento por escrito.
La aleatorización se realizó por medio de una tabla de número aleatorios, generada por computadora, tomando los pacientes en bloques de 4 para cada estrategia de tratamiento.
]]> Se definieron tres grupos:- Grupo I: pacientes que recibieron la terapia estándar con β2-agonistas nebulizados y esteroides sistémicos por vía endovenosa.
- Grupo II: pacientes que recibieron β2-agonistas nebulizados y esteroides por vía nebulizada.
- Grupo III: pacientes que recibieron β2-agonistas nebulizados, esteroides sistémicos por vía endovenosa y esteroides por vía nebulizada (terapia combinada).
El β2-agonistas usado fue el salbutamol (Salbutamol®, Laboratorio Medigen, 1 mL/5 mg) calculado a 0,15 mg x kg dosis, suministrado por un nebulizador tipo jet accionado por aire comprimido.
El esteroide sistémico fue la metilprednisolona (Solumedrol® Laboratorio Pfizer, ampollas de 500 mg) calculada en todos los casos a 1 mg x kg dosis, y administrada por vía endovenosa.
El esteroide inhalado fue la budesonida (Budecort®, Laboratorio Ofatlmi, 1 mL/1 000 μg), la cual se administró por medio de nebulizador igualmente tipo jet. La dosis usada fue de 500 μg por cada sesión de nebulización, con un máximo de 2 000 μg como dosis acumulada. El volumen máximo de las soluciones nebulizadas -solas o combinadas- fue de 3 cc completados con solución salina normal (0,9 %).
En los pacientes que recibieron solo las nebulizaciones con salbutamol, este fue nebulizado cada 15 minutos durante la primera hora de permanencia en la sala de emergencias. El esteroide sistémico fue colocado por vía endovenosa desde el mismo momento que la primera nebulización con el salbutamol. Los pacientes que recibieron el esteroide inhalado, recibieron nebulización con 500 μg (10 gotas) cada 15 minutos durante la primera hora.
La medición de la eficacia de cada intervención terapéutica se realizó por medio de la Escala de Severidad del Asma (ESA) o PIS siglas en inglés de Pulmonary Index Score, el cual incluye 4 parámetros de evaluación: la frecuencia respiratoria, la presencia de las sibilancias, la relación entre la inspiración y la espiración, y el uso de los músculos accesorios.16 A cada parámetro se le asignó un puntaje de 0 a 3 según la severidad observada, por lo cual la escala iba desde 0 a 12 puntos, desde el menor puntaje al máximo puntaje. Se consideró que la crisis era de presentación leve, si el puntaje fue ≤ de 4 puntos, moderada si era ≤ a 7, y severa si era ≥ 8. Adicionalmente se midió la saturación de O2.
]]> El resultado primario, objeto de este estudio, fue la diferencia obtenida en la media de la escala de severidad a las 2 horas después de la intervención terapéutica seleccionada, y se consideraron como significativas las variaciones mayores de 2 puntos. El análisis estadístico usado fue el Análisis de Varianza de una Vía (ANOVA), y cuando hubo diferencias fue seguido de una prueba a posteriori Student-Newman-Keuls (SNK) al 95 %.Los resultados secundarios estudiados fueron las diferencias observadas en el puntaje a las 2 horas para la frecuencia respiratoria, la presencia de sibilancias, el uso de los músculos accesorios y la saturación de O2. Este análisis también se realizó por ANOVA, y cuando hubo significancia se siguió de una prueba a posteriori SNK al 95 %.
Los otros análisis de interés del estudio, como la tasa de hospitalización, la duración de la hospitalización en relación con la estrategia de tratamiento, la severidad y los cambios a las 2 horas de la escala de severidad, se realizó por medio de la prueba chi cuadrado, con un nivel de significancia de p< 0,05.
RESULTADOS
Se incluyeron 165 pacientes, y las características basales se observan en la tabla 1. La edad promedio fue de 4,7±2,18 años, 57 % correspondieron al sexo masculino, la ESA fue de 4,3±1,05 puntos y saturación oxigeno de 94,7±2,10.
La mayoría correspondió a crisis moderadas, 125 (76 %), 35 (21 %) como leves, y el resto severos (5 pacientes, 3 %).
A las 2 horas de intervención terapéutica, se encontró que los tres grupos, de forma general, fueron capaces de modificar ESA en por lo menos 2 puntos, y no hubo diferencias significativas con respecto a las variaciones de la ESA (p= 0,3975).
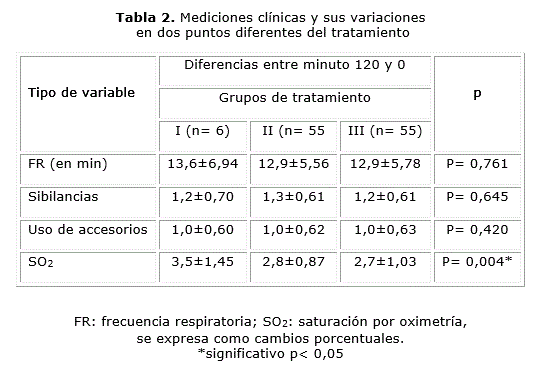
Las variaciones porcentuales fueron observadas para todos los pacientes independientemente de la severidad inicial. De los 35 pacientes con exacerbaciones leves, los asignados al grupo III prácticamente a las 2 horas estaban en 0 puntos; así mismo, en las clasificadas como moderadas a severas, el tratamiento con mayor variación, según el porcentaje inicial, estuvo a favor de los pacientes con la combinación de esteroides sistémicos adicionados a la terapia estándar. Sin embargo, no guardaron significación estadística (p> 0,05). Esta variación fue en promedio del 20 % para cada grupo de tratamiento. Las variaciones medidas entre el tiempo 120 y 0 minutos para los parámetros de severidad según la estrategia de tratamiento seleccionada, se muestran en la tabla 2.
]]> El único parámetro con significación estadística relacionado con el tratamiento fueron los cambios en la saturación de oxígeno (SO2).En 65 pacientes se demostró SO2 por debajo del 94 % de forma inicial, que representa el 39,3 % del total de los pacientes evaluados; de estos, el 40 % (26), el 35 % (23) y el 25 % (16) correspondieron a los grupos I, II, y III respectivamente. Para el final de la segunda hora se observó que solo 12 (18 %) aún continuaban con SO2< 94 %. Para este momento solo quedaron 3, 6 y 3 pacientes aún con SO2< 94 % para cada grupo de tratamiento respectivamente.
El ANOVA y el análisis a posteriori SKN al 95 % demostró que los pacientes del grupo I fueron los que experimentaron las mayores variaciones, lo cual se tradujo en una corrección mucho más rápida de la oxigenación, mientras que los del grupo II y III tuvieron variaciones menores (p< 0,0004).
En relación con la tasa de hospitalización, medida a la segunda hora de haber iniciado el tratamiento, fue del 26,06 %. No se encontraron diferencias significativas entre las tres estrategias de tratamiento y la tasa de hospitalizaciones (χ2= 0,92 NS; χ2= 5,991) (tabla 3).
Como se quería medir el impacto clínico que los esteroides inhalados pudieran tener sobre la tasa de hospitalización, se realizó un análisis post-hoc de los subgrupos de tratamiento y se comparó la terapia estándar versus terapia combinada. Este análisis por grupos de tratamiento encontró una variación del 30 % (18/60) para la terapia estándar, del 25,5 % (14/41) y del 22 % (11/39) para los grupos II y III respectivamente.
El riesgo relativo (RR) y las reducciones de los riesgos relativos (RRR) y absolutos (RRA), indican elementos de probable utilidad clínica más allá de la significación estadística. Para este estudio se encontró 73 % RR, 27 % RRR y 8 % de RRA; es decir, los pacientes que recibieron esteroides inhalados adicionados a la terapia estándar, tuvieron 73 % de posibilidades de no ser hospitalizados, 27 % de posibilidades de reducir el riesgo de hospitalizaciones, y por último, de cada 100 pacientes tratados con la combinación se pudieron prevenir 8 hospitalizaciones. Con estos mismos datos se calculó el número necesario de tratamiento (NNT), el cual fue de 13; o sea, se necesitarían tratar 13 pacientes con esteroides inhalados adicionados a la terapia estándar, para prevenir una hospitalización. Estos datos se expresan en la tabla 4.
De los 43 pacientes ingresados (20; 46,5 %) tuvieron una estadía hospitalaria entre 1 a 2 días, mientras que en el 53,49 % la estadía fue entre los 3 a 5 días. El análisis estadístico no permitió reconocer significación estadística entre la estrategia inicial de tratamiento y la estadía (p> 0,05). Es de resaltar que de los 11 pacientes que se ubicaron en el grupo III, 7 fueron egresados dentro de las primeras 48 horas (63 % de ellos en comparación con el egreso del 50 % para el grupo I y del 28 % del grupo II).
Este estudio también evaluó la relación existente entre la variación de la ESA y su asociación con el riego del ingreso y la permanencia en la hospitalización. En primer lugar, el riesgo de hospitalización estuvo estrechamente relacionado con las pocas variaciones en la ESA, aquellos pacientes que no fueron capaces de modificar en por lo menos 2 puntos el ESA inicial, a las 2 horas de finalizado el tratamiento, tuvieron mucho mayor riesgo de ser hospitalizado, y esto con significación estadística (X 2= 84,74; χ2= 13,815), lo que puede ser observado en la tabla 5; y en segundo lugar, la poca modificación de la ESA no estuvo relacionada con la estadía (p> 0,05). No se registraron abandonos, así como tampoco efectos adversos.
]]>DISCUSIÓN
La exacerbación del asma es una de las condiciones más vistas en las salas de emergencias pediátricas. El III Reporte del Panel de Expertos, así como las Guías Iniciativa Global para el Asma (GINA), recomiendan que los esteroides sistémicos deben ser usados muy precozmente en las emergencias junto con las nebulizaciones de salbutamol y oxígeno húmedo.17,18
Se seleccionó las 2 horas como punto de finalización del estudio, tal como ha sido sugerido basado en los aspectos farmacocinéticos de los esteroides nebulizados, en los que se ha estimado que el pico de budesonida inhalada se alcanza a los 20 minutos luego de nebulizar 1 mg, y que su vida media es de 2,3 horas.8,19
La respuesta inicial al tratamiento aplicado en la sala de emergencia es el mejor predictor de la necesidad de hospitalización, de allí que las escalas de severidad sean una herramienta útil de evaluación dinámica que permiten reconocer lo efectiva de una estrategia terapéutica.20-22
En el estudio en el cual se comparó budesonida 800 µg por nebulización versus prednisona oral a 2 mg/kg en niños de 2-12 años, encontraron que ambos tratamientos fueron capaces de mejorar la función pulmonar así como la escala de severidad, llamando la atención que el mayor efecto se consiguió con la budesonida nebulizada.23
En otro estudio, los pacientes recibieron dosis única de prednisona (2 mg/kg) o 1 600 µg de budesonida por turbuhaler, y no se encontraron diferencias estadísticas en la función pulmonar ni en la escala de síntomas, lo que sugiere que las altas dosis de esteroides inhalados tienen efectos similares a los esteroides sistémicos. El seguimiento de la función adrenal de estos concluyó que poseen un perfil de seguridad mayor.9 En otra publicación se concluye que los pacientes que habían recibido los inhalados combinados a los sistémicos, tuvieron mejor función pulmonar, pero no mejoría de la escala de síntomas.24
Este estudio demostró que el uso de esteroides inhalados posee equivalencia terapéutica a los esteroides sistémicos, ya sea como sustituto de estos o adicionado a la terapia estándar, ya que fueron capaces de modificar la severidad inicial a las dos horas de haberse usado. Esto está relacionado con los resultados de impacto clínico, porque pese a no existir significación estadística que demuestre la superioridad, el impacto clínico pareciera ser importante, ya que se observó que, para la primera hora de tratamiento, los pacientes asignados a la estrategia de la combinación modificaron su escala de gravedad de forma mucho más importante, llegando proactivamente a 0 puntos, tanto para los pacientes con exacerbación grave, como para los de exacerbaciones moderadas. Los cambios observados en la saturación de oxígeno fueron evidentes en todos los grupos de tratamiento.
En un estudio de 49 niños asmáticos que experimentaron una exacerbación moderada se comparó prednisona por vía oral versus budesonida inhalada, y se observó que el único parámetro que experimentó significativa variación fue la saturación de oxígeno, la cual fue mayor en el grupo que recibió prednisona.25 Una explicación a esto se le puede atribuir a la falta de estandarización de los estudios en los que se han utilizado distintos esteroides -tanto inhalados como sistémicos-, así como a las distintas dosis usadas, o que se están midiendo dos fenómenos distintos en el paciente asmático: los signos y síntomas con el funcionalismo pulmonar SO2, ya que ha sido demostrada la pobre correlación existente entre los valores del volumen espirado forzado en el primer segundo (VEF1) y los cambios de la gasometría arterial.26
Dos metaanálisis recientes, estudiaron exclusivamente el uso de esteroides inhalados en niños con asma aguda y concluyeron de la misma manera. El primero señala que no existen evidencias que hagan diferentes los esteroides sistémicos, en comparación a los inhalados, en términos de tasas de hospitalizaciones, visitas no programadas o necesidad de cursos adicionales de esteroides sistémicos durante una exacerbación asmática. El segundo señala que el uso de esteroides inhalados en niños con asma aguda mostró tasas similares de hospitalización, cuando se compararon con los esteroides sistémicos.27,28
]]> Probablemente sea la tasa de hospitalización uno de los resultados primarios medidos de manera uniforme en la mayoría de los estudios, sin diferencias significativas entre el uso de esteroides sistémicos versus los inhalados, que pueden ir desde 0 hasta 60 % en algunas publicaciones.6,7,29,30En una revisión sistemática se incluyeron 5 estudios en los que evaluaron el efecto sobre la tasa de hospitalización en 191 niños tratados con esteroides inhalados contra 180 que recibieron placebo, y se encuentra que los niños que recibieron el esteroide inhalado tuvieron menos probabilidad de ser hospitalizados (OR= 0,30; IC= 95 % 0,16-0,57).31
En 180 pacientes pediátricos, fue evaluada la relación existente entre los cambios de la escala de severidad a las 2 horas de tratamiento, y el riesgo de hospitalización para comparar budesonida inhalada versus placebo, y se encontró que no hubo diferencias en las variaciones de la escala de severidad y el riesgo siguiente de hospitalización.8
Bottaro,32 en su artículo Claves para la interpretación de conceptos estadísticos en estudios de investigación, plantea la interesante discusión entre relevancia clínica y la significación estadística, y sugiere que es el tamaño del efecto, no el tamaño de la significación lo que es relevante para la práctica.
Esa pudiera ser la situación de esta investigación, donde la p resultó sin significación estadística, pero el análisis post-hoc del estudio sugiere que el uso precoz desde la primera nebulización con esteroide combinado al esteroide sistémico, posee un impacto clínico que hace considerar su uso, como se pudo demostrar por los análisis de RR, RRR y reducción absoluta del riesgo (RAR). El NNT coloca a este estudio en esa posibilidad. Rowe y otros,33 en su estudio, ubicaron este número en 9, es decir 9 pacientes necesitaron recibir la budesonida inhalada para prevenir una recaída.
Un estudio pediátrico que incluye la adición de esteroides inhalados a la terapia estándar, es el de Akhtaruzzaman y otros,34 en el cual evaluaron 65 pacientes asignados doble ciego, placebo controlado, con exacerbaciones moderadas a severas, y señalaron que el efecto inmediato positivo de la budesonida nebulizada al tratamiento estándar de las exacerbaciones, es un hallazgo alentador para las posteriores investigaciones de su uso rutinario en el tratamiento de las exacerbaciones en los niños.
El segundo estudio, con un diseño de adición a la terapia estándar, es el de Razi y otros,35 en el cual adicionaron budesonida o placebo al estándar, y encontraron que los que habían recibido la combinación fueron niños con menores estadías hospitalarias, y los costos de atención se redujeron de forma significativa.
Las limitaciones que se pueden señalar es que no se trata de un estudio multicéntrico, probablemente limitado en su poder estadístico en la muestra para demostrar los cambios efectivos en la ESA, por ello, no se pudo demostrar la superioridad de los esteroides inhalados, y se logró establecer solo su efecto equiparable al uso de los sistémicos.
Los resultados del presente estudio permiten concluir que existe equivalencia terapéutica entre los esteroides sistémicos y los esteroides inhalados.
]]> Conflicto de intereses
Los autores declaran no tener conflicto de intereses en la realización del estudio.
Agradecimiento
Al doctor Isaac Sánchez, estadístico egresado de la Universidad Central de Venezuela, por su apoyo en los análisis aquí presentados.
REFERENCIAS BIBLIOGRÁFICAS
1. Masoli M, Fabian D, Holt S, Beasley R. The global burden of asthma: executive summary of the GINA Dissemination Committee Report. Allergy. 2004;59:469-78.
2. Weiss K, Sullivan S, Lyttle C. Trends in the cost of illness for asthma in the United States, 1985-1994. J Allergy Clin Immuno. 2000;106:493-9.
3. Roy S, Milgron H. Management of the acute exacerbation of asthma. J Asthma. 2003;40:593-604.
4. Urso D. Treatment for acute asthma in the Emergency Department: practical aspects. Eur Rev Med Pharmacol Sci. 2010;14(3):209-14.
5. Powell R. Acute severe asthma. Journal of Paediatrics and Child Health. 2016;52:187-91.
6. Schuh S, Reisman J, Alshehri M, Dupuis A, Corey M, Arseneault R, et al. A comparison of inhaled fluticasone and oral prednisone for children with severe acute asthma. N Engl J Med. 2000;343:689-94.
7. Volovitz B, Bentur I, Finkelstein Y. Effectiveness and safety of inhaled corticosteroids in controlling acute asthma attacks in children who were treated in the emergency department: a controlled comparative study with oral prednisolone. J Allergy Clin Immunol. 1998;102:605-9.
8. Upham B, Mollen C, Scarfone R, Seiden J, Chew A, Zorc J. Nebulized budesonide added to standard pediatric emergency department treatment of acute asthma: a randomized, double-blind trial. Acad Emerg Med. 2011;18:665-73.
9. Nuhoglu Y, Bahceciler N, Barlan I, Müjdat M. The effectiveness of high-dose inhaled budesonide therapy in the treatment of acute asthma exacerbations in children. Ann Allergy Asthma Immunol. 2001,86:318-22.
10. Edmonds M, Camargo C, Pollack C, Rowe B. The effectiveness of inhaled corticosteroids in the emergency department treatment of acute asthma: a meta-analysis. Ann Emerg Med. 2002;40:145-50.
11. Horvath G, Vasas A, Wanner A. Inhaled corticosteroids reduce asthma-associated airway hyperperfusion through genomic and nongenomic mechanisms. Pulm Pharmacol Ther. 2007;20:157-62.
12. Mendes E, Cadet L, Arana J, Wanner A. Acute effect of an inhaled glucocorticosteroid on albuterol-induced bronchodilation in patients with moderately severe asthma. Chest. 2015;147(4):1037-42.
13. Volovitz B, Nussinovitch M, Finkelstein Y, Harel L, Varsano I. Effectiveness of inhaled corticosteroids in controlling acute asthma exacerbations in children at home. Clin Pediatr. 2001;40:79-86.
14. Rodrigo G. Rapid effects of inhaled corticosteroids in acute asthma: an evidence-based evaluation. Chest. 2006;130:1301-11.
15. Vathenen A, Knox A, Wisniewski A, Tattersfield A. Time course of change in bronchial reactivity with an inhaled corticosteroid in asthma. Am Rev Respir Dis. 1991;143(6):1317-21.
16. Hsu P, Lam LT, Browne G. The pulmonary index score as a clinical assessment tool for acute childhood asthma. Ann Allergy Asthma Immunol. 2010;105:425-9.
17. Expert Panel Report 3 (EPR-3): guidelines for the diagnosis and management of asthma-summary report 2007. J Allergy Clin Immunol. 2007;120:S94-S138.
18. Global strategy for asthma management and prevention. Global Initiative for Asthma (GINA) [homepage en Internet]; GINA, 2016 [citado 28 de Agosto de 2016]. Disponible en: http://ginasthma.org/
19. Agertoft L, Andersen A, Weibull E, Pedersen S. Systemic availability and pharmacokinetics of nebulised budesonide in preschool children. Arch Dis Child. 1999;80:241-7.
20. Takeshi K, Kenichi T, Atsushi I, Eiji M, Yutaka U, Toshio K. Usefulness of modified Pulmonary Index Score (mPIS) as a quantitative tool for the evaluation of severe acute exacerbation in asthmatic children. Allergology International. 2015;64:139-44.
21. Ducharme FM, Chalut D, Plotnick L, Savdie C, Kudirka D, Zhang X. The Pediatric Respiratory Assessment Measure: a valid clinical score for assessing acute asthma severity from toddlers to teenagers. J Pediatr. 2008;152:476-80.
22. Buyuktiryaki A, Civelek E, Can D, Orhan F, Aydogan M, Reisli I. Predicting hospitalization in children with acute asthma. J Emerg Med. 2013;44:919-27.
]]>23. Devidayal S, Singhi S, Kumar L, Jayshree M. Efficacy of nebulized budesonide compared to oral prednisolone in acute bronchial asthma. Acta Paediatr. 1999;88:835-40.
24. Nuhoglu Y, Nuhoglu A. Acute effect of nebulized budesonide in asthmatic children. J Invest Allergol Clin Immunol. 2005;15:197-200.
25.Milani G, Rosário N, Riedi C, Figueiredo B. Nebulized budesonide to treat acute asthma in children. J Pediatr (Rio J). 2004;80:106-12.
26. McFadden E, Kiser R, DeGroot W. Acute bronchial asthma. Relations between clinical and physiologic manifestations. N Engl J Med. 1973;288:221-5.
27. Beckhaus A, Riutort M, Castro-Rodriguez JA.Inhaled versus systemic corticosteroids for acute asthma in children. A systematic review. Pediatric Pulmonology. 2014;49:326-34.
]]>28. Su X, Yu N, Kong L, Kang J. Effectiveness of inhaled corticosteroids in the treatment of acute asthma in children in the emergency department: A meta-analysis. Annals of Medicine. 2014;46:24-30.
29. Manjra A, Price J, Lenney W, Hughes S, Barnacle H. Efficacy of nebulized fluticasone propionate compared with oral prednisolone in children with an acute exacerbation of asthma. Respir Med. 2000;94:1206-14.
30. Nakanishi A, Klasner A, Rubin B. A randomized controlled trial of inhaled flunisolide in the management of acute asthma in children. Chest. 2003;124:790-4.
31. Volovitz B. Inhaled budesonide in the management of acute worsenings and exacerbations of asthma: A review of the evidence. Respir Med. 2007;101:685-95.
32. Bottaro F. Claves para la interpretación de conceptos estadísticos en estudios de investigación. Hematología. 2013;71:299-305.
]]>33. Rowe B, Bota G, Fabris L, Therrien S, Milner R, Jacono J. Inhaled budesonide in addition to oral corticosteroids to prevent asthma relapse following discharge from the emergency department: a randomized controlled trial. JAMA. 1999;281:2119-26.
34. Akhtaruzzaman M, Ahmed S, Hoque M, Choudhury A, Hossain M, Islam M, et al. Effects of nebulized budesonide as an adjunct to standard treatment of asthma exacerbations: a randomized, double-blind, placebo-controlled trial. Mymensingh Med J. 2014;23:418-25.
35. Razi C, Akelma K, Harmanci K, Kocak M, Kuras C. The addition of inhaled budesonideto standard therapy shortens the length of stay in hospital for asthmatic preschool children: A randomized, double-blind, placebo-controlled trial. Int Arch Allergy Immunol. 2015;166:297-303.
Recibido: 17 de diciembre de 2016.
Aprobado: 2 de enero de 2017.
]]>
Elías Kassisse. Hospital "Dr. Santos Aníbal Dominicci". Avenida Universitaria, Sector Primero de Mayo, Carúpano. Estado Sucre, Venezuela. Correo electrónico: ekassisse@gmail.com
]]>