Manejo terapéutico y supervivencia del cáncer de cuello uterino en el Instituto Nacional de Oncología y Radiobiología (2004-2010)
Therapeutic management and survival of cervical cancer at the National Institute of Oncology and Radiobiology (2004-2010)
Juan Mario Silveira Pablos, Madelaine Sarria Castro, Orlando Parellada Joa, Carlos Gurdián López, Roberto Esperón Noa, Omar Bosque Diego
Instituto Nacional de Oncología y Radiobiología. La Habana, Cuba.
]]>
RESUMEN
Introducción: el cáncer de cuello uterino es uno de los principales problemas de la salud pública en el mundo por sus altas tasas de incidencia y mortalidad en la mujer.
Objetivos: describir el manejo de las pacientes diagnosticadas con cáncer cérvico uterino admitidas y atendidas en el Instituto Nacional de Oncología y Radiobiología.
Método: estudio descriptivo, retrospectivo en una serie de 853 pacientes diagnosticadas con cáncer de cuello uterino (estadios IA-IVA, FIGO 2009). Se realizaron pruebas de hipótesis y análisis de supervivencia. Para la estimación de la supervivencia se utilizó el método estadístico de Kaplan-Meier. Se aplicó la prueba de Long Rank para comparar la supervivencia por estratos. Se consideró como diferencia estadísticamente significativa p< 0,05.
Resultados: edad promedio de las pacientes, 49,7 años (DS: ± 13,9), 56,6 % no se habían realizado la citología cervical. El seguimiento citológico, según establece el Programa de Diagnóstico Precoz del Cáncer de Cuello Uterino, se cumplió por 84,1 % de las mujeres pesquisadas; en 15,9 % de los casos, el periodo de seguimiento citológico fue superior a los 3 años. El carcinoma epidermoide fue la variedad histológica más frecuente (88,2 %). Del total de pacientes, 87,1 % fueron diagnosticadas en estadios localmente avanzados (FIGO IB2-IVA). La modalidad terapéutica más empleada fue la quimio radioterapia concurrente. La tasa de supervivencia global al diagnóstico fue de 47,2 %. La mediana de supervivencia fue de 4 años. La edad al diagnóstico y el estadio del tumor mostraron una asociación estadísticamente significativa con la supervivencia global (p< 0,005).
Conclusiones: la incidencia y mortalidad de cáncer de cuello uterino, así como su estabilidad en el último quinquenio, exigen la realización de estudios de mayor alcance e investigaciones dirigidas a la evaluación de los programas, sistemas y servicios de salud implicados.
Palabras clave: cáncer cervical; VPH; citología; supervivencia.
ABSTRACT
Introduction: cervical cancer is one of the main public health problems in the world due to its high incidence and mortality rates in women. ]]>
Objective: to describe the management of patients diagnosed with uterine cervical cancer admitted and treated at the National Institute of Oncology and Radiobiology.
Method: descriptive, retrospective study in a series of 853 patients diagnosed with cervical cancer (stages IA-IVA, FIGO 2009). Hypothesis testing and survival analysis were performed. The Kaplan-Meier statistical method was used to estimate survival. The Long Rank test was used to compare survival by strata. Statistically significant difference was considered p < 0.05.
Results: mean age of the patients, 49.7 years (DS: ± 13.9), 56.6 % had not performed the cervical cytology. Cytological follow-up, according to the Early Diagnosis Program of Cervical Cancer, was met by 84.1 % of the women surveyed; in 15.9 % of the cases, the cytological follow-up period was superior to 3 years. Epidermoid carcinoma was the most frequent histological variety (88.2 %). Of the total number of patients, 87.1 % were diagnosed in locally advanced stages (FIGO IB2-IVA). The most commonly used therapeutic modality was concurrent chemo radiotherapy. The overall survival rate at diagnosis was 47.2 %. The median survival was 4 years. Age at diagnosis and tumor stage showed a statistically significant association with overall survival (p < 0.005).
Conclusion: cervical cancer incidence and mortality, as well as its stability over the last five years, require more extensive studies and research aimed at evaluating the health programs, systems and services involved.
Key words: cervical cancer; HPV; cytology; survival.
INTRODUCCIÓN
El cáncer de cuello uterino (CCU) es uno de los principales problemas de la salud pública por sus altas tasas de incidencia y mortalidad en la mujer. Es una enfermedad controlable a partir de la efectividad de los programas de prevención y pesquisa; conjuntamente con el diagnóstico y tratamiento precoz de los casos.
]]> Según informes publicados por la Agencia Internacional de Investigaciones en Cáncer (IARC) sobre estimaciones de incidencia y mortalidad por cáncer en el mundo, en el año 2012 el cáncer de cérvix ocupó el cuarto lugar en incidencia y el quinto en mortalidad por cáncer en la población femenina. El número de mujeres diagnosticadas superó los 526 000 casos. El CCU solo fue precedido por el cáncer de piel no melanoma, el cáncer de mama y el cáncer colorectal. En cuanto a la mortalidad, fallecieron por cáncer de cérvix más de 265 000 mujeres en el año. El pronóstico para el año 2030 es que las cifras superen las 410 000 defunciones anuales.1,2El cáncer de cuello uterino es la principal causa de años de vida perdidos (por cáncer) en las mujeres de América Latina y el Caribe. Aquí se concentra 13 % de los casos y 12 % de las muertes que ocurren anualmente en el mundo, constituye uno de los ejemplos claros de inequidad en salud. La carga de la enfermedad difiere ampliamente entre países y regiones.
Al evaluar las tendencias en la mortalidad por CCU en la Región Latinoamericana y Caribeña, se aprecia que Puerto Rico es el único país que ha mantenido una tasa por debajo de cuatro muertes por 100 000 desde los años setenta. Chile, Costa Rica, México y Colombia, muestran reducciones significativas pero aún tienen tasas de mortalidad sobre 5 por 100 000, y países que ya tenían tasas de mortalidad por debajo de 10 por 100 000 en los setenta como Cuba, Argentina, Brasil y Uruguay, no han logrado mayor descenso en el riesgo de muerte por dicha enfermedad.3
En el año 2012 se reportaron en Cuba, 1 841 casos nuevos de CCU, para una tasa de incidencia de 32,8 por cada 100 000 mujeres (21,9 Tasa ajustada por edad a la población mundial). Estos resultados la ubica en el cuarto lugar en incidencia en el sexo femenino; solo precedido por el cáncer de piel no melanoma, mama y pulmón. En el año 2015, la tasa de mortalidad fue de 8,3 por 100 000 mujeres, periodo en el que se establece como la quinta causa de muerte por cáncer en la mujer cubana. En los últimos 5 años, más del 4,5 % de las defunciones en la mujer son por esta causa. Actualmente, se considera que la infección persistente por el virus de papiloma humano (VPH) es el factor más importante en el desarrollo del cáncer cervical y su incidencia.4-6
En los últimos 60 años, luego de la introducción de la Prueba de Papanicolaou, se ha percibido una reducción considerable de las tasas de incidencia y mortalidad por CCU de células escamosas, fundamentalmente en aquellos países en los que existen programas nacionales de pesquisaje.7 El tiempo del estadio preinvasivo del CCU, la alta tasa de prevalencia de VPH en poblaciones no pesquisadas, y la sensibilidad de la pesquisa citológica hacen del carcinoma cervical una meta ideal para la detección del cáncer. Un 90 % de las mujeres enfermas podrían ser diagnosticadas en etapas tempranas. No obstante, existe una baja adherencia de la mujer supuestamente sana a los controles periódicos fundamentalmente en los países en vías de desarrollo.
En consecuencia, aún se diagnostican innumerables casos con enfermedad localmente avanzada o enfermedad metastásica con pronóstico reservado, lo que resulta en una baja tasa de supervivencia. Solo aquellas naciones que han garantizado la calidad de los programas para el control y prevención del CCU y el perfeccionamiento de las técnicas de pesquisa, han experimentado una sustancial disminución en las tasas de incidencia y mortalidad por cáncer cervical. El diagnóstico en etapas tempranas de la enfermedad es garantía de tasas de supervivencia a los cinco años superiores al 92 %. En la actualidad, el CCU es una enfermedad prevenible y potencialmente curable.
Las políticas de salud pública establecidas en Cuba desde hace más de 4 décadas han permitido la incorporación de programas de salud con el interés de reducir la incidencia y mortalidad aportada por esta enfermedad, como es el caso del Programa de detección y diagnóstico precoz del cáncer cérvico uterino establecido desde 1967.8
No obstante, el problema en cuestión permanece vigente y con tendencias a incrementarse según las estadísticas de incidencia y mortalidad reportadas por el Registro Nacional de Cáncer. La presente investigación tiene por objetivo describir las pacientes con cáncer de cuello uterino que han sido atendidas y diagnosticadas en el Instituto Nacional de Oncología y Radiobiología –institución en la que son atendidos anualmente más del 13 % de los casos con cáncer ginecológico del país–, a partir de aspectos epidemiológicos y clínicos de la enfermedad, así como los principales resultados del manejo terapéutico de los casos.
MÉTODOS
]]> Se realizó un estudio descriptivo, retrospectivo. El universo estuvo constituido por las pacientes diagnosticadas de cáncer de cérvix inscriptas y atendidas en el Instituto Nacional de Oncología y Radiobiología (INOR), desde enero de 2004 hasta diciembre de 2010 con un período de seguimiento de 5 años posterior a su tratamiento oncoespecífico. El estadiamiento de los casos se realizó según los criterios de la Federación Internacional de Ginecología y Obstetricia (FIGO) 2009.Criterios de inclusión: Pacientes con diagnóstico histológico de carcinoma de cérvix, tratamiento oncoespecífico iniciado y concluido en la institución.
Criterios de exclusión: Pacientes con diagnóstico de carcinoma in situ. Pacientes que recibieron tratamiento oncológico previo en otro centro.
Fuentes de información: Historia clínica del paciente y certificados médicos de defunción. Se recolectó información relacionada con: datos generales y sociodemográficos, antecedentes de citología vaginal realizada, características clínico patológicas de la enfermedad, manejo terapéutico, evaluación de la respuesta al tratamiento según criterios de RECIST9 y deceso del paciente.
Análisis estadístico: Se emplearon medidas descriptivas. Para la estimación de la supervivencia global se utilizó el método estadístico de Kaplan-Meier. Para la comparación entre las curvas de supervivencia según variables de interés se utilizó la prueba de Log Rank. Se consideró como diferencia estadísticamente significativa valores de p< 0,05. Se calcularon Intervalos de Confianza con un 95 % de confiabilidad.
RESULTADOS
En el Instituto Nacional de Oncología y Radiobiología (INOR, La Habana, Cuba), la cifra de pacientes con cáncer que son admitidos anualmente, asciende a los 3 200 casos según estadísticas ofrecidas por el Departamento de Registros Médicos y Estadísticas de la institución. De ellos, aproximadamente 21 % corresponden a pacientes con cáncer ginecológico.
El cáncer cérvicouterino es la entidad que con mayor frecuencia es diagnosticada en el Servicio de Ginecología Oncológica. Históricamente, más del 50 % de las mujeres atendidas con cáncer ginecológico presentan dicho diagnóstico.
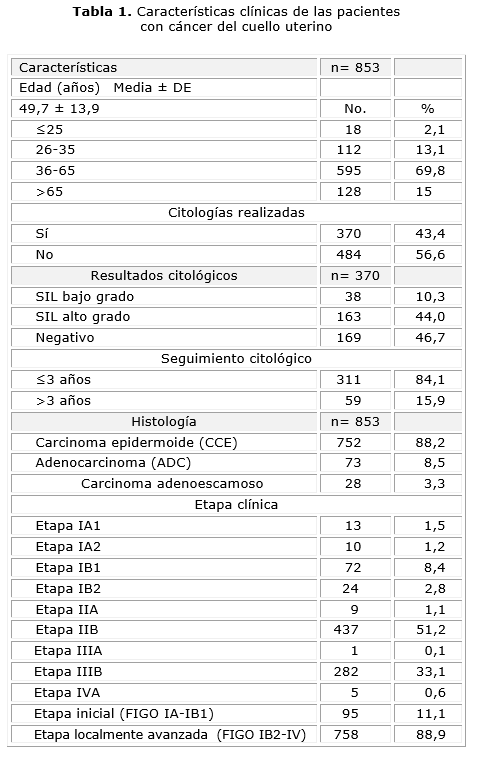
El estudio se realizó en una serie de 853 mujeres atendidas en el INOR con diagnóstico de CCU, desde 2007 hasta 2010. Se pudo constatar que 69,8 % de las pacientes con CCU (595 casos) tenían edades comprendidas entre 36 y 65 años al momento del diagnóstico, 15,2 % de ellas con edad ≥ 35 años. La media de edad cumplida de las pacientes fue 49 años (DS ± 13,9).
]]> En cuanto a los antecedentes de citología vaginal realizada, en 56,6 % (484 pacientes) no se realizó la prueba. Se examinaron 370 mujeres, de las cuales, 169 (45,7 %) resultaron negativas, 163 pacientes (44 %) se identificaron con lesiones escamosas intraepiteliales (SIL) de alto grado y las 38 pacientes restantes (10,3 %) presentaron lesiones escamosas intraepiteliales (SIL) de bajo grado. El seguimiento citológico, según lo establecido en el Programa de Detección del CCU, fue cumplimentado por 84,1 % de las mujeres pesquisadas; en 15,9 % de los casos, el periodo de seguimiento citológico fue superior a los 3 años (tabla 1).El carcinoma epidermoide (CCE) fue la variedad histológica más frecuente, presente en el 88,2 % de las mujeres, seguido en frecuencia por el Adenocarcinoma (ADC) (8,5 %) y el carcinoma adenoescamoso (3,3 %) (tabla 1).
Del total de pacientes, 88,9 % fueron diagnosticadas con enfermedad localmente avanzada (estadio clínico IB2 - IVA). Más del 50 % de las mujeres se encontraban en estadio IIB con una media de edad de 48 años (DS ± 13,5) y mínima de 20. Solo fueron diagnosticadas 95 pacientes (11,1 %) en estadios iniciales del CCU (IA1-IB1). Es importante señalar que 24,2 % de los casos en estadios iniciales tenían edades ≥ 35 y una edad mínima de 19 años (tabla 1).
Entre los tratamientos oncoespecíficos realizados, la radio-quimioterapia concurrente (RTP/QTP) fue la modalidad terapéutica más utilizada (83,9 %), tratamiento de elección a partir de la etapa IB2. En orden de frecuencia, le continuó la radio-quimioterapia concurrente asociada a la cirugía (Cir.-RTP/QTP), tratamiento efectuado en 7 % de las pacientes. La radioterapia (RTP) formó parte del esquema de tratamiento en 96,1 % de los casos.
Se realizó cirugía a 100 pacientes (12 %). Del total de casos quirúrgicos, 59 % fueron sometidos a histerectomía radical de Werthein-Meigs y al resto de las féminas se realizó histerectomía simple extrafacial (41 %).
Se evidenció una respuesta completa al tratamiento oncoespecífico en 84,4 % de las pacientes; en un 8,2 % se obtuvo respuesta parcial. Según los criterios anatomopatológicos y estadiamiento clínico, se observó mayor frecuencia de respuesta completa al tratamiento en los pacientes con diagnóstico histológico de carcinoma epidermoide, en tumores bien diferenciados y en estadios iniciales de la enfermedad (tabla 2).
Hubo recaída del tumor en 23,1 % de los pacientes que habían tenido una respuesta completa al tratamiento (167 casos); y en 76,6 % de ellos, la recaída fue locoregional, el 94 % de la recaída tumoral se produjo en pacientes con enfermedad localmente avanzada. Igualmente, se evidenció una asociación estadísticamente significativa entre la etapa clínica y el mal pronóstico de la enfermedad (p< 0,005) (tabla 2).
]]>La tasa de recaída, en igual periodo para las pacientes en estadio inicial de la enfermedad fue de 90,8 % (IC 95 %: 84,7-96,9); y un promedio de aproximadamente 90,6 meses (IC 95 %: 85,0-96,1). El indicador disminuyó drásticamente en las pacientes con enfermedad localmente avanzada, las cuales mostraron una tasa de supervivencia libre de eventos de 75 % (IC 95 %: 71,5-78,5) y una media de 76,8 meses (IC 95 %: 73,5-80,2) (tabla 3).
De las 853 mujeres estudiadas, fallecieron 450 (52,8 %); 428 de ellas (95,1 %) por CCU y 22 (4,9 %) por otras causas. El periodo de seguimiento mínimo fue de 5 años y máximo 10 años. La tasa de supervivencia global al diagnóstico de CCU, a los cinco años, fue de 47,2 % (IC: 43,7 %-50,7 %) y una mediana de 48 meses (IC 95 %: 36,4-59,6) (tabla 4, Fig. 1).
Se observó diferencias estadísticamente significativas entre las distribuciones de supervivencia para los diferentes grupos de edad (< 60 y ≥ 60 años). En las mujeres menores de 60 años, se estimó una tasa de supervivencia a los 5 años de 50,3 meses y una mediana de 64 (IC 95 %: 62,3; 65,7). Estos indicadores mostraron valores considerablemente menores en el grupo de 60 años y más (tabla 4).
No se observó diferencias estadísticamente significativas entre las distribuciones de supervivencia por variedad histológica al considerar los subtipos epidermoide y no epidermoide (tabla 4).
]]> Las tasas de supervivencia al diagnóstico disminuyeron considerablemente mientras más avanzada era la enfermedad. Se evidenció diferencias estadísticamente significativas entre las etapas clínicas (tabla 4, Fig. 2).
En estadios iniciales del CCU (IA1 a IB1), a los cinco años del diagnóstico se describió una tasa de supervivencia de 86,2 % (IC 95 %: 78,9-93,4). El promedio de supervivencia apreciado para estos casos fue de 98,5 meses (IC 95 %: 92,7-104,3). Al concluir el estudio habían fallecido 13,7 % de las mujeres que se encontraban en estas etapas clínicas; a diferencia de las pacientes con enfermedad localmente avanzada, en las que la tasa de supervivencia fue de 42,5 % (IC 95 %: 39,0-46,0) y la mediana de 39,0 meses (IC 95 %: 32,8-45,2).
DISCUSIÓN
El cáncer del cuello de útero (CCU) es uno de los principales problemas en la Salud Pública, fundamentalmente en las naciones en vías de desarrollo, con un vertiginoso crecimiento del riesgo en el último quinquenio. Es una enfermedad prevenible, controlable y de fácil diagnóstico en etapas tempranas debido al largo periodo de tiempo que transcurre entre la aparición de la lesión intraepitelial y su evolución al cáncer. El porcentaje de éxito del tratamiento en estadios iniciales es elocuente. Por lo que resulta paradójico, ante las condiciones antes enunciadas, que el CCU sea la causa de un número importante de defunciones en la mujer. En la actualidad, se muestran, apenas, discretas variaciones en cuanto a la reducción del volumen de pacientes que son diagnosticadas en estadios localmente avanzados de la enfermedad.
Estudios epidemiológicos plantean el incremento de la incidencia del CCU en la medida en que aumenta la edad de la mujer, alcanza su mayor frecuencia entre los 50 y 69 años ha sido caracterizado como un evento muy poco frecuente en la mujer joven. Esta descripción, relativamente estable durante años, pautó estrategias y políticas en cuanto a la realización del screening, indicado en mujeres mayores de 25 años.9,10 Estas pautas aún se mantienen vigentes en muchas naciones. El CCU es la neoplasia maligna del aparato ginecológico que más precoz aparece. Un elemento no menos importante, ha sido la disminución paulatina de la edad al diagnóstico. En los últimos años se ha observado el adelanto de una década en la edad de aparición de la enfermedad, el cual ha sido relacionado con el significativo aumento de la infección por Virus del Papiloma Humano (HPV) y el inicio de las relaciones sexuales en edades más tempranas. Algunos autores hacen referencia a una disminución en la edad del diagnóstico del cáncer de cuello uterino de más de 5 años, desde el pasado siglo.11-13
Múltiples han sido los estudios que han evidenciado una reducción significativa en las tasas de incidencia y mortalidad por CCU desde que se implementó la citología cervical como método de pesquisa. Se ha demostrado que la realización de la prueba citológica cada 3 años entre los 20 y 64 años reduce la tasa de incidencia acumulada de carcinoma invasor de cérvix en 91,2 % y el número de pruebas que se debe realizar disminuye a 15. Un programa de pesquisa organizado que cumpla esta recomendación ayudará a disminuir la mortalidad por cáncer de cérvix en un 60 %.14-18
En la investigación realizada es muy significativo el elevado número de pacientes que no fueron pesquisadas y menos de la mitad tenían seguimiento citológico. El CCU tiene la "bondad" de presentar una historia natural que involucra períodos de tiempo muy largos, por lo que muchos casos pueden prevenirse mediante prácticas de tamizaje apropiadas. Al detectar lesiones precursoras de manera temprana, se tiene un amplio margen para actuar en torno a ellas, lo cual hace posible su prevención y/o curación. La prevención de CCU requiere de la corresponsabilidad de la población en general, de las mujeres en particular y de los miembros del equipo de salud.
]]> El Programa de Prevención y Diagnóstico Precoz del CCU, en Cuba, cuenta con una experiencia de 49 años, e involucra el nivel de Atención Primaria del Sistema de Salud Pública, de manera que garantiza la accesibilidad de la totalidad de la población femenina. En el programa se establece la realización de la citología cérvico vaginal cada tres años en las mujeres de 25 a 65 años.8 El intervalo de pesquisa es un elemento muy importante, que influye en el decisivamente en el control de la enfermedad. Estudios realizados sobre el intervalo de la pesquisa en mujeres con citologías negativas, reportan un riesgo incrementado de cáncer después de los 3 años con control previo de citologías negativas.19El porcentaje de mujeres no pesquisadas, así como el número de casos con un intervalo de pesquisa superior a los 3 años, denotan fisuras en el cumplimiento de Programa de Prevención y Diagnóstico Precoz del CCU que deben ser evaluadas. Investigaciones realizadas en países con alta incidencia de la enfermedad, dirigidas a la evaluación de estrategias y programas de detección oportuna por citología cérvico vaginal han identificado, por lo general, un incumplimiento de las pautas establecidas en este, falta de calidad en los procesos y baja percepción del riesgo de morbilidad y mortalidad por parte de la población femenina.20
En cuanto a la histología, se plantea que el carcinoma epidermoide está presente, aproximadamente, en 80 % de los cánceres cervicales, mientras que el adenocarcinoma comprende aproximadamente 20 % de este. El carcinoma adenoescamoso y el carcinoma de células pequeñas son relativamente poco frecuentes; resultados similares fueron obtenidos en la presente investigación. Se han descrito ocasionalmente sarcomas primarios cervicales. Igualmente, se ha informado sobre la existencia de linfomas malignos cervicales, tanto primarios como secundarios. A pesar de la diversidad histológica, la mayoría de los estudios reportan un franco predominio del carcinoma epidermoide sobre la variedad adenoescamoso.
Sin embargo, reportes actualizados indican que los adenocarcinomas han aumentado su frecuencia en las últimas 3 décadas, los cuales llegan a presentarse hasta en 25 % de las pacientes. Algunos autores han asociado este incremento al uso de tabletas anticonceptivas sin ofrecer datos concluyentes.21,22 Otros sugieren que el adenocarcinoma de cuello uterino, ha aumentado su incidencia en los últimos años, probablemente, debido a que los métodos de detección por citología cervical son menos eficaces para esta variedad histológica.
La citología cérvico vaginal permite la detección temprana y el tratamiento de lesiones precursoras del carcinoma epidermoide. Sin embrago, la identificación del adenocarcinoma in situ por rutina citológica o colposcopia es menos efectiva, lo cual a su vez está influenciado por la calidad de la pesquisa.23,24
El Instituto Nacional de Oncología y Radiobiología, es una institución del tercer nivel de atención en el Sistema Nacional de Salud Pública en Cuba. Por ende, la mayoría de los casos que acuden al centro se encuentran en etapas localmente avanzadas de la enfermedad (estadios IB2-IVA, FIGO 200925). Sin embargo, a pesar de dicha distinción, no es despreciable la proporción de pacientes en todos los grupos de edades, que son admitidas con este diagnóstico al tomar en consideración las estrategias de prevención y diagnóstico oportuno disponibles en el país.
Las etapas localmente avanzadas tienen mayor prevalencia en los países emergentes y son un reflejo del funcionamiento no adecuado de los programas. La calidad de las estrategias y políticas de pesquisa garantizan el diagnóstico de más del 75 % de las pacientes en estadios clínicos tempranos.26,27
En etapas tempranas, el CCU suele ser asintomático y es detectado por los exámenes ginecológicos de rutina: especuloscopía o visión directa, la prueba de Papanicolaou y la colposcopia. En muchos tipos de cáncer, el progreso en el área del cribado y el tratamiento del cáncer ha ofrecido expectativas de una detección más precoz y mayores tasas de curación. Se aconseja a las mujeres que comiencen con el cribado del cáncer cervical dentro de los tres años siguientes a comenzar su actividad sexual y no después de los 21 años. El cribado generalmente incluye una prueba de Papanicolaou y puede incluir también una prueba de VPH. El seguimiento periódico garantiza el diagnostico precoz de la enfermedad y aumenta las probabilidades de éxito del tratamiento. El pronóstico de las pacientes con CCU empeora en correspondencia con la etapa clínica; en consecuencia, también varía el tratamiento indicado.
En las etapas tempranas, el tratamiento quirúrgico es el de elección con altas tasas de curación. En correspondencia con el diagnóstico de CCU en etapa localmente avanzada obtenidos en la mayoría de las pacientes, la Radio-Quimioterapia concurrente fue la modalidad más utilizada en el estudio; tratamiento estándar para estos casos.28,29
Desde el año 1999, la evidencia ha recomendado el uso concomitante de radioterapia y quimioterapia con cisplatino en mujeres que se diagnostican en etapas IB2 a IVA. Igualmente, ha sido sugerida esta terapéutica para las pacientes en estadio clínico inicial y que al momento de la cirugía primaria hayan sido identificados factores pronósticos desfavorables (ganglios pelvianos positivos, enfermedad parametrial o márgenes quirúrgicos positivos). Múltiples revisiones sistemáticas de estudios aleatorios y el análisis de varios estudios prospectivos randomizados demostraron que esta combinación presenta mayor supervivencia global e incrementa la supervivencia libre de enfermedad con respecto al tratamiento con radioterapia, en un 10 a 13 %, respectivamente. Por su parte la mortalidad disminuye entre un 30 a 50 %.27,28
]]> Es por ello que se recomienda el uso de la radioterapia concomitante con quimioterapia con cisplatino para todas las pacientes con tumores clínicamente mayores de 4 cm, o aquellas en las que los resultados anatomopatológicos tengan presente algunos de los factores desfavorables antes mencionados. Resultados similares se obtuvieron en estudios que mostraron bajos índices de pesquisa y, a consecuencia, la mayoría de las pacientes fueron diagnosticadas en estadios avanzados de la enfermedad. De igual modo, en estos casos, se les realizó cirugía a un reducido número de pacientes y en la mayoría, la quimio radioterapia concurrente fue el tratamiento primario de elección.30,31La vigilancia postratamiento es un elemento importante para el diagnóstico temprano de las recurrencias. Cuando la enfermedad es diagnosticada en forma temprana, mejora considerablemente la respuesta completa al tratamiento y los eventos de recaída se presentan en menos del 10 % de los casos. Mientras que en las pacientes con enfermedad localmente avanzada, se llegará a presentar recaída hasta en 33 % de las enfermas. Investigaciones observacionales han descrito un 17 % de recurrencia en las pacientes con estadio IB; en etapas avanzadas las tasas de recaída son mucho mayores. Los resultados arrojados por la investigación muestran correspondencia con los obtenidos en los estudios referenciados.
Las pautas de la National Comprehensive Cancer Network (NCCN) para la práctica clínica en oncología (versión 2.2015) establecidas para el Cáncer Cervical, plantean que los factores de riesgo potencialmente importantes para la recurrencia no están limitados a: invasión estromal mayor de un tercio, invasión del espacio linfovascular y tamaño del tumor ≥3 cm (todos ellos elementos que definen el estadiamiento clínico del tumor); otros factores de riesgo como la histología del tumor y los márgenes quirúrgicos positivos, deben ser considerados.32,33
Los expertos afirman que las tasas de supervivencia y de control de la enfermedad pélvica en las pacientes con CCU esta correlacionada con el estadio clínico. El pronóstico está sujeto a características histológicas no incluidas en el sistema de clasificación, independientemente del tratamiento oncoespecífico de primera línea recibido.34,35
Los países desarrollados exhiben tasas de supervivencia global a los 5 años entre 59 % y 69 %. Según estimados de la American Cancer Society, la tasa de supervivencia en Estados Unidos asciende a un 72 %. Estos resultados son atribuibles en gran medida a la existencia y efectividad de los programas de cribado del CCU que conducen al diagnóstico precoz de la mayoría de los casos. En los países en vías de desarrollo, el panorama es muy diferente, se ha alcanzado una tasa de supervivencia de un 49 % como valor máximo.36
La existencia de un programa de pesquisa efectivo, igualmente, ha tenido un impacto en la edad promedio al diagnóstico de CCU, que a su vez se relaciona con factores de riesgo natural como la exposición al VPH, la actividad sexual y el uso de anticonceptivos. Todos ellos tienen un impacto considerable en el pronóstico de la enfermedad y en la supervivencia de las pacientes. En el presente estudio, la supervivencia fue significativamente mayor en las pacientes con edad al diagnóstico ≥ 60 años; resultados similares han sido publicados. Otros parámetros como histología del tumor y etapa clínica no han quedado exentos de esta relación.11,14,36,37
En relación con la histología del tumor, análisis realizados en estudios retrospectivos previos, han ofrecido evidencias de que la histología no epidermoide del CCU es un factor pronóstico del intervalo libre de enfermedad y de la supervivencia.38 Otras investigaciones, como la actual, no han revelado los mismos resultados; es decir, no se han encontrado diferencias estadísticamente significativas entre las distribuciones de supervivencia de los grupos con histología epidermoide vs no epidermoide (ADC y otros).10,38-40 Obviamente, existen discrepancias en la literatura sobre el tema. Algunas guías internacionales señalan que la histología glandular puede ser un factor que incrementa el riesgo de recurrencia.41
La etapa clínica del tumor define la terapia del paciente y su pronóstico. En el CCU, es un reconocido factor pronóstico que modifica considerablemente los indicadores de supervivencia y riesgo de muerte. Estudios realizados en Brasil, Colombia y Chile, han mostrado resultados similares a los obtenidos en la presente investigación en cuanto a la frecuencia de casos por estadio del tumor y tasas de sobrevida.42,43
Los resultados de la investigación, a pesar de haber sido obtenidos en un contexto hospitalario, nos proveen de informaciones, que aún a pequeña escala, no deben ser desatendidas. La proporción de mujeres no pesquisadas, el volumen de casos con seguimiento citológico superior a los 3 años, el diagnóstico de CCU, en edades más tempranas (disminución gradual de la edad promedio al diagnóstico), el porcentaje de pacientes diagnosticadas en estadios avanzados de la enfermedad y las tasas de supervivencia observadas imponen un desafío. Los resultados obtenidos constituyen una alerta sugerente.
La incidencia y mortalidad del CCU, así como su estabilidad en el último quinquenio, exigen la realización de estudios de mayor alcance e investigaciones dirigidas a la evaluación de los programas, sistemas y servicios de salud implicados. Es necesario mejorar la calidad del Programa de Diagnóstico Precoz del Cáncer Cérvico Uterino en Cuba; así como proveer nuevas políticas públicas, estrategias de promoción, vigilancia y control más efectivas.
]]>Los autores no declaran tener conflictos de intereses.
REFERENCIAS BIBLIOGRÁFICAS
1. Ferlay J, Soerjomataram I, Ervik M, Dikshit R, Eser S, Mathers C, et al. GLOBOCAN 2012 v1.0, Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 11 [Internet]. Lyon, France: International Agency for Research on Cancer; 2013.
2. Siegel R, Naishadham D, Jemal A. Cancer statistics, 2012. CA Cancer J Clin. 2012;62:10-29.
3. Almonte M. Nuevos paradigmas y desafíos en la prevención y control del cáncer de cuello uterino en América Latina. Salud pública Méx. 2010;52(6).
4. Ministerio de Salud Pública. Anuario Estadístico de Salud 2015. Dirección de Cuba. Dirección de Registros Médicos y Estadísticas de Salud. La Habana; 2016.
5. Division of Cancer Prevention and Control, National Center for Disease Prevention and Health Promotion, Centers for Disease Control and Prevention. Cervical Cancer. Atlanta, GA. 2011;33:34-45.
6. Rodriguez AC, Schiffman M, Herrero R. Longitudinal study of human papillomavirus persistence and cervical intraepithelial neoplasia grade 2/3: critical role of duration of infection. J Natl Cancer Inst. 2010;102:315-24.
7. Jemal A, Bray F, Center MM. Global Cancer Statistics. CA Cancer J Clin. 2011;61:69-90.
8. Ministerio de Salud Pública. Programa Nacional de Diagnóstico Precoz del Cáncer Cérvico Uterino. La Habana; 2001.
9. Therasse P, Arbuck SG, Eisenhauer EA, Wanders J, Kaplan RS, Rubinstein L, et al. New guidelines to evaluate the response to treatment in solid tumors. J Nat Cancer Inst. 2000;92:205-16.
10. Xia X, Hongbin WZ, Zhonghai WY, Ronghua L, Shuang L. Analysis of Prognostic Factors Affecting the Outcome of Stage IB-IIB Cervical Cancer Treated by Radical Hysterectomy and Pelvic Lymphadenectomy. Am J Clin Oncol. 2014;00:1-5.
11. Romero K, Rojas J. Frecuencia de los factores de riesgo de Cáncer Cérvico uterino en mujeres de 14-65 años, Comunidad Ramadas, Provincia Tapacarí. Cochabamba. Rev Cient Cienc Méd. 2012;15:1.
12. International agency for research on cancer. Cervical cancer, estimated incidence mortality and prevalence worldwide in 2012. World in health organization; 2012.
13. Duque PA, Revolj M, Garred P, Lynge E. Immunosuppression and risk of cervical cancer. Expert Rev. Anticancer Ther. 2013;13:29-42.
14. Barnholtz-Sloan J, Patel N, Rollison D. Incidence trends of invasive cervical cancer in the United States by combined race and ethnicity. Cancer causes control. 2009;20:1129-38.
15. Safaeian M, Solomon D, Wacholder S. Risk of precancer and follow-up management strategies for women with human papillomavirus-negative atypical squamous cells of undetermined significance. Obstet Gyneacol. 2008;109:1325-31.
16. Katki HA, Kinney WK, Fetterman B. Cervical cancer risk for women undergoing concurrent testing for human papilloma virus and cervical cytology: a population-based study in routine clinical practice. Lancet Oncol. 2011;12:663-72.
17. Schiffman M, Glass AG, Wentzensen N. A long-term prospective study of type-specific human papillomavirus infection and risk of cervical neoplasia among 20,000 women in the Portland Kaiser Cohort Study. Cancer Epidemiol Biomarkers Prev. 2011;20:1398-1409.
18. Saraiya M, Berkowitz Z, Yabroff KR. Cervical cancer screening with both human papillomavirus and Papanicolaou testing v.s. Papanicolaou testing alone: what screening intervals are physicians recommending? Arch Intern Med. 2010;170:977-85.
19. Papanikolau A, Kalogiannidis I, Missalidou D, Goutziolis M, Stamatopoulos P, Makedos A, et al. Results on the treatment of uterine cervix cancer: ten years' experience. Eur J Gynecol Oncol. 2006;27(6):607-10.
20. Mathew A, George PS. Trends in incidence and mortality rates of squamous cell carcinoma and adenocarcinoma of cervix- worldwide. Asian Pac J Cancer Prev. 2009;10:645-50.
21. Ryu SY, kim MH, Nam BH. Intermediate risk propping of cervical cancer patients treated with radical hysterectomy: a Korean Gynecologic Oncology Group study. Br J Cancer. 2014;110:278-85.
22. Dahistrom LA, Ylitalo N, Sundstrom K. Prospective study of human papillomavirus and risk of cervical adenocarcinoma. Int J Cancer. 2010;127:1923-30.
23. Sasieni P, Castanon A, Cuzick J. Screening and adenocarcinoma of the cervix. Int J Cancer. 2009;125:525-9.
24. Pecorelli S, Zigliani L, Odicino F. Revised FIGO stating for carcinoma of the cervix. Int J Gynaecol Obstet. 2009;112:1874-6.
25. Dueñas-Gonzalez A, Cetina L, Mariscal I, de la Garza J. Modern management of locally advanced cervical carcinoma. Cancer Treat Rev. 2003;29:389-99.
26. Mathew A, George PS. Trends in incidence and mortality rates of squamous cell carcinoma and adenocarcinoma of cervix- worldwide. Asian Pac J Cancer Prev. 2009;10:645-50.
27. Mon BJ, Tewari KS, Koh W-J. Multimodality therapy for locally advanced cervical carcinoma:State of the art and future directions. J Clin Oncol. 2007;25:2952-2965.
28. Gaffney DK, Erickson- Wittmann BA, Jhingran A, et al. ACR Appropriateness Criteria(R) on advanced cervical cáncer expert panel on radiation Oncology-Gynecology. Int J Radiat OncolBiol Phys. 2011;81:609-14.
29. Haie-Meder C, Fervers B, Chauvergne J. Concomitant radiochemotherapy for cancer of the cervix: critical analysis based on the Standards, Options and Recommendations methodology. Cancer Radiother. 2000;4:60-75.
30. Long HJ, Bundy BN, Grendys EC. Randomized phase III trial of cisplatin with or without topotecan in carcinoma of the uterine cervix: a Gynecologic Oncology Group Study. J Clin Oncol. 2005;23:4626-33.
31. Salani R, Backes FJ, Fung MF. Posttreatment surveillance and diagnosis of recurrence in women with gynecologic malignancies: Society of Gynecologic Oncologists recommendations. Am J Obstet Gynecol. 2011;204:466-78.
32. Lim KC, Howells RE, Evans AS. The role of clinical follow up in early stage cervical cancer in South Wales. BJOG. 2004;111:1444-8.
33. Veerasarn V, Lorvidhaya V, Kamnerdsupaphon P. A randomized phase III trial of concurrent chemoradiotherapy in locally advanced cervical cancer: preliminary results. Gynecologic Oncology. 2007;104(1):15-23.
34. Kim YS, Shin SS, Nam H. Prospective randomized comparison of monthly 5-Flourouracil and cisplatin versus weekly cisplatin concurrent with pelvic radiotherapy and high dose rate brachytherapy for locally advanced cervical cancer. Gynecologic Oncology. 2008;108(1):195-200.
35. Mascarello KC, Zandonade E, Costa MH. Survival analysis of women with cervical cancer treated at a referral hospital for oncology in Espírito Santo State, Brazil, 2000-2005. Cad. Saúde Públical Brasil. 2013;29(4):823-31.
36. Hellman K, Hellström AC, Pettersson BF. Uterine cervix cancer treatment at Radiumhemmet: 90 years' experience. Time trends of age, stage, and histopathology distribution. Cancer Med. 2014;3:284-92.
37. Carmo CC, Luiz RR. Survival of a cohort of women with cervical cancer diagnosed in a Brazilian cancer center. Rev Saúde Pública. 2011;45:661-7.
38. Kodama J, Seki N, Nakamura K. Prognostic factors in pathologic parametrium-positive patients with stage IB-IIB cervical cancer treated by radical surgery and adjuvant therapy. Gynecol Oncol. 2007;105:757-61.
39. Dos Reis R, Frumovitz M, Milam MR, Capp E, Sun CC, Coleman RL, Ramirez PT. Adenosquamous carcinoma versus adenocarcinoma in earlystage cervical cancer patients undergoing radical hysterectomy: an outcomes analysis. Gynecol Oncol. 2007;107(3):458-63.
40. National Comprehensive Cancer Network Clinical Practice Guidelines in Oncology. Cervical Cancer. Version 2; 2015.
41. Pardo C, Cendales R. Supervivencia de pacientes con cáncer de cuello uterino tratadas en el Instituto Nacional de Cancerología. Biomédica, Colombia. 2009;29:437-47.
42. Sepúlveda PV, González FC, Napolitano CR, Roncone ED, Cavada GC. Cáncer de cuello uterino: sobrevida a 3 y 5 años en hospital San José. Rev Chil Obstet Ginecol. 2008;73:151-4.
43. Quinn MA, Benedet JL, Odicino F, Maisonneuve P, Beller U, Creasman WT. Carcinoma of the cervix uteri. FIGO 6th Annual report on the results of treatment in gynecological cancer. Int J Gynaecol Obstet. 2006;95(S1):43-103.
Recibido: 15 de diciembre de 2016.
Aprobado: 27 de enero de 2017.
Madelaine Sarria Castro. Instituto Nacional de Oncología y Radiobiología. La Habana, Cuba.
Correo electrónico: madelaine.sarria@infomed.sld.cu
]]>