
AVANCES EN EL CONOCIMIENTO DE LAS PROTEÍNAS TRANSPORTADORAS DE SACAROSA EN LAS PLANTAS MONOCOTILEDÓNEAS. UN NUEVO TRANSPORTADOR EN CAÑA DE AZÚCAR
ADVANCES IN KNOWLEDGE OF SUCROSE-binding proteins in monocot plants. A NEW CARRIER IN SUGAR CANE
Ms.C. Isabel MedinaI. E-mail: imedina@fbio.uh.cu y Dra.C. Rosa RodésII, Dra. Christina KuehnIII
I Profesora Asistente ]]>
II Profesora Titular del departamento de Biología Vegetal, facultad de Biología, Universidad de La Habana (UH), Cuba, CP 10400
III Docente del Laboratorio de Fisiología Vegetal, Instituto de Biología, Universidad Humboldt, Berlín 10115, Alemania
RESUMEN
Los transportadores de sacarosa tienen un papel fundamental en el transporte de este azúcar a través de las membranas y en su distribución a lo largo de la planta desde los tejidos fuentes hacia los sumideros y entre los diferentes sumideros. A pesar de que había sido sugerida la existencia de una proteína transportadora para la sacarosa desde los finales de la década de los 70, no es hasta 1992 que se comprobó su existencia, al ser identificada la primera secuencia de ADNc de un transportador de sacarosa en Spinacea oleracea y ser este sometido a análisis funcionales, bioquímicos y estructurales. El primero identificado en plantas monocotiledóneas fue en Oryza sativa en 1997, al que le siguieron posteriormente otros cuatro en O. sativa, Zea mays (3), Triticum aestivum (3), Hordeum vulgare (2), Saccharum híbrido (1), Ananas comosus (1), Bambusa oldhamii (1) y Sorghum bicolor (2). En este trabajo se pretende hacer una revisión del conocimiento actual acerca de los transportadores de sacarosa en estas plantas, a la vez que se muestran las primeras evidencias de un segundo transportador de sacarosa en Saccharum híbrido, ShSUT4. Esta proteína posee una secuencia deducida de alta identidad con transportadores de reconocida funcionalidad y, al igual que estos, le ha sido predicha una estructura secundaria de 12 dominios transmembrana. Por último, se ha localizado en el tonoplasto, al igual que otros transportadores del Clado SUT4 del árbol filogenético.
Palabras clave: transportador de sacarosa, plantas monocotiledóneas, caña de azúcar.
Sucrose transporters have a pivotal role in sucrose transport through membranes and its distribution along the plant from source tissues to sinks and among different sinks. Although a sucrose-transporting protein has been postulated since late 70´s, it was not proved until 1992, when the first DNAc sequence of a sucrose transporter was identified in Spinacea oleracea, which was subjected to functional, biochemical and structural analyses. The first sucrose transporter identified in monocotyledon plants was in Oryza sativa, 1997, followed by the other four in O. sativa, Zea mays (3), Triticum aestivum (3), Hordeum vulgare (2), Saccharum hybrid (1), Ananas comosus (1), Bambusa oldhamii (1) and Sorghum bicolor (2). This paper intends to review the current knowledge about sucrose transporters in these plants, besides presenting the first evidence of a second sucrose transporter in Saccharum hybrid, ShSUT4. This protein has a high identity deduced sequence with renowned functionality transporters and, similar to them, it has been predicted to possess a secondary structure of 12 transmembrane domains. Finally, it has also been spotted in the tonoplast, like some other sucrose transporters of Clade SUT4 in the phylogenetic tree.
]]>
Keywords: sucrose transporter, monocotyledon plants, sugarcane.
INTRODUCCIÓN
Las plantas superiores están constituidas por una mezcla de células autotróficas y heterotróficas. La fijación del CO2 tiene lugar en las células fotosintéticas de las hojas maduras, las cuales son órganos exportadores netos de azúcares y son conocidas como “fuentes de carbono”, mientras que las células heterotróficas de las raíces, las estructuras reproductivas y los órganos en desarrollo o de reserva, necesitan del suministro de azúcares y se conocen como “sumideros de carbono”. Para que todos los sumideros reciban el suplemento adecuado de azúcares a su crecimiento y desarrollo, existen diferentes mecanismos y los transportadores de azúcares tienen un papel fundamental en el transporte a través de las membranas y su distribución a lo largo de la planta.
El disacárido sacarosa se emplea para el transporte a larga distancia por toda la planta; algunas familias de plantas transportan rafinosa y estaquiosa o azúcares alcohol, junto a cantidades variables de sacarosa, la mayoría transporta exclusivamente sacarosa. La llamada carga del floema ocurre en las hojas fuente, y es un proceso que aumenta el contenido de sacarosa en las células acompañantes (CA) y los vasos cribosos (VC) del floema, a niveles muy superiores que las células que los rodean (1). De acuerdo con la hipótesis de Münch, el transporte de solutos en el floema está regulado principalmente por el flujo de masa, dirigido por gradientes osmóticos creados por los procesos de carga en los tejidos fuente y descarga en los sumideros (2).
La carga del floema en las hojas puede ocurrir por dos mecanismos: la vía simplástica y la apoplástica, en dependencia del paso de la sacarosa por el simplasto o el apoplasto. Si se asume que las células de las plantas están unidas entre sí por los plasmodesmos y conforman un sistema citoplasmático continuo (simplasto) con los vasos cribosos del floema, la sacarosa se distribuiría por la planta de célula en célula, esta sería la vía simplástica.
]]>
Se consideraba que la entrada pasiva de la sacarosa al floema de las hojas por la vía simplástica solo era posible termodinámicamente en las plantas que presentaban la llamada trampa de polímeros, como en las Cucurbitáceas, donde la sacarosa difunde a las células acompañantes de las venas menores de la hoja y es convertida en sus olígomeros rafinosa y estaquiosa. Estos compuestos son entonces trasladados a los vasos conductores con una cierta cantidad de sacarosa no oligomerizada (3). Sin embargo, también se ha planteado la posibilidad de una carga simplástica de la sacarosa, sin que ocurra una concentración de esta en el floema, siempre y cuando la concentración de sacarosa sea mayor en las células productoras y esté favorecida su difusión a través del plasmodesmo (4).
Se ha demostrado que existen ciertos tejidos que están prácticamente incomunicados por el simplasto; por ejemplo, el tejido maternal y filial en las semillas de legumbres y cereales, o el complejo CA/VC y el mesófilo en las hojas de Fabáceas (5). También puede suceder que no todos los plasmodesmos se encuentren abiertos y funcionales. En tales casos, para el transporte de este azúcar se necesitaría un paso por el apoplasto, formado por las paredes celulares y los espacios extracelulares, y una proteína que en cotransporte con protones (SUT o SUC, del inglés SUcrose Transporter o Carrier) incorpore la sacarosa de nuevo al simplasto de las células adyacentes (3, 6). La vía aparentemente más común para la carga del floema en las hojas es a través del apoplasto; no obstante, algunas plantas usan aparentemente más de una vía, como sucede en Alonsoa meridionalis (4).
A pesar de que se había propuesto la existencia de una proteína transportadora para la sacarosa (7) desde finales de la década de los 70, no es hasta 1992 que se identificó la primera secuencia de ADNc de un transportador de sacarosa en espinaca (Spinacea oleracea), SoSUT1, que fue sometido a análisis funcionales, bioquímicos y estructurales (2). La funcionalidad del transportador se comprobó cuando su expresión permitió a una línea mutante de levadura (SUSY7/ura3, Saccharomyces cerevisiae) importar sacarosa marcada con C14. Las células de esta levadura fueron transformadas genéticamente, para ser incapaces de crecer en sacarosa como única fuente de carbono; esto se logró con el bloqueo de la expresión de las invertasas citosólica y extracelular, y la inserción del gen de la enzima Sacarosa Sintasa (SS) de espinaca en su genoma. De este modo, la sacarosa del medio no puede ser hidrolizada y solo cuando el gen de un transportador de sacarosa haya sido expresado y la proteína funcional insertada en la membrana plasmática de la levadura, la sacarosa puede penetrar al citoplasma y ser escindida por la SS. La actividad del transportador se mostró dependiente del pH y el potencial de membrana con una Km de 1,5 mM, y fue inhibido por protonóforos, inhibidores de sistemas que generan ATP y por agentes modificantes de grupos tioles. La estructura primaria de la proteína deducida a partir del ADNc se ajustó a las características de alta hidrofobicidad requeridas para una proteína de membrana con 12 dominios transmembrana. Se propuso un modelo, donde la sacarosa fuera liberada al apoplasto desde la célula del mesófilo, por un mecanismo de difusión facilitada o un antiporte de sacarosa y H+, y posteriormente cargada al floema por medio de un simporte con protones, cuya fuerza motriz es generada por la H+-ATPasa de membrana. Los datos aportados en este trabajo señalan que SoSUT1 es un cotransportador de sacarosa y H+ del tipo simporte (2).
Esta secuencia se utilizó para el aislamiento del primer transportador de sacarosa en especies Solanáceas (8) y en otras plantas dicotiledóneas hasta un número de nueve, antes de que se reportara el primero en plantas monocotiledóneas (5). A medida que se fueron incorporando nuevas secuencias estas se agruparon por sus relaciones filogenéticas en un número creciente de grupos o clados, hasta completar cinco (9).
En este trabajo se pretende hacer una revisión del conocimiento actual acerca de los transportadores de sacarosa en las plantas monocotiledóneas, a la vez que se muestran las primeras evidencias de un segundo transportador de sacarosa en caña de azúcar (Saccharum híbrido), ShSUT4.
Mucho antes de que fuera descubierto el primer SUT en espinaca (SoSUT1), ya existían evidencias de la existencia de proteínas de membrana en plantas dicotiledóneas, que debían ser electrogénicas y funcionar como cotransporte con protones (10, 11). En la caña de azúcar, una planta monocotiledónea, también se publicaron trabajos iniciales con evidencias de la posibilidad de la entrada directa de sacarosa. Cuando se aplicó sacarosa-C14 externa a cortes de tejidos del tallo, se detectó muy baja presencia de marcaje isotópico en las hexosas libres del interior del tejido, lo que indicó que solo una parte pequeña de la sacarosa había sido hidrolizada (12, 13). Además, la entrada de la sacarosa marcada al interior del parénquima se mostró sensible a compuestos protonóforos, inhibidores de grupos sulfidrilos y modificadores de residuos arginil, a la vez que el análogo fluorosacarosa fue tomado por el tejido a una velocidad comparable a la sacarosa (13). Con estos resultados se rechaza la idea anterior de que toda la sacarosa debía ser hidrolizada por la invertasa ácida de la pared celular y que sus hexosas constituyentes son exclusivamente las que entran a las células de almacenamiento (14).
En 1997 se identificó el primer transportador de sacarosa de plantas monocotiledóneas en arroz: Oryza sativa, OsSUT1, (15). La proteína deducida a partir de la traducción del ADNc secuenciado mostró una similitud de los aminoácidos de 76,8-79,7 % con los SUT de especies dicotiledóneas identificados hasta ese momento. La dotación de SUT del arroz se completó en el 2003, cuando fueron identificados y clonados cuatro transportadores adicionales, designados OsSUT2, 3, 4 y 5 (16). Los péptidos de los cinco SUT de arroz difieren entre sí cuando se comparan con OsSUT1; OsSUT3 es el más similar con un 78 %, OsSUT4 y OsSUT5 muestran el 66 y 65 % de similitud respectivamente, mientras que OsSUT2 es el más distante con solo un 53 %. Los SUT encontrados en arroz presentaron una alta conservación de aminoácidos de la proteína deducida, en la región comprendida desde la primera hélice transmembrana hasta el primer lazo citoplasmático, formado entre las hélices transmembrana 2 y 3, al igual que todos los SUT conocidos en las plantas (16).
Con la utilización de la secuencia del ADNc del OsSUT1 como sonda, se logró la clonación de ZmSUT1 en la librería de ADNc de hojas de maíz, Zea mays (17). Este presentó una homología de aminoácidos del 82 % con el de arroz y del 40-45 % con otros SUT de plantas dicotiledóneas. El ZmSUT1 ha sido caracterizado cinéticamente mediante su expresión en oocitos de la rana sudafricana Xenopus laevis, los cuales son muy apropiados para el estudio del transporte de sacarosa, debido a que al pertenecer a un organismo animal estos no son capaces de transportar la sacarosa (18). Con el uso de la técnica patch clamp, se demostró que la proteína podía transportar sacarosa en ambas direcciones, en dependencia de las condiciones del pH, el voltaje y la concentración de sacarosa a ambos lados de la membrana, siendo esta la primera vez que se mostraron evidencias experimentales que sugieren que un mismo transportador pudiera entrar sacarosa a las células del floema en los tejidos fuente y liberar este azúcar de los vasos cribosos en el apoplasto del sumidero (18).
Además, otras dos secuencias han sido registradas para esta especie como ZmSUT2 (19) y ZmSUT4 (20), aún sin caracterizar.
En semillas de cebada (Hordeum vulgare) fueron identificados dos transportadores de sacarosa: HvSUT1 y HvSUT2. La secuencia peptídica deducida mostró una identidad del 47 % entre ellos, el HvSUT1 mostró similitud con los transportadores SUT1 de los cereales y HvSUT2 se asemejó filogenéticamente a los SUT4 de dicotiledóneas (21).
]]>
Al ser utilizado el OsSUT1 como sonda en trigo (Triticum aestivum), fueron hallados tres ADNc y designados como TaSUT1A, TaSUT1B y TaSUT1D. Estos mostraron ser idénticos entre sí en más del 98 % y solo diferían en las regiones no traducidas 5´- y 3´- del gen. En este trabajo se demostró que los SUT del cultivar de trigo hexaploide utilizado provenían de los progenitores diploides A, B y D. La secuencia proteica resultó ser muy similar a los transportadores de otras especies de cereales (86–97 %), pero difirió significativamente de HvSUT2 (54 % similar), así como de AtSUC3 (65 % similar), planta dicotiledónea Arabidopsis thaliana (22).
Investigadores del grupo de Grof en Australia encontraron una secuencia expresada etiquetada (EST, por sus siglas en inglés) en la librería de ADNc de la caña de azúcar en el 2003, con una identidad del 81 % con el SUT1 de maíz (23). Dos años más tarde, se registró la secuencia completa de ADNc del primer SUT en este cultivo (24).
A partir del ADNc de piña (Ananas comosus), se clonó y secuenció un posible SUT, denominado AcSUT1. La secuencia de nucleótidos mostró un 62-68 % de identidad con los transportadores del tipo SUT2. El polipéptido mostró las regiones conservadas presentes en el resto de los transportadores, mientras que el lazo citoplasmático entre los tramos transmembranas 6 y 7 parece ser más largo que el de los otros SUT del grupo (25).
En la base de datos GenBank se encuentran accesibles los registros de las secuencias proteicas deducidas de los transportadores de bambú (Bambusa oldhamii), BoSUT1 (26) y sorgo (Sorghum bicolor), SbSUT1 y SbSUT4 (27, 28), los cuales aún no han sido caracterizados. El completamiento reciente de los anteproyectos del genoma del sorgo, maíz y Brachypodium será la fuente para la caracterización de nuevos SUT de plantas monocotiledóneas (29).
La capacidad de estas proteínas para transportar la sacarosa a través de la membrana ha sido demostrada mediante la expresión de sus secuencias de nucleótidos en la cepa mutante SUSY7/ura3 de levadura y en oocitos de X. laevis (Tabla I). En algunos casos, se ha confirmado el transporte mediante la complementación del crecimiento de la levadura en medios, en los cuales la sacarosa o la maltosa constituían la única fuente de carbón, como se ha reportado para OsSUT1 y OsSUT3 (16) y TaSUT1A, 1B, y 1D (30). Para muchos SUT, se ha logrado la estimación de la Km en S. cerevisiae, así como en X. laevis; sin embargo, esta ha resultado diferente en los dos sistemas de expresión heteróloga. Los resultados cinéticos en oocitos han reportado valores de Km mucho mayores en HvSUT1 y ShSUT1 (Tabla I), así como en AtSUC2, por lo que se considera que estos han sido subestimados en la levadura (11, 31, 32, 33). En los análisis realizados en Xenopus con AtSUC2, HvSUT1, ZmSUT1, ShSUT1, LjSUT4 (Lotus japonicus, planta dicotiledónea) y OsSUT1 (18, 31, 32, 33, 34, 35), se ha demostrado que la afinidad de estas proteínas por la sacarosa es altamente dependiente del pH y el voltaje al cual se mida, aunque OsSUT5 demostró poca dependencia del pH a potenciales fisiológicos de membrana (35) y ShSUT1 poca dependencia del voltaje (33); por esta razón, las comparaciones de las Km se han de realizar a pH y voltaje similares.
]]>
El estudio de propiedades transportadoras adicionales permite caracterizar a los transportadores, como es la selectividad por otros sustratos diferentes de la sacarosa. Datos comparables se han obtenido en oocitos con AtSUC2 (31), HvSUT1 (32), ShSUT1 (33), AtSUC9 (36), LjSUT4 (34), OsSUT1 y OsSUT5 (35). Los transportadores HvSUT1, ShSUT1 y OsSUT1 manifestaron afinidad por la sacarosa, la maltosa y los a-glucósidos: a-fenilglucósido y a-paranitrofenilglucósido. De los ß-glucósidos ensayados el único por el que mostraron afinidad fue la salicina; por el contrario, su cercano arbustina no constituyó sustrato para estos transportadores (32, 33, 35).
La selectividad de los transportadores SUT1 de cebada, caña de azúcar y arroz fue similar, mientras que OsSUT5 fue capaz de transportar arbustina al igual que AtSUC2 y AtSUC9. Los transportadores de plantas dicotiledóneas, AtSUC2, AtSUC9 y LjSUT4, mostraron ser menos selectivos que los SUT de monocotiledóneas, pues aceptaron también a los derivados ß-fenil y -paranitrofenilglucósidos. Por último, se ha reportado inhibición de la actividad transportadora del HvSUT1 por el ß-paranitrofenilglucósido (32) y del ShSUT1 por el análogo artificial de la sacarosa, la sucralosa (33). Sin embargo, la sucralosa fue sustrato del transportador LjSUT4 (34). Las diferencias observadas en la transportación de los a- y ß-glucósidos por los transportadores estudiados sugieren que estas no son resultado solo de la disposición del enlace glicosídico, sino también de los sustituyentes de las moléculas (32).
En general, se ha resaltado la ventaja de la utilización de Xenopus en relación con la levadura, tanto para la determinación de la Km (11, 31, 32, 33) como para la distinción entre sustratos e inhibidores (33). En este sistema de expresión, un inhibidor no registrará corriente de entrada y disminuirá la provocada por la sacarosa, cuando ambas moléculas se aplican en conjunto, mientras que en la levadura no se puede discernir si el nuevo azúcar añadido es un inhibidor o efectivamente un sustrato, ya que solo es detectada la sacarosa marcada.
La predicción de la topología de todos los SUT de monocotiledóneas descritos hasta ahora, al igual que los de plantas dicotiledóneas, ha manifestado la presencia 12 dominios transmembranas de alta hidrofobicidad, 11 lazos hidrofílicos y los terminales amino y carboxilo en el citoplasma, características que los señalan como miembros de la superfamilia de las proteínas facilitadoras principales (MFS, del inglés Major Facilitator Superfamily) (37).
El estudio de la cuantificación de la expresión de los genes y las proteínas sintetizadas en diferentes órganos y tejidos, así como su localización a nivel tisular y celular, ha permitido predecir la función de los SUT. Así también la producción de líneas transgénicas, en las que se ha disminuido la expresión de estos genes, ha sido de gran ayuda para esclarecer su papel, basado en las alteraciones metabólicas y de crecimiento de las plantas. Por ejemplo, el análisis semi-cuantitativo de ARN en papa del tipo salvaje (Solanum tuberosum) mostró que la expresión del StSUT1 era alta en las hojas maduras y, por el contrario, baja en el tallo y los tejidos sumideros. Por su parte, la hibridación in situ del ARNm mostró una localización específica en el floema (9). La función en la carga del floema en las hojas fue ratificada en plantas transgénicas de papa con disminuciones significativas del ARNm de StSUT1, en las cuales incrementó grandemente la concentración de carbohidratos solubles y almidón de las hojas y, al mismo tiempo, el crecimiento de la raíz y el rendimiento en tubérculos se redujeron significativamente (38).
El ZmSUT1 del maíz (17) y los tres TaSUT1 del trigo (22) se expresaron en las hojas fuentes de estas plantas, proponiéndose que sean activos en la carga del floema. Con la utilización de plantas mutantes de maíz deficientes de SUT1, se ha concluido que esta proteína es crucial para la carga del floema, ya que la exportación de sacarosa-C14 desde las hojas maduras disminuyó grandemente, lo que debió provocar la hiper-acumulación de carbohidratos observada, por lo que el crecimiento de la planta se vio seriamente afectado (39). La proteína de TaSUT1 ha sido localizada en la membrana plasmática de los VC en todas las clases de venas de las hojas maduras, así como en las vainas y el tallo.
Por los resultados contrastantes del colorante fluorescente Carboxifluoresceína en hojas y tallos, se han propuesto funciones diferentes para este transportador en estos órganos. En las hojas del trigo las venas menores están restringidas en su transporte simplástico, por lo que se ha sugerido que el transportador pudiera actuar en la carga apoplástica del floema. Por el contrario, debido a que el colorante puede salir del floema a los entrenudos por el simplasto, la presencia del TaSUT1 se ha justificado con un posible papel en la recuperación de la sacarosa que se escapa a lo largo del transporte a larga distancia (40).
Una característica de los transportadores OsSUT1, HvSUT1 y TaSUT1A, B y D, es la alta expresión que ha sido detectada en el endospermo de las semillas y los tejidos relacionados, la cual correlacionó con el llenado del grano; por ello, se ha sugerido que estén involucrados en el movimiento de la sacarosa hacia el grano en desarrollo, para mantener su crecimiento y la síntesis de almidón (15, 21, 22). A pesar de que se ha encontrado una alta expresión del OsSUT1 en órganos fuentes, como la lámina y la vaina de la hoja bandera (15, 16), las líneas transgénicas de arroz con la supresión anti-sentido de la expresión de este transportador no mostraron síntomas de acumulación de carbohidratos en las hojas ni disminución de la fotosíntesis, por lo que fue descartada la carga del floema como función principal de este transportador (41). Debido a que las semillas de estas plantas mostraron retardo en la germinación, se ha resaltado la importancia de este SUT en el transporte de la sacarosa para la formación de una semilla viable y en la germinación (16). Además, se ha encontrado que TaSUT1A, B y D manifestaron un incremento de su expresión en las semillas de trigo en germinación, por lo que se ha indicado que la actividad de estos faciliten la carga del floema del escutelo de la semilla, para garantizar el desarrollo del embrión (22, 30).
]]>
La cantidad de ARNm de OsSUT2 fue similar en todos los tejidos vegetativos y reproductivos investigados, mientras que OsSUT3 y 5 manifestaron la más alta expresión en las hojas sumideros y la más baja en las semillas germinadas. El OsSUT4 se expresó preferentemente en las hojas sumideros (16). La expresión de un transportador en los órganos sumidero señala que este pudiera actuar en el proceso de descarga del floema o en la entrada a las células de la sacarosa, que ha sido previamente descargada al apoplasto de los tejidos de estos órganos, pero aún no hay información suficiente sobre la función de estos transportadores en el arroz.
Por su parte, la expresión del transportador HvSUT2 tuvo niveles similares en varios tejidos fuentes y sumideros, así como durante el desarrollo del cariópside en los días después de la floración, por lo que se consideró como un gen de expresión basal no dependiente del tipo de tejido ni del desarrollo (21).
La expresión de ShSUT1 en la caña de azúcar se manifiesta predominantemente en las hojas maduras y en los entrenudos que están en acumulación activa de sacarosa. En las hojas, este pudiera actuar en la carga del floema, mientras que debido a que la proteína se ha identificado con anticuerpos específicos en las células de la periferia de los haces vasculares del tallo, se ha propuesto que su función pudiera ser posiblemente la de la salida de la sacarosa desde estas células hacia el apoplasto del tejido de almacén, y recobrar esta sacarosa apoplástica de nuevo al simplasto (24). Ya se había demostrado que la proteína ZmSUT1 tenía la capacidad de permitir el paso de la sacarosa en ambas direcciones en las condiciones diferentes de pH, voltaje y concentración de sacarosa características de los tejidos fuente y sumidero (18).
En A. comosus, la expresión de AcSUT1 fue más abundante en las hojas que en los frutos, así como se detectó la mayor expresión en los tejidos fotosintéticos de la hoja en relación con los no fotosintéticos (25). Esta localización diverge de la que ha sido reportada para los transportadores de las plantas dicotiledóneas del Clado SUT2, en las cuales se presume que estos SUT estén relacionados con la descarga de la sacarosa en el apoplasto de los órganos sumideros (11). Según el análisis filogenético de las secuencias de los transportadores de sacarosa de las plantas mono y dicotiledóneas, estos se encuentran separados en dos subgrupos dentro del clado, lo que pudiera estar en concordancia con la diferencia en la anatomía y disposición de los haces vasculares entre estas plantas e implicar diferencias en las funciones de los transportadores mencionados (25).
LOCALIZACIÓN SUBCELULAR DE LOS TRANSPORTADORES DE SACAROSA
La localización de las proteínas transportadoras en el sistema de membranas de la célula es menos conocida y actualmente se encuentra en debate la localización de algunos SUT. Se supone que los que han sido detectados en los VC del floema, se encuentren en la membrana plasmática, debido a que estas células han perdido la mayoría de sus organelos, entre ellos la vacuola. Este es el caso de las especies Solanáceas, tales como el tomate (Solanum lycopersicum), la papa (Solanum tuberosum) y el tabaco (Nicotiana tabacum) (SUT1, SUT2 y SUT4), Plantago major (PmSUC1) (6, 11) y el trigo (TaSUT1) (40), aunque se ha publicado un estudio reciente muy minucioso, sobre la localización inmunoquímica de SUT1 en papa, tomate y tabaco en las células acompañantes (CA), que contradice los reportes iniciales (42). En las CA han sido localizados, además, los transportadores AtSUC2, AtSUC3, AtSUC4, OsSUT1 y PmSUC2 (6, 11). ]]>
La localización sub-celular en la membrana citoplasmática fue confirmada mediante microscopía fluorescente confocal, cuando la fusión de la proteína transportadora con la proteína fluorescente verde (GFP, del inglés Green Fluorescent Protein) fue expresada transitoriamente en células foliares de A. thaliana y se detectó la membrana fluorescente en posición externa al núcleo teñido de las células. Esta técnica permitió confirmar a AtSUCT1 y AtSUC2 como proteínas de plasmalema (43).
Al igual que sucede para otros compuestos e iones (44), deben existir proteínas en la membrana vacuolar (tonoplasto), que realicen la función de transportar la sacarosa entre el citoplasma y la vacuola. El primer evento ocurre cuando la sacarosa producida en el citoplasma de las células fotosintéticas es almacenada transitoriamente en la vacuola de estas células durante el fotoperíodo; la sacarosa puede atravesar el tonoplasto en sentido contrario, para ser exportada a los tejidos sumideros, en un transporte que ocurre generalmente en mayor magnitud durante los períodos de oscuridad. En los sumideros, la sacarosa será utilizada en el metabolismo, para el crecimiento o almacenamiento en forma de polisacáridos; sin embargo, en pocas plantas se almacena en altas concentraciones en las vacuolas como disacárido, por ejemplo, los casos de la remolacha y caña de azúcar (7, 45). Es por ello que estas constituyen plantas modelos, para el estudio del transporte y almacenamiento de la sacarosa.
Los estudios de la entrada de la sacarosa en vacuolas aisladas y vesículas de tonoplasto, en tejidos que acumulan sacarosa, tales como las raíces de remolacha azucarera y roja (Beta vulgaris) y el tallo de caña de azúcar, han indicado la presencia de un transporte mediado por proteínas. Se ha demostrado que este transporte es activo en remolacha, ya que la entrada de la sacarosa mostró dependencia del pH, estimulación por Mg/ATP e inhibición por protonóforos y bloqueadores del canal de H+-ATPasas (45, 46). Sin embargo, en la caña de azúcar no se ha podido relacionar el movimiento de sacarosa, a través del tonoplasto, con ningún sistema dependiente de ATP ni de H+, por lo que se ha sugerido un mecanismo de difusión facilitada (47, 48, 49, 50).
Para las vacuolas de hojas de cebada, las cuales no acumulan sacarosa en contra de un gradiente de concentración, también ha sido propuesto un transporte pasivo facilitado (51) y para las hojas de A. comosus se concluyó que la entrada de sacarosa no involucraba un cotransporte con H+ (52).
En el 2006, los transportadores AtSUT4 (también llamado AtSUC4) y HvSUT2, que habían sido previamente descritos como proteínas de membrana plasmática, fueron aislados de protoplastos del mesófilo de hojas de arabidopsis y cebada, y localizados en el tonoplasto de Allium cepa y A. thaliana mediante la expresión transitoria de su ADN en fusión con GFP, convirtiéndose así en los primeros identificados como transportadores de sacarosa vacuolares (43). Teniendo en consideración que estos transportadores fueron caracterizados como un simporte con H+ cuando se expresaron en levadura (21, 53), que están localizados en el tonoplasto (43) y que el pH en el interior de la vacuola es ácido, se ha asumido que la función de ambos es la de extraer la sacarosa de la vacuola de las hojas, pero se sugiere que debe entonces existir un antiporte para la acumulación transitoria de este azúcar en la vacuola durante la fotosíntesis, el cual aún no ha sido descrito (9, 44). ]]>
En el 2008 se reportó otro transportador, localizado en el tonoplasto de las células de nódulos radicales maduros en Lotus japonicus (LjSUT4); el análisis de su secuencia reveló que este pertenece al mismo grupo filogenético que AtSUT4 y HvSUT2. Debido a que la adición del protonóforo m-clorofenilhidrazona cianuro de carbonilo (CCCP) disminuyó fuertemente la entrada de sacarosa a los oocitos de Xenopus, que expresaban la proteína transportadora en su membrana citoplasmática, este se caracterizó como un transporte acoplado al flujo de protones. Esta característica, unida a su localización y gradiente de pH existente a través del tonoplasto, permitió a los autores sugerir su función en la salida de este azúcar de la vacuola hacia el citoplasma (34), como ya había sido planteado para AtSUT4 y HvSUT2 (44).
En A. comosus, el AcSUT1 fue colocalizado en vesículas junto con la proteína BP80 marcadora del compartimiento prevacuolar, mediante la expresión transitoria de SUT-GFP en células epidérmicas de tabaco. Debido a que los compartimentos prevacuolares medían el transporte intracelular de proteínas y solutos en las células vegetales, se propuso que AcSUT1 podría participar en la liberación de la sacarosa, mediada por vesículas, al apoplasto de las hojas para su posterior carga al floema (25).
A causa de que las proteínas SUT han podido ser expresadas y unidas a la membrana plasmática de las células de levadura y oocitos para los estudios funcionales, se ha presupuesto que esta sería el blanco en las células vegetales. Pero más recientemente se ha advertido que los transportadores de otras membranas, por ejemplo del tonoplasto, pudieran no insertarse en el plasmalema o que este fuera un blanco equivocado en estos sistemas de expresión heteróloga (11, 34, 43). Por tanto, se ha sugerido que es necesario confirmar la localización subcelular de los transportadores de sacarosa, mediante la expresión transitoria de la fusión transportador-GFP in planta (43). Esto también pudiera ser la causa de los intentos no exitosos de expresar las proteínas en estas células y, por ende, la no disponibilidad de datos funcionales y cinéticos de muchos de los transportadores.
UN SEGUNDO TRANSPORTADOR DE SACAROSA EN Saccharum spp. HÍBRIDO
Hasta el momento solo se ha identificado y caracterizado un SUT en caña de azúcar, denominado ShSUT1 (24, 33), cuyas principales características han sido referidas previamente. En este trabajo se expone la amplificación del ADNc de un nuevo SUT en las hojas fuente del cultivar cubano de caña de azúcar C 1051-73. La utilización de la técnica de RT-PCR (del inglés Reverse Transcription-Polymerase Chain Reaction) y cebadores degenerados, diseñados a partir del análisis de las secuencias conservadas de los SUT de monocotiledóneas encontrados en bases de datos públicas, con énfasis en el arroz y el maíz, permitió obtener la secuencia completa del marco abierto de lectura. Los resultados de la secuenciación automatizada se procesaron con los programas Chromas 1.45 (54) y Vector NTI 9.0.0 (55).
]]>
El análisis de la secuencia de nucleótidos (1503 pares de bases), así como de la proteína deducida (501 aminoácidos), se realizó en el sitio NCBI (del inglés National Center of Biotechnology Information) con las herramientas correspondientes del BLAST (del inglés Basic Local Aligment Search Tool) (56). De las 100 secuencias de proteína que produjeron alineamientos altamente significativos, el 84 % estaban definidas como proteínas transportadoras de sacarosa.
En la Tabla II se presentan las cuatro primeras accesiones que se correspondieron con plantas monocotiledóneas, que poseían un alto porcentaje de identidad y cobertura con la secuencia en cuestión.
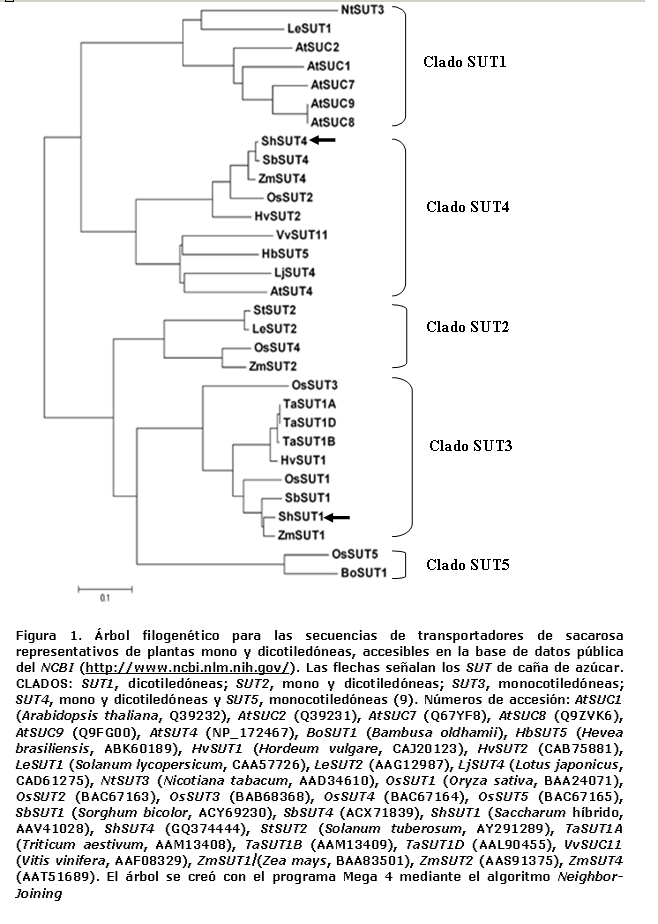
Los análisis filogenéticos de este trabajo se realizaron con el programa Mega versión 4.0 (57), utilizando la secuencia de la proteína y la de 30 de los SUT encontrados en bases de datos públicas, entre los cuales se encontraban la casi totalidad de los reportados para las plantas monocotiledóneas y algunos de los pertenecientes a las dicotiledóneas, con el objetivo de que estuvieran representados los cinco clados en el árbol filogenético (Figura 1). Como se puede observar, la nomenclatura de los transportadores de sacarosa no es homogénea, pues estos se han nombrado para cada especie en el orden en que han sido descubiertos. Además, los transportadores de arabidopsis y otras pocas plantas se han nombrado SUC. Por esta razón y para evitar confusiones, se ha propuesto que las nuevas proteínas sean nominadas según el grupo al que pertenecen por sus relaciones filogenéticas (26).
El Clado SUT1 está integrado hasta el momento solo por plantas dicotiledóneas; sin embargo, en el Clado SUT2 se han reportado transportadores homólogos en plantas dicotiledóneas y monocotiledóneas. La mayoría de los transportadores de monocotiledóneas registrados se encuentran en el Clado SUT3, en el cual se halla el transportador de caña de azúcar ShSUT1; este clado es específico para monocotiledóneas, al igual que el SUT5 (9). Por último, en el Clado SUT4 se observan dos subgrupos, donde se separan los transportadores de las plantas mono y dicotiledóneas; aquí se ha incorporado el segundo transportador de sacarosa, que hemos identificado en la caña de azúcar, el cual se ha denominado ShSUT4, teniendo en cuenta su homología con los integrantes de este clado, también denominado grupo 4 (11).
La Figura 2 muestra la comparación de la secuencia proteica de ShSUT4 y los transportadores de sacarosa presentados en la Figura 1, en la región más conservada de todos los SUT, entre las hélices trasmembranas 1 y 2 (16, 17).
En el alineamiento se observa que la mayor parte presenta fondo negro y gris oscuro y claro, en representación de los residuos iguales, conservados y similares, respectivamente, mientras por el contrario hay muy pocas zonas de fondo blanco, que representan a los aminoácidos desiguales. En esta región se destaca la alta similitud (aminoácidos idénticos y similares) de ShSUT4 con el resto de los transportadores, a pesar de que algunos de ellos están alejados filogenéticamente; esta se calculó en un 98,2 %. La máxima identidad se encontró con los del Clado SUT4, en especial con los de las plantas monocotiledóneas: SbSUT4, ZmSUT4, OsSUT2 y HvSUT2, los cuales se encontraron en el tope de la búsqueda en la base de datos del NCBI (Tabla I). El residuo Histidina (H), situado en el primer lazo extracitoplasmático de ShSUT4 (H54), es común para todos los transportadores de sacarosa, el cual fue demostrado mediante mutación dirigida en la H65 de AtSUC1, que es importante para la actividad transportadora, donde parece estar involucrado en la unión de la sacarosa en el proceso de transporte (58).

Según se observa en la Figura 3, la proteína ShSUT4 se dispone en la membrana con 12 regiones hidrofóbicas insertadas y 11 lazos hidrofílicos que las une, presentando el lazo central y los extremos amino y carboxilo hacia el citoplasma, al igual que todos los SUT identificados hasta el momento a nivel molecular; esta es una característica distintiva de las proteínas de las familias pertenecientes a la superfamilia MFS (37). Esta predicción se realizó con el programa TOPPRED (59) en el sitio web: Sistema Experto de Análisis de Proteínas (ExPASy, del inglés Expert Protein Analysis System); un resultado similar se obtuvo con otros 11 programas de predicción consultados en ese sitio (60).
]]>
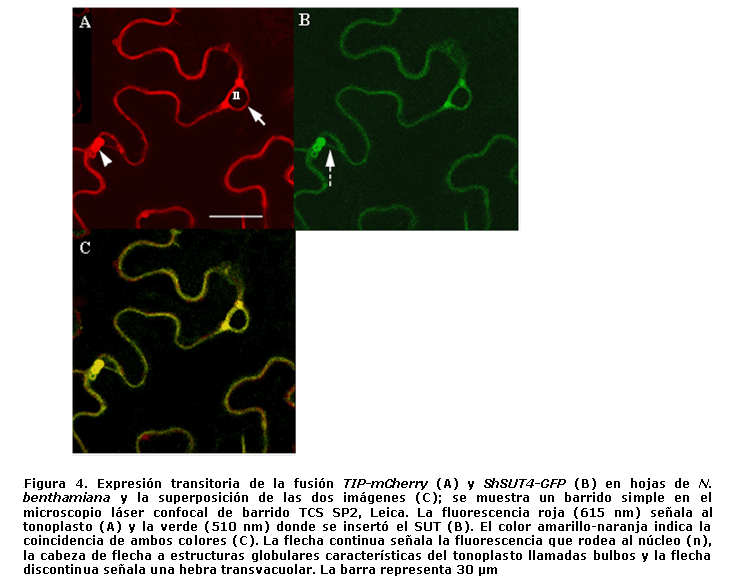
Además de los estudios filogenéticos y de predicción estructural de la secuencia, se determinó la localización subcelular de la proteína. Para ello se utilizó la coexpresión transitoria de las construcciones ShSUT4-GFP y TIP-mCherry en las células epidérmicas de Nicotiana benthamiana, mediada por Agrobacterium tumefaciens (25, 61). Los grupos fluorescentes GFP y mCherry permitieron observar la localización del transportador en color verde (? emisión: 510 nm) y la proteína marcadora del tonoplasto (TIP, del inglés Tonoplast Intrinsic Protein) en rojo (? emisión: 615 nm).
En la Figura 4 se presentan las fotos del microscopio de fluorescencia confocal, donde se observa en el centro del campo visual el núcleo (n) de la célula y la fluorescencia en rojo que marca la vacuola (A). La fluorescencia de la GFP unida al SUT4 rodea el núcleo por la parte interior de la célula (B), al igual que la fusión TIP-mCherry y se observan estructuras globulares y hebras transvacuolares que son características del tonoplasto (A y B).
Estos resultados permiten concluir que la proteína del transportador ha sido insertada en el tonoplasto. La foto C permite comprobar que existe una concordancia en la localización de las dos proteínas a lo largo de la membrana vacuolar de la célula, que se manifiesta en una coloración de amarilla a naranja resultante de la combinación de los colores rojo y verde. Este resultado refuerza que la localización en tonoplasto pudiera ser una propiedad común de algunos de los transportadores de sacarosa del grupo SUT4 (9, 11) y pudiera contribuir a la aclaración de las funciones de los integrantes de este grupo.
CONSIDERACIONES GENERALES
El avance acelerado de la biotecnología vegetal ha permitido la identificación del primer transportador de sacarosa a nivel molecular en 1992 y el estudio detallado de la funcionalidad de este y varios de los siguientes SUT descubiertos, aunque todavía se cuenta con datos de muy pocos de ellos. La localización de las proteínas transportadoras en los tejidos y células se ha ido perfeccionando, pero con el desarrollo de la técnica de la expresión transitoria in planta de proteínas unidas a una molécula fluorescente reportera, se ha facilitado la localización subcelular y permitido confirmar o reevaluar la ubicación de algunas de ellas.
]]>
En este trabajo se mostró la detección de una secuencia de ADNc en caña de azúcar, la cual debe corresponder a un transportador de sacarosa, debido a sus características estructurales denominado ShSUT4. Este transportador posee una alta conservación de aminoácidos respecto a varios transportadores, para los cuales se ha demostrado la actividad transportadora (AtSUT4, LjSUT4, HvSUT1, HvSUT2, OsSUT1, ShSUT1 y ZmSUT1) y presenta el residuo histidina característico de todos los SUT identificados hasta el presente. La predicción de la disposición de la proteína en la membrana, a partir de su estructura primaria, reveló que posee 12 segmentos hidrofóbicos transmembrana, lo que la ubica como miembro de la superfamilia de las proteínas facilitadoras principales (MFS). Su localización subcelular en el tonoplasto contribuye a elevar el interés que ha despertado el grupo de los transportadores SUT4, de los cuales esta sería la cuarta proteína ubicada en esa membrana. Los resultados mostrados permitieron realizar el registro de la secuencia de ADNc del segundo SUT para la caña de azúcar en la base de datos GenBank/NCBI (Número de accesión: GQ374444).
REFERENCIAS
1. LALONDE, S. /et al./. Phloem loading and unloading of sugars and amino acids. Plant Cell Environ, 2003, vol. 26, p. 37–56.
2. RIESMEIER, J. W. /et al./. Isolation and characterization of a sucrose carrier cDNA from spinach by functional expression in yeast. The EMBO Journal, 1992, vol. 11, p. 4705-4713.
3. TURGEON, R. y Medville, R. Phloem loading. A reevaluation of the relationship between plasmodesmatal frequencies and loading strategies. Plant Physiology, 2004, vol. 136, p. 3795–3803.
4. TURGEON, R. y Wolf, S. Phloem transport: cellular pathways and molecular trafficking. Annu. Rev. Plant Biol., 2009, vol. 60, p. 207-21.
5. KÜHN, C. A comparison of the sucrose transporter systems of different plant species. Plant Biology, 2003, vol. 5, p. 215-232.
6. LALONDE, S. /et al./. Transport mechanisms for organic forms of carbon and nitrogen between source and sink. Annual Review of Plant Biology, 2004, vol. 55, p. 341-372.
7. LEMOINE, R. Sucrose transporters in plants: update on function and structure. Biochimica et Biophysica Acta, 2000, vol. 1465, p. 246-262.
8. RIESMEIER, J. W. /et al./. Potato sucrose transporter expression in minor veins indicates a role in phloem loading. The Plant Cell, 1993, vol. 5, p. 1591-1598.
9. KÜHN, C. y Grof, C. P. Sucrose transporters of higher plants. Curr. Opin. Plant Biol., 2010, vol. 16.
10. BUSH, D. Proton-coupled sucrose transport in plasmalemma vesicles isolated from sugar beet (Beta vulgaris L. cv Great Western) leaves. Plant Physiology, 1989, vol. 89, p. 1318-1323.
11. SAUER, N. Molecular physiology of higher plant sucrose transporters. FEBS Letters, 2007, vol. 581, p. 2309–2317.
12. LINGLE, S. E. Evidence for the uptake of sucrose intact into sugarcane internodes. Plant Physiol., 1989, vol. 90, p. 6-8.
13. THOM, M. y Maretzki, A. Evidence for direct uptake of sucrose by sugarcane stalk tissue. Journal of Plant Physiology, 1992, vol. 139, p. 555-559.
14. BOWEN, J. E. y Hunter, J. E. Sugar transport in immature internodal tissue of sugarcane II. Mechanism of sucrose transport. Plant Physiol. 1972, vol. 49, p. 789-793.
15. HIROSE, T. /et al./. cDNA cloning and tissue specific expression of a gene for sucrose transporter from rice (Oryza sativa L.). Plant Cell Physiol., 1997, vol. 38, p. 1389-1396.
16. AOKI, N. /et al./. The sucrose transporter gene family in rice. Plant Cell Physiol., 2003, vol. 44, p. 223–232.
17. AOKI, N. /et al./. Molecular cloning and expression analysis of a gene for a sucrose transporter in maize (Zea mays L.). Plant Cell Physiol., 1999, vol. 40, p. 1072-1078.
18. CARPANETO, A. /et al./. Phloem-localized, proton-coupled sucrose carrier ZmSUT1 mediates sucrose efflux under the control of the sucrose gradient and the proton motive force. The Journal of Biological Chemistry, 2005, vol. 280, p. 21437–21443.
19. WANG, Y. D. /et al./. ZmSUT2, a putative sucrose sensor in maize (Zea mays L.). Registrado en GenBank, 2004.
20. WRIGHT, D. P. /et al./. European and African maize cultivars differ in their physiological and molecular responses to mycorrhizal infection. New Phytol., 2005, vol. 167, p. 881-896.
21. WESCHKE, W. /et al./. Sucrose transport into barley seeds: molecular characterization of two transporters and implications for seed development and starch accumulation. Plant Journal, 2000, vol. 21, p. 455–467.
22. AOKI, N. /et al./. Three sucrose transporter genes are expressed in the developing grain of hexaploid wheat. Plant Molecular Biology, 2002, vol. 50, p. 453–462.
23. CASU, R. E. /et al./. Identification of a novel sugar transporter homologue strongly expressed in maturing stem vascular tissues of sugarcane by expressed sequence tag and microarray analysis. Plant Molecular Biology, 2003, vol. 52, p. 371–386.
24. RAE, A. L. /et al./. Sucrose partitioning between vascular bundles and storage parenchyma in the sugarcane stem: a potential role for the ShSUT1 sucrose transporter. Planta, 2005, vol. 220, p. 817-825.
25. ANTHONY, E. /et al./. Cloning, localization and expression analysis of vacuolar sugar transporters in the CAM plant Ananas comosus (pineapple). Journal of Experimental Botany, 2008, vol. 59, p. 1895–1908.
26. LIN, Y.-T. y Wang, A.-Y. Molecular characterization of the sucrose transporter from shoots of bamboo (Bambusa oldhamii). Registrado en GenBank, 2008.
27. LIU, G. S. /et al./. Cloning and function analysis of sorghum (Sorghum bicolor (L.) Moench) sucrose transporter gene SbSUT1. Registrado en GenBank, 2009.
28. LIU, G. S. /et al./. Cloning and function analysis of sorghum (Sorghum bicolor (L.) Moench) sucrose transporter gene SbSUT4. Registrado en GenBank, 2009.
29. BRAUN, D. M. y Slewinski, T. L. Genetic control of carbon partitioning in grasses: roles of sucrose transporters and tie-dyed loci in phloem loading. Plant Physiology, 2009, vol. 149, p. 71-81.
30. AOKI, N. /et al./. Pathway of sugar transport in germinating wheat seeds. Plant Physiology, 2006, vol. 141, p. 1255–1263.
31. CHANDRAN, D. /et al./. Substrate specificity of the Arabidopsis thaliana sucrose transporter AtSUC2. The Journal of Biological Chemistry, 2003, vol. 278, p. 44320–44325.
32. SIVITZ, A. B. /et al./. Analysis of the transport activity of barley sucrose transporter HvSUT1. Plant and Cell Physiology, 2005, vol. 46, p. 1666-1673.
33. REINDERS, A. /et al./. Sugarcane ShSUT1: analysis of sucrose transport activity and inhibition by sucralose. Plant, Cell and Environment, 2006, vol. 29, p. 1871–1880.
34. REINDERS, A. /et al./. Functional analysis of LjSUT4, a vacuolar sucrose transporter from Lotus japonicus. Plant Mol Biol., 2008, vol. 68, p. 289-299.
]]>35. SUN, Y. /et al./. Transport activity of rice sucrose transporters OsSUT1 and OsSUT5. Plant and Cell Physiology, 2010, vol. 51, p. 114-122.
36. SIVITZ, A. B. /et al./. Arabidopsis sucrose transporter AtSUC9. High-affinity transport activity, intragenic control of expression and early flowering mutant phenotype. Plant Physiology, 2007, vol. 143, p. 188–198.
37. CHANG, A. B. /et al./. Phylogeny as a guide to structure and function of membrane transport proteins. Molecular Membrane Biology, 2004, vol. 21, p. 171-181.
38. RIESMEIER, J. W. /et al./. Evidence for an essential role of the sucrose transporter in phloem loading and assimilate partitioning. The EMBO Journal, 1994, vol. 13, p. 1–7.
39. SLEWINSKI, T. L. /et al./. Sucrose transporter1 functions in phloem loading in maize leaves. J. Exp. Bot., 2009, vol. 60, p. 881–892.
]]>40. AOKI, N. S. /et al./. Expression and localisation analysis of the wheat sucrose transporter TaSUT1 in vegetative tissues. Planta, 2004, vol. 219, p. 176-184.
41. ISHIMARU, K., Hirose, T. /et al./. Antisense expression of a rice sucrose transporter OsSUT1 in rice (Oryza sativa L.). Plant Cell Physiology, 2001, vol. 42, p. 1181-1185.
42. SCHMITT, B. /et al./. Immunolocalization of Solanaceous SUT1 proteins in companion cells and xylem parenchyma: new perspectives for phloem loading and transport. Plant Physiology, 2008, vol. 148, p. 187-199.
43. ENDLER, A. /et al./. Identification of a vacuolar sucrose transporter in barley and Arabidopsis mesophyll cells by a tonoplast proteomic approach. Plant Physiology, 2006, vol. 141, p. 196–207.
44. NEUHAUS, H. E. Transport of primary metabolites across the plant vacuolar membrane. FEBS Letters, 2007, vol. 581, p. 2223-2226.
]]>45. GETZ, H. P. /et al./. lmmunological evidence for the existence of a carrier protein for sucrose transport in tonoplast vesicles from Red Beet (Beta vulgaris L.) root storage tissue. Plant Physiol., 1993, vol. 102, p. 751-760.
46. GETZ, H. P. y Klein, M. Characteristics of sucrose transport and sucrose-induced H+ transport on the tonoplast of Red Beet (Beta vulgaris L.) storage tissue. Plant Physiology, 1995, vol. 107, p. 459-467.
47. MARETZKI, A. y Thom, M. A group translocator for sucrose assimilation in tonoplast vesicles of sugarcane cells. Plant Physiol., 1986, vol. 80, p. 34-37.
48. MARETZKI, A. y Thom, M. UDP-glucose-dependent sucrose translocation in tonoplast vesicles from stalk tissue of sugarcane. Plant Physiology, 1987, vol. 83, p. 235- 237.
49. WILLIAMS, L. /et al./. Characterization of a proton translocating ATPase and sucrose uptake in a tonoplast-enriched vesicle fraction from sugarcane. Physiologia Plantarum, 1990, vol. 80, p. 169-176.
]]>50. PREISSER, J. y Komor, E. Sucrose uptake into vacuoles of sugarcane suspension cells. Planta, 1991, vol. 186, p. 09-114.
51. MARTINOIA, E. /et al./. Transport processes of solutes across the vacuolar membrane of higher plants. Plant Cell Physiol., 2000, vol. 41, p. 1175–1186.
52. McRAE, S. /et al./. Sucrose transport across the vacuolar membrane of Ananas comosus. Functional Plant Biology, 2002, vol. 29, p. 717-724.
53. WEISE, A. /et al./. A new subfamily of sucrose transporters, SUT4, with low affinity/high capacity localized in enucleate sieve elements of plants. The Plant Cell, 2000, vol. 12, p. 1345–1355.
54. CHROMAS 1.45. Disponible en: http://www.technelysium.com.au/chromas.html.
]]>55. VECTOR NTI 9. Disponible en: http://vector-nti.software.informer.com/9.0/download/.
56. BLAST. Disponible en: http://blast.ncbi.nlm.nih.gov/Blast.cgi.
57. TAMURA, K. /et al./. MEGA4: Molecular evolutionary genetic analysis (MEGA) software version 4.0. Molecular Biology and Evolution, 2007, vol. 24, p. 1596-1599.
58. LU, J. M. Y. y Bush, D. His-65 in the proton–sucrose symporter is an essential amino acid whose modification with site-directed mutagenesis increases transport activity. Proc. Natl. Acad. Sci. USA, 1998, vol. 95, p. 9025-9030.
59. TOPPRED. Disponible en: http://mobyle.pasteur.fr/cgi-bin/portal.py?form=toppred.
]]>60. ExPASy. Disponible en: http://ca.expasy.org/tools/.
61. CHINCINSKA, I. A. /et al./. Sucrose transporter StSUT4 from potato affects flowering, tuberization and shade avoidance response. Plant Physiology, 2008, vol. 146, p. 515-528.
Recibido: 30 de abril de 2009
Aceptado: 21 de Julio de 2010