Arbuscular mycorrhizae symbiosis in plants of rice (Oryza sativa L.) subject to hydric stress. Part I. Physiological response improvement
M.Sc. Michel Ruiz Sánchez,I y Dr.C. Ricardo Polón Pérez,II Bannie Vázquez Del Llano,III M.Sc. Yaumara Muñoz Hernández,IV y M.Sc. Nelson Cuéllar Olivero,V Dr.C. Juan M. Ruiz-Lozano,VI
I Investigador Agregado de la Unidad Científico Tecnológica de Base «Los Palacios»
IIInvestigador Auxiliar de la Unidad Científico Tecnológica de Base «Los Palacios»
IIIEspecialista del departamento de Biofertilizantes y Nutrición de las Plantas, Instituto Nacional de Ciencias Agrícolas (INCA), gaveta postal 1, San José de las Lajas, Mayabeque, Cuba, CP 32 700.
IVProfesora Asistente de la Filial MES «Los Palacios», calle 22 e/ 19 y 21, no. 1916, Los Palacios, Pinar del Río, Cuba, CP 22 900. ]]>
VProfesor Auxiliar de la Filial MES «Los Palacios», calle 22 e/ 19 y 21, no. 1916, Los Palacios, Pinar del Río, Cuba, CP 22 900.
VIProfesor Titular del Departamento de Microbiología del Suelo y Sistemas Simbióticos, Estación Experimental Del Zaidín, CSIC, Granada, España.
RESUMEN
El arroz (Oryza sativa L.) es el cultivo más importante para el consumo humano, convencionalmente es cultivado en condiciones de inundación durante todo su ciclo. Sin embargo, aproximadamente la mitad de la superficie de arroz en el mundo no tiene agua suficiente para mantener condiciones óptimas de crecimiento. Una forma posible de aumentar la producción de arroz para satisfacer la demanda es mejorar el uso eficiente del agua por medio de los hongos micorrízicos arbusculares (HMA). La investigación se realizó en la Estación Experimental del Zaidín, Granada, España, con plantas de arroz micorrizadas y no micorrizadas en condiciones controladas y con tres manejos de agua; sin estrés (25 mL), estrés moderado (10 mL) y estrés intenso (5 mL), durante 15 días, con el objetivo de evaluar el efecto de la inoculación de HMA en plantas de arroz sometidas a estrés hídrico y después de recuperadas las plantas. Los resultados muestran que el arroz se puede beneficiar de la simbiosis MA y mejorar su desarrollo a largo plazo después de un período de estrés hídrico. De hecho, en cada nivel de riego, las plantas micorrizadas mostraron incremento de un 50 % de masa fresca aérea y un 40 % la eficiencia fotosintética en comparación con las plantas no micorrizadas. Además se incrementó el contenido de prolina a medida que fue más intenso el estrés hídrico tanto en plantas micorrizadas como en las no micorrizadas.
Palabras clave: simbiosis micorrízica arbuscular, arroz, estrés hídrico, eficiencia, prolina.
ABSTRACT
Rice (Oryza sativa L.) is the most important crop for human consumption is grown conventionally in flooded conditions throughout their cycle. However, approximately half the surface of rice in the world does not have sufficient water to maintain optimal growth conditions. One possible way to increase rice production to meet demand is to improve the efficient use of water by arbuscular mycorrhizal fungi (AMF). The research was conducted at the Experimental Station of Zaidín, Granada Spain, with mycorrhizal and non-mycorrhizal rice plant under controlled conditions and with three water management, without stress (25 mL), moderate stress (10 mL) and severe stress (5 mL) for 15 days, in order to evaluate the effect of AMF inoculation of rice plants subjected to hydric stress and after the plants recovered. The results show that rice can benefit from the symbiosis MA and improve long-term development after a period of water stress. In fact, at each level of irrigation, the mycorrhizal plants showed a 50 % increase in aerial fresh mass and 40 % photosynthetic efficiency compared to non-mycorrhizal plants. Besides, the proline content increased with hydric stress in mycorrizal and non-mycorrizal plants.
Key words: arbuscular mycorrhizal symbiosis, rice, water stress, ephycacy, proline.
INTRODUCCIÓN
El arroz (Oryza sativa L.) es el cultivo más importante para el consumo humano, constituyendo el alimento básico para más de la mitad de la población mundial. Tiene la particularidad evolutiva de ser semi-acuático y convencionalmente se cultiva en condiciones de inundación continua durante la mayor parte de su ciclo de crecimiento (1). Necesita gran cantidad de agua, cuya escasez tiene una influencia negativa sobre el crecimiento de la planta, el rendimiento y la determinación de la calidad (2).
Sin embargo, aproximadamente la mitad de la superficie de arroz en el mundo no tiene agua suficiente para mantener condiciones de inundación y el rendimiento se reduce en cierta medida por la sequía. Incluso el estrés de agua intermitentes en las etapas críticas puede resultar en una considerable reducción del rendimiento y el fracaso de los cultivos (3).
La demanda de la producción de arroz sigue en aumento debido al continuo crecimiento de la población mundial, se prevé llegar a unos 8 mil millones en 2030 y por tanto hay necesidad de seguir aumentando su producción en un 40 % en los próximos 20 años (3).
Se ha demostrado que la simbiosis de micorrizas arbusculares (MA) puede proteger a las plantas hospederas contra los efectos perjudiciales del déficit de agua (4). Los estudios realizados hasta la fecha, han sugerido varios mecanismos por los que la simbiosis MA puede aliviar el estrés por sequía en las plantas hospederas. Los más importantes son: la absorción directa y la transferencia de agua a través de las hifas fúngicas a la planta huésped (5); cambios en las propiedades de retención de agua del suelo; mejor ajuste osmótico de las plantas MA (6); la mejora del intercambio de gases en la planta y uso eficiente del agua, así como la protección contra el daño oxidativo generado por el estrés hídrico (7). ]]>
Una forma posible de aumentar la producción de arroz para satisfacer la demanda de crecimiento de la población es mejorar la eficiencia del uso del agua en condiciones de déficit hídrico en el arroz por medio de la simbiosis MA. El objetivo de esta primera parte es evaluar la respuesta fisiológica de algunos parámetros en las plantas de arroz micorrizadas y no micorrizadas sometidas a estrés hídrico a los 30 días después del trasplante (DDT).
MATERIALES Y MÉTODOS
Diseño experimental y análisis estadístico
La investigación se realizó en la Estación Experimental del Zaidín, Granada, España, en el cultivo del arroz (Oryza sativa L.), variedad comercial de ciclo corto INCA LP-5, en condiciones controladas (cámara de cultivo) durante su fase vegetativa de crecimiento. El experimento parte de una etapa inicial de semillero inoculado y no inoculado con el hongo micorrízico arbuscular (Glomus intraradices) a una dosis de 100 g por cada kg de sustrato. Las plantas fueron trasplantadas a los 14 días después de germinación (DDG) a macetas de 400 g de sustrato. También se realizó otra inoculación en el momento del trasplante (5 g de inóculo por maceta), justo debajo de las plántulas de arroz.
Tratamientos:
]]>
T1. Plantas MA + 25 mL (Control)
T2. Plantas MA + 10 mL
T3. Plantas MA + 5 mL
T4. Plantas noMA + 25 mL (Control)
T5. Plantas noMA + 10 mL
T6. Plantas noMA + 5 mL
Los tratamientos fueron distribuidos siguiendo un diseño experimental completamente aleatorizado. Los datos de cada muestreo fueron sometidos a análisis de varianza simple (ANOVA), seguido por la prueba de Duncan para (p£0,05) (8).
Condiciones de crecimiento ]]>
Las plantas fueron cultivadas entre 60-70 % de humedad relativa, las temperaturas de día y noche fueron de 23 y 19ºC, respectivamente, con un fotoperíodo de 16 horas luz y ocho horas de oscuridad, a una intensidad de la luz de 250 µE.m-2s-1 medido, con un Licor (Lincoln, NE, EE.UU., modelo LI - 188B).
Durante los primeros 30 días después del trasplante, cada planta recibió 25 mL de solución nutritiva (9), a excepción del fósforo (P), que se redujo a un 25 % a fin de evitar la inhibición de la colonización de las micorrizas arbusculares. Este volumen de solución nutritiva se aplicó tres veces por semana en días alternos. Los tratamientos controles (sin estrés hídrico) recibieron 25 mL de solución nutritiva tres veces por semana. El estrés hídrico moderado, consistió en la aplicación de la misma cantidad de nutrientes diluidos en 10 mL de agua. El estrés hídrico intenso, consistió en la aplicación de la misma cantidad de nutrientes diluidos en 5 mL de agua.
Suelo y material biológico
El sustrato empleado consistió en una mezcla de suelo procedente de la Estación Experimental del Zaidín, Granada, España, tamizado (2 mm), con arena (<1 mm) y vermiculita, en proporción 1 suelo: 2 arena:6 vermiculita (v/v/v). La arena y la vermiculita fueron autoclaveadas a 120oC, durante 20 minutos y el suelo se esterilizó a vapor fluente (a 100oC, durante 1 hora, tres días consecutivos). El suelo tenía un pH de 8,1 (agua); 1,81 % de materia orgánica, y las siguientes concentraciones de nutrientes (mg.kg-1): nitrógeno (N) 2,5; fósforo (P) 6,2 (NaHCO3- P extraíble); potasio (K) 132.
El hongo micorrízico arbuscular utilizado fue Glomus intraradices (Schenck y Smith), perteneciente a la colección de la Estación Experimental del Zaidín, Granada, España (aislado EEZ 01). ]]>
Se realizaron mediciones antes del estrés (AE), después del estrés (DE) y de la recuperación (DR), coincidiendo con los 30, 45 y 70 DDT respectivamente, donde se evaluó la eficiencia fotosintética del fotosistema II, por ciento de colonización simbiótica en la raíz, masa fresca parte aérea y radical. Además se determinó la prolina en las plantas a los 45 DDT y 70 DDT.
Indicadores evaluados
Porcentaje de colonización y producción de biomasa. A los 30, 45 y 70 DDT se separó el sistema radical de la parte aérea de las planta y se determinó la masa fresca de ambas y el por ciento de colonización del sistema radical (10). La parte aérea se fraccionó en muestras de 1 g, las cuales se congelaron en el momento del muestreo con nitrógeno líquido para determinar el contenido de prolina.
Eficiencia fotosintética. La eficiencia del fotosistema II, se midió con un FluorPen FP100 (Photon Systems Instruments, Brno, República Checa), que permite una evaluación no invasiva del funcionamiento del aparato fotosintético de las plantas mediante la medición de la fluorescencia de la clorofila A. El FluorPen cuantifica el rendimiento cuántico del fotosistema II como la relación entre el rendimiento actual del fotosistema adaptados a la luz (Fv) y el máximo rendimiento del fotosistema II adaptado a la luz (Fm), (11). Las mediciones se tomaron en el tercio superior de plantas, repitiendo la evaluación cuatro veces en cada planta (12).
Contenido de prolina. Se determinó por el método de Bates et al., 1973 (13) y se expresó en nmol.g-1 de masa seca. Utilizando reactivo de ninhidrina. Para lo cual se realizó una curva patrón a partir de una solución de prolina (1 mM) con las siguientes concentraciones: 0, 25, 50, 100, 200 y 300 µM) de prolina y se midió la absorbancia a 530 nm.
RESULTADOS Y DISCUSIÓN
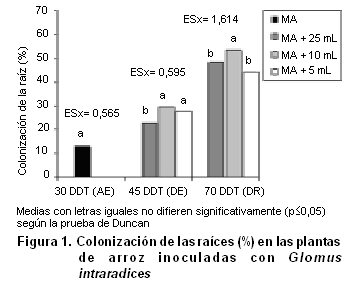
No se observó colonización micorrízica en las plantas no inoculadas con el hongo MA, como era de esperar. Los valores de colonización de las raíces aumentaron con el tiempo (Figura 1).

Antes de iniciar el estrés (30 DDT), el porcentaje de colonización de las raíces fue solo del 13 %. Después del período del estrés hídrico inducido durante 15 días (45 DDT) la colonización de las raíces aumentó hasta el 23 %, presentando las plantas que recibieron 10 o 5 mL de solución nutritiva un porcentaje ligeramente superior a las que habían permanecido como control (25 mL de solución nutritiva).
Después de la recuperación del estrés durante 25 días adicionales (70 DDT) en el sistema radical se alcanzó más del 45 % de colonización MA. Los tratamientos que recibieron 10 mL de solución nutritiva mostraron los porcentajes de colonización de la raíz más altos (53 %).
En la actualidad, se acepta que la simbiosis MA protege a la planta hospedadora frente a los efectos negativos del déficit hídrico, mejorando la tolerancia de planta frente a la sequía mediante una combinación de efectos nutricionales, físicos y celulares (14). ]]>
La simbiosis MA generalmente aumenta el crecimiento de la planta hospedadora debido a la mejor nutrición de la misma (15). Los efectos beneficiosos de los hongos micorrízicos sobre el crecimiento de plantas en condiciones de sequía se han demostrado en varias especies de plantas (16). En esta investigación, los efectos positivos de la simbiosis MA sobre el crecimiento de las plantas solo se precian a los 70 DDT. Esto indica que, en las plantas de arroz y en las condiciones de cultivo ensayadas, la colonización por G. intraradices estimuló el crecimiento de la planta, aunque tardó más tiempo que en otras plantas hospedadoras. Por lo tanto, para obtener beneficios de la simbiosis, el arroz debe ser cultivado en condiciones no inundadas. Las condiciones aeróbicas en el suelo estimulan la colonización de raíces de arroz por los hongos MA (2).
La masa fresca de la parte aérea (MFA) y de la raíz (MFR) antes del inicio del estrés (30 DDT) fueron similares en plantas MA y plantas noMA (Figura 2A, B).
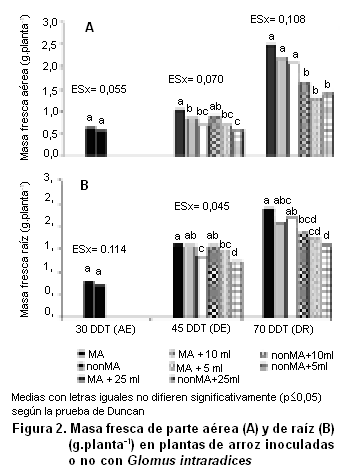
Después del período de estrés (45 DDT), tanto la MFA como la MFR disminuyeron significativamente en los tratamientos bajo estrés intenso (5 mL de solución nutritiva) en comparación con el tratamiento control bien regado (25 mL de solución nutritiva), esta disminución fue similar en las plantas MA y en las noMA, provocada por el estrés hídrico inducido (17). Tras la recuperación de la sequía durante 25 días, la MFA mostró un aumento significativo en las plantas MA, en comparación con las plantas noMA. De hecho, en cada manejo de agua aplicado, las plantas MA mostraron un incremento del 50 % de MFA en comparación con plantas noMA.
]]>
Una tendencia similar se observó para la MFR, pero, en ese caso, las diferencias no fueron significativas para las plantas que habían sido regadas con 10 mL de solución nutritiva, resultados que corresponden a los de otros autores (18).
Este resultado puede estar relacionado con el hecho de que solo a los 70 DDT las plantas de arroz alcanzaron un nivel considerable de la colonización MA (entre 44 a 53 %). La literatura sobre la simbiosis MA refleja que no hay un valor umbral de colonización de las raíces para que se produzca la mejora del crecimiento vegetal. Esto depende más bien, de las especies vegetales y fúngicas que participan en la simbiosis y de las condiciones específicas de cultivo.
Sin embargo, generalmente se asume que una mayor tasa de colonización de las raíces por el hongo mejorará los efectos de la MA sobre el desarrollo de la planta (19, 20). Otros investigadores encontraron niveles comparables de colonización MA (que van desde 14 a 51 %) en las raíces de 13 variedades de arroz cultivadas también en condiciones aeróbicas (2). En cualquier caso, para determinar con más precisión la causa de la mejora del crecimiento de las plantas de arroz estudiadas, se evaluaron los efectos de la micorrización sobre una variedad de procesos bioquímicos en la planta.
Eficiencia fotosintética
La eficiencia del fotosistema II se evaluó mediante la fluorescencia de la clorofila A (Figura 3). Antes de que se iniciara el período de estrés (30 DDT) la eficiencia fotosintética del fotosistema II fue similar en plantas MA y noMA. Después del período de sequía (45 DDT) las plantas MA exhiben una mayor eficiencia fotosintética, en comparación con las plantas noMA.
En esta investigación, las plantas MA mostraron un mejor rendimiento del fotosistema II cuando se sometieron a estrés hídrico. Los valores más altos de eficiencia fotosintética en las plantas MA (cercanos al máximo teórico de 0,83) indican que el aparato fotosintético de estas plantas fue menos dañado por el estrés impuesto (21). Este efecto puede haber contribuido al crecimiento alcanzado por las plantas MA, probablemente mediante la mejora de la fijación de CO2 durante y después del estrés. De hecho, varios estudios han demostrado una correlación positiva entre la tolerancia al estrés hídrico y el mantenimiento de la eficiencia del fotosistema II, que a su vez también mantiene la productividad de la plantas (22, 23).
Contenido de prolina
El contenido de prolina a los 45 DDT en la parte aérea de las plantas MA y las plantas noMA se incrementó a medida que disminuyó el estatus hídrico en la planta, comportamiento que nos asevera que las plantas se estresaron por efecto del estrés hídrico inducido (Figura 4). De hecho, las plantas regadas con 10 o 5 mL de solución nutritiva mostraron mayor contenido de prolina en comparación con su correspondiente control (25 mL), comportamiento opuesto a la respuesta de la eficiencia fotosintética, que pudo ver favorecida por influencia de la micorrízación y un estado hídrico superior en las plantas controles (23).
En cualquier caso, la cantidad de prolina en cada régimen hídrico fue ligeramente superior en las plantas noMA que en las plantas MA. Después de la recuperación de la sequía (70 DDT) el contenido de prolina continuó siendo mayor en las plantas que habían sido previamente sometidos a la sequía (10 o 5 mL).
]]>
Sin embargo, no hubo diferencias significativas entre las plantas MA y las plantas noMA para cada régimen hídrico.
Muchas especies vegetales disminuyen el potencial osmótico de sus células mediante la síntesis y acumulación de osmolitos compatibles, tales como la prolina, que participa en el ajuste osmótico. De esta manera, las plantas mejoran su tolerancia frente a la sequía (24, 25). Además de actuar como un osmoprotector, la prolina también sirve como un regulador de radicales hidroxilo, como soluto que protege a las macromoléculas frente a la desnaturalización y como medio para reducir la acidez en la célula (26). Este efecto se relaciona con la protección de la planta frente a la deshidratación a través de mecanismos de defensa primarios de sequía. Así, las plantas MA podrán necesitar una menor cantidad de prolina que el resto de los tratamientos noMA (23, 27, 28).
Conclusiones
De esta investigación se puede concluir que las plantas de arroz se micorrizaron en condiciones aeróbicas durante su fase vegetativa a partir de los 30 DDT, con valores porcentuales entre 12 y 50 %, condición que les permitió a las mismas tolerar el déficit hídrico impuesto y mejorar su respuesta en las variables evaluadas. Se incrementó a largo plazo el crecimiento de las plantas de arroz micorrizadas, su eficiencia fotosintética y el contenido de prolina con respecto a las plantas no micorrizadas, aunque el grado de intensidad del estrés hídrico fue intenso.
Agradecimiento
Al Dr.C. Juan Manuel Ruiz Lozano (Investigador Científico del CSIC) por todo su apoyo y guía durante la investigación.
REFERENCIAS
1. Kamoshita, A.; Babu, R. C.; Boopathi, N. M. y Fukai, S. Phenotypic and genotypic analysis of drought-resistance traits for development of rice cultivars adapted to rainfed environments. Field Crops Res., 2008, vol. 109, p. 1-23.
2. Vallino, M.; Greppi, D.; Novero, M.; Bonfante, P. y Lupotto, E. Rice root colonization by mycorrhizal and endophytic fungi in aerobic soil. Ann. Appl. Biol., 2009, vol. 154, p. 195-204.
3. Bernier, J.; Atlin, G. N.; Serraj, R.; Kumar, A. y Spaner, D. Breeding upland rice for drought resistance. J. Sci. Food Agric., 2008, vol. 88, p. 927-939.
4. Ruiz-Lozano, J. M.; Porcel, R. y Aroca, R. Evaluation of the possible participation of drought-induced genes in the enhanced tolerance of arbuscular mycorrhizal plants to water deficit. In: Varma A, editor. Mycorrhiza: state of the art, genetics and molecular biology, eco-function, biotechnology, eco-physiology, structure and systematics, 3rd ed. Germany: Springer-Verlag. 2008. p. 185-205.
5. Alberdi, Miren; Álvarez, Maricel; Valenzuela, E.; Godoy, R.; Olivares, E. y Barrientos, Mónica. Respuesta al déficit hídrico de plantas de Nothofagus dombeyi inoculadas con un hongo ectomicorrícico específico (Descolea antárctica Sing) y no específico (Pisolithus tinctorious (Pers.) Coker & Couch). Revista Chilena de Historia Natural, 2007, vol. 80, p. 479-491. ISSN: 0716-078X.
6. Ghneim, H. T.; Rosales, A.; Aguilar, M.; Pieters, A.; Pérez, I. A. y Torrealba, G. Identificación de cultivares de arroz con alta capacidad de ajuste osmótico para el mejoramiento genético de la tolerancia a la sequía. Agronomía Tropical, 2003, vol, 56, no. 4, p. 677-687.
7. Porcel, R.; Azcón, R. y Ruiz-Lozano, J. M. Evaluation of the role of genes encoding for D1-pyrroline-5-carboxylate synthetase (P5CS) during drought stress in arbuscular mycorrhizal Glycine max and Lactuca sativa plants. Physiol Mol Plant Pathol., 2004a, vol. 65, p. 211-221.
8. Duncan, D. B. Multiple range and multiple F-tests. Biometrics, 1955, vol. 11, p. 1-42.
9. Hoagland, D. R. y Arnon, D. I. The water-culture method for growing plants without soil. Calif Agric Exp Station Circular, 1950, vol. 347, p. 1-32.
10. Phillips, J. M. y Hayman, D. S. Improved procedure of clearing roots and staining parasitic and vesicular-arbuscular mycorrhizal fungi for rapid assessment of infection. Trans Br Mycol Soc., 1970, vol. 55, p. 159-161.
11. Oxborough, K. y Baker, N. R. Resolving chlorophyll a fluorescence images of photosynthetic efficiency into photochemical and non-photochemical components-calculation of qP and Fv´/Fm´ without measuring Fo´. Photosynth Res., 1997, vol. 54. pp. 135-142.
12. Dell’Amico, J.; Rodríguez, P.; Torrecillas, A.; Morte, Asun y Sánchez-Blanco, María de J. Influencia de la micorrización en el crecimiento y las relaciones hídricas de plantas de tomate sometidas a un ciclo de sequía y recuperación. Cultivos Tropicales, 2002, vol. 23, no. 1, p. 29-34.
13. Misra, N. y Saxena, P. Effect of salicylic acid on proline metabolism in lentil grown under salinity stress. Plant Science, 2009, vol. 177, p. 181-189.
14. Ruiz-Lozano, J. M. Arbuscular mycorrhizal symbiosis and alleviation of osmotic stress: new perspectives for molecular studies. Mycorrhiza, 2003, vol. 13, p. 309-317.
15. Porras-Soriano, A.; Soriano-Martín, M. L.; Porras-Piedra, A. y Azcón, R. Arbuscular mycorrhizal fungi increa,sed growth, nutrient uptake and tolerance to salinity in olive trees under nursery conditions. Journal of Plant Physiology, 2009, vol. 166, p. 1350-1359.
16. Azcón, R. y Barea, J. M. Mycorrhizosphere interactions for legume improvement. In: Khanf MS, Zaidi A, Musarrat J, editors. Microbes for legume improvement. Vienna: Springer; 2010, p. 237-271.
17. Barnabás, B.; Jäger, K. y Free, A. The effect of drought and heat stress on reproductive processes in cereals. Plant, Cell and Environment., 2008, vol. 31, p. 11-38.
18. Bolandnazar, S.; Aliasgarzad, N.; Neishabury, M. R. y Chaparzadeh, N. Mycorrhizal colonization improves onion (Allium cepa L.) yield and water use efficiency under water deficit condition. Scientia Horticulturae, 2007, vol. 114. p. 11-15.
19. Gutjahr, C.; Banba, M.; Croset, V.; An, K.; Miyao, A.; An, G.; Hirochika, H.; Imaizumi-Anraku, H. y Paszkowski, U. Arbuscular mycorrhizaspecific signaling in rice transcends the common symbiosis signalling pathway. Plant Cell, 2008, vol. 20, p. 2989-3005.
20. Gutjahr, C.; Casieri, L. y Paszkowski, U. Glomus intraradices induces changes in root system architecture of rice independently of common symbiosis signalling. New Phytologist., 2009, vol. 182, p. 829-837.
21. Loggini, B.; Scartazza, A.; Brugnoli, E. y Navari-Izzo, F. Antioxidative defense system, pigment composition and photosynthetic efficiency in two wheat cultivars subjected to drought. Plant Physiol., 1999, vol. 119, p. 1091-1099.
22. Germ, M.; Kreft, I. y Osvald, J. Influence of UV-B exclusion and selenium treatment on photochemical efficiency of photosystem II, yield and respiratory potential in pumpkins (Cucurbita pepo L.). Plant Physiol Biochem., 2005, vol. 43. p. 445-448.
23. Porcel, R. y Ruiz-Lozano, J. M. Arbuscular mycorrhizal influence on leaf water potential, solute accumulation and oxidative stress in soybean plants subjected to drought stress. J. Exp. Bot., 2004, vol. 55, p. 1743-1750.
24. Saccardi, K.; Pineau, B.; Roche, O. y Cornic, G. Photochemical efficiency of photosystem II and xantophyll cycle components in Zea mays leaves exposed to water stress and high light. Photos Res., 1998, vol. 56, p. 57-66.
25. Cattivelli, L.; Rizza, F.; Badeck, F. W.; Mazzucotelli, E.; Mastrangelo, A. M.; Francia, E.; Mare, C.; Tondelli, A. y Stanca, M. Drought tolerance improvement in crop plants: An integrated view from breeding to genomics. Field Crops Research., 2008, vol. 105, no. 1-2, p. 1-14.
26. Vendruscolo, E. C. G.; Schuster, I.; Pileggi, M.; Scapim, C. A.; Molinari, H.B.C.; Marur, C. J. y Vieira, L. G. E. Stress-induced synthesis of proline confers tolerance to water deficit in transgenic wheat. Journal of Plant Physiology, 2007, vol. 164, no. 10, p. 1367-1376.
27. Mostajeran, A. y Rahimi-Eichi, V. Effects of Drought Stress on Growth and Yield of Rice (Oryza sativa L.) Cultivars and Accumulation of Proline and Soluble Sugars in Sheath and Blades of Their Different Ages Leaves. American-Eurasian J. Agric. & Environ. Sci., 2009, vol. 5, no. 2, p. 264-272.
28. Aroca, R.; Aguacil, M.; Vernieri, P. y Ruiz-Lozano, J. M. Plant responses to drought stress and exogenous ABA application are differently modulated by mycorrhization in tomato and an ABA-deficient mutant (sitiens). Microb Ecol., 2008, vol. 56, p. 704-719.
]]>
Recibido: 23 de febrero de 2012
Aceptado: 17 de julio de 2012
M.Sc. Michel Ruiz Sánchez, Investigador Agregado de la Unidad Científico Tecnológica de Base «Los Palacios». Email: mich@inca.edu.cu
]]>