
Searching of a new culture medium for in vitro mycorrhization of potato (Solanum tuberosum L.) plantlets
Dra.C. Kalyanne Fernández Suárez,I Dr.C. Félix Fernández Martín,II Dr.C. Stéphane DeclerckIII
IInvestigador Agregado del departamento de Biofertilizantes y Nutrición de las Plantas, Instituto Nacional de Ciencias Agrícolas, gaveta postal 1, San José de las Lajas, Mayabeque, CP 32 700, Cuba.
IIInvestigador Titular del departamento de Biofertilizantes y Nutrición de las Plantas, Instituto Nacional de Ciencias Agrícolas, gaveta postal 1, San José de las Lajas, Mayabeque, CP 32 700, Cuba.
IIIDr.C. Stéphane Declerck, Unidad de Microbiología, Universidad Católica de Lovaina, Bélgica.
]]>
RESUMEN
El medio de cultivo constituye un eslabón clave para garantizar el establecimiento de la simbiosis micorrízica arbuscular en plantas in vitro, pues involucra a organismos con requerimientos nutricionales muy diferentes. Este trabajo se realizó con el objetivo de desarrollar un medio de cultivo a partir de modificaciones nutricionales realizadas al medio MS, que permitiera el establecimiento de la micorrización in vitro de plantas de papa con un estado nutricional adecuado. Se realizaron dos experimentos utilizando diferentes medios de cultivo (SRM, MS y ½ MS), así como variaciones en las concentraciones de nutrientes del medio MS empleando Diseños Completamente Aleatorizados. En estos medios se inocularon plántulas de papa, de entre siete y diez días de micropropagadas, con esporas de Glomus clarum, en un sistema autotrófico parcialmente in vitro. Se realizaron muestreos del desarrollo fúngico y de las plántulas a los 20, 30 y 40 días de cultivo. Se observó un comportamiento diferenciado tanto en los parámetros de crecimiento vegetal como fúngicos, dependiendo del medio de cultivo en el cual se desarrollaron, siendo en el medio E (¼P-¼N-¼K con respecto a MS) en el que se encontraron, de forma integral, los mayores valores de las variables evaluadas. Durante el tiempo de duración de los experimentos no se detectaron diferencias entre las plántulas inoculadas y las controles.
Palabras clave: medio de cultivo, micorrización in vitro, papa.
ABSTRACT
The culture medium is the key stone to guarantee the establishment of arbuscular mycorrhizal symbiosis on in vitro plants, because it includes organisms with different nutritional requirements. The aim of this investigation was to develop a culture medium, starting from nutritional modifications made to MS medium, in order to allow the in vitro mycorrhization of potato plants with an adequate nutritional state. Two experiments were carry out using three culture media (SRM, MS and ½MS), as well as different nutrients concentrations of MS medium. Potato plantlets, of seven and ten days old, were inoculated in these media with Glomus clarum spores in a partially in vitro autotrophic system. Fungal and potato development were sampled after 20, 30 and 40 days of culture. A differentiated behavior of fungal and potato growth parameters were observed, depending of the culture medium used, been the E medium (¼P - ¼N - ¼K respect to MS) the one where the major values of variables were found. Not differences between inoculated and controls plantlets were found during the experiments.
Key words: culture medium, in vitro mycorrhization, potato.
]]>
INTRODUCCIÓN
El medio de cultivo constituye un eslabón clave para garantizar el establecimiento de la simbiosis micorrízica arbuscular en plantas in vitro sin afectar el estado fisiológico de las plántulas, pues involucra a organismos con requerimientos nutricionales muy diferentes (1).
La selección del medio es muy importante pues algunos tipos de agar contienen inhibidores propios debido a la presencia de trazas de metales pesados. Además, determinadas concentraciones de sulfato de sodio, fósforo y sacarosa en el medio de cultivo son de relevante importancia para el establecimiento de los hongos micorrízicos (2, 3, 4) ya que retardan o inhiben el proceso de germinación y colonización, por lo que se encuentran disminuidos en los medios en los que estos se cultivan.
Las plantas obtenidas a través de las técnicas de cultivo de tejidos se producen sobre medios sólidos, semisólidos y líquidos, cuya composición varía dependiendo de la especie de planta que se esté cultivando y de los propósitos del productor; pero en general, son ricos en nutrientes minerales, en especial los que de alguna manera pueden retardar la colonización micorrízica e incluso inhibirla (5, 6).
En cambio, los cultivos duales de raíces y hongos micorrizógenos son establecidos en medios sólidos, particularmente en los medios White modificado (Mínimo, M) y Strullu & Romand modificado (SRM) (7, 8, 9), los cuales presentan una concentración de macroelementos mucho más baja que las encontradas en el medio Murashige & Skoog (MS) (10), comúnmente utilizado para la micropropagación de plantas. La composición del medio M es incluso más pobre que el medio SRM y fue desarrollado comparando el efecto de la concentración de diferentes elementos sobre la formación de micorrizas (2). Por su parte, el medio SRM fue desarrollado empíricamente (11) para optimizar la fase intrarradical del hongo in vitro. La composición de macroelementos es similar en ambos y las diferencias mayores se encuentran en la composición de oligoelementos y vitaminas.
]]>
Algunos autores (12) publicaron un sistema de micorrización autotrófico parcialmente in vitro de plantas de Solanum tuberosum L. (papa), utilizando solo placas Petri y el medio de cultivo SRM, que es el adecuado para el establecimiento micorrízico en raíces transformadas. En dicho sistema las raíces se desarrollan dentro de la placa, en un ambiente totalmente in vitro y los vástagos, expuestos a condiciones medioambientales de cuarto de crecimiento.
Estos autores obtuvieron una intensa colonización micorrízica y la producción de miles de esporas después de 22 semanas de cultivo, las cuales fueron capaces de colonizar nuevas plantas bajo las mismas condiciones. Sin embargo, al concluir el experimento, las plantas mostraban numerosas afectaciones en su desarrollo y estado fisiológico, debido al prolongado tiempo de cultivo y la escasez de nutrientes presentes en el medio empleado (SRM). Por tal motivo, las plantas producidas en dicho sistema no podían ser utilizadas con otros fines, como por ejemplo, el de ser trasladadas a invernadero para la producción de tubérculos como semilla.
Hasta el momento no existe un sistema de cultivo de micorrización in vitro de plantas que haya sido diseñado tomando en consideración los requerimientos nutricionales de las plantas utilizadas.
Teniendo en cuenta los antecedentes presentados se realizó esta investigación con el principal objetivo de diseñar un medio de cultivo a partir de medios conocidos que permitiera la micorrización rápida de plantas de papa in vitro con un estado nutricional adecuado.
MATERIALES Y MÉTODOS
Para cumplimentar el objetivo propuesto se llevaron a cabo tres experimentos encaminados a la búsqueda de un medio de cultivo en el que se garantizara la micorrización rápida y eficiente de plántulas de papa. ]]>
Aspectos generales de los experimentos
Material biológico
Se utilizaron vitroplantas de Solanum tuberosum L. cv Desirée suministradas por los laboratorios de la Estación de Haute, Libramont, Bélgica. Las plántulas se subcultivaron por micropropagación de los cortes nodales y se colocaron 20 explantes en cajas de cultivo (90 x 60 x 50 mm) estériles conteniendo 50 mL de medio MS (Duchefa, Biochemlie, Haarlem, The Netherlands) suplementado con 20 g.L-1 de sacarosa, 3 g.L-1 Gel GroTM (ICN, Biomedicals, Inc., Irvine, CA, USA), ajustado a pH 5,7 antes de la esterilización (121°C, 15 min.). Las cajas de cultivo fueron transferidas a cámara de crecimiento bajo condiciones controladas (22°C, fotoperíodo de 16 h.día-1 y flujo fotosinténtico de 225 µmol.m-2.s-1).
El inóculo fúngico utilizado (Glomus clarum Nicolson & Schenck, MUCL 46238), de cuatro meses de cultivo, fue adquirido en GINCO (BCCM/MUCL, Unidad de Microbiología, Universidad católica de Lovaina, Bélgica, http://www.mbla.ucl.ac.be/ginco-bel), suministrado en placas Petri (90 mm diámetro) en asociación con raíces transformadas (Ri T-DNA) de zanahoria (Daucus carota L.) en medio SRM (Strullu y Romand modificado) (13) solidificado con 3 g.L-1 Gel GroTM. La cepa fue subcultivada utilizando la metodología descrita por Cranenbrouck et al. (14), produciendo miles de esporas en un periodo de cinco meses.
Experimento 1. Análisis cualitativo de las potencialidades de los medios MS, ½MS y SRM para el establecimiento del HMA Glomus clarum en plántulas de papa, utilizando un sistema autotrófico de cultivo parcialmente in vitro. ]]>
En este experimento se evaluaron las posibilidades de los medios de cultivo MS, ½MS y SRM (Tabla I) para garantizar la germinación, colonización y establecimiento micorrízico de esporas de HMA en plántulas de papa, en un sistema autotrófico de cultivo, parcialmente in vitro (SA-PIV).

El SA-PIV utilizado fue propuesto por Voets (12) para producir inóculo micorrízico in vitro asociando esporas de HMA a plántulas de papa. Como puede apreciarse en la Figura 1 en este sistema la planta se desarrolla en dos condiciones diferentes, el sistema radical se encuentra dentro de una placa Petri (90 mm diámetro.) previamente preparada, creciendo en medio de cultivo sólido bajo condiciones estrictas de cultivo in vitro y el sistema aéreo se desarrolla totalmente fuera, expuesto a condiciones ambientales de cuarto de crecimiento.
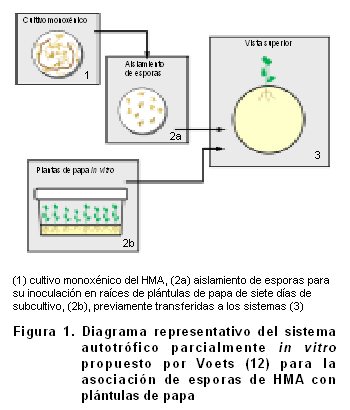
Para establecer el sistema se procedió a desarrollar la metodología descrita por Voets (12), la cual consistió en realizar un orificio (± 2 mm diámetro), con ayuda de un pinza caliente, en la base y la tapa de las placas Petri (90 mm diámetro) y adicionar 30 mL del medio correspondiente (MS, ½MS y SRM) en cada placa, sin azúcar y sin vitaminas.
Para solidificar los medios se añadieron 4 g.L-1 de Gel GroTM. Se tomaron plántulas de papa de entre siete y diez días de subcultivadas en medio MS (entre dos y tres hojas y entre tres y cuatro raicillas por plántula) y se transfirieron a las placas con ayuda de pinzas, depositándolas en los orificios y colocando suavemente las raíces sobre el medio de cultivo. ]]>
Las esporas de G. clarum empleadas como inóculo fueron extraídas de un cultivo monoxénico de cuatro meses de edad por solubilización del medio SRM (utilizando una solución de ácido cítrico-0,1 M y citrato de sodio-0,1 M) y mantenidas en agua desionizada estéril (121°C, 15 min.), según la metodología descrita por Doner y Bécard (15).
Se inocularon alrededor de 50 esporas por plántula, con ayuda de una micropipeta Eppendorf (200 µL), en la vecindad de las raíces de papa y se establecieron 10 sistemas para cada medio de cultivo. Posteriormente, las placas fueron selladas con Parafilm (Pechiney, Plastic Packaging, Chicago, IL 60631) y el orificio fue cubierto con grasa de silicona (VWR International, Belgium) estéril (121°C, 15 minutos) para evitar contaminación. Las placas fueron cubiertas con bolsas de polietileno negro para mantener a los propágulos fúngicos y a las raíces en la oscuridad. Los sistemas fueron transferidos a cámara de crecimiento bajo condiciones controladas (22°C, 70 % de humedad relativa, fotoperiodo de 16 h.día-1 y flujo fotosintético de 225 µmol m-2 s-1) y mantenidos en posición vertical durante los 30 días de duración del ensayo.
Semanalmente, partiendo del día 15 de establecidos los sistemas, se añadieron en cada placa 5 mL de medio solidificado con 4 g.L-1 Gel GroTM sin azúcar ni vitaminas, refrescado en baño de agua hasta una temperatura aproximada de 40°C. Este suministro de medio fresco fue necesario debido a la rápida disminución del volumen de medio que ocurrió en las placas producto del activo crecimiento de las plantas.
Experimento 2. Efecto de la inoculación con esporas de G. clarum en plántulas de papa en el SA–PIV utilizando diferentes medios elaborados a partir de MS.
Se evaluó el comportamiento de la colonización micorrízica en diferentes medios de cultivo (A, B, E, F y G), elaborados a partir de variaciones en las concentraciones de P y N del medio MS (teniendo en cuenta los resultados del experimento anterior), cuyas características se presentan en la Tabla I y su composición en la Tabla II. Los medios SRM y ½MS fueron utilizados como controles.
]]> RESULTADOS
Experimento 1. Análisis cualitativo de las potencialidades de los medios MS, ½MS y SRM para el establecimiento del HMA Glomus clarum en plántulas de papa, utilizando un sistema autotrófico de cultivo parcialmente in vitro.
En este sistema las plantas de papa presentaron, de manera general, un comportamiento diferenciado dependiendo del medio de cultivo en el cual se desarrollaron, lo cual se aprecia en la Figura 2. Las plantas que crecieron en el medio de cultivo ½MS presentaron una mejor respuesta, exhibiendo tallos de mayor tamaño y vigor, mayores hojas y un profuso crecimiento del sistema radical, en comparación con el resto de las plantas, incluso con las desarrolladas en medio MS. Por tanto, en el medio MS no se presentó la conducta esperada, al mostrar las plantas un reducido crecimiento del sistema aéreo y radical, materializado en hojas pequeñas y tallos más delgados, así como un escaso número de raíces.

En el medio SRM las plantas mostraron un crecimiento atrofiado y poco armónico, caracterizado por hojas pequeñas, dispuestas prácticamente paralelas a los tallos, que se revelaron delgados y poco vigorosos, mostrando ambos un cambio de coloración de verde a purpúreo. El sistema radical presentó un crecimiento adecuado aunque no tan intenso como en el medio ½MS.
El comportamiento fúngico, en relación con los diferentes medios de cultivo, no estuvo en correspondencia con el desarrollo de las plántulas de papa, de tal forma que en el medio SRM fue donde se observaron mayor número de esporas germinadas (≈ 70 %), así como también mayor número de puntos de contacto (aproximadamente el 50 % de las esporas germinadas) entre los tubos germinativos y las raíces, indicadores de acción colonizadora. En el caso del medio ½MS se observó germinación de algunas esporas (15-20 %) después de 20 días de cultivo y el contacto de los tubos germinativos con las raíces, no siendo así en el medio MS en el que no hubo germinación.
]]>
Experimento 2. Efecto de la inoculación con esporas de G. clarum en plántulas de papa en el SA–PIV utilizando diferentes medios elaborados a partir de MS.
Se obtuvo un efecto significativo de los tratamientos sobre el desarrollo de las plantas y de los propágulos fúngicos, apreciable a partir de los primeros siete días y hasta la conclusión del ensayo (40 días) (Figuras 3 y 4). El contenido nutricional de los medios influyó notablemente no solo sobre el crecimiento de las plantas, sino también sobre la germinación y el establecimiento micorrízico.

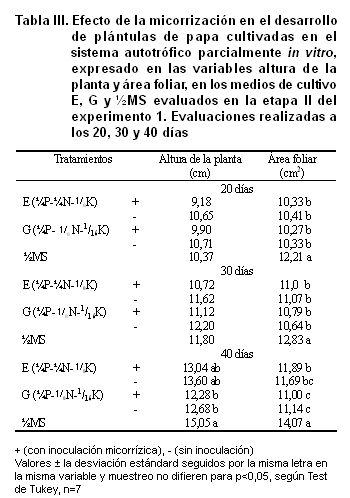
Los mayores valores de altura se alcanzaron en las plantas desarrolladas en los medios ½MS, E y G (Figura 4). Sin embargo, para el caso del área foliar y la masa seca aérea de las plantas, los mayores valores se encontraron en el medio ½MS, seguidas por las que crecieron en medio E y G, con una diferencia de casi el 50 % en el caso de la de la masa seca aérea. En los medios A, B y SRM se alcanzaron los valores más bajos de todas las variables, siendo la masa seca aérea y el área foliar 90 % y 45 % menores respectivamente, que en el medio ½MS.
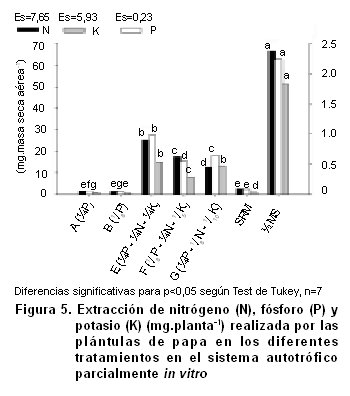
En cuanto a la extracción realizada de los elementos que sufrieron variación en la concentración (N, P y K), pudo observarse que las plantas que crecieron en el medio ½MS realizaron una extracción significativamente mayor de los tres nutrientes (>100 %), comparado con el resto de los tratamientos (Figura 5).
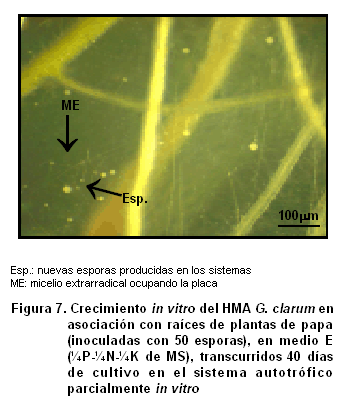
En cuanto al comportamiento fúngico se observó un patrón similar al encontrado en el ensayo anterior, en relación con la germinación de las esporas inoculadas, el desarrollo del micelio y la producción de nuevas esporas (Figura 7), reflejado en un crecimiento activo de las hifas dentro de los medios E y G a partir de los 30 días de inoculación, hasta abarcar toda la placa, con la producción de numerosas ERAs.
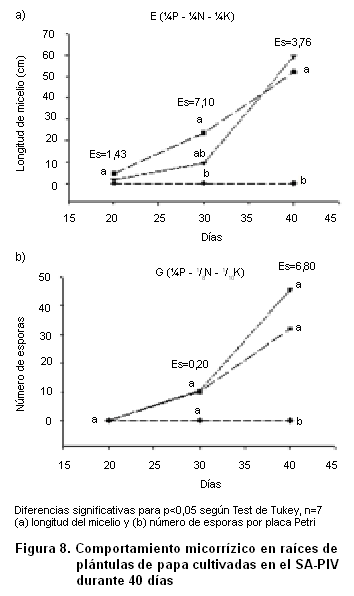
También puede apreciarse en la Figura 8 que a pesar de presentarse valores más altos de las variables en el medio E, al finalizar el ensayo, estos no fueron significativamente diferentes a los encontrados en el medio G; pero ambos sí superaron a los alcanzados en el medio ½MS, en el cual las esporas mantuvieron un comportamiento similar al del ensayo anterior, relacionado con la germinación y el crecimiento de los tubos germinativos.
DISCUSIÓN
Para lograr el éxito de la micorrización de plantas in vitro es necesario considerar tres aspectos fundamentales: los componentes del medio de cultivo, las condiciones en las cuales se desarrollan las plántulas y la fuente de inoculante utilizada; teniendo en cuenta que bajo estas condiciones, los componentes del medio de cultivo controlan la fisiología de la planta hospedera y consecuentemente influencian las relaciones con su cosimbionte micorrízico, así como también la concentración de nutrientes del medio de cultivo afecta la colonización de las plantas por parte de los propágulos fúngicos (23). Por tanto, la definición de los medios de cultivo adecuados para el desarrollo exitoso de ambos organismos es una de las etapas más críticas de este proceso y depende en gran medida de las especies utilizadas en cada caso; partiendo de los eventos de reconocimiento que condicionan el establecimiento de una simbiosis funcional entre el HMA y su planta hospedera (24, 25).
El cultivo in vitro de hongos micorrízicos arbusculares en asociación con cultivos de raíces se desarrolla usualmente en medios pobres en nutrientes, fundamentalmente fósforo, nitrógeno y sacarosa, para garantizar el establecimiento de los propágulos fúngicos (1, 3); sin embargo, los medios adecuados para la micropropagación de plantas se elaboran a partir de sus requerimientos nutricionales, por lo que poseen estos elementos en altas concentraciones. De ahí que definir un medio balanceado, que permita tanto el desarrollo de las plantas como de la asociación micorrízica arbuscular, constituye un factor clave para garantizar la micorrización de plantas in vitro.
]]>
Los resultados descritos en el segundo experimento reflejan cómo las variaciones de concentración estudiadas en el medio MS permitieron elaborar un medio en el cual se podían desarrollar de manera exitosa tanto los propágulos del hongo micorrízico arbuscular Glomus clarum como las plántulas de papa. Con el medio E (¼P-¼N-¼K con respecto a MS) se aseguró no solo el normal desarrollo de las estructuras fúngicas intra y extrarradicales, sino también la producción de plantas de papa micorrizadas in vitro con condiciones fisiológicas adecuadas, aunque sin satisfacer aún las expectativas, ya que al requerirse de un tiempo tan prolongado (30 días) para garantizar el establecimiento micorrízico, las plantas mostraban un crecimiento excesivo, al menos para ser utilizadas posteriormente con otros fines.
En el medio E, a diferencia del resto de los medios elaborados a partir de las modificaciones realizadas al medio MS, se mantuvo el balance normal de elementos que poseía el medio inicial MS. Esto pudo haber influido en que las plantas se comportaran mejor en este medio en comparación con F y G, en los que se encontraban desbalanceadas las concentraciones de estos elementos en mayor medida (1/8P-¼N-1/5K y ¼P-1/8N-1/10K, respectivamente). En el caso de los medios A (¼P) y B (1/8P), sus efectos sobre el desarrollo de las plantas fueron más drásticos, probablemente por presentar solamente reducciones de P.
El fósforo y el nitrógeno son dos de los nutrientes considerados dentro del grupo de los macronutrientes y además, componentes esenciales de las plantas para completar su ciclo de vida. Su deficiencia afecta numerosos procesos relacionados con el crecimiento y el desarrollo de las plantas, así como con el metabolismo.
Los medios de cultivo para la micropropagación de plantas in vitro usualmente contienen todos los minerales y vitaminas necesarios para el crecimiento y la diferenciación de las plantas y las concentraciones se encuentran en las proporciones adecuadas para que no existan interacciones entre ellos que dificulten su asimilación o funcionamiento y puedan ser utilizados en un número considerable de especies vegetales (26). Por tanto, un exceso o reducción en el medio de cultivo de alguno de estos elementos puede ocasionar dificultades en la absorción de otros, o impedir que estos tengan el efecto esperado.
El fósforo, por ejemplo, influencia o es influenciado por la disponibilidad o el uso de muchos otros elementos, ya sean o no esenciales (27), dentro de los que se destaca el nitrógeno y viceversa. Los conocimientos actuales reflejan el efecto sinérgico que se establece entre P y N cuando son aplicados al suelo conjuntamente, pero siempre debe existir un balance entre ellos.
]]>
En un estudio realizado en el que se suministraron diferentes dosis de P y N a plantas de tomate, se demostró (28) que la absorción de N y por tanto, su concentración en las plantas, disminuyó cuando estaban en presencia de concentraciones limitadas de fósforo.
La posible interacción entre P y K aun no está demostrada, pero según Adams (27), de existir, probablemente sea en el sistema de balance de aniones-cationes en el cual los ácidos orgánicos juegan un papel significativo.
Por otra parte, aunque la transferencia de nutrientes no es el único beneficio para los simbiontes sí representa ciertamente un factor de gran importancia en las interacciones micorrízicas (28), por lo que en estos medios (A, B) también se encontró un efecto negativo de su composición nutricional sobre los parámetros de germinación de esporas y por tanto de la colonización.
Estos resultados se correspondieron con los obtenidos por Bressan (29), quien encontró, utilizando diferentes medios de cultivo con variaciones en las concentraciones de P y N, que la adición de N al medio con reducidas concentraciones de P ocasionaba una disminución drástica de la germinación en esporas de G. etunicatum y aseguró que la interacción entre P y N afectó no solo la germinación de las esporas en mayor o menor medida, sino también el crecimiento de las raíces y la extensión de la colonización.
También en las plantas desarrolladas en los medios A, B y SRM, además del efecto reducido en el crecimiento se encontró un marcado cambio de coloración en las plantas. Estos síntomas coinciden con los descritos por Fernández et al. (6) en un estudio realizado en plántulas de papa en un sistema de cultivo totalmente in vitro. Según estos autores, la afección no parece estar relacionada con ninguna deficiencia nutricional simple, pues las variaciones de color observadas y el estado de las plantas no coinciden con ninguno de los síntomas provocados por el déficit individual de los elementos esenciales en el cultivo de la papa (30, 31). La marcada reducción del crecimiento y la delgadez de los tallos sí pudiera ser atribuido al desbalance ocasionado al reducir las concentraciones de P sin alterar el nitrógeno. Por otra parte, se señala que la deficiencia de fósforo en plantas de papa podría ocasionar crecimiento reducido, tallos delgados y oscurecimiento de las hojas (30, 32).
]]>
La micorrización de plantas de papa con esporas de G. clarum en el sistema parcialmente in vitro no produjo efectos sobre el crecimiento, durante los 40 días de duración del experimento. Esto podría estar relacionado con las condiciones artificiales de cultivo o simplemente a una baja dependencia micorrízica del cultivar.
La micorrización de plantas de papa ya había sido publicada anteriormente por Voets (12) utilizando el sistema autotrófico parcialmente in vitro. Si se comparan estos resultados con los presentados en el artículo, podrá notarse una gran diferencia en cuanto a producción de esporas y desarrollo del micelio obtenido. Estos autores informan una producción de 12 000 esporas de G. intrarradices (MUCL 43194) al cabo de 22 semanas de cultivo, comparable con la obtenida con la misma cepa y con dos cepas diferentes de la misma especie en asociación con raíces transformadas de zanahoria en medio SRM (33 y 34). Sin embargo, dichos autores no realizan ninguna valoración sobre el estado fisiológico de las plantas de papa después de transcurrir 22 semanas creciendo en este sistema y en el medio SRM (elaborado para el crecimiento de los HMA, el cual no garantiza el normal crecimiento y desarrollo de las plantas por presentar una drástica disminución de los macroelementos que lo componen). Por tanto, su propuesta resultó muy adecuada para la producción de estructuras fúngicas en presencia de plantas de papa in vitro, pero no para producir plantas micorrizadas que posteriormente pudiesen ser utilizadas con otros fines. La gran variabilidad observada entre este experimento y el desarrollado por Voets (12), en cuanto al comportamiento de los simbiontes, es el resultado de la estrecha interacción que existe entre los hongos micorrízicos, su hospedero y el medio en el cual ambos se desarrollan (25).
CONCLUSIONES
La investigación realizada permitió demostrar que las concentraciones y las proporciones de fósforo, nitrógeno y potasio del medio MS son un factor importante a tener en cuenta a la hora de diseñar medios de cultivo que permitan la micorrización acelerada de plantas en un Sistema Autotrófico Parcialmente in vitro.
Como resultado del estudio se obtuvo un medio de cultivo (E) que, a diferencia del resto de los medios evaluados, favoreció tanto el desarrollo de las plántulas de S. tuberosum cv. Desiré, como el establecimiento de la colonización micorrízica a partir de esporas de G. clarum. Hasta el momento ningún estudio anterior había tenido en cuenta los requerimientos nutricionales del cultivo utilizado, pues solamente estaban enfocados en la producción masiva de inóculo, obviando las necesidades de las plantas. Tener en cuenta estos aspectos en estudios posteriores permitirá estandarizar este y otros medios, así como mejorar los sistemas de cultivo ya existentes con el fin de producir plantas micorrizadas de forma rápida, que al ser trasplantadas reproduzcan la colonia fúngica y se beneficien con la asociación en una etapa tan crítica para las plantas micropropagadas como es la de adaptación.
REFERENCIAS
]]> 1. Bressan, W. Factors affecting in vitro plant development and root colonization of sweet potato by Glomus etunicatum Becker & Gerd. Brazilian Journal of Microbiology, 2002, vol. 33, p. 31-34.
2. Bécard, G. y Fortin, J. A. Early events of vesicular-arbuscular mycorrhiza formation on Ri T-DNA transformed roots. New Phytol., 1988, vol. 108, p. 211-218.
3. Bécard, G. y Piché, Y. Establishment of vesicular–arbuscular mycorrhiza in root organ culture: review and proposed methodology. In: Techniques for the study of mycorrhiza. Norris, J.; Read, D. y Varma, A. New York. Academic Press, 1992, p. 89-108.
4. Elmeskaoui, A.; Damont, J.-J. P. y Piché, Y. A culture system for endomycorrhizal inoculation of micropropagated strawberry plantlets in vitro. Mycorrhiza, 1995, vol. 5, p. 313-319.
5. Bressan, W.; De Carvalho, C. H. y Sylvia, D. M. Inoculation of somatic embryos of sweet potato with an arbuscular mycorrhizal fungus improves embryo survival and plantlet formation. Canadian Journal of Microbiology. 2000, vol. 46, no. 8, p. 741-743.
]]>
6. Fernández, K.; Fernández, F.; Rivera, R. y Olalde, V. Micorrización in vitro e in vivo de plántulas de papa (Solanum tuberosum var. Alfa). Cultivos Tropicales, 2010, vol. 31, p. 21-31.
7. Bago, B.; Vierheilig, H.; Piché, Y. y Azcón-Aguilar, C. Nitrate depletion and pH changes induced by extraradical mycelium of the arbuscular mycorrhizal fungus Glomus intraradices grown in monoxenic culture. New Phytol., 1996, vol. 133, p. 273-280.
8. Pawloska, T. E.; Douds, D. D. y Charvat, I. In vitro propagation and life cycle of the arbuscular mycorrhizal fungus Glomus etunicatum. Mycol. Res., 1999, vol. 103, p. 1549-1556.
9. Dupré de Boulois, H.; Voets, L.; Delvaux, B.; Jakobsen, Y. y Declerck, S. Transport of radiocaesium by arbuscular mycorrhizal fungi to Medicago truncatula under in vitro conditions. Environmental Microbiology, 2006, vol. 11, p. 1926-1934.
10. Murashige, T. y Skoog, F. A revised medium for rapid growth and bioassays with tobacco tissue cultures. Physiol. Plant., 1962, vol. 15, p. 473-497.
]]>
11. Declerck, S.; Strullu, D. G. y Plenchette, C. Monoxenic culture of the intraradical forms of Glomus sp. Isolated from a tropical ecosystem: a proposed methodology for germplasm collection. Mycologia, 1998, vol. 90, p. 579-585.
12. Voets, L.; Dupré de Boulois, H.; Renard, L.; Strullu, D. G. y Declerck, S. Development of an autotrophic culture system for the in vitro mycorrhization of potato plantlets. FEMS Microbiology Letters, 2005, vol. 248, p. 111-118.
13. Strullu, D. G. y Romand, C. Méthode d’obtention d’endomycorhizes à vésicules et arbuscules en conditions axéniques. Comptes Rendus de l’Académie Des Sciences Paris, 1986, vol. 303, p. 245-250.
14. Cranenbrouck, S.; Voets, L.; Bivort, C.; Renard, L.; Stullu, D. G. y Declerck, S. Methodologies for in vitro cultivation of arbuscular mycorrhizal fungi with root organs. In: In vitro culture of mycorrhizas. Springer, Berlin, 2005, p. 341-348.
15. Doner, L. W. y Bécard, G. Solubilization of gellan gels by chelation of cations. Biotechnology Techniques, 1991, vol. 1, p. 25-28.
]]>
16. Torres, W. y García, D. Estimación del área foliar en plantas de papa (Solanum tuberosum L.). Cultivos Tropicales, 1987, vol. 9, no. 1, p. 66-70.
17. Paneque, V. M. Análisis de suelo y planta. La Habana. Ediciones_INCA. 2002. 160 p. ISBN: 968-959-7023-51-7.
18. Newman, E. I. A method of stimating the total length of root in a sample. J. Appl. Ecol., 1966, vol. 3, p. 136-145.
19. Giovanetti, M. y Mosse, B. An evaluation of techniques to measure vesicular-arbuscular infection in roots. New Phytologist, 1980, vol. 84, p. 489-500.
20. Vierheilig, H.; Coughlan, A. P.; Wyss, U. y Piché Y. Ink and vinegar, a simple staining technique for arbuscular-mycorrhizal fungi. Applied and Environnemental Microbiology, 1998, vol. 64, p. 5004-5007.
]]>
21. Plenchette, C. y Morel, C. External phosphorus requirements of mycorrhizal and non-mycorrhizal barley and soybean plants. Biology and Fertility of Soils, 1996, vol. 21, p. 303-308.
22. StatSoft Inc. Statistica® Release 6. StatSoft Inc, Tulsa. 2001.
23. Cano, C.; Dickson, S.; González-Guerrero, S. y Bago, A. In vitro cultures open new prospects for basic research in arbuscular mycorrhizas. En: Mycorrhiza. State of the art, Genetics and molecular biology, Eco-Function, Biotechnology, Eco-Physiology, Structure and Systematics. Ed.: Varma, A. Springer-Verlag, Berlin Heidelberg. 2008, p. 627-654.
24. Mohammadi, G. E.; Rezaee, D. Y.; Prasad, R. y Varma, A. Mycorrhizal fungi: What we know and what should we know? In: Mycorrhiza. State of the art, Genetics and molecular biology, Eco-Function, Biotechnology, Eco-Physiology, Structure and Systematics. Ed.: Varma, A. Springer-Verlag Berlin Heidelberg. 2008, p. 3-28.
25. IJdo, M.; Cranenbrouck, S. y Declerck, S. Methods for large-scale production of AM fungi: past, present and future. Mycorrhiza DOI 10.1007/s00572-010-0337-z. 2010.
]]>
26. Cassells, A. C. y Gahan, P. B. Plant Tissue Culture Dictionary. 2006, p. 265.
27. Adams, F. Interactions of phosphorus with other elements in soils and in plants. In: The role of phosphorus in agriculture. Khazawneh, F. E.; Sample, E. C.; Kamprath, E. J. (Eds.) American Society of Agronomy. Madison, Wisconsin, EUA. p. 655-680.
28. Hause, B. y Fester, T. Molecular and cell biology of arbuscular mycorrhizal symbiosis. Planta, 2005, vol. 221, p. 184-196.
29. Bressan, W. The interactive effect of phosphorus and nitrogen on in vitro spore germination of Glomus etunicatum Becker & Gerdemann, root growth and mycorrhizal colonization. Brazilian Journal of Microbiology, 2001, vol. 32, p. 276-280.
30. Wallace, T. Las deficiencias minerales en las plantas: su diagnóstico a través de los síntomas visuales. Barcelona: Editorial Ariel, 1970, p. 169.
]]>
31. Westermann, D. T. Nutritional requirements of potatoes. American Journal of Potato Research, 2005, p. 11-19.
32. Van der Zagg, D. E.; Asscheman, E. y Brinkman, H. Potato diseases. The Netherlands: NIVAA, 1996, 179 p. ISBN 90-802036-2-9.
33. Declerck, S.; D´Or, D.; Cranenbrouck, S. y Le Boulengé, E. Modelling the sporulation dynamics of arbuscular mycorrhizal fungi in monoxenic culture. Mycorrhiza, 2001, vol. 11, p. 225-230.
34. De la Providencia, E. I.; de Souza, F. A.; Fernández, F.; Séjalon Delmas, N. y Declerck, S. Arbuscular mycorrhizal fungi reveal distinct patterns of anastomosis formation and hyphal healing mechanisms between different phylogenic groups. New Phytol., 2005, vol. 165, p. 261-271.
]]> Recibido: 22 de febrero de 2011
Dra.C. Kalyanne Fernández Suárez, Investigador Agregado del departamento de Biofertilizantes y Nutrición de las Plantas, Instituto Nacional de Ciencias Agrícolas, gaveta postal 1, San José de las Lajas, Mayabeque, CP 32 700, Cuba. Email:kalyanne@inca.edu.cu
]]>