
Caracterization of rizobia isolates from soybean nodules (Glycine max (L.) Merril) with potenciality to promote
the plant growth
Ionel Hernández Forte, Dra.C. María C. Nápoles García, Belkis Morales Mena
Instituto Nacional de Ciencias Agrícolas (INCA), gaveta postal 1, San José de las Lajas. Mayabeque, CP 32700, Cuba.
]]>
RESUMEN
El objetivo del presente trabajo fue caracterizar cuatro aislados de rizobios y la cepa Bradyrhizobium elkanii ICA 8001 provenientes de nódulos de plantas de soya, en cuanto a su capacidad para exhibir tres atributos positivos que caracterizan estas rizobacterias promotoras del crecimiento vegetal. Se determinó su capacidad de producir sideróforos; AIA (ácido 3-indolacético) y la actividad específica de la enzima 1-aminociclopropano-1-ácido carboxílico (ACC) desaminasa. Solo el aislado S11 produjo sideróforos en el medio de cultivo. Aunque todos los aislados y la cepa produjeron AIA, S11 produjo las mayores concentraciones de esta fitohormona. Todos los aislados, excepto S11, mostraron actividad de la enzima ACC desaminasa cuando se cultivaron en presencia del precursor 1-aminociclopropano-1-ácido carboxílico. La caracterización realizada permitió conocer atributos beneficiosos que brindan ventajas en la competitividad de estas bacterias en la rizosfera del cultivo, los que en conjunto con su capacidad de realizar la Fijación Biológica del Nitrógeno (FBN), pudieran incrementar el crecimiento de plantas de soya.
Palabras clave: sideróforos, Rhizobium, rizobacterias.
ABSTRACT
The objective of this work was to characterize four rhizobia and isolated from soybean nodules about three positive attributes which characterize these promoting growth plant rizobacterias. The siderophores and indol acetic acid (AIA) production and the specific activity of 1-aminocyclopropane-1-carboxylate (ACC) desaminase enzyme, were determinated. Siderophore was produced only by S11 isolated. All bacterial isolates and the strain produced IAA, but S11 produced the highest concentrations. All isolates, except S11, showed ACC deaminase enzyme activity when they were cultivated with the ACC precursor. The characterization allowed to know beneficial attributes, which represent advantages in the competitiveness of these bacterias in the crop rhizosphere, which together with their ability to perform the biological nitrogen fixation, could promote soybean plants growth.
Key words: siderophores, Rhizobium, rhizobacteria.
INTRODUCCIÓN
]]> Las bacterias promotoras del crecimiento vegetal PGPB, por sus siglas en inglés, se asocian a muchas especies de plantas presentes en la mayoría de los ecosistemas (1). Este grupo bacteriano tiene la capacidad de aumentar la disponibilidad de nutrientes, transformarlos a formas asimilables por la planta, producir sustancias promotoras del crecimiento fitohormonas o servir como control biológico de fitopatógeno denominándose entonces de biocontrol-PGPB (2). Dentro del primero de estos grupos bacterianos se encuentran los rizobios, microorganismos que se asocian simbióticamente con las leguminosas, alojándose en el interior de estructuras especializadas denominadas nódulos. Estos órganos constituyen el hábitat propicio donde se realiza la Fijación Biológica de Nitrógeno (FBN) (3).
MATERIALES Y MÉTODOS
El estudio se realizó en el Departamento de Biología de la Universidad de Waterloo, Canadá y en el Departamento de Fisiología y Bioquímica Vegetal, del Instituto Nacional de Ciencias Agrícolas (INCA), Cuba.
Material microbiano
Se emplearon cuatro aislados de rizobios S1, S10, S11, Snb y la cepa Bradyrhizobium elkanii ICA 8001 (10). Todos estos microorganismos provienen de nódulos de plantas de soya (Glyxine max) y actualmente pertenecen al cepario del Laboratorio de Bacteriología, del Departamento de Fisiología y Bioquímica Vegetal del INCA. Según estudios anteriores, donde se aplicaron los métodos convencionales de identificación de rizobios velocidad de multiplicación y producción de ácido-base, S11 pertenece al género Rhizobium y el resto de los aislados al género BradyrhizobiumA.
Se realizaron tres ensayos, donde se determinó la producción de sideróforos, la producción de metabolitos del tipo AIA y la actividad de la enzima ACC desaminasa. Se prepararon cultivos de los diferentes aislados bacterianos en Erlenmeyers de 25 mL de volumen, conteniendo 5 mL de medio líquido Manitol Extracto de Levadura YEM, por sus siglas en inglés (11). Los medios se inocularon con una asada de cada aislado de rizobio previamente conservados a 4 oC en tubos de ensayo en el mismo medio de cultivo sólido. Los cultivos líquidos se incubaron a 30 oC, en condiciones de agitación a 150 r min-1 Optic ivimen system-Comecta durante 24 h para el aislado S11 y 72 h para el resto. En el caso específico de la determinación de producción de metabolitos del tipo AIA, los medios de cultivo se suplementaron con dos concentraciones de triptófano 200 y 500 µg mL-1 en el momento de su preparación. Como control del experimento se emplearon medios de cultivo sin triptófano. ]]>
Determinación de la producción de sideróforos
Se tomaron tres alícuotas de 10 µL de los cultivos bacterianos y se colocaron en placas Petri que contenían medio sólido Cromo Azurol Sulfonato CAS Agar (12). Las placas se incubaron WiseCube-Daihan-brand de tres a cinco días a 28 oC. Finalmente se evaluó la producción de sideróforos, a partir de la presencia de halos de coloración naranja formados alrededor del crecimiento microbiano (13). Alícuotas de 10 µL de medio de cultivo estéril se colocaron en placas con el medio CAS Agar, las que se utilizaron como control del experimento.
Producción de metabolitos del tipo ácido 3-indolacético (AIA)
Los cultivos bacterianos inducidos se centrifugaron a 8000 r min-1 y 4 oC durante 10 min Centrífuga 5804R, Eppendorf. Se añadió 1 mL de cada sobrenadante obtenido en 4 mL del reactivo de Salkowski (14) y se incubaron durante 20 minutos a temperatura ambiente. La producción de metabolitos del tipo AIA se detectó en espectrofotómetro Genesys 6, Thermospectronic a 535 nm. La concentración de AIA se determinó mediante una curva de calibración, con un rango de concentración de 10-400 µg mL-1 de AIA (SIGMA) y los resultados se expresaron en µg mL-1.
Determinación de la actividad de la enzimática ACC desaminasa ]]>
Los cultivos bacterianos se centrifugaron a 8000 r min-1 y 4 oC durante 10 min Centrífuga 5804R, Eppendorf. Para inducir la síntesis de la ACC desaminasa, los sedimentos celulares se lavaron dos veces con 5 mL del medio mínimo salino M9 estéril (15). Posteriormente se resuspendieron con 7,5 mL del mismo medio estéril suplementado con 0,05 Mol L-1 de 1-aminociclopropano-1-ácido carboxílico (ACC) (SIGMA), como única fuente de nitrógeno. Los aislados se cultivaron entonces a 150 r min-1 Optic ivimen system-Comecta y una temperatura de incubación que osciló entre los 28-30 oC, durante 24 horas para el aislado S11 y 72 h para el resto. Seguidamente, se determinó la actividad ACC desaminasa mediante la cuantificación de la producción de a-cetobutirato generado a partir del ACC (16).
Simultáneamente, para calcular la actividad específica de la enzima ACC desaminasa, se determinó la concentración de proteínas totales en el extracto bacteriano, según el método de Bradford (17). Se utilizó albúmina de suero bovino SIGMA como estándar para la curva de calibración, con un rango de concentración de 10-100 µg mL-1. La actividad específica de la enzima ACC desaminasa se expresó en µg de a-cetobutirato µg-1 proteína h-1.
Diseño y análisis estadístico
Los datos obtenidos de los ensayos donde se evaluó la producción de metabolitos del tipo AIA y la actividad de la enzima ACC desaminasa, se sometieron a la prueba de normalidad test de Bartlett y homogeneidad de varianza test de Kormogorov-Smirnov y se aplicó análisis de varianza de clasificación simple, utilizando el Test de comparación de medias de Tukey para p<0,05 para discriminar diferencias entre las medias (18). Los datos se graficaron utilizando el programa SigmaPlot 2001. En cada caso, incluyendo el ensayo de determinación de sideróforos, se realizaron cuatro réplicas por tratamiento.
RESULTADOS Y DISCUSIÓN ]]>
Producción de sideróforos por los aislados de rizobios
De los cuatro aislados de rizobios empleados en este estudio y la cepa B. elkanii ICA 8001, solo S11 tuvo la capacidad de producir sideróforos (Figura 1).

Se observaron halos de coloración naranja intensa alrededor de las colonias producidas por este aislado, a diferencia del resto de los microorganismos estudiados que no se multiplicaron en este medio. Este medio de cultivo, con una coloración azul al momento de su preparación, se torna naranja en aquellas zonas donde crecen microorganismos con la capacidad de producir sideróforos (13).
]]>
Similares resultados a los obtenidos en este ensayo fueron observados en estudios realizados con diez cepas del género Rhizobium, procedentes de garbanzo (Cicer arietinum), donde en seis de ellas se detectaron halos de coloración naranja con diámetros entre 1,0-2,22 mm (19).
El medio de cultivo Cromo Azurol Sulfonato es usualmente empleado para la determinación cualitativa de sideróforos, pues presenta muy bajas concentraciones de hierro (1 mM FeCl3.6H2O), condición esencial para que se induzca la síntesis de sideróforos en aquellos microorganismos con capacidad de producirlos (20). En tales condiciones, el Fe2+ presente en el interior de la célula microbiana, se disocia de las proteínas represoras que se encuentran unidas al ADN para impedir la síntesis de los sideróforos ante altas concentraciones de hierro. Las PGPR que producen sideróforos utilizan el complejo Fe3+-sideróforos para incorporar este metal al interior celular mediado por un receptor específico localizado en la membrana bacteriana. Este secuestro de hierro disminuye su disponibilidad en el medio para otros microorganismos carentes de este sistema y que en ocasiones son patógenos para las plantas (13).
Se conoce que los rizobios tienen la capacidad de producir diversos tipos de sideróforos; sin embargo, solo algunos de ellos han sido estructuralmente caracterizados. En bacterias del género Rhizobium en forma de vida libre en la rizosfera, se han detectado sideróforos del tipo hidroxamatos (21). Aun está por determinar cuáles son los mecanismos que utilizan los bacteroides en el interior del nódulo radicular para la incorporación del hierro, ya que se ha detectado que aproximadamente el 44 % del hierro presente en las plantas de soya se encuentra localizado en estas estructuras (22).
Se ha demostrado la importancia que tiene para los rizobios la captación de hierro en el proceso de FBN, que realizan en simbiosis con las plantas leguminosas. La nitrogenasa, metaloenzima esencial en este proceso y que constituye del 10-12 % del total de las proteínas de las células de rizobio, cataliza la reducción del nitrógeno molecular a amonio, por medio de reacciones redox dependientes de hierro. De manera indirecta también este metal contribuye a la FBN, ya que forma parte importante de los citocromos, moléculas esenciales en el proceso de respiración celular, a partir del cual se obtiene la energía necesaria para el proceso de fijación del nitrógeno (23). Evidencias del papel importante que juega la captación de hierro por los rizobios en simbiosis con las leguminosas, se muestran explícitamente en experimentos realizados con Sinorhizobium meliloti, donde se observó una disminución en la ocupación de los nódulos por las cepas mutantes con deficiencias en la síntesis de sideróforos, en comparación con las cepas salvajes (24).
Producción de metabolitos del tipo ácido 3-indolacético por los aislados de rizobios
]]>
Todos los aislados bacterianos y la cepa B. elkanii ICA 8001 produjeron AIA, aunque con diferencias en su concentración. Los valores de AIA obtenidos en los medios que fueron suplementados con triptófano, oscilaron aproximadamente entre 3 µg mL-1 (para S10) y 47 µg mL-1 para S11 (Figura 2). Estas concentraciones fueron inferiores a los encontrados en otros estudios realizados con diferentes cepas de rizobios, donde en las mismas condiciones de cultivo, las cantidades de esta fitohormona fueron de 126 µg mL-1 (25) y 142,5 µg mL-1 (26). El aislado S11 mostró la capacidad de producir las mayores concentraciones de AIA, de 29 y 45 µg mL-1 en los medios suplementados con 200 y 500 µg mL-1 de triptófano, respectivamente.
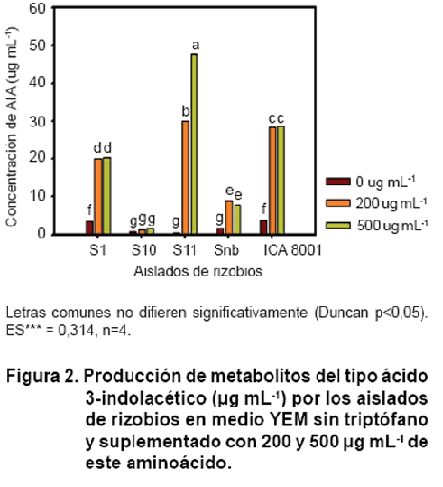
En los aislados de rizobios y la cepa B. elkanii ICA 8001, excepto S11, no se evidenció una relación directamente proporcional entre la concentración de triptófano y la concentración de AIA producida, ya que el aumento en la concentración de triptófano en el medio de cultivo no significó un incremento en la concentración de AIA. Desde el punto de vista bioquímico existen varias causas que pudieran dar explicación a este fenómeno, sobre todo los aspectos relacionados con las enzimas que participan en cada una de las vías metabólicas involucradas. Para esclarecer esto sería necesario realizar determinados análisis isoenzimáticos e incluso genéticos que permitan dilucidar la verdadera causa de este comportamiento en los diferentes microorganismos estudiados.
Para todos los microorganismos estudiados, con excepción del aislado S10 se observa una inducción en la síntesis de AIA cuando fueron cultivados en medios suplementados con triptófano. Este precursor se utiliza comúnmente para la inducción de la síntesis del AIA pues se conoce que la formación de esta fitohormona es producto de determinadas rutas metabólicas cuyo precursor es este aminoácido. Hasta el momento se han descrito cuatro vías dependientes de triptófano presentes en las rizobacterias: la del ácido indol-3-pirúvico (IPyA), la vía de la triptamina (TAM), del indol-3-acetonitrilo (IAN) y la vía de la indol-3-acetamida (IAM). Se ha descrito, fundamentalmente en plantas, una quinta vía de síntesis de AIA independiente de triptófano, en la que se presume que el precursor de la misma es el indol-3-glicerol fosfato (27). Los resultados en este trabajo indican que el aislado S10, aunque en concentraciones muy bajas, tuvo la capacidad de producir AIA en ausencia de triptófano.
Resultados similares se obtuvieron en investigaciones llevadas a cabo con aislados de rizobios nativos de suelos amazónicos en los que incrementos de las concentraciones de triptófano en el medio de cultivo no aumentaron la producción de AIA por estos aislados bacterianos (25).
Estudios realizados con determinadas cepas de Azospirillum, concluyen que la vía independiente de triptófano se convierte en la mayor fuente de AIA cuando las bacterias son crecidas en medios sin el precursor (28). Existen referencias en cepas de Streptomyces sp. y Flavobacterium sp., donde se ha comprobado que el amonio es el precursor de la síntesis de AIA, ya que en ausencia de esta molécula las cepas son incapaces de sintetizar esta auxina. Se presume que esto se deba a la competencia de esta molécula y el triptófano por los sitios activos de determinadas enzimas en el proceso biosintético del AIA (29). Tales resultados podrían sugerir la existencia de vías independientes del triptófano para la síntesis del AIA en el aislado S10. Los niveles moderados de AIA obtenidos en el aislado S1 y Snb y la cepa ICA 8001, crecidos en los medios sin triptófano, podrían también sustentar esta hipótesis. ]]>
Tal como se ha dicho, muchos estudios se han enfocado en la determinación cuantitativa de AIA producido por cepas de rizobios pertenecientes al género Rhizobium. Sin embargo, es en ejemplares del género Bradyrhizobium mayoría de los microorganismos aquí estudiados, donde más se ha estudiado el efecto de esta auxina en la tolerancia a determinados tipos de estrés abióticos y por tanto en el aumento de su sobrevivencia en la rizosfera (30).
El AIA también desempeña un papel importante en el proceso de FBN que tiene lugar entre las plantas leguminosas y los rizobios. A través de este proceso metabólico, la enzima nitrogenasa presente en estos microorganismos, cataliza la reducción del nitrógeno molecular a amonio. El amonio también se ha encontrado como uno de los precursores en la síntesis del AIA, pero muy pocos estudios se han realizado para esclarecer el papel de esta molécula. Se ha observado que cepas de Rhizobium no solo tienen la capacidad de producir AIA cuando se encuentran en vida libre en el suelo, sino también dentro de los nódulos de las plantas de soya como bacteroides, una vez establecida la simbiosis (31). Los rizobios dentro del nódulo radicular pudieran utilizar parte del NH+4, producto del proceso de FBN, para la síntesis de AIA.
Estudios realizados con cepas mutantes hiperproductoras de AIA de B. japonicum en el cultivo de la soya demostraron un incremento del volumen y número de los nódulos radicales efectivos en la FBN, trayendo consigo un efecto positivo en los rendimientos del cultivo (32). De manera similar, en investigaciones realizadas con plantas de soya el número de nódulos se redujo al inocular cepas con incapacidad para producir AIA (33).
La síntesis de fitohormonas como el AIA por microorganismos del suelo, que además tienen la capacidad de fijar el nitrógeno atmosférico, constituye un beneficio adicional que permite promover el crecimiento de los cultivos de leguminosas y con ello incrementar los rendimientos y la calidad de las cosechas.
Actividad de la enzima 1-aminociclopropano-1-carboxilato (ACC) desaminasa ]]>
Al analizar la actividad enzimática ACC desaminasa de los diferentes extractos bacterianos, todos los aislados, excepto S11, mostraron actividad de esta enzima cuando se cultivaron en presencia del inductor. Un comportamiento similar se evidenció cuando se observó un incremento significativo en la actividad de la enzima ACC desaminasa de los medios inducidos con respecto al control de estos aislados sin inducir (Figura 3).
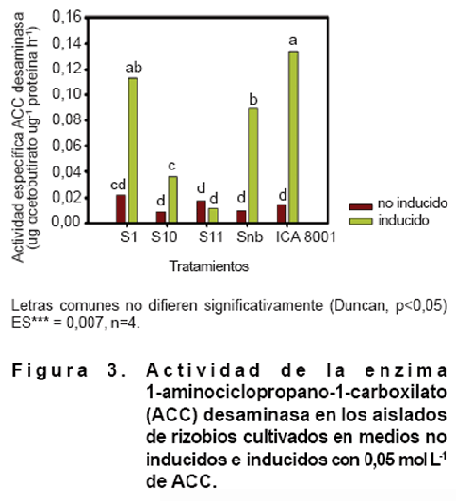
La actividad de la enzima ACC desaminasa en los aislados estudiados fluctuó entre 0,01 (S11) y 0,13 (ICA 8001) a-cetobutirato µg-1 proteína h-1. La presencia de la enzima ACC desaminasa en los rizobios ha sido ampliamente descrita en la literatura (9). Sin embargo, la actividad de esta enzima varía, incluso entre cepas del mismo género. Esto se debe a que la secuencia de nucleótidos que forman el gen acdS (que codifica para la ACC desaminasa) es muy variable entre géneros bacterianos, incluso entre especies del mismo género (34). Esto pudiera explicar las diferencias encontradas en los valores de actividad enzimática en los aislados S1, S10, Snb y la cepa ICA 8001, todos del género Bradyrhizobium.
Estudios filogenéticos sugieren que el gen acdS no siempre se localiza en el cromosoma microbiano, sino que también se ha detectado con cierta estabilidad en plásmidos bacterianos. Además se ha planteado que estos paquetes genómicos pueden transferirse horizontalmente, provocando la pérdida, en alguna medida, de la capacidad de sintetizar la enzima ACC desaminasa (35). Esto pudiera ser una posible explicación de los bajos niveles de actividad enzimática obtenidas en el aislado S11, aun en el medio suplementado con el inductor. En este sentido, se han utilizado técnicas de biología molecular con el objetivo de potenciar la producción de la ACC desaminasa en los rizobios y con ello crear cepas más competitivas en el proceso de nodulación (36). Esta tecnología pudiera utilizarse para la elaboración de inoculantes más efectivos para las leguminosas, que contribuyan positivamente a lograr mayores rendimientos agrícolas, teniendo en cuenta además, el papel de esta enzima en la disminución de los efectos adversos de determinados estreses bióticos y abióticos (34, 37).
La enzima ACC desaminasa degrada el ACC, precursor del etileno, en a-cetobutirato y amonio, metabolitos muy comunes en las plantas y otros organismos (38). Se conoce que la promoción del crecimiento vegetal se estimula no sólo por un decremento en el contenido de etileno, sino también por la generación de amonio a partir del ACC llevada a cabo por rizobacterias como los rizobios (35). Con esta estrategia las plantas disponen de una fuente extra de nitrógeno y los microorganismos asociados tienen una alternativa más para su supervivencia en la rizosfera. De esta manera, las PGPR con capacidad de producir la enzima ACC desaminasa, incrementan su proliferación en los sitios de colonización de las raíces y son favorecidas ante la competencia con otros microorganismos. En el caso particular de la interacción simbiótica rizobio-leguminosa, se ha observado que el etileno determina el sitio específico de la raíz donde se formará el primordio nodular, ya que mutantes de leguminosas insensibles a esta fitohormona presentan un mayor número de primordios nodulares que las plantas salvajes (39). De esta forma, el rizobio degrada el ACC exudado por la raíz, disminuyendo las concentraciones de etileno en la planta y con ello la disminución de sus efectos inhibitorios sobre la nodulación (9).
Para explicar el efecto promotor del crecimiento que realizan las PGPR en las plantas, se han identificado dos tipos de mecanismos, los indirectos o de biocontrol y los directos de promoción del crecimiento vegetal. El primero se caracteriza por la existencia de una actividad antagónica entre el microorganismo de interés con un fitopatógeno, provocando la disminución de los efectos dañinos de este último sobre la planta (40). La competencia por nutrientes, minerales y espacio, la detoxificación de factores de virulencia de los patógenos, la inducción de resistencia sistémica en la planta y la síntesis de metabolitos como los antibióticos y los sideróforos son algunos de estos mecanismos (41). Los mecanismos directos de promoción del crecimiento se evidencian en ausencia de otros microorganismos e incluyen además de la FBN, la producción de enzimas como la ACC desaminasa, la solubilización de minerales como el fósforo y la síntesis de fitohormonas como las giberelinas, citoquininas y el AIA (42). La clasificación anteriormente descrita solo ha servido para estudiar con un mayor nivel de profundidad cada uno de ellos, pues se conoce que la actividad promotora del crecimiento que realizan las PGPB como los rizobios, es el resultado de la acción de múltiples de estos mecanismos simultáneos. ]]>
Tanto los mecanismos directos como los indirectos pueden funcionar, además, potenciándose entre ellos y contribuyendo a la realización de procesos beneficiosos para la planta como la FBN. La captación de hierro por los rizobios a través de los sideróforos, favorece la síntesis de la nitrogenasa, así como de otras moléculas que participan en la generación de la energía necesaria para llevar a cabo la fijación. El amonio que se genera de este proceso, así como el obtenido de la degradación del ACC por la ACC desaminasa y el triptófano presente en las células radicales, pudieran utilizarse por los microorganismos para sintetizar el AIA, que de conjunto con el AIA producido por la planta, estimulan la proliferación y la elongación celular. El AIA, a su vez, induce la síntesis de la ACC sintasa, la cual cataliza la formación de ACC (43) y además estimula la producción de la ACC desaminasa (39), con lo cual varios procesos se interconectan favorablemente. Al aumentar la concentración de ACC en la raíz, ocurre su degradación por la ACC desaminasa producida por los rizobios, disminuyendo la concentración de etileno y favoreciendo una mayor cantidad de sitios para la proliferación nodular. De esta manera se pudiera pensar en un complejo diálogo molecular entre los rizobios y la planta leguminosa, desde su acercamiento y durante el establecimiento de la simbiosis, garantizando una mayor efectividad en el proceso de fijación del nitrógeno y en la promoción del crecimiento vegetal.
La caracterización realizada en este trabajo a cuatro aislados de rizobios y la cepa B. elkanii ICA 8001, obtenidos de nódulos de soya, permitió conocer que todos produjeron AIA, mientras que el aislado S11 fue el único con la capacidad de producir sideróforos y sin actividad de la enzima ACC desaminasa. Estos atributos positivos, presentes de manera particular en estas bacterias, ejercen diferentes efectos sensibles sobre la planta y constituyen a su vez ventajas en la competencia con otros microorganismos que también colonizan la rizosfera. El aporte de hormonas del crecimiento vegetal, la posibilidad de asimilar formas insolubles de nutrientes como el hierro y de tolerar estreses bióticos y abióticos, sin mencionar que participan indirectamente en procesos tan importantes como la FBN, son algunos beneficios directos derivados de esta contribución.
Estos resultados, junto a otros estudios de caracterización de estos aislados en su interacción con los cultivos, constituyen un aporte en la selección de cepas que pudieran tributar positivamente sobre la nutrición, protección y desarrollo de cultivos de interés.
CONCLUSIONES
Los cuatro aislados y la cepa B. elkanii ICA 8001, además de fijar nitrógeno, exhiben al menos dos de las características evaluadas: producción de AIA, sideróforos y actividad de la enzima ACC desaminasa; características que los hacen atractivos para su utilización como posibles biofertilizantes que ayuden a promover el crecimiento y rendimiento del cultivo de la soya.
]]> BIBLIOGRAFÍA
1. Martinez-Viveros, O.; Jorquera, M. A.; Crowley, D. E. /et al./. Mechanisms and practical considerations involved in plant growth promotion by rhizobacteria. J. Soil. Sci. Plant. Nutr., 2010, vol. 10, pp. 293-319. ISSN 1522-2624.
2. Bashan, Y. y Holguin, G. Proposal for the division of Plant Growth-Promoting Rhizobacteria into two classification: biocontrol-PGPB (Plant Growth-Promoting Bacteria) and PGPB. Soil Biol. Biochem., 1998, vol. 30, no. 8-9, pp. 1225-1228. ISSN 0038-0717.
3. Verma, J. P.; Yadav, J.; Tiwari, K. N. /et al./. Impact of plant growth promoting rhizobacteria on crop production. Int. J Agric. Res., 2010, vol. 5, no. 11, pp. 954-983. ISSN 0976-058X.
4. Bashan, Y. y de-Bashan, L. E. How the plant growth-promoting bacterium Azospirillum promotes plant growth-a critical assessment. Chapter two. Adv. Agron., 2010. vol. 108, pp. 77-136. ISSN 0065-2113.
5. Machado, R. G.; Saccol de Sá, E. L.; Bruxel, M.; Giongo, A.; da Silva Santos, N. y Schönhoffen, A. Indoleacetic acid producing rhizobia promote growth of Tanzania grass (Panicum maximum) and Pensacola grass (Paspalum saurae). Int. J. Agric. Biol., 2013, vol. 15, pp. 827-834. ISSN 15608530, 18149596.
6. Arif, K.; Archana, G. y Desai Anjana, J. Engineering heterologous iron siderophore complex utilization in rhizobia: Effect on growth of peanut and pigeon pea plants. Applied Soil Ecology, 2012, vol. 53, pp. 65-73. ISSN 0929-1393.
7. Maksimov, I. V.; Abizgildina, R. R. y Pusenkova, L. I. Plant growth promoting rhizobacteria as alternative to chemical crop protectors from pathogens (Review). Appl Biochem Microbiol., 2011, vol. 47, pp. 333-345. ISSN 1608-3024.
8. Takahashi, K.; Hayashi, K. I. y Kinoshita, T. Auxin activates the plasma membrane H+-ATPase by phosphorylation during hypocotyl elongation in Arabidopsis. Plant physiology, 2012, vol. 159, no. 2, pp. 632-641. ISSN 1532-2548.
9. Desbrosses, G.; Contesto, C. y Varoquaux, F. PGPR-Arabidopsis interactions is a useful system to study signalling pathways involved in plant developmental control. Plant Signal Behav., 2009, vol. 4, pp. 321-323. ISSN 1559-2324.
10. Nápoles, M. C.; Martínez, J.; Costales, D. /et al./. Avances en la reidentificación de la cepa ICA 8001 (Bradyrhizobium japonicum) como perteneciente a Bradyrhizobium elkanii. Revista Biología, 2006, vol. 20, no. 1-2, pp. 43-46. ISSN 1336-9563.
11. Vincent, J. M. A manual for the practical study of root-nodule bacteria /J. M. Vincent. En: International Programme Handbook. No. 15. Blackwele scientific publications, Oxford, England, 1970.
12. Verma, V.; Joshi, K. y Mazumdar, B. Study of Siderophore Formation in Nodule-Forming Bacterial Species. Research Journal of Chemical Sciences, 2012, vol. 2, no. 11, pp. 26-29. ISSN 2231-606X.
13. Aguado, G. A.; Moreno, B.; Jiménez, B. /et al./. Impacto de los sideróforos microbianos en la asimilación del hierro por las plantas: una síntesis. Rev. Fitotec. Mex., 2012, vol. 35, no. 1, pp. 9-21. ISSN 0187-7380.
14. Salkowski, E. Über das verhalten der skatolcarbonsäure im organismus. Physiol Chem., 1885, vol. 9, pp. 23-33. DOI: 10.1515/bchm1.885.9.1.23.
15. Sambrook, J.; Fritsch, E. F. y Maniatis, T. Molecular Cloning. En: Crimi, M. y Cremonese, G. Molecular Biology. 2nd Ed. New York : Plainview: Cold Spring Harbor Lab. 1989. pp. 3-5.
16. Penrose, D. M. y Glick, B. R. Methods for isolating and characterizing ACC deaminase containing plant growth-promoting rhizobacteria. Physiol. Plant., 2003, vol. 118, pp. 10-15. ISSN 0031-9317.
17. Bradford, M. M. A Rapid and Sensitive Method for the Quantitation of Microgram Quantities of Protein Utilizing the Principle of Protein-Dye Binding. Anal. Biochem., 1976, vol. 72, pp. 248-254. ISSN 0003-2697.
18. Sigarroa, A. Biometría y Diseño Experimental. Primera parte. Editorial Pueblo y Educación. Ciudad de La Habana, Cuba, 1985. pp. 319-328.
19. Pooja, A. Molecular identification of root nodule bacteria from Cicer arietinum. Research Journal of Biotechnology, 2012, vol. 7, no. 1, pp. 73-79. ISSN 2278-4535.
20. Bhattacharya, A. Siderophore mediated metal uptake by Pseudomonas fluorescens and its comparison to iron (III) quelation. Cey. J. Sci. Bio. Sci., 2010, vol. 39, no. 2, pp. 147-155. ISSN 0069-2379.
21. Wright, W. H. Isolation and Identification of the Siderophore "Vicibactin" Produced by Rhizobium leguminosarum ATCC 14479. J. Sci. Bio. Sci., 2010, vol. 40, no. 1, pp. 157-160. DOI: 10.1007/s10534-013-9609-3.
22. Brear, E. M.; Day, D. A. y Smith, P. M. C. Iron: an essential micronutrient for the legume-rhizobium symbiosis. Front Plant Sci., 2013, vol. 4, no. 359, pp. 1-15. ISSN 1664-462X.
23. Kobayashi, T. y Nishizawa, N. K. Iron uptake, translocation, and regulation in higher plants. Annual review of plant biology, 2012, vol. 63, pp. 131-152. ISSN 1543-5008.
24. Battistoni, F.; Platero, R.; Noya, F. /et al./. Intracellular Fe content in?uences nodulation competitiveness of Sinorhizobium meliloti strains as inocula of alfalfa. Soil Biol. Biochem., 2002, vol. 34, pp. 593-597. ISSN 0038-0717.
25. Dubler, M. R.; Sacool da Sá, E. L.; Goulart, R. /et al./. Caracterización e influencia de rizobios aislados de alfalfa en la geminación y crecimiento de plántulas de arroz. Ciencia Rural, Santa María, 2011, vol. 41, no. 10, pp. 1738-1743. ISSN 0103-8478.
26. Kumar, P.; Saha, P.; Mayilraj, S. /et al./. Role of IAA metabolizing enzymes on production of IAA in root, nodule of Cajanus cajan and its PGP Rhizobium sp. Biocatalysis and Agricultural Biotechnology, 2013, vol. 2, no. 3, pp. 234-239. ISSN 1878-8181.
27. Patten, C. L.; Blakney, A. J. y Coulson, T. J. Activity, distribution and function of indole-3-acetic acid biosynthetic pathways in bacteria. Critical reviews in microbiology, 2013, vol. 39, no. 4, pp. 395-415. ISSN 1549-7828.
28. Princen, E.; Costacurta, A.; Michiels, K.; Vanserleyden, J. y Van Onckelen, H. Azospirillum basilence indile-3-acetic acid biosyntesis: evidence for a non-tryptophan dependent pathway. Mol Plant-Microb Interect, 1993, vol. 6, pp. 609-615. ISSN 0894-0282.
29. Merzaeva, O. V. y Shirokikh, I. G. The production of auxins by the endophytic bacteria of winter rye. Appilied Biochemistry and Microbiology, 2010, vol. 46, no. 1, pp. 44-50. ISSN 1608-3024.
30. Donati, A. J.; Lee, H. I.; Leveau, J. H. J. /et al./. Effects of Indole-3-Acetic Acid on the Transcriptional Activities and Stress Tolerance of Bradyrhizobium japonicum. PLoS ONE., 2013, vol. 8, no. 10, pp. 1-11. ISSN 1932-6203.
31. Kumar, P. G.; Saha, P.; Mayilraj, S. /et al./. Role of IAA metabolizing enzymes on production of IAA in root, nodule of Cajanus cajan and its PGP Rhizobium sp Original. Biocatalysis and Agricultural Biotechnology, 2013, no. 3, pp. 234-239. ISSN 1878-8181.
32. Kaneshiro, T. y Kwoleck, W. Stimulated nodulation of soybean by Rhizobium japonicum mutant (B-14075) that catabolizes the conversion of tryptophan to indol-3yl-acetic acid. Plant Sci., 1985, vol. 42, pp. 141-146. ISSN 0168-9452.
33. Fukuhara, H.; Minakawa, Y.; Akao, S. /et al./. The involvement of indole-3-acetic acid produced by Bradyrhizobium elkanii in nodule formation. Plant Cell Physiol., 1994, vol. 35, pp. 1261-1265. ISSN 471-9053.
34. Esquivel, R.; Gavilanes, M.; Cruz, R. /et al./. Importancia agrobiotecnológica de la enzima ACC desaminasa en rizobacterias, una revisión. Rev. Fitotec. Mex., 2013, vol. 36, no. 13, pp. 251-258. ISSN 0187-7380.
35. Glick, B. R; Todorovic, B.; Czarny, J. /et al./. Promotion of plant growth by bacterial ACC deaminase. Rev. Plant Sci., 2007, vol. 26, pp. 227-242. ISSN 0735-2689.
36. Conforte, V. P.; Echeverria, M.; Sánchez, C. /et al./. Engineered ACC deaminase-expressing free-living cells of Mesorhizobium loti show increased nodulation efficiency and competitiveness on Lotus spp. J. Gen. Appl. Microbiol, 2010, vol. 54, no. 4, pp. 331-338. ISSN 1349-8037.
37. Sharma, D.; Chauhan, S.; Kumar, G. /et al./. Cadmium stabilization by plant growth promotory fluorescent pseudomonas in combination with Indian mustard var. Kranti, South Asean. J. Exptl. Biol., 2012, vol. 3, no. 2, pp. 128-135. ISSN 1477-9129.
38. Glick, B. R. Modulation of plant ethylene levels by the bacterial enzyme ACC deaminase. FEMS Microbiol., 2005, vol. 251, pp. 1-7. ISSN 1465-2080.
39. Glick, B. Bacteria with ACC deaminase can promote plant growth and help to feed the world. Special Issue on Plant Growth Promotion, 2014, vol. 169, no. 1, pp. 30-39. ISSN 1435-8107.
40. Acebo, Y.; Hernández, A.; Rives, N. /et al./. Perspectivas del uso de bacterias rizosféricas en el control de Pyricularia grisea (CookeSacc.) en el cultivo del arroz (Oryza sativa L.). Rev Colomb Biotecnol, 2011, vol. 13, no. 1, pp. 16-22. ISSN 1909-8758.
41. Hernández, A.; Rives, N.; Acebo, Y. /et al./. Potencialidades de las bacterias diazotróficas asociativas en la promoción del crecimiento vegetal y el control de Pyricularia oryzae (Sacc.) en el cultivo del arroz (Oryza sativa L.). Rev. Protección Veg., 2014, vol. 29, no. 1, pp. 1-10. ISSN 2224-4697.
42. Hernández, A.; Heydrich, M.; Diallo, B. /et al./. Cell-free culture medium of Burkholderia cepacia improves seed germination and seedling growth in maize (Zea mays) and rice (Oryza sativa). Plant Growth Regul., 2010, vol. 60, pp. 191-197. ISSN 1573-5087.
43. Hontzeas, N. J.; Zoidakis, B. R.; Glick, M. M. /et al./. Expression and characterization of 1-aminocyclopropane-1-carboxylate deaminase from rhizobacterium Pseudomonas putida UW4: a key enzyme in bacterial plant growth promotion. Bioch. Biophys., 2004, vol. 1703, pp. 11-19. ISSN 0006-291X.
Recibido: 3 de abril de 2014 ]]> Aceptado: 28 de agosto de 2014
Ionel Hernández Forte, Instituto Nacional de Ciencias Agrícolas (INCA), gaveta postal 1, San José de las Lajas. Mayabeque, CP 32700, Cuba. Email: ionel@inca.edu.cu
]]>