Effect of inoculation density of somatic embryos for obtaining plantain FHIA-21 (AAAB) cultivars
Dra.C. Leyanis García-Águila,I Dr.C. Rafael Gómez-Kosky,I Dra.C. Yelenys Alvarado Capó,I M.Cs. Zoe Sarría Hernández,I M.Cs. Nilca Albany,II M.Cs. Jorge Vílchez,II M.Cs. Maritza Reyes Vega,I Blanca Pérez Pérez,I Alexis Rodríguez ConcepciónI
IInstituto de Biotecnología de las Plantas (IBP), Universidad Central Marta Abreu de Las Villas, carretera a Camajuaní km 5.5, Santa Clara, Villa Clara, CP 54 830, Cuba.
IIFacultad de Agronomía, Universidad del Zulia, AP 15205, Maracaibo, Estado de Zulia (4005ZU), República Bolivariana de Venezuela.
]]>
RESUMEN
La regeneración de plantas por embriogénesis somática en plátanos y bananos puede convertirse en una tecnología para la propagación a escala comercial, debido al elevado coeficiente de multiplicación de los embriones somáticos. Sin embargo, para lograr tasas superiores de germinación y conversión de plantas, es importante obtener embriones de calidad con un desarrollo morfológico sincrónico. Por tanto, el objetivo del trabajo fue determinar el efecto de la densidad de inoculación de embriones somáticos en la obtención de plántulas de plátano cv. FHIA-21 (AAAB). Para ello, se estudiaron cuatro tratamientos correspondientes a la inoculación de 0,2; 0,4; 0,6 y 0,8 gramos de masa fresca (gMF) de embriones en medio de cultivo líquido de maduración. A los 30 días, se evaluaron las características morfológicas e histológicas de los embriones y se transfirieron a un medio de cultivo semisólido de germinación. Los resultados mostraron una mejor sincronización en el desarrollo morfológico de los embriones somáticos cuando se cultivaron con 0,6 gMF, aspecto que se evidenció por la uniformidad de su longitud, formación de los meristemos caulinar y radical, así como la acumulación de sustancias de reserva. Estos embriones alcanzaron un mayor porcentaje de germinación y formación de plantas completas, con diferencias estadísticas respecto al resto de los tratamientos. Las plantas se caracterizaron por una mayor longitud del pseudotallo, más de dos hojas abiertas y mayor número de raíces. El presente estudio es fundamental para la propagación masiva de plátano cv. FHIA-21 por embriogénesis somática.
Palabras clave: embriogénesis somática, histología, maduración, morfología, sincronía.
ABSTRACT
Plant regeneration through somatic embryogenesis in plantain and banana may become a commercial propagation technology, due to the high multiplication coefficient of somatic embryos. However, it is important to get quality embryos with a synchronous morphological development to achieve higher rates of germination and plant conversion. Therefore, the aim of this study was to determine the effect of inoculation density of somatic embryos for obtaining plantain FHIA-21 (AAAB) cultivars. Then, four inoculation treatments were studied: 0,2; 0,4; 0,6 and 0,8 grams of fresh mass (gMF) of embryos on liquid culture medium of maturation. The morphological and histological characteristics of somatic embryos were evaluated after 30 days and transferred to a semisolid germination culture medium. Results showed a better synchronization in the morphological development of somatic embryos when cultured with 0,6 Gmf, which was evident by their length uniformity, the apical and root meristem formation, as well as the accumulation of reserve substances. Such embryos reached a higher percentage of germination and whole plant formation, with statistical differences compared to other treatments. These plants were characterized by a longer pseudostem, more than two open leaves and greater root number. This study is essential for the mass propagation of plantain cv. FHIA-21 by somatic embryogenesis.
Key words: somatic embryogenesis, histology, maturation, morphology, synchrony.
INTRODUCCIÓN
]]> La embriogénesis somática es un proceso mediante el cual las células somáticas se diferencian en embriones somáticos y conservan íntegramente el genotipo de la planta donante. Los métodos para la realización de este tipo de morfogénesis se han descrito en un gran número de especies de plantas, cada una con sus propias características (1).
MATERIALES Y MÉTODOS
Material vegetal
Los embriones somáticos se obtuvieron en medio de cultivo líquido, a partir de suspensiones celulares embriogénicas de plátano cv. FHIA-21 (AAAB), siguiendo el procedimiento descrito por otros autores (10). Se utilizó un medio de cultivo compuesto por el 100 % de las sales inorgánicas de Schenk e Hildebrandt (11), al que se adicionaron vitaminas de Murashige y Skoog (12) al 100 %, 0,5 mg L-1 de biotina, 100 mg L-1 de extracto de malta, 100 mg L-1 de L-glutamina, 230 mg L-1 de L-prolina, 10 mg L-1 de lactosa, 0,05 mg L-1 de zeatina, 100 mg L-1 de mio-inositol, 0,2 mg L-1 de ácido naftalenacético (ANA), 0,2 mg L-1 de isopenilaminopurina (2ip), 0,1 mg L-1 de Kinetina y 45 g L-1 de sacarosa. El pH se ajustó a 5,3 antes de la esterilización. Los embriones se encontraban en etapa globular y se caracterizaron por presentar una longitud entre 0,20 a 0,50 mm.
Efecto de la densidad de inoculación en la maduración de los embriones somáticos
Se estudiaron cuatro densidades de inoculación durante la fase de maduración de los embriones somáticos. Para ello, se adicionaron 0,2; 0,4; 0,6 y 0,8 gramos de masa fresca (gMF) de embriones en Erlenmeyers de 250 mL de capacidad, que contenían 30 mL de medio de cultivo líquido. El medio de cultivo estaba compuesto por el 100 % de las sales y vitaminas MS (12), 1,0 mg L-1 de biotina, 0,5 mg L-1 de 6-bencilaminopurina (6-BAP), 1,0 mg L-1 de ácido indol-3-acético (AIA) y 30 g L-1 de sacarosa. ]]>
Los Erlenmeyers se colocaron en agitador orbital (INFORS HT) a 90 rpm de velocidad de rotación, en condiciones de oscuridad total y 27±2,0 ºC. Se establecieron cinco repeticiones por cada tratamiento con un diseño experimental completamente aleatorizado. A los 30 días de cultivo, se evaluaron las características morfológicas e histológicas de los embriones somáticos en las cuatro densidades de inoculación. Posteriormente, se transfirieron a medio de cultivo semisólido de germinación propuesto por otros investigadores (13), el cual estaba compuesto por las sales y vitaminas MS, 0,5 mg L-1 de 6-BAP, 2,0 mg L-1 de AIA, 100 mg L-1 de mio-inositol, 0,01 mg L-1 de Biobrás-6 (análogo de brasinoesteroide procedente de la Facultad de Química de la Universidad de La Habana) y 30 g L-1 de sacarosa. En ambos medios de cultivo el pH fue ajustado a 5,8±0,01.
Morfología e histología de los embriones somáticos
Se realizó una descripción morfológica de los embriones somáticos, con el objetivo de identificar sus principales características, durante la fase de maduración. Las observaciones se efectuaron bajo un microscopio estereoscópico (OLYMPUS) (10x), así como la medición de su longitud (mm) a través de una escala micrométrica acoplada al ocular. Para facilitar la observación y medición de los embriones, se extrajeron, de cada tratamiento, 1,0 mL de medio de cultivo líquido que contenía los embriones somáticos. Las muestras se depositaron en vasos de precipitado (50 mL de capacidad) con 30 mL de una solución de Gelrite® (SIGMA) (2,5 g L-1) y agua desionizada. Posteriormente, las soluciones de los vasos de precipitado se vertieron en placas de Petri de 70 mm de diámetro y quedaron inmovilizados los embriones después de solidificada la solución. Los valores de las mediciones se agruparon en tres rangos de longitudes, de 1,0 a 3,0; de 3,1 a 5,0 y de 5,1 a 7,0 mm, para determinar su frecuencia de aparición en los diferentes tratamientos y con ello identificar la densidad de inoculación que aporta mayor sincronía al cultivo.
El análisis histológico se realizó con el objetivo de identificar estructuras anatómicas y bioquímicas, que confirmen el desarrollo de los embriones somáticos y su preparación para la germinación. Para ello, se extrajeron dos muestras de cada tratamiento y se colocaron los embriones somáticos en una solución de fijación que contenía formaldehído al 37 % (v/v), ácido acético al 100 % (v/v) y etanol al 70 % (v/v), en una proporción 5:5:90 durante 24 horas. Seguidamente, estos fueron deshidratados en un gradiente ascendente de etanol y embebidos en parafina. Se efectuaron cortes seriados de 10 µm de grosor con un micrótomo de rotación (Zeiss, Alemania), se fijaron en portaobjetos, se hidrataron y se realizó una tinción con safranina al 0,5 %. Las secciones histológicas de las muestras se examinaron en microscopio óptico (AXIOSKOP) (40x) y las imágenes fueron captadas con una cámara digital (OLYMPUS DP70) que se encontraba acoplada al microscopio.
Germinación de los embriones somáticos ]]>
Los embriones somáticos maduros, correspondientes a cada densidad de inoculación, se colocaron en frascos plásticos de cultivo (500 mL de capacidad total) sobre 50 mL de medio de cultivo semisólido de germinación. Los frascos se colocaron en cámara de crecimiento de luz artificial (tubos fluorescentes de luz blanca), con un fotoperiodo de 16 horas de luz a una densidad de flujo de fotones fotosintéticos (FFF) de 62-68 µmol m-2 s-1) y 27±2,0 ºC. Se establecieron ocho réplicas por cada densidad de inoculación, con 20 embriones somáticos cada una en un diseño experimental completamente aleatorizado.
Durante la fase de geminación de los embriones somáticos, se realizaron observaciones a los 10, 20 y 30 días de cultivo, con la ayuda de un microscopio estereoscópico (OLYMPUS) (10x); además, a los 30 días se cuantificó el número de embriones germinados y se expresaron los valores en porcentaje de germinación. Al mismo tiempo, se evaluaron las características morfológicas de las plantas, como la longitud del pseudotallo (cm) desde la base hasta la inserción de la primera hoja, el número de hojas abiertas y número de raíces. Posteriormente, las plantas fueron transferidas y mantenidas durante 30 días en medio de cultivo semisólido de elongación, previo a su traslado a condiciones ex vitro en casa de cultivo.
Análisis estadístico
Para el análisis estadístico se utilizó el paquete computacional SPSS (Statistical Package for the Social Sciences) versión 20 sobre Windows (14). A los datos experimentales se les comprobaron los supuestos de distribución normal y homogeneidad de varianza. La comparación de los valores medio se efectuó mediante la prueba de Kruskall Wallis, con un nivel de significación de 0,05 %.
RESULTADOS Y DISCUSIÓN
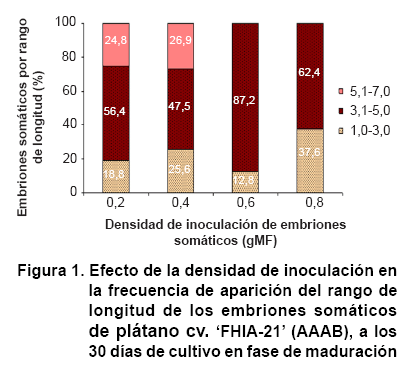
]]> Efecto de la densidad de inoculación en la maduración de los embriones somáticos A pesar del carácter asincrónico de los cultivos embriogénicos, la densidad de inoculación de 0,6 gMF proporcionó una mayor sincronía, porque logró mayor homogeneidad en la longitud de sus embriones somáticos, en relación con el resto de los tratamientos estudiados. El mayor porcentaje de estos embriones (87,2 %) se ubicó en uno de los rangos establecidos con una longitud de 3,1 a 5,0 mm (Figura 1).
Estos embriones se caracterizaron por presentar forma circular con una coloración amarillo pálido (Figura 2 D). Las secciones histológicas mostraron una epidermis regular de estos embriones, además de la presencia de los meristemos caulinar y radicular. También se observó en la región del escutelo la acumulación de estructuras de reservas (Figura 2 E, F, G).
]]>
Por otra parte, los embriones cultivados con 0,8 gMF de densidad de inoculación mostraron mayor frecuencia de aparición de embriones pequeños (37,6 %), entre 1,0 y 3,0 mm de longitud, aunque el 62,4 % de sus embriones se ubicó en el rango de longitud medio entre 3,1 y 5,0 mm (Figura 1). En este tratamiento se observaron daños sobre la epidermis de los embriones, dado posiblemente por la fricción entre ellos, debido a la alta densidad de inoculación (Figura 2 H). Además, se observó el oscurecimiento del medio de cultivo, lo cual pudo estar relacionado con la exudación de compuestos fenólicos y su posterior oxidación.
Las secciones histológicas de los embriones somáticos cultivados con 0,8 gMF evidenciaron la definición de la epidermis regular y la presencia de estructuras de reserva en el centro del embrión. Sin embargo, no se observaron los meristemos caulinar y radicular (Figura 2 I).
Germinación de los embriones somáticos
Durante la germinación de los embriones somáticos se observaron diferencias en su aspecto morfológico, relacionadas con la densidad de inoculación utilizada durante la fase de maduración. A los 10 días, los embriones cultivados con 0,6 gMF mostraron la emisión del ápice caulinar como pequeños brotes de color verde. Estos se elongaron con el aumento de los días de cultivo hasta la formación de plantas completas, las cuales se observaron a los 30 días de cultivo (Figura 3 A, B, C). El mayor porcentaje de germinación correspondió a estos embriones (62,0 %), con diferencias significativas con el resto de los tratamientos (Figura 4).
CONCLUSIONES
]]> Los resultados mostraron la influencia de la densidad de inoculación en el desarrollo morfológico de los embriones somáticos de plátano cv. FHIA-21 (AAAB). Los embriones que se cultivaron a 0,6 gMF presentaron una mayor uniformidad de su longitud, formación de los meristemos caulinar y radical, así como la acumulación de sustancias de reserva. Estos embriones alcanzaron mayor porcentaje de germinación y formación de plantas completas. El presente estudio es fundamental para la propagación in vitro de plátano cv. FHIA-21 a gran escala por embriogénesis somática.
AGRADECIMIENTOS
Los autores agradecen a la Dra.C. Novisel Veitía (IBP, Cuba), por su colaboración en el análisis estadístico de los datos. Esta investigación fue apoyada por el Ministerio de Ciencia, Tecnología y Medio Ambiente de Cuba, en el marco del proyecto Aplicación de la embriogénesis somática como una vía alternativa para la propagación masiva del cultivar de plátano vianda FHIA-21 (Musa AAAB).
BIBLIOGRAFÍA
1. von Arnold, S. Somatic embryogenesis [en línea]. En: eds. George E. F., Hall M. A., y Klerk G. J. D., Plant Propagation by Tissue Culture, edit. Springer Netherlands, Dordrecht, 2007, pp. 335-354, ISBN 978-1-4020-5004-6, [Consultado: 8 de diciembre de 2015], Disponible en: <http://link.springer.com/10.1007/978-1-4020-5005-3> .
2. Dai, X. M.; Xiao, W.; Huang, X.; Zhao, J. T.; Chen, Y. F. y Huang, X. L. Plant regeneration from embryogenic cell suspensions and protoplasts of dessert banana cv. Da Jiao (Musa paradisiacal ABB Linn.) via somatic embryogenesis. In Vitro Cellular & Developmental Biology - Plant, vol. 46, no. 5, 5 de octubre de 2010, pp. 403-410, ISSN 1054-5476, 1475-2689, DOI 10.1007/s11627-010-9314-7. ]]>
3. Uma, S.; Lakshmi, S.; Saraswathi, M. S.; Akbar, A. y Mustaffa, M. M. Plant regeneration through somatic embryogenesis from immature and mature zygotic embryos of Musa acuminata ssp. burmannica. In Vitro Cellular & Developmental Biology - Plant, vol. 48, no. 5, 13 de septiembre de 2012, pp. 539-545, ISSN 1054-5476, 1475-2689, DOI 10.1007/s11627-012-9462-z.
4. Meenakshi, S.; Shinde, B. N. y Suprasanna, P. Somatic embryogenesis from immature male flowers and molecular analysis of regenerated plants in banana Lal Kela(AAA). Journal of Fruit and Ornamental Plant Research, vol. 19, no. 2, 2011, pp. 1530, ISSN 1231-0948.
5. Deo, P. C.; Tyagi, A. P.; Taylor, M.; Harding, R. y Becker, D. Factors affecting somatic embryogenesis and transformation in modern plant breeding. The South Pacific Journal of Natural and Applied Sciences, vol. 28, no. 1, 1 de enero de 2010, pp. 27-40, ISSN 1013-9877, 1726-0787, DOI 10.1071/SP10002.
6. Monteiro, T. R.; Luis, Z. G.; Freitas, E. de O.; Matsumoto, K. y Scherwinski, P. J. E. Cell differentiation and plant regulators on banana. Revista Brasileira de Fruticultura, vol. 33, no. SPE1, octubre de 2011, pp. 213-221, ISSN 0100-2945, DOI 10.1590/S0100-29452011000500025.
7. Korneva, S.; Flores, J.; Santos, E.; Piña, F. y Mendoza, J. Plant regeneration of plantain Barraganete from somatic embryos using a temporary immersion system. Biotecnología Aplicada, vol. 30, no. 4, 2013, pp. 267270, ISSN 0864-4551, 1027-2852.
8. Ducos, J. P.; Lambot, C. y Pétiard, V. Bioreactors for coffee mass propagation by somatic embryogenesis. International Journal of Plant Developmental Biology, vol. 1, no. 1, 2007, pp. 112, ISSN 1749-4753.
9. Jalil, M.; Chee, W. W.; Othman, R. Y. y Khalid, N. Morphohistological examination on somatic embryogenesis of Musa acuminata cv. Mas (AA). Scientia Horticulturae, vol. 117, no. 4, 18 de agosto de 2008, pp. 335-340, ISSN 0304-4238, DOI 10.1016/j.scienta.2008.05.018.
10.García, Á. L.; Gómez, K. R.; Alvarado, C. Y. y Reyes, Z. S. y M. Effect of inoculum density on formation and morphology of plantain somatic embryos (Musa spp. AAAB, cv. Hybrid FHIA-21). Revista Colombiana de Biotecnología, vol. 12, no. 2, diciembre de 2010, pp. 240-247, ISSN 0123-3475.
11. Schenk, R. U. y Hildebrandt, A. C. Medium and techniques for induction and growth of monocotyledoneous and dicotyledoneous plant cell cultures. Canadian Journal of Botany, vol. 50, no. 1, 1 de enero de 1972, pp. 199-204, ISSN 0008-4026, DOI 10.1139/b72-026.
12. Murashige, T. y Skoog, F. A Revised Medium for Rapid Growth and Bio Assays with Tobacco Tissue Cultures. Physiologia Plantarum, vol. 15, no. 3, 1 de julio de 1962, pp. 473-497, ISSN 1399-3054, DOI 10.1111/j.1399-3054.1962.tb08052.x. ]]>
13. Kosky, R.; Gilliard, T.; Barranco, L. y Reyes, M. Embriogénesis somática en medios líquidos. Maduración y aumento de la germinación en el cultivar híbrido «FHIA-18» (AAAB). InfoMusa, vol. 9, no. 1, 2000, pp. 12-16, ISSN 1023-0076.
14. IBM SPSS Statistics [en línea]. Versión 20, [Windows], edit. IBM Corporation, U.S, 2011, Disponible en: <http://www.ibm.com>.
15. Cabrera, M.; López, J.; Kosky, R.; Montano, N.; Reyes, M.; Reinaldo, D.; Ventura, J. C.; Medero, V.; Santos, A.; García, M.; Basail, M. y Espinosa, E. Multiplicación, histo-diferenciación y regeneración de suspensiones celulares embriogénicas en plátanos vianda «Navolean» (AAB). Biotecnología Vegetal, vol. 2, no. 2, 2002, pp. 115-117, ISSN 2074-8647.
16. Ramírez, V. M. y de García, E. Características marcadoras en suspensiones celulares embriogénicas de banano cien bta-03 (AAAA) y su parental williams (AAA). Bioagro, vol. 24, no. 2, agosto de 2012, pp. 73-82, ISSN 1316-3361.
17. Remakanthan, A.; Menon, T. G. y Soniya, E. V. Somatic embryogenesis in banana (Musa acuminata AAA cv. Grand Naine): effect of explant and culture conditions. In Vitro Cellular & Developmental Biology - Plant, vol. 50, no. 1, 13 de agosto de 2013, pp. 127-136, ISSN 1054-5476, 1475-2689, DOI 10.1007/s11627-013-9546-4. ]]>
18. Gupta, P. K. y Timmis, R. Mass propagation of conifer trees in liquid cultures progress towards commercialization [en línea]. En: eds. Hvoslef E. A. K. y Preil W., Liquid Culture Systems for in vitro Plant Propagation, edit. Springer Netherlands, 2005, pp. 389-402, ISBN 978-1-4020-3199-1, [Consultado: 10 de diciembre de 2015], Disponible en: <http://link.springer.com/chapter/10.1007/1-4020-3200-5_30> .
19. Youssef, M.; James, A.; Mayo, M. A.; Ku, C. J. R.; Grijalva, A. R. y Escobedo, G. R. M. Influence of genotype and age of explant source on the capacity for somatic embryogenesis of two Cavendish banana cultivars (Musa acuminata Colla, AAA). African Journal of Biotechnology, vol. 9, no. 15, 2010, pp. 2216-2223, ISSN 1684-5315, DOI 10.4314/ajb.v9i15.
20. García, Á. L.; Alvarado, C. Y.; Kosky, R. G.; Sarría, Z.; Chong, P. B.; Reyes, M.; Pérez, B.; Concepción, A. y Mollineda, Á. Análisis del contenido de nutrientes minerales durante la formación y maduración de embriones somáticos deFHIA-21 (Musa AAAB). Biotecnología Vegetal, vol. 12, no. 1, 2012, pp. 33-40, ISSN 1609-1841, 2074-8647.
]]> Recibido: 7 de octubre de 2014
Dra.C. Leyanis García-Águila, Instituto de Biotecnología de las Plantas (IBP), Universidad Central Marta Abreu de Las Villas, carretera a Camajuaní km 5.5, Santa Clara, Villa Clara, CP 54 830, Cuba. Email: leyanis@ibp.co.cu
]]>