Lic. JUAN CARLOS VILASECA,1 Lic LILIANA PÉREZ,2 Lic CLARA SAVÓN,3 Lic. DANAY CHACÓN,4 Dra. SUSET OROPESA FERNÁNDEZ,5 Lic. HERMIS RODRÍGUEZ,6 Dr. ÁNGEL GOYENECHEA7 y Lic. ANSELMO OTERO8
Se purificó una inmunoglobulina G de ratón a partir de suero por cromatografía de afinidad en proteína A. Con esta preparación se inmunizaron los conejos cuyos sueros fueron capaces de reconocer al antígeno inyectado mediante inmunodifusión doble. Los anticuerpos fueron precipitados del suero de conejo y purificados mediante cromatografía de intercambio iónico. Esta preparación fue conjugada a isotiocianato de fluoresceína según la tecnología convencional. El conjugado obtenido fue evaluado con las cepas de referencia de virus Parainfluenza 1, 2, 3; Adenovirus; virus sincitial respiratorio y virus influenza A y B, por una técnica de inmunofluorescencia indirecta y muestras positivas de VIH mediante citometría de flujo. En ambos casos se utilizaron anticuerpos monoclonales específicos. Se evaluaron muestras clínicas de pacientes con infección respiratoria aguda.
Descriptores DeCS: IGG/aislamiento & purificación; CITOMETRIA DE FLUJO/métodos; TECNICA DEL ANTICUERPO FLUORESCENTE INDIRECTA/métodos; RATONES/sangre; CROMATOGRAFIA POR INTERCAMBIO IONICO; CROMATOGRAFIA DE AFINIDAD; PUNCIONES; PROTEINA ESTAFILOCOCICA A.
Las técnicas inmunoquímicas han contribuido considerablemente a la práctica, la investigación y el diagnóstico virológicos.1,2 Los métodos que utilizan la reacción específica de un anticuerpo con un antígeno para revelar la presencia de anticuerpos en el suero u otros fluidos corporales, o para identificar antígenos en los tejidos, las células y los microorganismos, difieren de acuerdo con los mecanismos mediante los cuales se revela esta interacción.3
Una de las herramientas empleadas es el marcaje de uno de los componentes, frecuentemente el anticuerpo, y su utilización como marcador topográfico. Los métodos con anticuerpos fluorescentes han mostrado su capacidad para la identificación de antígenos virales. Los conjugados con fluorocromos, al igual que los marcados con enzimas, brindan una rápida localización del sitio de la interacción antígeno-anticuerpo, donde uno de los componentes forma parte de la célula, el tejido u otra estructura biológica.4,5
El objetivo de nuestro trabajo fue la preparación de anticuerpos anti-IgG de ratón conjugados con isotiocianato de fluoreceína (FITC), su evaluación y aplicación en el diagnóstico virológico. Al contar con estos anticuerpos conjugados puede evitarse la preparación o adquisición frecuentemente costosa, de monoclonales conjugados.
Inmunización. Se purificó IgG de ratón mediante una columna empaquetada con una matriz de Proteína A- Sepharose, Pharmacia, en un tampón de aplicación que contenía NaCl 3 mol/L y glicina 1,5 mol/L.6 Los anticuerpos obtenidos en el pico de elución a pH 3 se cuantificaron espectrofotométricamente. Se inmunizaron conejos chinchilla (hembras jóvenes) con 100 mg de IgG de ratón, por vía subcutánea, se utilizó adyuvante completo de Freund. Se aplicaron repetidas inmunizaciones subcutáneas con el mismo inmunógeno en adyuvante incompleto de Freund hasta obtener un título de 1:32 por inmunodifusión doble.2
Obtención de la fracción IgG. Los anticuerpos fueron precipitados con (NH4)2SO4 al 50 % a partir de los antisueros de conejo y purificados por cromatografía de intercambio iónico en una columna de Q-Sepharose Fast Flow, Pharmacia, se utilizó solución tamponadora de fosfatos (PBS) a la mitad de su concentración habitual (1/2x).7 Las fracciones no unidas a la columna se dializaron contra tampón carbonato de sodio 0,2 mol/L pH 9,5 a 4 °C y se ajustó la concentración de proteínas a 20 mg/mL. La especificidad de los anticuerpos se comprobó mediante inmunodifusión doble.
CONJUGACIÓN
La conjugación se realizó según las técnicas convencionales.8 Brevemente, se disolvió 1 mg de FITC (isómero 1, BDH, No. Cat. 44041) en 1 mL de tampón carbonato de sodio 0,2 mol/L pH 9,5 y la solución resultante se añadió a 2,5 mL de la anti-IgG de ratón purificada, gota a gota a temperatura ambiente, con agitación suave y se dejó en reposo 24 h a 4 °C. La mezcla de conjugación se añadió a una columna empaquetada con Sephadex G-25 (Pharmacia), con la cual la fluoresceína interactúa específicamente,9 y se colectaron por goteo fracciones de 1 mL. Para esto se utilizó PBS. Se determinó la densidad óptica (DO) a 280 y 495 nm y se calculó la relación FITC/proteína (F/P) según la fórmula:
2,87 x DO495 F/P = ---------------------------- DO280 - 0,35 x DO495
Se agruparon las fracciones con valores de F/P entre 2 y 4.
EVALUACIÓN DEL CONJUGADO
Inmunofluorescencia indirecta (IFI). Se prepararon las láminas de inmunofluorescencia de 12 circunferencias con improntas de Adenovirus, virus sincitial respiratorio (VSR), Parainfluenza 1, 2 y 3 e influenza A y B, replicados in vitro y sus respectivos controles celulares. Se utilizaron los anticuerpos monoclonales comerciales específicos a dichos virus provenientes del juego comercial para la determinación de virus respiratorio por IFI (Chemicon International Inc., EE.UU.). Se ensayaron las diluciones en PBS del conjugado producido desde 1:2 hasta 1:128 y se utilizó el conjugado de referencia proveniente del mismo juego comercial, en su dosis de trabajo. Las pruebas se realizaron simultáneamente y se compararon los resultados.
Se estudiaron 47 casos clínicos con infecciones respiratorias agudas (26 exudados nasofaríngeos de niños y 21 gargarismos de adultos), se aplicaron por duplicado, mediante la metodología recomendada por los productores del juego diagnóstico de Chemicon International Inc. y se utilizaron el conjugado comercial y el que se evalúa en sus dosis de trabajo.
]]> Citometría de flujo. Se añadieron 20 mL de los anticuerpos monoclonales anti-CD3 (ior T3), anti-CD4 (ior T4) y anti-CD8 (ior T8) diluidos 150 veces, todos producidos en el Centro de Inmunología Molecular (La Habana, Cuba), a tubos para citometría de flujo que contenían 100 mL de sangre periférica de pacientes VIH positivos y se incubaron durante 20 min a temperatura ambiente. Posteriormente, se añadieron 20 mL del conjugado comercial (DAKO, F0313) y del conjugado que se proponía a evaluar, se ensayaron diluciones desde 1:20 hasta 1:160, y se incubaron bajo las mismas condiciones anteriores. Se añadieron 2 mL de solución de lisis (NH4CI 0,15 mol/L, EDTA tetrasodio 0,19 mmol/L, NaHCO3 0,012 mol/L) a cada tubo para lisar los eritrocitos de la sangre y evitar interferencias en la lectura. Se dejó en reposo 10 min y se procedió a la lectura en el citómetro de flujo (Johnson & Johnson, EE.UU.).Se determinó la dilución óptima de trabajo del conjugado que se iba a evaluar y del conjugado comercial, y se compararon con los resultados obtenidos al utilizar los anticuerpos monoclonales comerciales anti-CD3 (M0835, DAKO), anti-CD4 (M0716, DAKO) y anti-CD8 (M0707, DAKO).
Se realizó un análisis de correlación entre los valores de los conteos obtenidos con ambos conjugados para los 3 anticuerpos monoclonales de producción nacional, mediante el paquete estadístico Statgraphic.®
Cuando se observan los resultados de la IFI con las improntas de las cepas virales al utilizar los anticuerpos monoclonales específicos diluidos (juego comercial Chemicon International Inc. para diagnóstico por IFI, EE.UU.) y las distintas diluciones del conjugado que se iba a evaluar, encontramos que se obtuvieron 4 cruces de fluorescencia (4x) con la dilución 1:32, lo que coincide con los resultados que se obtuvieron al utilizar el conjugado comercial. Se obtuvo una adecuada especificidad reflejada al no encontrarse fluorescencia en los controles celulares.
Utilizando la misma metodología y en forma paralela se investigaron 47 casos clínicos representados por las principales muestras que se usan para el diagnóstico rápido de las IRA (exudados nasofaríngeos y gargarismos), de los cuales 10 (21,3 %) resultaron ser positivos tanto con el conjugado evaluado como por el juego comercial. En este caso se utilizó el conjugado evaluado en la dilución 1:20 para evitar la pérdida de casos positivos y el comercial en su dosis de trabajo (tabla 1).
TABLA 1. Casos de infecciones respiratorias agudas diagnosticadas por inmunofluorescencia indirecta
|
| Niños ]]> (n = 26) | Adultos (n = 21) | Totales ( n = 47) | ||
| IRA | CE | CC | CE | CC | ]]> Totales |
| Influenza A | 3 | 3 | 3 | 3 | 6 |
| VSR | 2 | 2 | ]]> - | - | 2 |
| Adenovirus | 1 | 1 | - | - | 1 |
| Para influenza 3 | ]]> 1 | 1 | - | - | 1 |
| Total | 7 | 7 | 3 | 3 | ]]> 10 |
| % | (26,9 %) | (26,9 %) | (14,3 %) | (14,3 %) | (21,3 %) |
CE: Conjugado evaluado. CC: Conjugado comercial.
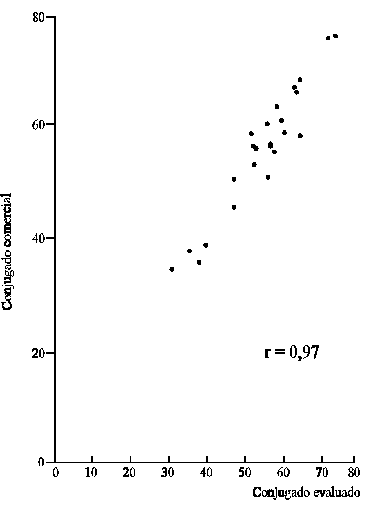
Para la citometría de flujo, se determinó que la dilución óptima de trabajo del conjugado que se iba a evaluar era de 1:160 y del conjugado comercial 1:20 al comparar estos resultados con los obtenidos con los anticuerpos monoclonales comerciales, con los cuales los conteos fueron de 78,5; 58,1 y 25,1 %, respectivamente (tabla 2). Se realizó la correlación de los conteos de células CD3, CD4 y CD8 en sangre periférica de pacientes VIH+, se utilizaron un conjugado comercial y el conjugado titulado (figura), ésta fue 0,97.
]]> TABLA 2. Conteos de células CD3, CD4 y CD8 (%) con diferentes diluciones del conjugado evaluado y del comercial mediante citometría de flujo
|
| CE | CC | ||||
| Diluciones | Ior T3 | Ior T4 | Ior T8 | ]]> Ior T3 | Ior T4 | Ior T8 |
| 1:20 | 80,6 | 54,0 | 27,2 | 78,3 | 55,4 | 23,8 |
| ]]> 1:40 | 80,8 | 54,4 | 23,9 | 79,9 | 57,3 | 22,2 |
| 1:80 | 78,8 | 56,9 | ]]> 24,5 | 82 | 56,9 | 22,4 |
| 1:160 | 77,5 | 57,2 | 22,6 | 81,1 | 56,5 | ]]> 21,6 |
CE: Conjugado evaluado. CC: Conjugado comercial.
FIGURA. Correlación de los conteos (%) de células CD3, CD4 y CD8 obtenidos con el conjugado evaluado y con el comercial mediante citometría de flujo.
Al realizar la titulación del conjugado con las cepas de referencia de Adenovirus, VSR, Parainfluenza 1, 2 y 3 e influenza A y B, se tomó en cuenta que con la dilución de trabajo del conjugado del juego comercial para diagnóstico por IFI se obtienen 4 cruces de fluorescencia.
En la titulación del conjugado con las cepas de referencia se obtuvo una fluorescencia de 4 cruces con una dilución de 1:32, similar a lo obtenido con el conjugado comercial. Sin embargo, para garantizar la no presencia de casos falsos negativos y aprovechar la alta especificidad, se decidió evaluar las muestras clínicas con una dilución de 1:20, se obtuvieron los mismos resultados con ambos tipos de muestra.
En cuanto a la citometría de flujo, el conjugado evaluado trabaja a una dilución mayor que el conjugado comercial y se obtuvo una correlación que demuestra la especificidad de éste, lo que lo hace competir como posible producto a comercializar.
Esta preparación conjugada mostró una eficiencia similar y en algunos casos superior a los conjugados comerciales del mismo tipo. Consideramos que la calidad de los anticuerpos empleados constituye un factor decisivo en los elevados títulos de trabajo de esta preparación, así como de los niveles de fondo encontrados, tanto en las muestras de referencia como en muestras clínicas.10
La producción de este conjugado permite el diagnóstico virológico rápido de las muestras de pacientes mediante IFI, la identificación de cepas aisladas en cultivos celulares y la tipificación de subpoblaciones linfocitarias mediante citometría de flujo. Este producto permite la utilización de un panel de anticuerpos monoclonales no conjugados a fluoresceína, lo cual lo hace de uso universal en este tipo de diagnóstico.
isothiocyanate according to the conventional technique. The conjugated obtained was evaluated with the reference strains of Parainfluenza virus 1, 2, 3; Adenovirus; respiratory syncytial virus; and influenza virus A and B, by an indirect immunofluorescence technique and HIV positive samples by flow citometry. Specific monoclonal antibodies were used in both cases. Clinical specimens of patients with acute respiratory infection were evaluated.
Subject headings: IGG/isolation & purification; FLOW CITOMETRY/methods; FLUORESCENT ANTIBODY TECHNIQUE, INDIRECT/methods; MICE/blood; CHROMATOGRAPHY, AFFINITY; CHROMATOGRAPHY; AFFINITY PUNCTURES; STAPHYLOCOCCAL PROTEIN A.
Recibido: 3 de septiembre de 1996. Aprobado: 12 de enero de 1997.
Lic. Juan Carlos Vilaseca. Instituto de Medicina Tropical "Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba.
]]>