El objetivo de este estudio fue realizar la identificación de los principales componentes presentes en los antígenos de excreción-secreción de parásitos adultos que son reconocidos por los sueros de ratas infectadas experimentalmente con metacercarias de Fasciola hepatica, mediante la técnica de Western Blot. Además, se determinó la cinética de anticuerpos con un ELISA indirecto. Los resultados obtenidos permitieron identificar 31 componentes con pesos moleculares aproximados de 11 a 136 kD, donde las fracciones predominantes fueron: 11-13 kD, 14-16 kD, 23-33 kD, 55-57 kD, 65-71 kD y 86-136 kD. Se detectaron anticuerpos a partir de la 2da. semana de infección en el 80 % de los animales y en la 3ra. semana en el 100 % de ellos, no se detectaron en la 1ra. semana de la infección. La identificación de estos antígenos podría contribuir a una mejor comprensión de los mecanismos de la inmunidad vinculados a la infección por F.hepatica.
Descriptores DeCS: WESTERN BLOTTING/métodos; ANTIGENOS HELMINTICOS/sangre; FASCIOLA HEPATICA/inmunología; FASCIOLIASIS/inmunología; ELECTROFORESIS EN GEL DE POLIACRILAMIDA/métodos; RATAS WISTAR; PEPTIDOS/sangre.
Los antígenos de excreción-secreción (ES) han sido considerados importantes inductores de la formación de anticuerpos en la fascioliasis1-4 y tanto su especificidad como su utilidad diagnóstica han sido ampliamente demostradas en estudio previos de fascioliasis humana y animal.5-6
Nuestro grupo de laboratorio desarrolló recientemente un ensayo inmunoenzimático sobre fase sólida (sandwich ELISA) para la detección de coproantígenos en pacientes y animales infectados, se empleó para ello el AcM ES78, que sólo reconoce antígenos de ES de Fasciola hepatica.7,8 Mediante el uso de este procedimiento pudimos detectar la infección activa en pacientes y animales que se encontraban tanto en la fase aguda como en la crónica de ésta.7,9 lo cual sugirió la existencia de epitopes comunes a los diferentes estadios de desarrollo del parásito.
Existen varios reportes que demuestran la utilidad de los antígenos de ES en inmunoprotección;1,3,10 por esta razón, la identificación de aquellos componentes que inducen la respuesta mediada por anticuerpos durante la infección primaria sería de gran utilidad y podría contribuir a una mejor comprensión de los mecanismos de inmunidad en la fascioliasis.
En el presente trabajo nos propusimos identificar por Western Blot cuáles componentes presentes en los antígenos de ES de parásitos adultos son mayoritariamente reconocidos por sueros de ratas infectadas con metacercarias de F. hepatica durante el transcurso de una infección experimental.
Mediante el procedimiento descrito por Espino y otros en 1988,11 se prepararon antígenos de excreción-secreción (ES) a partir del mantenimiento in vitro de parásitos adultos de Fasciola hepatica, los cuales fueron extraídos de los conductos biliares de reses sacrificadas en el combinado cárnico de Candelaria, en la provincia de Pinar del Río.
Transcurridas las primeras 24 h de mantenimiento, los parásitos fueron eliminados y el medio de cultivo que contenía los productos de ES fue inmediatamente colectado y se le añadió una mezcla de inhibidores de proteasas compuesta por iodo-acetamida, EDTA y fenilmetilsulfonil fluoruro (PMSF) a una concentración final de 2mM, 5 mM y 8 mM, respectivamente. El medio fue posteriormente centrifugado a 3 000 rpm a 4 oC durante 10 min, el sobrenadante fue colectado, concentrado 100 veces por ultrafiltración con el empleo de una membrana YM-10 que excluye moléculas de peso molecular menor de 10 kD (AMICON Corp), y finalmente desalinizado con una columna PD-10 (Sephadex G-25). Los antígenos así obtenidos fueron conservados a -70 oC en alícuotas de 100 mL hasta ser utilizados más tarde.
]]> La concentración de proteínas de estos antígenos, que generalmente osciló entre 2 y 3 mg/mL, fue determinada por el método de Smith y otros, 12 que utiliza el ácido bicinconínico (BCA).Fue infectado un total de 10 ratas wistar de 160 g de peso, por vía oral con 25 metacercarias de F. hepatica. Todos los animales fueron sangrados antes de la infección, por punción de la vena retroorbital, luego semanalmente durante las primeras 4 semanas, posterior a lo cual el sangrado fue realizado quincenalmente hasta la semana 14ta. de la infección.
A partir de la 6ta. semana de la infección se colectaron muestras de heces a todos los animales, las cuales fueron examinadas microscópicamente en busca de huevos de F. hepatica. Al finalizar el experimento todas las ratas fueron sacrificadas y sus hígados examinados para cuantificar los parásitos alojados en los conductos biliares.
El curso de la infección fue seguido mediante un ensayo inmunoenzimático de detección de anticuerpos (ELISA indirecto), se emplearon como antígenos los productos de ES de F.hepatica. El procedimiento seguido en esta técnica fue el previamente reportado por Espino y otros, en 1997,9 para estos fines.
Los antígenos de ES de F.hepatica fueron estudiados por electroforesis en gel de poliacrilamida (SDS-PAGE) y Western Blot mediante el procedimiento descrito por Laemmli en 1970,13 y Towbin y otros en 1974,14 respectivamente.
Un total de 150 mg de los antígenos preparados en una solución tris-HCl, DSS, bromofenol azul y glicerol (0,01 M de tris-HCL pH 6,8; 2,5 % de DSS; 0,1 % de bromofenol azul y 10 % de glicerol), fue calentado a 100 oC durante 3 min. Más tarde, fue aplicado sobre toda la superficie de un minigel al 12 % y fue sometido a corriente constante (25 mA/75 mm de gel) durante aproximadamente 40 min en un equipo de electroforesis vertical (mini protean II, Bio RAD).
Al finalizar la corrida se realizó la transferencia del patrón electroforético hacia una membrana de nitrocelulosa de 0,2 mm, para ello se empleó un equipo de transferencia semiseco (mini protean Transfer Unit, Bio RAD) a 15 volt durante 2 h. Al transcurrir este tiempo, la nitrocelulosa fue bloqueada con leche descremada al 2,5 % disuelta en solución salina tamponada con fosfato (SSTF) que contenía 0,05 % de Tween 20 (SSTF-T) y posteriormente fue cortada en tiras de 5 mm de ancho, las cuales fueron incubadas toda la noche a 4 oC con los sueros de las ratas a diferentes semanas de infección diluidos 1:200 con SSTF-T.
Después, se realizaron 3 lavados de 5 min cada uno, más tarde las tiras fueron incubadas durante 2 h a 37 oC con la solución de conjugado (anti-IgG de rata peroxidasa; Sigma) diluida 1:1 000 en SSTF-T. Luego de otros 3 lavados las tiras fueron incubadas con la solución de sustrato (10 mg de 3,3-diami-nobenzidine tetrahydrocloride [Sigma] + 10 mL de H2O2 30 % w/v + 10 mL de SSTF). Una vez visualizadas las bandas se detuvo la reacción al sumergir las tiras en agua destilada.
El peso molecular de cada una de las bandas observadas fue estimado a través del cálculo de su movilidad relativa mediante una curva de calibración previamente confeccionada a partir de proteínas patrones (fosforilasa B: 94,0 kD; albúmina bovina: 67,0 kD; ovoalbúmina: 43,0 kD; anhidrasa carbónica: 30,0 kD; inhibidor de tripsina: 20,1 kD; a _lactoalbúmina:14,4 kD), que fueron corridas en la electroforesis en iguales condiciones que los antígenos de ES y cuyos pesos moleculares fueron transformados en logaritmos y graficados contra sus correspondientes movilidades relativas mediante un tratamiento de correlación lineal simple (r2= 0,98).
Todas las ratas fueron sacrificadas en la semana 14ta. de la infección y en el 100 % de los hígados se comprobó la presencia de parásitos adultos en un número de 2 a 4 por animal, para un promedio de 3 parásitos (DE=0,7). Todos los hígados examinados mostraron además signos evidentes de infección dado por el estado esclerosado de los conductillos biliares.
]]> Los exámenes parasitológicos realizados demostraron la presencia de huevos de F. hepatica a partir de la semana 10 de la infección, momento en el cual se reconoció el inicio del período patente de la enfermedad en este modelo experimental.Cuando los sueros de las ratas infectadas con Fasciola hepatica fueron estudiados por ELISA contra los antígenos de ES, se pudo detectar la presencia de anticuerpos a partir de la 2da. semana en 8 de las 10 ratas infectadas (80 %) y en el 100 % de éstas a partir de la 3ra. semana; en el 50 % de los animales se observó un máximo de absorbancia en las semanas 6ta. y 10ma. de la infección. Ninguno de los sueros colectados antes de la infección o en la 1ra. semana posterior a ésta dieron reacción positiva en este ensayo.
Cuando los sueros de las ratas infectadas fueron examinados por Western Blot contra los antígenos de ES se observó un total de 31 polipéptidos de variados pesos moleculares (11 a 136 kD) identificados indistintamente por uno u otro de los animales, de los cuales 14 componentes (45 %) en el rango de 11 a 71 kD, resultaron ser predominantemente reconocidos por la mayoría de los animales infectados.
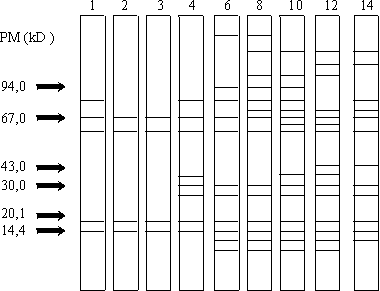
Dentro de este conjunto de polipéptidos se destaca la presencia de 2 a 3 componentes mayoritarios en los rangos de 14 a 16 kD y de 55 a 57 kD que fueron observados en el 100 % de los animales desde la 1ra. semana de la infección y que se mantuvieron claramente detectables durante todo el experimento (figura).
Fig. Representación esquemática del análisis por Western Blot de los polipéptidos mayoritariamente reconocidos por los sueros de ratas infectadas durante las diferentes semanas de infección (1-14).
Del mismo modo, fue observado otro grupo de 4 polipéptidos en el rango de 23 a 33 kD, los cuales fueron intensamente detectados entre el 60 y el 100 % de los animales entre las semanas 4ta. y 14ta. de la infección. Otro grupo de 3 polipéptidos en el rango de 65 a 71 kD fue progresivamente reconocido por los sueros de las ratas después de la 4ta. semana de la infección, y alcanzó su máximo reconocimiento (100 %) en la 10ma.. semana. Posterior a este tiempo se observó una notable disminución del reconocimiento hacia los polipéptidos de 65 y 67 kD. El componente de 65 kD desapareció en todos los animales a partir de la semana 14ta.. en tanto que el polipéptido de 67 kD en esa misma semana se identificó en sólo el 10 % de los animales.
Otros 2 polipéptidos de 11 a 30 kD fueron reconocidos por los sueros de las semanas 6ta. y 8va. de infección en sólo 4 de los animales infectados (40 %). Estos componentes fueron más tarde reconocidos por todas las ratas entre las semanas 10ma. a 12da. de la infección, este reconocimiento disminuyó notablemente en la semana 14ta.
Ninguno de los polipéptidos de elevado peso molecular (86 a 136 kD) fue significativamente reconocido durante las primeras 4 semanas de la infección, se observó una gran variabilidad en su reconocimiento a partir de la 6ta. semana del 40 al 70 % de los animales infectados.
En la tabla se muestra un resumen de la positividad encontrada entre las semanas 1ra. y 14ta. de la infección para los grupos de polipéptidos anteriormente mencionados.
]]> TABLA. Polipéptidos más reconocidos, mediante Western Blot, por los sueros de ratas infectadas experimentalmente con metacercarias de Fasciola hepatica
| No. de polipéptidos | Rango PM | Semanas de infección | ||||||||
| 1 | 2 | 3 | ]]> 4 | 6 | 8 | 10 | 12 | 14 | ||
| 11-13 kD | 2 |
|
| ]]> |
| + | + | ++ | ++ | + |
| 14- 16 kD | 3 | ++ | ]]> |
| + | + | ++ | ++ | ++ | ++ |
| 23- 33 kD | 4 | ]]> |
|
| ++ | ++ | ++ | ++ | ++ | ++ |
| 55-57 kD | ]]> 2 | ++ | ++ | ++ | ++ | + | + | ++ | ++ | ++ |
| ]]> 65-71 KD | 3 |
|
|
| + | + | + | ++ | ++ | ]]> |
| 86-136 kD | 7 |
|
|
|
| + | + | + | ]]> + | + |
++: Positividad encontrada en más del 60 % de los animales infectados.
+: Positividad encontrada entre el 30 y el 60 % de los animales infectados.
Se ha demostrado que Fasciola hepatica en su desarrollo dentro del huésped sufre un importante recambio en la superficie tegumentaria que constituye un mecanismo de evasión a la respuesta inmunológica del hospedero.15 En relación con este recambio, sobre el tegumento del parásito se ha identificado la presencia de gránulos secretorios que se transforman desde gránulos T0 característicos del parásito joven recién desquistado, a gránulos de tipo T1 y T2 que caracterizan al parásito inmaduro y maduro, respectivamente,16 a su vez se demuestra que estas estructuras fisiológicamente diferentes, poseen componentes antigénicos comunes que están muy relacionados con los antígenos de ES, que en cada estadio el parásito libera al medio circundante.17
En 1983, Hanna y Trudgett18 desarrollaron hibridomas productores de anticuerpos monoclonales altamente reactivos a células tegumentarias de tipo T1 que reconocían en menor grado las estructuras tegumentarias del parásito adulto. Estos anticuerpos monoclonales inmunoprecipitaron, entre otros, polipéptidos de 50 kD y de 25 a 40 kD. En nuestro estudio, identificamos polipéptidos de 23 a 33 kD y de 55 a 57 kD mediante sueros de ratas con apenas 1 y 4 semanas de infección, respectivamente. Este reconocimiento se mantuvo aun después de iniciada la ovoposición.
Debido a que en la 4ta. semana de la infección el parásito se encuentra migrando por el parénquima hepático en forma inmadura, y dado que algunos de los polipéptidos identificados por nosotros en este estudio (23 a 33 kD, 55 a 57 kD ) poseen un rango de peso molecular muy cercano o incluido dentro del rango reportado por los autores antes mencionados, es muy probable que éstos sean antígenos de ES producidos por los gránulos secretorios de tipo T1 que poseen comunidad antigénica con los productos de ES del parásito adulto.
Estas observaciones se corresponden con los resultados obtenidos por Sanderman y Howell, quienes analizaron por dobleinmunodifusión antígenos de parásitos en diferentes estadios, y encontraron que los antígenos que formaron líneas de precipitación alrededor de los antígenos de parásitos jóvenes e inmaduros eran también producidos por el parásito adulto.4
En el presente estudio resultó interesante la obtención de un amplio reconocimiento de los polipéptidos de 14 a 16 kD y de 55 a 57 kD desde la 1ra. semana de infección; sin embargo, por ELISA, la presencia de anticuerpos no fue detectada en el 100 % de los animales hasta la 3ra. semana de infección. Debido a que ninguno de los sueros estudiados por Western Blot antes de la infección mostró reactividad con los antígenos de ES, la presencia de estas bandas como consecuencia de reacciones inespecifícas en el Western Blot debe ser descartada. La diferencia entre los resultados de ambas técnicas se podría explicar si tenemos en cuenta que en el ELISA se considera positivo todo suero que cumpla la condición de exceder en absorbancia un valor de corte previamente establecido (0,3), con el cual se garantiza excluir la posible presencia de reacciones cruzadas tal como se ha demostrado en trabajos previos;5 pero, no se excluye la posibilidad de una baja sensibilidad del ELISA a la 1ra. semana de infección, donde el reconocimiento antigénico es mucho menor. Los polipéptidos identificados desde la primera semana de infección parecen ser moléculas de gran poder immunogénico liberadas primeramente por las formas inmaduras.
]]> Los máximos valores de absorbancia detectados en el ELISA en las semanas 6ta. y 10ma. se corresponden con los resultados previamente obtenidos por nuestro grupo en este mismo modelo experimental9 y pueden estar relacionados con los cambios tegumentales que precisamente ocurren en estas 2 semanas. El pico de anticuerpos observado por ELISA en la 10ma. semana se corresponde también con un incremento en la intensidad y número de las bandas identificadas por Western Blot.El débil e irregular reconocimiento de los polipéptidos de mayor peso molecular (86 a 136 kD) por los sueros de las ratas durante las 10 primeras semanas de infección, sugiere que éstos no son componentes antigénicos característicos de los estadios inmaduros del parásito y dado que algunos reportes en humanos hacen referencias a moléculas de elevado peso molecular en etapas avanzadas de la infección,19 es muy probable que el reconocimiento a estos antígenos se incremente con el transcurso de la fase crónica.
Otros autores han reportado la existencia de un polipéptido de 17 kD que fue reconocido por Western Blot a partir de la 4ta. semana de infección en conejos infectados experimentalmente y que fue detectado a partir de la 8va. semana en carneros y bovinos.10 Este polipéptido también ha sido identificado por sueros de pacientes con más de 1 año de infección,19 debido a lo cual se reconoce como un importante marcador de la infección por F. hepatica en su fase aguda y crónica. El polipéptido de 16 kD identificado en nuestro estudio podría ser el Fh-17 anteriormente mencionado y de este modo constituir una molécula de importante valor diagnóstico.
Aunque en el presente estudio no se incluyeron sueros de animales infectados con Schistosoma mansoni u otros parásitos para identificar los posibles componentes de reacción cruzada, otros estudios han demostrado que los polipéptidos de 17 kD y 23 a 28 kD son específicos de F. hepatica a diferencia de los de 63 kD y de mayor peso molecular, para los cuales se reporta reactividad cruzada con sueros de animales infectados con Schistosoma mansoni y Trichinella spiralis.10,20,21
Muchos investigadores han destacado la importante función que desempeñan los antígenos de ES en la inmunidad, debido que al inmunizar con ellos ratas y ratones han logrado inducir elevados niveles de protección.1,3,10 Teniendo en cuenta estos antecedentes es muy probable que alguno de los antígenos identificados por nosotros en este estudio puedan ser importantes en la inducción de mecanismos de protección, por lo cual están siendo diseñados nuevos estudios dirigidos a dilucidar estos aspectos.
Este trabajo ha sido financiado por la Academia de Ciencias del Tercer Mundo (TWAS) Proyecto NE 95-018 RG/BIO/LA.
SUMMARY
This paper was aimed at identifying the main components present in the excretory-secretory antigens of adult parasite which are recognized by the sera of rats experimentally infected with metacercariae of Fasciola hepatica, by using the Western Blot technique. The cynetics of antibodies was also determined with and indirect ELISA. The results obtained allowed to find 31 components with approximate mollecular weights from 11 to 136 kD. The predominant fractions were the following: 11-13 kD, 14-16 kD, 23-33 kD, 55-57 kD, 65-71 kD, and 86-136 kD. Antibodies were detected from the 2nd. week of infection in 80 % of the animals and from the 3rd. week in 100 % of them. There were no antibodies during the first week. The identification of these antibodies may contribute to a better understanding of the mechanisms of immunity linked with the infection by F. hepatica.
Subject headings: BLOTTING; WESTERN/methods; ANTIGENS; HELMINTH/blood; FASCIOLA HEPATICA/immunology; FASCIOLIASIS/immunology; ELECTROPHORESIS POLYA-CRYLAMIDE GEL/methods; RATS, WISTAR; PEPTIDES/blood.
Recibido: 25 de marzo de 1997. Aprobado: 12 de julio de 1997.
Lic. Ailén Díaz. Instituto de Medicina Tropical " Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba.
1 Licenciada en Química. Reserva Científica.
2 Licenciada en Farmacia. Estudiante de Maestría. Facultad de Medicina Veterinaria. Universidad de San Marcos. Perú.
3 Técnico A en Procesos Biológicos.
4 Técnico A en Laboratorio Clínico.
5 Doctora en Ciencias Médicas. Licenciada en Bioquímica. Investigadora Auxiliar. Jefa del Laboratorio de Fasciola hepatica. Responsable del Proyecto TWAS.