Dra. María Teresa Illnait Zaragozí,1 Dr. Gerardo Martínez Machín2 y Lic. Carlos Fernández Andreu3
Con el objetivo de obtener una IgG anti-Cryptococcus neoformans, se llevaron a cabo simultáneamente 2 esquemas de inmunización en conejos con una cepa autóctona. Para ambos se emplearon células enteras formalinizadas que se diferenciaban entre sí en cuanto a dosis y vías de inmunización. Los sueros obtenidos fueron titulados y se seleccionó el de mayor título (1: 1 024 por el método de aglutinación en lámina) el cual fue purificado mediante precipitación salina y cromatografía de intercambio iónico, con la obtención de una IgG de pureza y actividad biológica altas.
Descriptores DeCS: CRYPTOCOCCUS NEOFORMANS/inmunología; CROMATOGRAFIA POR INTERCAMBIO IONICO; TEST DE AGLUTINACION/métodos; CONEJOS/inmunología.
Cryptococcus neoformans, hongo levaduriforme, constituye el agente causal de la criptococosis. Esta enfermedad puede iniciarse como una infección pulmonar con tendencia a diseminarse con especial predilección hacia el sistema nervioso central, aparece con frecuencia como infección oportunista en pacientes con daño inmunológico. (Hay RI. Extrameningeal manifestations of Cryptococcosis. 3rd International Conference on Cryptococcus & Cryptococcosis. Abstract, 1996: 117-8).
La levadura está rodeada de una cápsula polisacarídica que ha sido estudiada de forma amplia, ya que resulta el principal factor de virulencia del microorganismo; se encuentra estrechamente relacionada con su taxonomía, y su detección en los fluidos corporales ha permitido el diagnóstico rápido y la evaluación del pronóstico de la enfermedad.1,2
El polisacárido capsular (PSC) está compuesto por manosa, xilosa, ácido glucurónico y grupos O-acetil.3 Los diferentes grados de acetilación de las cadenas laterales determinan la presencia de serotipos cuya com plejidad estructural aumenta del serotipo D al A, al B, al C.4,5 Estos serotipos, se encuentran agrupados en 2 variedades: C. neoformans var. neoformans (serotipos A y D) y C. neoformans var. gattii (serotipos B y C).6
La estructura antigénica de la levadura resulta ser un inmunogéno pobre, tanto para el hombre como en modelos experimentales en animales, por lo que la producción de anticuerpos específicos ocurre sólo en una parte de los pacientes con criptococosis y los títulos son usualmente bajos.2,6
Esta característica ha hecho difícil la obtención de anticuerpos específicos anti-Cryptococcus neoformans útiles en el desarrollo de técnicas para el diagnóstico rápido como las de aglutinación, en especial aquéllas asociadas al látex y otras novedosas como los ensayos inmunoenzimáticos.
El objetivo de este trabajo fue la obtención de IgG específica anti-Cryptococcus neoformans con vistas a su posterior utilización en el desarrollo de técnicas para detección de antígenos que permitan ampliar las posibilidades diagnósticas del laboratorio.
Inmunización de los animales. Se emplearon 2 grupos de 3 conejos cada uno, de la raza Nueva Zelandia de aproximadamente 2 kg de peso, procedentes del Centro para la Producción de Animales de Laboratorio (CENPALAB).
Al primer grupo se le aplicó el esquema de inmunización propuesto por Palmer7 y al otro uno propuesto por el Centro de Control de Enfermedades de Atlanta (CDC) (M. Dolande, comunicación personal).
Para el primer esquema los animales fueron inmunizados con 3 mL de la suspensión antigénica vía endovenosa (e.v.) de lunes a viernes durante 2 semanas. Después de 7 d de reposo, se repitió el mismo procedimiento.
El segundo esquema se inició con la administración intramuscular (i. m.) de 0,5 mL de la suspensión antigénica en 0,5 mL de Adyuvante Completo de Freund en cada pata posterior, lo cual se repitió en Adyuvante Incompleto de Freund a los 14 y 21 d en las patas anteriores. Luego se continuó a partir del día 23 de iniciado el esquema con inmunizaciones e.v. de 1 mL de la suspensión antigénica en días alternos hasta el día 33. Pasados de 7 a 10 d de finalizados los esquemas, se realizó una extracción de sangre para la titulación.
Titulación y procesamiento de los sueros. Los sueros de los animales fueron titulados por inmunofluorescencia indirecta (IFI), aglutinación en tubo (AT) y aglutinación en lámina (AL).7,8
Se seleccionó el suero de más alto título para la obtención de la IgG por precipitación salina con sulfato de amonio al 50 % y cromatografía de intercambio iónico en una columna de HiLoad Q Sepharosa FF XK 26/10 (Pharmacia).9
Al producto se le determinó la concentración de proteínas por el método de Lowry10 y se ajustó a 10 mg/mL mediante ultrafiltración con membrana de AMICON.9 Después se evaluó en términos de pureza y actividad biológica mediante SDS-PAGE11 y titulación en lámina respectivamente.
De los conejos inmunizados según el esquema propuesto por Palmer, 1 alcanzó altos títulos (1:1 024). Los 2 restantes sólo llegaron a tener 1:128. Los que recibieron el esquema del CDC tuvieron títulos de 1:32 (2 de ellos) y el otro 1:16.
La AL fue definitivamente la más factible debido a su fácil interpretación y rapidez, los resultados coinciden (100 %) con los obtenidos mediante IFI. A su vez ésta fue más rápida, fácil de realizar e interpretar que la aglutinación en tubo, cuyos resultados fueron imprecisos y no se tuvieron en cuenta.
]]>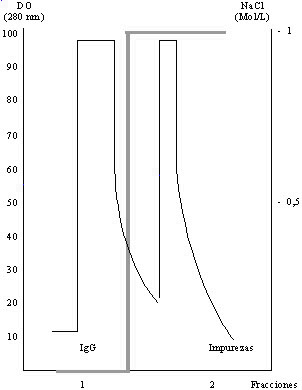
Fig 1. Purificación cromatográfica de IgG anti-Cryptococcus neoformans
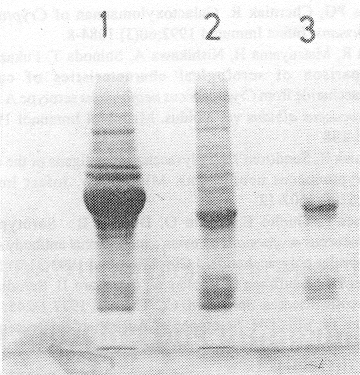
Fig.2. SDS-PAGE de las fracciones obtenidas en la purificación de la IgG anti-C. neoformans. 1) Suero de conejo anti-C. neoformans. 2) Precipitado globulínico del suero de conejo anti-C. neoformans. 3) IgG anti-C. neoformans.
Tabla. Control del material obtenido en el proceso de purificación de la IgG de conejo anti-Cryptococcus neoformans
|
| Volumen | ]]> Concentración de proteínas | Actividad |
|
| (mL) | (mg/mL) | (título) |
| Fracción gamma precipitada | 5 | 30 | 1/1 000 |
| ]]> IgG purificada | 16 | 10 | 1/1 000 |
De la representación gráfica del proceso de purificación se obtuvo un cromatograma (fig. 1). El primer pico mostró un patrón característico de IgG. Esta fracción fue recolectada y durante su evaluación mostró poseer alta pureza y actividad biológica específica (tabla). En la figura 2 puede observarse el alto grado de pureza que se obtuvo para la IgG.
Entre las principales propiedades biológicas del PSC, se destaca su pobre inmunogenicidad, evidenciada en lo difícil que resulta desarrollar una adecuada respuesta de anticuerpos, tanto durante el curso de la infección natural como tras la inmunización activa con este microorganismo.12
El uso de cepas de C. neoformans var. neoformans en los esquemas de inmunización es un elemento importante para la obtención de sueros con altos títulos y suficiente reactividad cruzada con otros serotipos, requisitos ambos imprescindibles para la utilización de un suero hiperinmune en el diseño de pruebas serológicas.13
En nuestro trabajo la utilización de una cepa autóctona de C. neoformans var. neoformans estuvo motivada por 2 razones fundamentales. Primero, el 100 % de las cepas estudiadas en nuestro país procedentes tanto de muestras clínicas como ambientales, corresponden a esta variedad,14 y segundo, debido al escaso desarrollo de la cápsula alcanzado por esta cepa.
La importancia del tamaño de la cápsula y su relación con la inmunogenicidad, fue demostrada temprano por los trabajos de Neil y otros. Ellos comprobaron que las suspensiones preparadas con cepas capsuladas de forma débil, mostraban una mayor capacidad inmunogénica que las preparadas con cepas fuertemente capsuladas.15
]]> En el presente trabajo, donde se comparan 2 métodos de inmunización, sólo 1 conejo de los inoculados según el esquema de Palmer alcanzó títulos de 1: 1 024, mientras que en el resto de los animales la respuesta de anticuerpos en general resultó débil, y fue algo más baja en los inoculados con el esquema del CDC. Este hecho pudiera ser explicado porque la respuesta de anticuerpos es susceptible de ser enmascarada por un exceso de antígeno polisacarídico circulante,16 o según lo señalado por Murphy y otros autores, los cuales demostraron que el PSC es capaz de inducir un estado de tolerancia inmunológica, la cual resulta de una disminución del número de células productoras de anticuerpos más que una simple neutralización de éstos por el antígeno.17 También, y debido a la pobre inmunogenicidad del PCS ya descrita, se ha señalado que en el curso de la enfermedad pudiera presentarse una inmunosupresión, la cual involucra, al menos como a uno de sus mecanismos probables, la producción de células supresoras.18Nuestros resultados no coinciden plenamente con los reportados por algunos autores, los cuales prefieren más de una vía de inoculación y la multipuntura17 como en el esquema del CDC. No obstante, la pobre respuesta de anticuerpos obtenida pudiera deberse más que al tipo de esquema utilizado, a la capacidad de respuesta de cada animal en particular, criterio fundamentado en la baja repetibilidad alcanzada en los resultados.
El empleo de diferentes técnicas para la titulación de los sueros, permitió no sólo precisar al título de anticuerpos circulantes, sino también evaluar la factibilidad y utilidad de cada una de ellas al compararlas entre sí.
Ya ha sido reportado que la IFI presenta resultados satisfactorios en el diagnóstico a causa de su sensibilidad, especificidad y porque resulta más fácil de realizar e interpretar en relación con otras.19
La AL ha sido empleada con éxito en la serotipificación de C. neoformans, ya sea mediante anticuerpos policlonales previamente adsorbidos o monoclonales específicos.8 No encontramos antecedentes de su empleo en la titulación de sueros; no obstante, teniendo en cuenta los resultados obtenidos, esta prueba presenta un comportamiento similar a la IFI, por lo que sumado a sus otras ventajas (rapidez, bajo costo, etcétera) recomendamos su empleo con este propósito.
La AT fue utilizada por Gordon y Vadder, quienes demostraron que era segura para el diagnóstico. Ellos encontraron aglutininas en las primeras etapas de la infección del sistema nervioso central y en infecciones sin compromiso de éste.20 Es, probablemente, uno de los métodos más específicos para la detección de anticuerpos, sin embargo, en nuestra experiencia resultó ser una prueba engorrosa y de difícil interpretación.
Por último, como resultado del proceso de purificación se obtuvo una IgG con alta actividad biológica y pureza ensayadas por algutinación en láminas e inmunoelectroforesis, respectivamente, útil en el diseño de procedimientos rápidos para el diagnóstico mediante la detección de antígenos de C. neoformans.
Two immunization schemes were applied to rabbits with an autoctonous strain aimed at obtaining an anti-Crytococcus neoformans IgG. Whole cells treated with formalin were used. Dosages and immunization routes were different. The sera obtained were titered and that with the highest titer was selected (1:1 024 by the laminar agglutination method) and purified by saline precipitation and ion exchange chromatography. An IgG of high purity and biological activity was obtained.
Subject headings: CRYPTOCOCCUS NEOFORMANS/immunology; CHROMATOGRAPHY; ION EXCHANGE, AGGLUTINATION TEST/methods; RABBITS/immunology.
Dra. María Teresa Illnait Zaragozí. Instituto de Medicina Tropical "Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba.
1 Especialista de I Grado en Microbiología.
2 Especialista de I Grado en Microbiología. Investigador Agregado. Jefe del Departamento de Bacteriología-Micología.
3 Licenciado en Microbiología. Investigador Auxiliar. Jefe del Laboratorio de Micología.