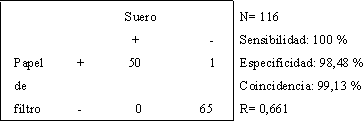
Se describe la utilidad de la toma de muestra total en papel de filtro para la detección de la IgM antivirus de la hepatitis A (VHA). Se compararon simultáneamente 168 muestras de suero y papel de filtro, en las 52 muestras que conformaron el grupo control, no se detectaron alteraciones en la especificidad del ELISA de captura de IGM, y en las 116 restantes, que procedían de pacientes con sospecha clínica de hepatitis viral aguda, se obtuvo una sensibilidad, una especificidad y una coincidencia de 100 % al comparar el papel de filtro con la dilución 1:500 y el suero. La correlación entre los valores de densidad óptica de los resultados positivos a la IgM anti-VHA entre el papel de filtro a la dilución 1:500 y el suero, fue de 0,895. Al aplicar este tipo de colecta de muestra en un grupo de enfermos hospitalizados, se obtuvo 100 % de coincidencia con la sospecha clínica; además, se demostró su utilidad en el diagnóstico de un brote de hepatitis viral. Nuestros resultados recomiendan la introducción de este tipo de recolección de muestras en el diagnóstico de la hepatitis A.
Descriptores DeCS: ELISA/métodos; HEPATITIS VIRAL HUMANA/sangre; HEPATITIS VIRAL HUMANA/epidemiología; BROTES DE ENFERMEDADES; IGM/análisis.
La hepatitis viral es una enfermedad generalizada que afecta de forma primaria al hígado y que puede ser causada por los virus de la hepatitis A, B, C, D, E y los recientemente reportados agentes GB y HGV.1
La hepatitis A, conocida también como hepatitis de incubación corta o hepatitis infecciosa, es causada por el virus de igual nombre, y se caracteriza por inflamación aguda del hígado, fiebre, síntomas gastrointestinales e ictericia. Su vía fundamental de transmisión es fecal-oral, aunque en ocasiones ésta puede ocurrir por vía parenteral. Tiene mayor incidencia en adultos jóvenes y en niños, en estos últimos la infección puede pasar inadvertida.2
Esta enfermedad, de amplia distribución mundial, se presenta con frecuencia como brotes epidémicos producto de aguas o alimentos contaminados, lo que ocurre comúnmente en instituciones cerradas: círculos infantiles, escuelas y unidades militares.3
El diagnóstico de la infección por el virus de la hepatitis A (VHA) se basa en la clínica, la epidemiología y el estudio virológico. Este último puede realizarse mediante la detección del ARN viral en suero, heces fecales e hígado, así como del antígeno viral en heces, o de anticuerpos circulantes en respuesta a la infección por el agente. Para ello se utilizan varias técnicas como la microscopia a inmunomicroscopia electrónica (ME e IME), radioinmunoensayos (RIA), ensayos inmunoenzimáticos (ELISA) y ensayos de biología molecular (hibridación molecular [dot blot] y reacción en cadena de polimerasa [RCP]).4,5
El método más práctico y disponible es el diagnóstico serológico, por lo que su empleo en amplio, se utiliza la detección de IgM anti-VHA como herramienta principal en el diagnóstico rápido de la enfermedad. Esta determinación se realiza generalmente por ELISA y es de gran importancia para enfrentar y controlar los brotes de hepatitis viral, ya que el conocimiento del agente causal permite aplicar cuanto antes las medidas de control y el tratamiento necesarias.
La colecta de sangre en papel de filtro, ha sido ampliamente utilizada en el diagnóstico virológico, tanto para la detección de IgM,6 como de IgG,7 así como en diferentes técnicas: RCP,8 inhibición de la hemaglutinación (IH)9 y ELISA.10,11
]]> Debido a las ventajas que posee este método, tales como la posibilidad de un transporte de muestras más seguro y un mejor almacenamiento, la utilización de una menor cantidad de materiales, así como que es un método menos molesto para el paciente y no necesita de personal especializado, nos propusimos conocer su utilidad en la detección de la IgM anti-VHA, fundamentalmente en el estudio de brotes de hepatitis A.Muestras. Se recolectaron, de forma simultánea 168 muestras de suero y sangre total en papel de filtro (Blood Samplig Paper, Nobuto´s tipo I, Toyo Roshi Kaisha, Ltd Tokyo, Japan) en los laboratorios clínicos del Instituto de Medicina Tropical "Pedro Kourí" (IPK) y del Instituto de Gastroenterología, con las siguientes características:
Para el estudio de aplicación del método de recolección de muestras de sangre total en papel de filtro, en el diagnóstico virológico de la hepatitis A, se tomaron 4 muestras de casos clínicos sospechosos de hepatitis viral tipo A en la sala de Gastroenterología del Hospital Militar "Luis Díaz Soto" Se recolectaron además 97 muestras procedentes de un brote de hepatitis viral ocurrido en el Círculo Infantil "Juan Alvarado", del municipio La Lisa, en Ciudad de La Habana.
Toma de muestra en papel de filtro. Se obtuvo por punción con lanceta estéril del pulpejo del dedo pulgar, previa limpieza de la zona. Se dejó absorber la sangre por el área indicada por el fabricante (zona A, de 30 mm de largo y 5 mm de ancho) de forma uniforme y por ambos lados. Cada papel de filtro había sido rotulado previamente (zona B, 18 mm de largo y 10 mm de ancho). Una vez que la sangre fue absorbida, se dejó secar en posición vertical, con la zona B hacia abajo a temperatura ambiente. En todos los casos se siguieron las instrucciones siguientes: evitar la exposición a temperaturas elevadas, a la luz solar directa y a gases tóxicos que pudieran inhibir la extracción del anticuerpo del papel de filtro. Se guardó el papel de filtro a 4 oC hasta el momento en que se realizó la elución.
Procesamiento de la elución de los anticuerpos. El papel de filtro tipo I está diseñado para absorber un volumen fijo de sangre en el área señalada y la elución es el proceso que permite que los anticuerpos sean extraídos.
El día anterior a la realización de la prueba serológica, el área de absorción sanguínea fue cortada con unas tijeras en 3-4 partes y colocada en 400 mL de solución tamponada de fosfato pH 7,2 (PBS) en tubos Eppendorf, los que fueron guardados a la temperatura de 4 oC durante toda la noche. La solución tomó un color rojo vino, lo que visualmente nos indicó una buena elución de los anticuerpos, que se corresponde con una dilución aproximada de 1:10 del suero.
ELISA de captura de IgM anti-VHA. Se utilizó el ELISA de captura de IgM, normalizado y validado en el Laboratorio de Hepatitis Viral del IPK.12
]]> Se fijaron a la placa de poliestireno (MaxiSorp, F8 Nunc, Dinamarca, desmontable en 12 tiras) 100 mL de anti-IgM (específica a cadena m) humana (Centro de Inmunoensayo, La Habana, Cuba) a una concentración de 20 mL en buffer carbonato-bicarbonato pH 9,5. Al día siguiente se añadieron 50 mL de los sueros controles (4 negativos y 2 positivos) y sueros problemas diluidos 1:1 000 en PBS-Tween 20 al 0,05 % (PBS-T) y los eluados correspondientes en 3 diluciones 1:100, 1:500 y 1:1 000, y se incubaron durante 1 h a 37 oC. Luego de 4 lavados con PBS-T, se adicionaron 50 mL del antígeno del VHA estabilizado e inactivado con formaldehído 1:2 000 a la dilución de 1:5 en PBS-T + 5 % de suero humano negativo a los marcadores de VHA; este reactivoju se incubó 2 h a 37 oC. Después se agregó el conjugado anti-VHA/peroxidasa (50 mL) a la dilución 1:1 000 en un buffer de igual contenido al utilizado para el antígeno. Por último, se añadió la misma cantidad de sustrato, compuesto por 5 mg de ortofenilendiamina, 5 mL de buffer fosfato-citrato pH 5 y 2 mL de peróxido de hidrógeno (30 %), la reacción se detuvo a los 15 min con 50 mL de ácido sulfúrico al 12,5 %. La lectura se realizó en un lector microELISA (Titertek Multiskan) a una longitud de onda de 492 nm.Procesamiento estadístico de los resultados. Se determinaron los porcentajes de sensibilidad, especificidad y coincidencia para comparar ambos métodos de recolección de muestras, mediante el uso de tablas de contingencia. Se halló el coeficiente de correlación de Spearman (R) a los valores de DO de los casos positivos por ambos métodos.
Con el objetivo de normalizar la toma de muestra de sangre total en papel de filtro para la detección de la IgM anti-VHA, primero se procedió a analizar 52 muestras de suero y papel de filtro procedentes de individuos con enfermedades no relacionadas con la hepatitis viral, los cuales constituyeron nuestro grupo control. Se realizaron diluciones 1:100, 1:500 y 1:1 000 del eluado del papel de filtro (PF) (dilución primaria 1:10) y se procesaron simultáneamente con el suero a la dilución usual de trabajo (1:1 000).
Exceptuando el proceso de elución de la muestra de sangre total colectada en papel de filtro, las condiciones requeridas para la determinación de la presencia de anticuerpos IgM mediante el ELISA de captura fueron iguales a las utilizadas para los sueros.
Las 52 muestras (suero y PF) que conformaban el grupo control resultaron negativas a la presencia de IgM anti-VHA. Ambos tipos de muestras se comportaron de manera similar, resultado que nos permitió definir que la utilización de la sangre colectada en papel de filtro no alteraba la especificidad de la técnica. Por tanto, los parámetros establecidos para el ELISA de captura de IgM anti-VHA no fueron modificados.
Teniendo en cuenta los resultados anteriores, analizamos los 116 casos clínicamente sospechosos de hepatitis viral, que solicitaban algún tipo de análisis relacionado con esta enfermedad. Las muestras diluidas de suero y papel de filtro se probaron en paralelo, o sea, en la misma placa de reacción, con las mismas condiciones para una y otra muestras.
]]> De las 116 muestras de sueros evaluadas para la detección de IgM anti-VHA, 50 resultaron positivas (43,1 %) y 66 negativas (56,8 %), por lo que la proporción de casos positivos y negativos resultó bastante similar.En la figura 1 se recogen los resultados de la comparación del suero y el papel de filtro a la dilución 1:100. En un total de 116 muestras, 50 fueron positivas con ambos tipos de muestras y 65 negativas; 1 muestra de suero negativa fue positiva al utilizar el papel de filtro, con una DO muy cercana al valor de corte. Estos resultados arrojaron una sensibilidad de 100 %, una especificidad de 98,48 % y una coincidencia de 99,13 %. El valor de R fue de 0,661.
Fig 1. Comparación de los resultados de la detección de IgM anti-VHA en suero y papel de filtro a la dilución 1:100.
En la figura 2 se muestran los resultados de la comparación del suero y el papel de filtro a la dilución 1:500. En este caso no se obtuvieron muestras discordantes, lo que condujo a una especificidad, sensibilidad y coincidencia de 100 %. El valor de R fue de 0,895.
Fig. 2. Comparación de los resultados de la detección de IgM anti-VHA en suero y papel de filtro a la dilución 1:500.
La figura 3 recoge la comparación de los 2 tipos de muestras a igual dilución (1:1 000). De las 116 muestras evaluadas, 49 fueron positivas y 66 negativas en ambos casos, 1 suero resultó positivo a la IgM anti-VHA, mientras su homólogo recogido en papel de filtro fue negativo. La DO de este suero estuvo muy cercano al valor de corte. En esta dilución R tuvo un valor de 0,886.
Fig. 3. Comparación de los resultados de la detección de IgM anti-VHA en suero y papel de filtro a la dilución 1:1 000.
]]> Teniendo en cuenta los resultados anteriores, decidimos realizar un pequeño estudio de aplicación de este tipo de recolección en casos clínicamente sospechosos de hepatitis viral, internados en la sala de Gastroenterología del Hospital Militar "Luis Díaz Soto", y en el diagnóstico de un brote de hepatitis viral en un círculo infantil de Ciudad de La Habana. La dilución de trabajo establecida fue 1:500, por ser ésta en la que se obtuvo mayor concordancia y un valor de R cercano a la unidad.En la tabla se recogen los resultados obtenidos tanto de los casos clínicos como del brote. El 100 % de los casos clínicos sospechosos fue positivo a la detección de IgM anti-VHA, mientras que 13 muestras (13,4 %) del brote fueron positivas a este mismo marcador.
TABLA. Resultados de la detección de IgM anti-VHA en casos clínicos sospechosos de hepatitis A y casos del brote en el círculo infantil
| Procedencia | Positivos (%) | Negativos (%) | Total |
| Casos clínicos sospechosos de hepatitis A | ]]> 4 (100 %) | 0 (0 %) | 4 |
| Casos del brote en el círculo infantil | 13 (13,4 %) | 84 (86,6 %) | 97 |
n=101
La utilidad de la toma de muestra de sangre total en papel de filtro (PF) ha sido reportada por muchos autores, y ha demostrado ser un proceder sencillo, fácil y aplicable en el diagnóstio de múltiples enfermedades.
]]> En los trabajos realizados por Guzmán y otros en la normalización del uso del PF en la serología de dengue por IH, no se obtuvieron diferencias significativas entre éste y el suero.13 Estos resultados coinciden con los encontrados por Vázquez y otros en la detección de anticuerpos antidengue por ELISA de inhibición, quienes encontraron concordancia, tanto en resultados positivos y negativos, como en los títulos de anticuerpos entre el suero y el PF a los 15 d, a los 3 y a los 6 meses de conservación a -20 oC.14Farzadegan y otros, en 1987,15 emplearon esta técnica en la detección de anticuerpos contra el VIH con resultados muy satisfactorios. De igual forma la toma de muestras en papel de filtro ha sido empleada en la detección de IgM e IgC antivirus de la rubéola.9
Burke y otros utilizaron la toma de muestra en papel de filtro para el establecimiento del diagnóstico serológico de la encefalitis japonesa (EJ), al comparar la detección de IgM mediante ELISA de captura y la detección de anticuerpos inhibidores de la hemaglutinación, demostraron la superioridad del método de captura de IgM para el diagnóstico serológico de la EJ mediante muestras de sangre absorbidas en PF; estos mismos autores reportaron la utilidad de este tipo de muestra para la detección de anticuerpos IgM a virus dengue, hepatitis A y hepatitis B.6
Este método también fue utilizado por Vázquez y otros para la determinación de anticuerpos IgM a virus dengue en muestras procedentes del Sistema de Vigilancia de Costa Rica y Nicaragua y reportaron 100 % de coincidencia entre el suero y el papel de filtro conservado a 4 oC.16
Por otra parte, Adler y Shouval desarrollaron un método simple de detección de anticuerpos totales contra el VHA mediante la colecta de sangre en discos de papel, con una concordancia de un 100 % con el suero homólogo.17
Nuestras experiencias permiten demostrar la utilidad de este tipo de recolección de muestras en el diagnóstico virológico de la hepatitis A.
En el grupo de pacientes clínicamente sospechosos de hepatitis viral, la dilución 1:100 del papel de filtro mostró una especificidad de 98,48 %. Esto puede ser debido a un falso positivo del papel de filtro y no a un falso negativo del suero, ya que la muestra en papel de filtro se trabajó a una dilución menor que la del suero, por lo que pueden quedar contaminantes que afecten la especificidad del sistema, los cuales se eliminan al diluir el suero 1:1 000.
Por el contrario, en la dilución 1:1 000 se afectó la sensibilidad del sistema (98 %). En este caso pensamos en un falso negativo del papel de filtro, ya que los valores de DO del suero estaban cercanos al valor de corte, lo que parece indicar que la concentración de IgM en el suero era baja, y por tanto, en el papel de filtro, y esto impedía que alcanzara el criterio de positividad de la prueba. El eluado del PF de esta muestra era de un color rojo vino intenso, lo que demuestra una buena elución de los anticuerpos. Aunque algunos autores han planteado que la IgM es altamente lábil cuando las muestras son tomadas en papel de filtro y conservadas,18 no es explicable este resultado si nos basamos en la pérdida de la IgM a través del tiempo, ya que las muestras fueron procesadas de 1 a 2 d después de su colecta, y en algunos casos el mismo día.
Basándonos en los valores de R de los casos positivos a la IgM encontrados en el suero y en las diferentes diluciones del PF, así como en la alta coincidencia entre los resultados positivos y negativos, decidimos establecer la dilución 1:500 como la óptima cuando se usara este tipo de muestra. El resto de los parámetros del ELISA de captura de IgM, como se planteó anteriormente, no se modificaron.
La aplicación de este método de recolección de muestras en la práctica, además de mostrar una coincidencia de 100 % con la sospecha clínica inicial, demostró una vez más sus ventajas, ya que permitió confirmar en un período corto (3 d), lo cual no es usual, que el agente causal de un brote de hepatitis viral en un círculo infantil de Ciudad de La Habana, era el virus de la hepatitis A, además facilitó el transporte de las muestras de sangre que fueron tomadas por personal no especializado, sin requerir más materiales que alcohol, lancetas, algodón y papel de filtro, así como evidenció ser un método más factible para el trabajo con niños.
]]> Estos resultados avalan la introducción de este tipo de muestra en el diagnóstico de la hepatitis A, se recomienda fundamentalmente en el estudio de brotes, sobre todo, en niños pequeños, en los que se dificulta la obtención de sangre venosa, y aquéllos que ocurren en concentrados militares y colectivos de difícil acceso, donde la lejanía (transporte de las muestras) y la falta de personal especializado, hacen atrayente este tipo de toma de muestra.The usefulness of the whole sample taking in filter paper for the detection of anti-HAV IgM is described. 168 serum and filter paper samples were simultaneously compared. No alterations were observed in the specificity of the enzyme-linked immunosorbent assay for the catchment of IgM in the 52 samples of the control group or in the other 116 from patients with clinical suspicion of acute viral hepatitis. A sensitivity, specificity and coincidence of 100 % was obtained on comparing the filter paper with the dilution 1:500 with the serum. The correlation established between the values of optical density of the positive results to anti-HAV IgM, the filter paper at dilution 1:500 and the serum was of 0.895. On applying this type of sample taking in a group of hospitalized patients, 100 % of coindicence with clinical suspicion was attained. Besides, it was proved its usefulnes for the diagnosis of a viral hepatitis outbreak. According to our results, it is recommended the introduction of this type of sample taking in the diagnosis of hepatitis A.
Subject headings: ENZYME-LINKED IMMUNOSORBENT ASSAY/methods; VIRAL HEPATITIS, HUMAN/blood; VIRAL HEPATITIS, HUMAN/epidemiology; DISEASE OUTBREAKS; IGM/analysis
Recibido: 3 de marzo de 1997. Aprobado: 1 de septiembre de 1997.
Dra. Licel de los Ángeles Rodríguez Lay. Instituto de Medicina Tropical " Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba.
1 Especialista de II Grado en Microbiología. Investigadora Agregada.
2 Especialista de I Grado en Microbiología.
3 Licenciado en Microbiología.
4 Técnico Medio en Procesos Biológicos.