Se realizó un ensayo clínico controlado, a doble ciegas, con la participación de 80 voluntarios adultos, de los 2 sexos, sanos en apariencia, que fueron distribuidos de forma aleatoriamente en 2 grupos de 40 cada uno, se constituyó un grupo de estudio (que recibió la vacuna) y un grupo control (que recibió un placebo) para conocer la seguridad, el comportamiento de la reactogenicidad y comenzar los estudios de inmunogenicidad de la primera vacuna cubana contra la leptospirosis humana. La vacuna utilizada en el grupo de estudio fue una vacuna inactivada y trivalente en cuya composición se encuentran cepas de Leptospira canicola, icterohaemorrhagiae y pomona, por ser las de mayor circulación en el país. Los resultados obtenidos demostraron la inocuidad de la vacuna, al no presentarse reacciones adversas graves. La sintomatología general observada fue baja, la febrícula fue el síntoma general encontrado en mayor proporción. Aparece durante los primeros 3 d de observación, sin encontrarse diferencias significativas entre el grupo vacunado y el placebo. Como síntoma local sólo fue referido el dolor ligero en el sitio de la inyección, en el grupo vacunado se presentó con mayor frecuencia que en el grupo control (7,8 contra 1,5 %, respectivamente). La seroconversión obtenida fue de 29 % mediante la microaglutinación, y 34,2 % por la técnica de ELISA. Los resultados obtenidos permiten concluir que ésta es segura para adultos humanos en las edades comprendidas en el estudio y permiten continuar otros estudios es fases más avanzadas para completar los requerimientos para su licenciamiento.
Descriptores DeCS: LEPTOSPIROSIS/inmunología; VACUNAS/inmunología; ENSAYOS CONTROLADOS ALEATORIOS.
La leptospirosis, zoonosis de amplia distribución mundial, tiene gran importancia actual tanto en medicina humana como veterinaria,1-4 dada las afectaciones que produce a la salud del hombre y los animales, así como a la economía. El clima, el suelo, las prácticas agrícolas y la abundante fauna de extensas zonas de nuestro país son apropiados para la propagación de la leptospirosis en el hombre y los animales, y al igual que en muchos otros, la agricultura y la ganadería desempeñan una función fundamental. Estos sectores han alcanzado un notable desarrollo en los últimos años, lo que ha permitido una utilización más amplia de los productos derivados de la agricultura y de los animales, un incremento del número de trabajadores incorporados a las labores agrícolas de forma temporal y permanente, así como de las personas expuestas al riesgo de enfermar.
Esta enfermedad ha presentado una tendencia ascendente, sobre todo en los últimos años, fundamentalmente a partir del año 1991, donde la mayoría de las provincias incrementan sus tasas de incidencia.5-7 Entre las medidas de prevención de la enfermedad en el hombre se encuentran la utilización de medios de protección como son el uso de botas y guantes en los trabajadores expuestos, así como evitar el nadar o vadear en aguas que puedan estar contaminadas; sin embargo, la vacunación a grupos de riesgo con vacunas que utilizan en su composición cepas autóctonas, unido a las anteriores medidas pueden tener un impacto positivo en el control de este problema de salud, y aunque no se ha aplicado de forma amplia, se ha utilizado con buenos resultados en Italia, Polonia, Israel, Rusia y China.8-10
Desde el año 1983, en nuestro país eran inmunizados todos los trabajadores expuestos al riesgo de enfermar con una vacuna de procedencia soviética integrada por gérmenes muertos por el calor, correspondientes a los serogrupos icterohaemorrhagiae, pomona, gripotyphosa y hebdomadis, elaborada por el Instituto de Sueros y Vacunas de Stavropol, del Ministerio de Salud Pública de la antigua URSS, hasta el año 1991, fecha en que dejó de aplicarse por dificultades en el suministro. Con el objetivo de continuar la inmunización a los grupos de riesgo del país se desarrolló en el Instituto "Finlay", Centro de Investigación-Producción de Vacunas y Sueros, una vacuna adyuvada con cepas autóctonas de gran importancia epidemiológica por ser las de mayor circulación, que de acuerdo con los resultados en los ensayos preclínicos, al compararla con la variante no adsorbida evidenció resultados favorables. Durante los estudios preclínicos se pudo comprobar que la formulación propuesta representada por una bacterina trivalente de células completas inactivadas y adsorbidas en gel de hidróxido de aluminio era inmunógena y protectora, comprobado esto último por confrontación de ésta frente a 10 000 DL50 de los serogrupos implicados en la vacuna. Los estudios toxicológicos (toxicidad por aplicación única y repetida) evidenciaron la no toxicidad del producto en cuestión, además de haberse demostrado por estudios anatomopatológicos- macro y microscópicos que no existían efectos indeseables en órganos inmunocompetentes como bazo, timo y médula ósea.
Los ensayos de estabilidad de la vacuna durante 1 año de conservación a 4 0C y a temperatura ambiente climatizada, demostraron que el producto era capaz de inducir protección en los animales vacunados al cabo del tiempo y condiciones de conservación. Por estos resultados obtenidos se decidió la realización del ensayo clínico de la fase I de esta vacuna, para comprobar su seguridad en los humanos e iniciar los estudios de evaluación de la inmunogenicidad.
La investigación se llevó a cabo desde el 5 de diciembre de 1994 hasta el 8 de marzo de 1995. Se realizó un ensayo clínico controlado, a doble ciegas con la participación de 80 voluntarios adultos, de los 2 sexos, en apariencia sanos, que fueron distribuidos de forma aleatoria en 2 grupos de 40 cada uno, y se constituyó un grupo de estudio y un grupo control para realizar la comparación de la reactogenicidad. Los voluntarios procedían del Instituto Capitán "San Luis", del municipio Lisa en Ciudad de La Habana. Y la condición de sanos se estableció mediante el examen clínico que incluyó interrogatorio, examen físico y pruebas de laboratorio. Estuvo previsto el tratamiento sistemático específico ante cualquier acontecimiento o reacción adversa grave que pudiera presentarse por personal capacitado, con el fin de garantizar la seguridad del voluntario.
La selección de las personas en los diferentes grupos se realizó al azar por medio de una tabla de números aleatorios. Esta selección fue realizada por un bioestadístico ajeno a la investigación.
]]> Los criterios de inclusión establecidos en el ensayo fueron voluntariedad de participación, edad entre 18 y 40 años, no presentar anticuerpos antileptospirales al realizarles las pruebas serológicas utilizadas (microaglutinación ELISA) y que el resultado de los análisis hematológicos y hemoquímicos realizados expresaran valores dentro de límites normales.Los exámenes previos a la inclusión de los voluntarios fueron: hemoglobina, leucograma, eritrosedimentación, transaminasa glutámico pirúvica, bilirrubina, orina, creatinina, glicemia y serología para VIH, las cuales se realizaron mediante las técnicas convencionales establecidas antes de comenzar el estudio.
Los criterios de exclusión establecidos fueron antecedentes referidos de enfermedades crónicas, enfermedad infecciosa aguda en el momento de realizada la investigación, tratamiento inmunosupresivo, enfermedades del sistema hematopoyético e hipersensibilidad al timerosal.
El biológico utilizado en el grupo de estudio fue la vacuna cubana, bacterina trivalente (adsorbida), las cepas y componentes básicos por dosis de 0,5 mL fueron los siguientes:
| Células de Leptospira canicola | 50 a 80 x 106 |
| Células de Leptospira icterohaemorrhagiae | 50 a 80 x 106 |
| ]]> Células de Leptospira pomona | 50 a 80 x 106 |
| Gel de hidróxido de aluminio | 1 mg |
| Timerosal | 0,05 mg |
| TFS (tampón fosfato salino) (c.s.p.) | 0,5 mL |
En el grupo control se aplicó un placebo (gel de hidróxido de aluminio) los componentes básicos fueron:
]]>| Hidróxido de aluminio | 1 mg |
| Timerosal | 0,05 mg |
| TFS (tampón fosfato salino) (c.s.p. ) | 0,5 mL |
La vacuna y el placebo fueron aplicados en dosis de 0,5 mL por vía intramuscular profunda en el músculo deltoides izquierdo. El intervalo entre dosis fue de 6 semanas.
]]> Para evaluar la reactogenicidad se tuvo en cuenta la frecuencia en que se presentarían las principales reacciones adversas con un rango que permitiera aceptar la seguridad y tolerancia a la vacuna, que fue: fiebre menor que 30 % , síntomas locales menor que 40 %, síntomas generales menor que 30 %, no presentación de reacciones severas.Los voluntarios fueron sometidos a una vigilancia médica estricta durante las 72 h posteriores a cada dosis, en la Sala de Medicina del Hospital del Instituto de Medicina Tropical "Pedro Kourí" (IPK) y se extendió su observación hasta completar 7 d de forma controlada en el centro del cual provenían, bajo la responsabilidad de los médicos clínicos del IPK que participaron en la investigación. Después se realizó una vigilancia médica pasiva durante 5 d más en el centro de procedencia por el mismo personal médico ya referido. Este procedimiento se realizó de forma similar tras la administración de la segunda dosis. Se midió la reactogenicidad de cada dosis mediante la observación diaria por el especialista clínico de las reacciones posvacunales, cada 2 h durante las primeras 12 h y cada 6 h hasta completar las 72 h restantes durante la hospitalización, o sea, que se realizaron 320 observaciones a cada grupo durante el primer día y 160 en los días restantes que duró la observación, por tanto se llegaron a realizar 640 observaciones a cada grupo en los 3 primeros días de hospitalización. Luego se midió la reactogenicidad de forma ambulatoria por el mismo especialista cada 12 h en el centro de procedencia de los voluntarios hasta completar los 7 d de observación controlada.
Las reacciones posvacunales que se evaluaron fueron:
La fiebre fue definida como la temperatura constatada por termometría axilar igual o mayor que 38 oC y la febrícula como la temperatura igual o mayor que 37 y menor que 38 oC.
Se realizó el cálculo de los porcentajes según el tipo de reacción posvacunal que se presentó tanto en el grupo de estudio como en el de control. Para la comparación entre los 2 grupos se utilizaron las pruebas de chi cuadrado, diferencia de proporciones y probabilidad exacta de Fischer, con un nivel de significación de 0,01.
La inmunogenicidad fue medida de forma cuantitativa por los títulos de anticuerpos antileptospirales. Para ello se recogieron muestras de sangre seriadas de cada uno de los participantes, a fin de evaluar la inmunogenicidad provocada por la vacuna mediante las pruebas de microaglutinación con cepas vivas según el método descrito por la OMS2 y ELISA. Fue evaluado un total de 71 muestras pertenecientes a los voluntarios incluidos en el estudio, de éstos se excluyó un total de 9 por haber causado baja del centro, y no podérselos realizar la extracción de los 21 d de la segunda dosis.
El criterio de positividad válido para la prueba de microaglutinación de serogrupos consistió en considerar como reacción cualitativa positiva aquélla en la que se obtuviese 50 % de leptospiras aglutinadas, a la cual se le cuantificó el título mediante el mismo criterio de positividad.
]]> Para el ELISA (técnica normalizada por el Laboratorio Nacional de Referencia de Leptospira del IPK en el año 1992), se tomó como criterio de positividad el valor de corte establecido considerando el valor del título a punto final (TPF) de 1/167.3.Todas las pruebas realizadas en el laboratorio fueron a ciegas, en cuanto al grupo de estudio del que provenía el suero. Las muestras de sangre fueron extraídas con la periodicidad siguiente, la primera a las 6 semanas, o sea, inmediatamente antes de aplicar la segunda dosis y la siguiente a los 21d después de la segunda dosis.
Del total de voluntarios 36 fueron del sexo femenino (45 %) y 44 del masculino (55 %). El 62,5 % de los varones recibió vacuna y el 47,5 % placebo; mientras que en el sexo femenino, el 37,5 % recibió vacuna y el 52,5 % placebo.
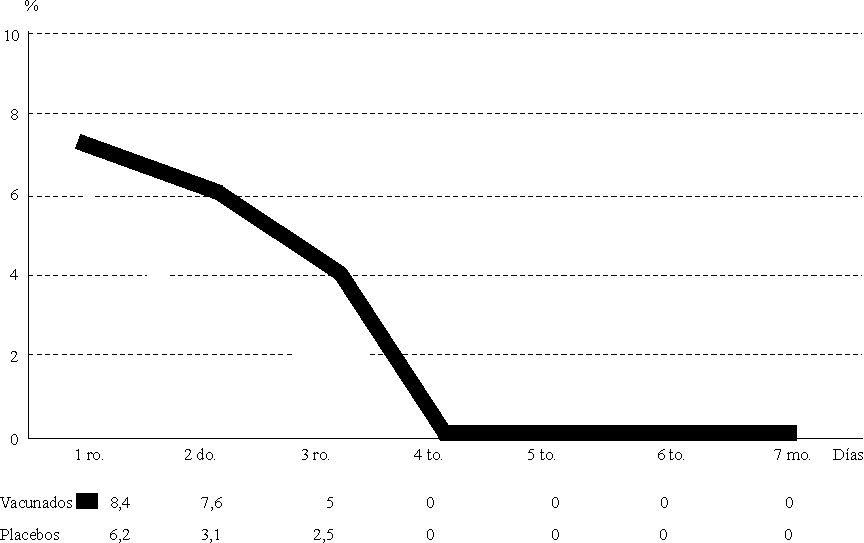
Según la frecuencia de observaciones, en la primera dosis la febrícula se presentó en el 8,4 % de los vacunados durante el primer día, mientras aparece en el 6,2 % de los que recibieron placebos sin ser estas cifras estadísticamente significativas (p 0,01). En el segundo y tercer días, la frecuencia de febrícula fue también mayor en el grupo vacunado que en el placebo, sin tener significación estadística (p 0,01) (fig.1).
Fig.1 Febrícula en vacunados y placebos. Frecuencia de observaciones según días de evaluación. Primera dosis.
Al comparar la frecuencia de febrícula entre vacunados y placebos durante la segunda dosis, observamos que fue algo menor en el grupo vacunado, no así en el grupo placebo que presenta cierto aumento, sin tener significación estadística (p 0,01) (fig.2).
Fig.2. Febrícula en vacunados y placebos. Frecuencia de observaciones según días de evaluación. Segunda dosis.
El dolor local ligero en el sitio de la inyección fue más frecuente en el grupo que recibió la vacuna que en el que recibió el placebo, durante los 3 primeros días de la primera dosis, y mostró valores significativos durante el primer día de observación (p < 0,01) (fig.3). Durante la segunda dosis disminuye en relación con la primera en los voluntarios que recibieron la vacuna, estas cifras fueron estadísticamente significativas (p < 0,01). Al analizar la frecuencia de vacunados y placebos observamos que existe un aumento del dolor en los que recibieron placebo, sobre todo durante el primer día de observación (6,5 contra 3,1 %), sin diferencia significativa entre ellos (p 0,01) (fig.4).
]]>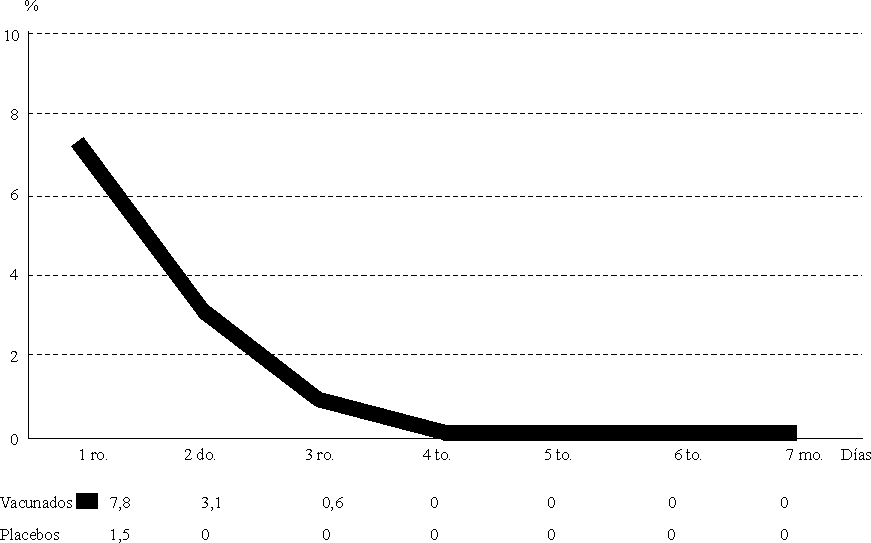
Fig.3. Dolor local en vacunados y placebos. Frecuencia de observaciones según días de evaluación. Primera dosis.
Fig.4. Dolor local en vacunados y placebos. Frecuencia de observaciones según días de evaluación. Segunda dosis.
La frecuencia de otros síntomas (tabla) se muestra baja, tanto en vacunados como en los voluntarios que recibieron placebos. Sólo se presentó cefalea y malestar general, que fueron más frecuentes durante la primera dosis (1,5 y 0,9 % en los que recibieron la vacuna contra 0,6 % en los que recibieron placebo, respectivamente).
TABLA. Cefalea y malestar general en vacunados y placebos. Frecuencia de observaciones según días de evaluación. Primera y segundas dosis
|
| Vacunados | ]]> Placebos | ||||||
|
| Cefalea | Malestar general | Cefalea | Malestar general | ||||
| Días | No. | % | No. | ]]> % | No. | % | No. | % |
| Primera dosis | ||||||||
| 1ro. | 5 | 1,5 | 3 | ]]> 0,9 | 2 | 0,9 | 2 | 0,6 |
| 2do. | 0 | 0 | 0 | 0 | ]]> 0 | 0 | 0 | 0 |
| 3ero. | 0 | 0 | 0 | 0 | 0 | ]]> 0 | 0 | 0 |
| Total | 5 | 0,7 | 3 | 0,4 | 2 | 0,3 | ]]> 2 | 0,3 |
| Segunda dosis | ||||||||
| 1ro. | 0 | 0 | 0 | 0 | 1 | 0,3 | ]]> 0 | 0 |
| 2do. | 0 | 0 | 0 | 0 | 0 | 0 | 0 | ]]> 0 |
| 3ro. | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| ]]> Total | 0 | 0 | 0 | 0 | 1 | 0,1 | 0 | 0 |
Al utilizar la técnica MAT resultaron positivos 11 voluntarios dentro del grupo vacunado para 29 %; mientras que dentro de los placebos 2 resultaron positivos para 6 %.
De los serogrupos detectados en los sueros reactivos mediante la MAT, 4 correspondieron a pomona, 4 al serogrupo ictero haemorrhagiae y 3 mostraron reacción cruzada entre los serogrupos icterohaemorrhagiae y pomona dentro del grupo vacunado. Dentro de los placebos, en un voluntario se detectó anticuerpos contra el sero-grupo pomona y otro presentó reactividad cruzada a los serogrupos icterohaemorrhagiae y canicola.
Al evaluar las muestras por la técnica ELISA, 13 vacunados estudiados fueron positivos para 34,2 % y 2 de los placebos para 6 %.
Cuando se analizan los efectos adversos de las vacunas, es importante categorizarlos en locales y sistémicos. Entre los primeros se destacan dolor, tumefacción y enrojecimiento. y entre los sistémicos, fiebre, febrícula, cefalea, malestar general, manifestaciones neurológicas y anafilaxia, entre otros.
El presente ensayo a doble ciegas mostró que la vacuna antileptospirósica cubana no produce reacción sistémica adversa severa. De las reacciones adversas asociadas con la vacuna, las más frecuentes fueron la febrícula y el dolor local ligero en el sitio de la inyección. Fue menor durante la segunda dosis y la duración fue en general de 3 d, ya que después de esos días de observación los voluntarios no presentaron sintomatología alguna.
Tanto la primera como la segunda dosis fueron recibidas por el total de voluntarios previstos, para el 100 %.
No se presentaron voluntarios con fiebre tras la aplicación de la vacuna o el placebo. La temperatura media fue de 36,2 oC en la primera dosis y 36,3 oC en la segunda.
Estos resultados son similares a los obtenidos con otro tipo de vacunas antileptospirósicas,9,10 aunque los productores de la vacuna soviética señalan que dentro de las reacciones generales que pueden presentarse en las primeras 24 h está la elevación de la temperatura corporal hasta 38,5 oC, lo que puede estar relacionado con una mayor masa de células por mililitro de estas vacunas.
Por otra parte, se diferencian notablemente de las reacciones producidas por otras vacunas con características antigénicas diferentes como los toxoides, donde algunos autores refieren que entre el 2 y el 6 % de los vacunados con TD y T T presentan fiebre de 39,0 oC o más.11
]]> Como síntoma local sólo fue referido dolor ligero en el sitio de la inyección, tanto en la primera como en la segunda dosis. Durante la primera dosis fue más frecuente en el grupo que recibió la vacuna que en el que recibió el placebo, sobre todo durante el primer día de observación. Al igual que en la febrícula, el dolor local disminuye a medida que pasan los días y está del todo ausente al tercer día de observación en ambos grupos.El dolor local es reportado por la mayoría de las vacunas que utilizan como adyuvante el hidróxido de aluminio, se reporta además, que puede producir inflamación, enrojecimiento, induración y abscesos.11 En el estudio sobre la reactogenicidad de la vacuna antileptospirósica soviética en Cuba realizado por Cruz de la Paz y otros12 no se recoge la referencia de dolor en el sitio de la inyección, aunque dicha vacuna se administra en la región interescapular por vía subcutánea en mayor volumen (2 mL). Por otro lado, en la evaluación clínica de una nueva vacuna humana contra la leptospirosis realizado por M. Torten en Israel,9 reporta haber encontrado ligeras reacciones locales posteriores a la administración de la vacuna, entre las que se destacan inflamación, enrojecimiento e induración en el sitio de inyección.
Otros síntomas generales (cefalea y malestar general) se presentaron en un número reducido de voluntarios.
No se presentaron síntomas ni signos en los 7 d siguientes que duró la observación en el centro de procedencia de los voluntarios.
La vacuna produjo una seroconversión de 29 y 34,2 % mediante las técnicas de microaglutinación y ELISA, respectivamente. Estos resultados coinciden con estudios realizados con otras vacunas (bacterinas) contra la leptospirosis humana, donde se observaron bajos títulos de anticuerpos con una buena protección (mediante la microaglutinación), medida por reto, se considera que pueden estar implicados otros mecanismos inmunológicos (respuesta celular) y que los títulos de aglutininas y la protección no se relacionan de forma necesaria.9,10 En relación con 2 voluntarios que recibieron placebos y seroconvirtieron durante el estudio, consideramos pueda deberse entre otras causas a que éstos participaron en labores agrícolas y pudieron haber adquirido la infección de forma asintomática.
Estos resultados permiten concluir que la vacuna cubana trivalente contra la leptospirosis humana es totalmente segura y muy poco reactogénica para adultos humanos en las edades comprendidas en la investigación. Las principales reacciones adversas observadas fueron febrícula y dolor local ligero en el sitio de la inyección, que desaparecen a los pocos días de observación.
A controlled double blind trial was conducted with the participation of 80 adult volunteers of both sexes, who were randomly divided into groups of 40 individuals each one. The case-base study received the vaccine and the control group was administered placebo to know the safety, the behaviour of reactogenecity, and to star the immunogenecity studies of the first Cuban vaccine against human leptospirosis. The vaccine used in the case-base study was an inactivated and trivalent vaccine containing strains of Leptospira canicola, incterohaemorrhagiae and pomona, since they have the highest circulation in the country. The results obtained showed the inocuity of the vaccine as no adverse severe reactions were detected. The general symptomatology observed was low, where as febricula was the most common general symptom. It appeared during the first 3 days of observation and there were no significant differences between the 2 group. Only a mild pain at the site of the injection was reported as a local symptom, which was more frequent in the vaccinated group than in the control group (7,8 against 1,5 %, respectively). The seroconversion obtained was of 29 % by microagglutination, and of 34,2 % by ELISA. The final results allowed to conclude that this vaccine is safe for human adults at the ages under study, and give the possibility to continue other studies in more advanced stages to complete the requierements for obtaining its license.
Subject headings: LEPTOSPIROSIS/IMMUNOLOGY; VACCINES/immunology; RANDOMIZED CONTROLLED TRIALS.
Recibido: 12 de mayo de 1997. Aprobado: 21 de julio de 1997.
Dra. Raydel Martínez Sánchez. Instituto de Medicina Tropical "Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba.