b-mercaptoetanol, e inmunotransferencia para la determinación de su especificidad. Se detectó IgA secretora en muestras de saliva comparando el AcM anti-CS obtenido en el laboratorio del Instituto de Medicina Tropical "Pedro Kourí" (IPK) con uno comercial (Sigma Chemical Co.) y se obtuvo similitud de comportamiento. El AcM contra CS (IPK) se utilizó para detectar IgA específica a LPS ogawa en personas vacunadas con una cepa atenuada de Vibrio cholerae y se encontraron diferencias evidentes entre los niveles antes y después de la inmunización. El AcM anti-CP fue utilizado para la confección de un sistema simulado, tipo ELISA. El límite de detectabilidad fue de 9,89 ng/mL.]]>
b-mercapto-ethanol. Immunotrasnference was also carried out to determine their specificity. Secretory IgA was detected in saliva specimens. The anti-SC monoclonal antibody obtained in the laboratory of the "Pedro Kourí" Institiute of Tropical Medicine (IPK) was compared with a commercial one (Sigma Chemical Co.), and a similar behaviour was observed. The monoclonal antibody against SC (IPK) was used to detect IgA specific to LPS ogawa in persons vaccinated with an attenuated strain of Vibrio cholerae. Marked differences were found between the levels before and after immunization. The anti-HC monoclonal antibody was utilized to make an ELISA-like simulated system. The detection limit was 9.89 ng/mL.]]>
Con el objetivo de determinar los niveles de IgA en las secreciones, los autores se propusieron obtener anticuerpos monoclonales (AcMs) contra esta inmunoglobulina y demostrar su posible utilización en el desarrollo de métodos de cuantificación. Se obtuvieron 6 AcM, 1 contra el componente secretor (CS) y 5 contra cadena pesada (CP) de la inmunoglobulina A (IgA) humana. Se utilizó como inmunógeno IgA purificada a partir de calostro humano. A 2 AcMs, uno contra CS y otro contra CP se les determinó el isotipo de inmunoglobulina (IgG2a e IgG1, respectivamente), se les realizó electroforesis en gel de poliacrilamida en presencia de duodecilsulfato de sodio y b-mercaptoetanol, e inmunotransferencia para la determinación de su especificidad. Se detectó IgA secretora en muestras de saliva comparando el AcM anti-CS obtenido en el laboratorio del Instituto de Medicina Tropical "Pedro Kourí" (IPK) con uno comercial (Sigma Chemical Co.) y se obtuvo similitud de comportamiento. El AcM contra CS (IPK) se utilizó para detectar IgA específica a LPS ogawa en personas vacunadas con una cepa atenuada de Vibrio cholerae y se encontraron diferencias evidentes entre los niveles antes y después de la inmunización. El AcM anti-CP fue utilizado para la confección de un sistema simulado, tipo ELISA. El límite de detectabilidad fue de 9,89 ng/mL.
Descriptores DeCS: ANTICUERPOS MONOCLONALES/inmunología; IgA SECRETORA/inmunología; COMPONENTE SECRETORIO/inmunología; HIBRIDOMAS; INMUNOGLOBULINA DE CADENA PESADA.
Las superficies del cuerpo recubiertas por mucosas, que incluyen los tractos gastrointestinal, respiratorio y urogenital, representan una amplia zona del cuerpo que es vulnerable a la colonización por muchos microorga-nismos y parásitos. La IgA secretora (IgAs) es un dímero tetravalente que predomina en la respuesta inmune humoral y puede ser beneficiosa en prevenir enfermedades de transmisión sexual, el cólera, la giardiasis y otras donde la vía principal de infección son las mucosas. Estudios recientes han demostrado que la IgAs puede neutralizar los virus dentro de las células epiteliales y puede desencadenar citotoxicidad mediada por anticuerpos en cooperación con los linfocitos, los macrófagos y potencialmente los eosinófilos. Su cuantificación en las secreciones puede ser útil en el diagnóstico de la fase aguda de algunas de estas enfermedades y para conocer los niveles de IgA específica y total que es capaz de inducir un preparado vacunal.1,2
Con el objetivo de determinar los niveles de IgA en las secreciones, nos propusimos obtener anticuerpos monoclonales (AcMs) contra esta inmunoglobulina y demostrar su posible utilización en el desarrollo de métodos de cuantificación.
Obtención del componente secretor (CS). La IgA purificada se sometió a electroforesis en gel de poliacrilamida al 10 % en presencia de duodecilsulfato de sodio (SDS) y ß-mercaptoetanol, siguiendo el método reportado por Neville.4 Las bandas obtenidas en la electroforesis fueron transferidas a papel de nitrocelulosa (0,45 mm) según el procedimiento descrito por Burnett.5 Después éste fue sumergido en solución bloqueadora (albúmina de suero bovino [BSA] 5 % en tampón carbonato-bicarbonato 0,01M pH 9,5) durante 1 h a 37 °C. La membrana fue cortada en tiras y luego éstas fueron sumergidas en solución de AcM anti-CS comercial (Sigma Chemical Co.) (1:100 en SSTF-Tween 20 al 0,05 %) durante 16 h a 4 °C. Las tiras se lavaron con SSTF-Tween 20 y se enfrentaron a una solución de conjugado anti-IgG de ratón-peroxidasa (Sigma Chemical Co.) diluido 1:500 en SSTF-T20 que contenía 0,1 % de leche descremada. La reacción antígeno-anticuerpo fue revelada sumergiendo las membranas en una solución de sustrato (4 mg de diaminobencidina, 10 mL H2O2 30 % y 10 L SSTF) y detenida con lavados de agua destilada. La zona de la banda identificada por el AcM contra CS fue cortada y utilizada como inmunógeno.
Inmunización de animales. Se emplearon ratones Balb/c hembras hembras de 18 ± 2 g de peso al inicio del experimento. La banda correspondiente al CS en el gel fue disuelta en 450 ± 50 mL de dimetilsulfóxido (DMSO) y se mezcló con adyuvante completo en la primera inoculación y con incompleto en las 2 inmunizaciones restantes. Se calculó aproximadamente 20 mg por ratón en cada dosis. La primera por vía intraperitoneal y las restantes por vía subcutánea. La última inoculación y el booster (vía intravenosa) se le administró al ratón con IgA secretora total purificada. El tiempo entre dosis fue de 15 d.
Fusión con polietilenglicol (PEG). Los hibridomas fueron obtenidos a partir de las células esplénicas de los ratones inmunizados y células de un mieloma de ratón (SP20.Ag14), se utilizó como agente fundente el PEG 3700 (Sigma Chemical Co.). Los procedimientos básicos para la producción de hibridomas, así como el cultivo de éstos, han sido descritos por otros autores.6
Tamizaje primario de hibridomas por ELISA. Las placas de poliestireno (Nunc Maxisorp) se recubrieron con IgAs purificada a concentraciones de 5 mg/mL con tampón carbonato-bicarbonato 0,01 M; pH 9,6. Luego de 16 h en cámara húmeda las placas se lavaron 4 veces con SSTF-Tween 20 al 0,05 % durante 5 min y se bloquearon durante 1 h con leche descremada al 5 %. Más tarde se añadieron los sobrenadantes que se iban a ensayar y se incubaron durante 1 h, se procedió a un nuevo lavado y a la adición de una anti-Igs de ratón conjugada con peroxidasa (1: 1 000) (Sigma Chemical Co.). Al final se incubaron durante 1 h y se lavaron de igual forma y se les añadió el sustrato (20 mg de ortofenilendiamina, 20 mL H2O2, 50 mL tampón citrato- fosfato pH 5). La reacción se detuvo con ácido sulfúrico al 12,5 % y la absorbancia se leyó a 492 nm. Se utilizaron como controles positivos un anticuerpo monoclonal anti-componente secretor comercial (Sigma Chemical Co.), suero de los ratones inmunizados y como control negativo suero de ratón normal y medio de cultivo de pocillos donde no se observaba el crecimiento de híbridos. Como valor de corte para determinar los híbridos positivos se tomó 5 veces el valor de la densidad óptica de los sobrenadantes de los pozos donde no se observaba crecimiento celular.
Selección de hibridomas positivos a CS y cadena pesada (CP). La selección de los hibridomas positivos a CS y CP se realizó por inmunotransferencia utilizando como controles un AcM anti-CS comercial y el suero policlonal de ratones inmunizados con IgAs, con este último se reconocieron las 3 bandas características (CS, CP y cadena ligera [CL]) correspondientes a IgAs pura en condiciones de reducción.
Clonaje y reclonaje de hibridomas. Los hibridomas de interés fueron clonados y reclonados por el método de dilución limitante.7
Determinación de isotipos de inmunoglobulinas. Se realizó con las indicaciones del kit comercial de isotipaje Iso-1 (Sigma Chemical Co.).
Producción in vivo de anticuerpos monoclonales. Para la obtención de líquido ascítico se utilizaron ratones Balb/c previamente irritados en la cavidad peritoneal con 0,3 mL de Pristane (Sigma Chemical Co.), los hibridomas en fase exponencial de crecimiento en medio de cultivo RPMI-1640 suplementado con 10 % de suero fetal de ternera, fueron desprendidos, lavados 2 veces en SSTF y centrifugados a 1 500 rpm durante 10 min a 4 EC. Más tarde las células se contaron en cámara de Neubauer y se inocularon por vía intraperitoneal en ratones Balb/c a la concentración de 1 x 106 en 1 mL de SSTF por ratón. Entre los 10 y 14 d, se procedió a extraer el líquido ascítico. Los restos celulares y coágulos de fibrina fueron eliminados mediante centrifugación a 3 000 rpm durante 30 min, filtrados a través de una membrana de 0,45 mm y guardados a -70 °C hasta su posterior utilización.
Purificación de los anticuerpos monoclonales. La purificación se realizó mediante una cromatografía de afinidad y se utilizó como matriz proteína A sepharose fast flow. Se equilibró la columna con SSTF, pH 7,2; seguidamente se procedió a la aplicación del líquido ascítico diluido 5 veces en este mismo tampón. La elución específica del AcM se realizó con tampón citrato al pH correspondiente según el isotipo de éste ( IgG1, pH 6 y IgG2a, pH 5).A las fracciones de los AcMs colectadas se les determinó la concentración de proteínas y su actividad biológica mediante el ELISA antes descrito.
]]> Determinación del componente secretor por ELISA. Para evaluar la presencia de IgAs en muestras de saliva se utilizó un sistema de ELISA de doble anticuerpo. Las placas fueron recubiertas durante toda la noche con 10 mg/mL de un anti-IgA total producido en carnero (Sigma Chemical Co.). Éstas fueron lavadas y bloqueadas con leche descremada al 5 %. Después se adicionaron 100 mL de 10 muestras de saliva (1:2) en los pozos de las placas e incubadas a 37 °C durante 1 h. Después de lavados sucesivos se adicionó comparativamente un AcM anti-CS comercial, subclase IgG1 (Sigma Chemical Co.) y el AcM anti-CS IPK (obtenido en el Instituto de Medicina Tropical "Pedro Kourí" [IPK]), a las diluciones de trabajo correspondientes 1:5 000 y 1:500, de forma respectiva. Se incubaron durante 1h a 37 °C, se lavaron con SSTF-Tween 20 e incubaron 1h a 37 °C con una anti-IgG de ratón conjugada con peroxidasa (Sigma Chemical Co.) a una dilución de 1:1 000. Después de una nueva etapa de lavado la reacción se reveló con la adición del sustrato (20 mg de ortofenilendiamina, 20 mL de H202 al 30 % en 50 mL de tampón citrato- fosfato 0,1 M; pH 5,0) durante 15 min a temperatura ambiente. La reacción se detuvo entonces por la adición de H2SO4 al 12,5 % y fue leída a una absorbancia de 492 nm (Reader 510 Organon Tecknika).Determinación de IgA anti-LPS ogawa de cólera en saliva por ELISA. Se estandarizó un sistema de ELISA para detectar IgA específica a LPS ogawa de cólera en saliva. Fueron recubiertas con este antígeno placas (Nunc Maxisorp) a una concentración de 25 mg/mL durante 16 h. Los sitios de unión no específicos fueron bloquedos con 5 % de leche descremada. Más tarde se adicionaron las muestras de saliva (1:2) de 7 voluntarios a tiempo 0 y 9 (días) después del inóculo de una cepa atenuada de cólera (4 casos) o placebo (3 casos). Luego de lavados con SSTF-Tween 20 se adicionó el AcM anti-CS IPK a una dilución de 1:500. Las placas fueron lavadas de nuevo posteriormente y se añadió un conjugado anti-ratón peroxidasa (Sigma Chemical Co.) 1:500. La reacción se reveló con la adición del sustrato (20 mg de ortofenilendiamina, 20 mL de peróxido de hidrógeno al 30 % en 50 mL de tampón citrato-fosfato 0,1 M; pH 5,0), detenida con H2SO4 al 12,5 % y leída a 492 nm.
Sistema simulado para la detección de IgA sérica. Se utilizó el AcM anti-CP humana (IPK) como recubrimiento (Placa Nunc Maxisorp) a una concentración de 5 mg/mL y se incubó toda la noche a 4 °C. Se lavaron las placas con SSTF-Tween 20 al 0,05 %. Los sitios libres se bloquearon con leche descremada al 5 % en SSTF; posteriormente se incubaron diluciones seriadas de IgA purificada a partir de sueros (cromatografía de afinidad agarosa-jacalina) a concentraciones desde 4 mg/mL- 3,9 ng/mL en SSTF. Luego de 1h a 37 °C de incubación la placa fue lavada con SSTF-Tween 20 y después se le adicionó una solución de conjugado anti-IgA humana peroxidasa (Sigma Chemical Co.) en una dilución de 1:1 000. La reacción fue revelada utilizando como sustrato (20 mg de ortofenilendiamina, 20 mL de H2O2 al 30 % en 50 mL de tampón citrato-fosfato 0,1M, pH 5,0), detenida con la adición de H2SO4 12,5 % y leída a 492 nm.
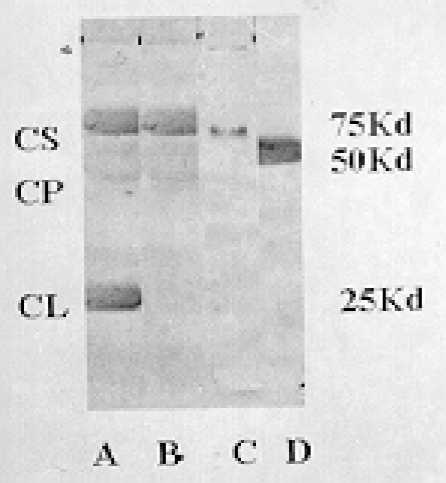
Se obtuvo la IgAs a partir de una cromatografía de afinidad agarosa-jacalina. La fracción específica fue sometida a SDS-PAGE en condiciones de reducción, se obtuvieron las 3 bandas características correspondientes a la molécula de IgAs: CS,CP y CL (cadena ligera) con pesos moleculares aproximados de 75,50 y 25 kD, respectivamente (fig. 1).
Fig. 1. Inmunotransferencia de IgAs purificada.
Carril A: Suero de ratón inmunizado con IgAs. Carril B: AcM anti-componente secretor comercial (Sigma). Carril C: AcM purificado anti-componente secretor. 2B2 (IgG2a). Carril D: AcM purificado anti-cadena pesada. 2A2 (IgG1).
Revelado con anti-IgG de ratón conjugado con peroxidasa.
]]> Los títulos anticuerpos obtenidos en suero con el esquema de inmunización utilizado fueron superiores a 1/20 000. Los sueros detectaron fundamentalmente las bandas correspondientes a CS y CP.A partir de la fusión con PEG se originaron cultivos primarios de hibridomas de los cuales 45 fueron positivos a IgA en el tamizaje primario. De los híbridos positivos seleccionamos 1 que reconocía la banda correspondiente a CS y 5 a la CP. Estos hibridomas fueron clonados y reclonados, y se seleccionó el clon correspondiente a CS (IgG2a) y uno a CP (IgG1). Aquellos hibridomas que reconocieron CL fueron descartados del estudio.
A continuación, estos anticuerpos fueron utilizados en sistemas tipo ELISA para determinar sus posibilidades en el diagnóstico y cuantificación de la IgA. Para evaluar la presencia de IgA secretora en muestras de saliva se utilizó un sistema de ELISA de doble anticuerpo. En este sistema se compararon los valores medios de densidad óptica (DO) 492 nm obtenidos mediante el AcM anti-CS (IPK) con uno comercial (Sigma Chemical Co.). Los 2 anticuerpos mostraron comportamientos similares. Los valores de absorvancia para los AcM (IPK) y comercial (Sigma) fueron 1,12 ± 0,06 y 0,85 ± 0,05.
En la figura 2 se observa que el AcM anti-CS del IPK es capaz de detectar niveles de IgAs específica a LPS ogawa en individuos vacunados con una cepa atenuada de Vibrio cholerae.
Fig. 2. Determinación de IgAs anti-LPS ogawa en saliva de inmunizados con cepa atenuada y placebo.
Para la realización de un sistema simulado para la detección de IgA sérica se confeccionó una curva patrón, con la parte lineal se determinó el límite de detección de IgA. El AcM anti-CP (IPK) fue capaz de detectar 9,89 ng de IgA utilizando como criterio de sensibilidad la media de los blancos + 2 DE (fig. 3).
Un número significativo de evidencias clínicas y experimentales sugieren que la IgA desempeña una función importante en la protección contra aquellas enfermedades que tienen como vía de entrada las mucosas.8,9
La jacalina, una lectina obtenida del fruto de Artocarpus heterophyllus, es capaz de precipitar IgA humana (IgA1 mayoritariamente), tanto en suero como en secreciones, por su capacidad de unión a D-galactosa.3
El componente secretorio es una molécula con muy baja inmunogenicidad, por lo que era necesario, para obtener monoclonales contra ella, diseñar algún procedimiento que permitiera de una forma sencilla su purificación y un incremento en su capacidad inmunogénica.
Por tal motivo se realizó un primer paso de purificación mediante precipitación por punto isoeléctrico, se eliminaron algunas proteínas contaminantes del calostro humano por centrifugación y el sobrenadante que contenía IgAs se purificó por cromatografía de afinidad en una columna agarosa-jacalina. La fracción específica se sometió a una electroforesis en geles de poliacrilamida en presencia de SDS en condiciones reductoras con el objetivo de verificar la pureza de la IgAs (fig.1).10
Los altos títulos obtenidos en los sueros de los ratones indican que la metodología utilizada fue satisfactoria. La mezcla DMSO-nitrocelulosa-proteína no fue toxigénica para los ratones utilizados. Los sueros de los ratones inmunizados detectaron fundamentalmente las bandas de CS y CP por que en el esquema de inmunización, hubo 2 enfrentamientos (última inoculación y booster) del sistema inmune a la molécula de IgAs completa. Similares resultados fueron encontrados por Knudsen11 en 1985, cuando utilizaron este procedimiento para obtener anticuerpos policlonales monoespecíficos en conejos.
En la figura 2 se encontró que existen diferencias evidentes en los niveles de IgA específica antes y después de la inmunización en 3 de los 4 casos inmunizados y no respuesta en los placebos. Sólo estos 3 positivos mostraron niveles de IgA específica en saliva.
Los sistemas de detección tipo ELISA han sido ampliamente utilizados para medir los niveles de IgA.12,13 Con este objetivo el AcM anti-CP se utilizó para la confección de un sistema simulado tipo ELISA, que demostró una alta sensibilidad en este ensayo (fig. 3).
De estos resultados se puede concluir que estos anticuerpos monoclonales pueden ser útiles en la detección de IgA secretora y sérica en inmunoenzayos tipo ELISA así como en la purificación de esta inmunoglobulina. ]]>
Queremos agradecer la asistencia técnica de Ana Rosa Martínez en algunos experimentos y en el manejo de los animales de experimentación.
In order to determine the IgA levels in secretions, the authors engaged themselves to obtain monoclonal antibodies against this immunoglobulin and to show their possible utilization in the development of quantitation methods. 6 monoclonal antibodies were obtained: one against the secretoy component (SC) and five against the heavy-chain (HC) of IgA. IgA purified from human colostrum was used as immunogen (HC). The immunoglobulin isotypes (IgG2a and IgG1) were determined in 2 monoclonal antibodies, one against SC and the other against HC. Polyacrylamide gel electrophoresis was performed in the presence of sodium dodecyl sulphate and b-mercapto-ethanol. Immunotrasnference was also carried out to determine their specificity. Secretory IgA was detected in saliva specimens. The anti-SC monoclonal antibody obtained in the laboratory of the "Pedro Kourí" Institiute of Tropical Medicine (IPK) was compared with a commercial one (Sigma Chemical Co.), and a similar behaviour was observed. The monoclonal antibody against SC (IPK) was used to detect IgA specific to LPS ogawa in persons vaccinated with an attenuated strain of Vibrio cholerae. Marked differences were found between the levels before and after immunization. The anti-HC monoclonal antibody was utilized to make an ELISA-like simulated system. The detection limit was 9.89 ng/mL.
Subject heading: ANTIBODIES, MONOCLONAL/immunology; IGA, SECRETORY/; immunology; SECRETORY COMPONENT/immunology; HYBRIDOMAS; IMMUNOGLOBULINS, HEAVY-CHAIN.
Recibido: 4 de marzo de 1998. Aprobado: 10 de septiembre de 1998.
Lic. Ricardo Marcet Sánchez. Instituto de Medicina Tropical "Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba. E.mail: ciipk@infomed.sld.cu
1 Investigador Agregado. Instituto de Medicina Tropical "Pedro Kourí" (IPK).
2 Especialista en Inmunología. IPK.
3 Estudiante de Doctorado (IPK). Universidad del Quindío. BID-Colciencias. Colombia.
4 IPK.
5 Especialista en Microbiología. Investigadora Titular. Instituto "Finlay".
6 Especialista en Inmunología y Microbiología. Investigador Titular. Instituto "Finlay". ]]>