Dra. Beatriz Sierra Vázquez,1 Dra. Ana B. Pérez Díaz,1 Lic. Valexis Vázquez Villasuso,2 Lic. Rayner Rodríguez Díaz,3 Lic. Gissell García Menéndez4 y Dra. María Guadalupe Guzmán Tirado5autores
Se estudió la respuesta inmune celular a la proteína de envoltura del dengue 2. Para ello se evaluó la capacidad linfoproliferativa de linfocitos T obtenidos a partir de esplenocitos de los ratones inmunizados con dicha proteína al ser estimulados con la proteína en cuestión y con virus dengue 2. Se pudo comprobar que los esplenocitos de los animales inmunizados con la proteína de envoltura del virus dengue 2 proliferaron significativamente en respuesta a ambos tipos de antígenos virales, por lo general, fueron más altos los valores de los índices de estimulación en respuesta al virus completo que a la proteína. De lo anterior se concluyó que la proteína de envoltura del virus dengue 2 purificada es capaz de generar respuesta de células T antígeno específica y de memoria contra el virus dengue 2.
Descriptores DeCS: VIRUS DEL DENGUE; INMUNIZACION; LINFOCITOS T; VACUNAS VIRALES/uso terapéutico.
La familia Flaviviridae incluye un gran número de arbovirus patogénicos para los humanos, causantes de serios problemas de salud en muchas partes del mundo, entre los que se destaca el virus del dengue.1 El reto para el desarrollo de una nueva vacuna es estimular la respuesta inmune protectora sin los riesgos de las consecuencias inmunopatológicas.2 Los datos obtenidos de los estudios acerca de la inmunogenicidad de esta proteína así como de protección pasiva y activa han mostrado que las proteínas estructurales son primariamente responsables de la inducción de respuesta inmune protectora contra la enfermedad.3-5 Por esto, la mayor parte de los estudios encaminados al desarrollo de vacunas de subunidad han utilizado estas proteínas como inmunógenos potenciales.
Las investigaciones llevadas a cabo con glicoproteínas de envoltura recombinantes han mostrado que ellas no exhiben necesariamente la misma actividad de la proteína nativa, esto sugiere que la presencia de epitopes específicos capaces de inducir respuesta inmune protectora pudiera depender de la estructura terciaria de las proteínas, por lo que se debe obtener un plegamiento correcto de la proteína en el desarrollo de vacunas a partir de proteínas recombinantes, lo cual no siempre se logra. Es de interés entonces continuar y profundizar los estudios inmunológicos sobre las proteínas nativas como una alternativa de vacuna de subunidad.6
En el trabajo se evalúa la capacidad de la proteína de envoltura del virus dengue 2, purificada por cromatografía de afinidad, de inducir respuesta inmune celular serotipo específica. Los resultados obtenidos contribuyen a valorar su participación en los mecanismos inmunológicos protectores, aspecto de gran importancia en la evaluación de este antígeno con vistas a una vacuna de subunidad a partir de este virus.
Se inmunizaron 15 ratones Balb/C, machos entre 6 y 8 semanas de edad, con la proteína de envoltura del dengue 2 obtenida por cromatografía de afinidad,7 a razón de 60 mg de proteína en 250 mL de tampón fosfato salina (PBS) más 250 mL de adjuvante completo de Freund en la primera dosis e incompleto en las restantes, por vía intramuscular (100 mL), intraperitoneal (200 mL) y subcutánea (200 mL, 50 mL por sitio de inoculación) cada 15 d durante 8 semanas. Se usaron como controles 15 ratones con iguales características, los cuales fueron inmunizados en idénticas condiciones utilizando PBS.
Los animales se sacrificaron 10 d después de la última dosis, se les extrajeron los bazos y por perfusión repetida de éstos con solución balanceada de Hank se obtuvo una suspensión celular que se centrifugó a razón de 200 gravedades, a 4 ° C durante 10 min. El botón de células obtenido se sometió a una solución hemolisante de NH4Cl por 10 min a 4 ° C y se lavó en 3 ocasiones en condiciones idénticas a las ya mencionadas. Las células se contaron, se ajustaron a 2 + 106 células por mL y se cultivaron a razón de 200 000 células por pozo en 100 m L de RPMI 1640 suplementado (penicilina 100 UI/mL, estreptomicina 10 m g/mL, glutamina 1mM, suero de ternera fetal al 10 %), a 37 ° C, 5 % de CO2, ambiente húmedo frente a 2 concentraciones de la proteína de envoltura del dengue 2 y del virus dengue 2 (1 y 10 m g/mL) obtenido este último a partir de cultivo en células Vero por ultracentrifugación en gradiente continuo de sacarosa.8 Después de 4 d de cultivo y tras un pulso con [3H] timidina (1 m Ci/pozo) por 18 h se cosecharon las células y se midió la incorporación de timidina. Los resultados se expresaron como índice de estimulación (cociente de los conteos por minuto de las muestras entre los conteos por minuto del control de síntesis espontánea de ADN). Todos los casos se montaron por triplicados y se empleó como control positivo un mitógeno (Phytohemaglutinina) y como control de la especificidad de la respuesta se utilizó antígeno de células Vero.9
Los esplenocitos de los animales inmunizados con la proteína de envoltura del virus dengue proliferaron en respuesta a ambos tipos de antígenos virales, por lo general fueron más altos los valores de los índices de estimulación en respuesta al virus completo que a la proteína (fig.).
]]>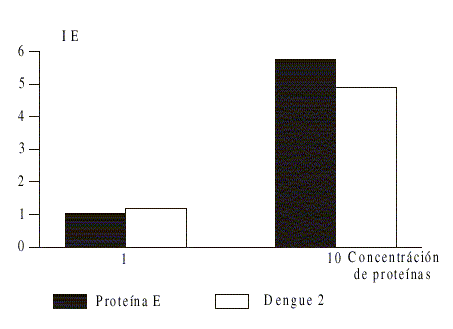
Fig. Respuesta proliferativa al virus dengue 2 y a la proteína de envoltura. Los esplenocitos de los ratones inmunizados con la proteína de envoltura del virus dengue 2 fueron incubados con 2 concentraciones de ambos antígenos. Se obtuvo una respuesta con 10 m g / mL (índice de estimulación ³ 2).
IE: Índice de estimulación .
La respuesta fue dengue virus específica, como lo demostró el fallo de antígeno de células Vero en inducir respuesta proliferativa. Los esplenocitos de los ratones inmunizados con PBS no mostraron respuesta proliferativa específica a los antígenos de virus dengue. La respuesta dependió de las concentraciones de los antígenos, observándose estimulación a la dosis de 10 m g/mL.
Definir los epitopes del virus dengue que pueden estar involucrados en la protección o en la reacción inmunopatológica o ambos es de extremo interés en el desarrollo de vacunas.1 En el trabajo se ha demostrado que la proteína de envoltura del virus dengue 2 purificada por cromatografía de afinidad es capaz de generar respuesta de memoria de linfocitos T CD4+ específicos de virus dengue capaces de reconocer y de proliferar ante el virus completo.
Esto reviste gran importancia si se analiza la proteína como posible candidato vacunal ya que, en primer lugar, la eficiencia de una vacuna de subunidad depende de su capacidad para generar una respuesta inmune contra el microorganismo completo. En segundo lugar uno de los parámetros que confieren efectividad a un posible inmunógeno es su potencialidad de inducir una respuesta celular significativa, más aun si se trata de lograr inmunidad contra un microorganismo intracelular obligado como los virus, para cuya eliminación los efectores de la respuesta inmune celular desempeñan una función central.
En la actualidad, los autores evalúan la capacidad de la proteína de envoltura de generar respuesta proliferativa serotipo cruzada, es decir, a los serotipos 1, 2 y 3 de virus dengue, lo cual reviste extrema importancia puesto que en el caso de este virus es necesario lograr un candidato vacunal que produzca protección contra los 4 serotipos. Aunque en este primer acercamiento al estudio de la respuesta inmune celular al virus dengue por parte del laboratorio donde se realizó el trabajo no se ha llegado hasta la caracterización fenotípica y funcional de las células estimuladas, se ha reportado que son las células CD4+ del fenotipo auxiliador, las involucradas en la respuesta de hipersensibilidad retardada a virus dengue10 y según se ha reportado por Kurane y otros son también responsables de respuesta citotóxica contra las células infectadas por el virus.11 De forma alternativa estas células podrían proporcionar ayuda para la producción de anticuerpos o la generación de células T citotóxicas y producir gamma interferón, el cual podría incrementar la expresión de receptores para el fragmento Fc de los anticuerpos y contribuir al proceso inmunopatológico que origina la fiebre hemorrágica por dengue observada en infecciones secundarias.12 Se hace necesario entonces en próximos estudios profundizar en la caracterización fonotípica y funcional de las células inducidas por la proteína de envoltura a fin de conocer en qué medida está compuesta esta población por linfocitos CD4+, qué patrón de citoquinas predomina, y qué medida puede el predominio de unas citoquinas sobre otras intervenir en la aparición de protección o daño inmunopatológico.13
No obstante, los autores consideran que la conclusión a la cual se arriba en el trabajo acerca de la capacidad de la proteína de envoltura del virus dengue purificada por ellos de generar respuesta de células T antígeno específica y de memoria contra virus dengue 2 es un aporte a los estudios encaminados al desarrollo de vacunas de subunidad contra virus dengue.
The cellular immune response to dengue type 2 virus envelope protein was studied. To this end, the lympho-proliferative capacity of T-lymphocytes obtained from splenocytes of animals inmunized with the protein when they were stimulated by such protein and dengue 2 virus. It was realized that splenocytes proliferated significantly in response to both types of viral antigens and that the values of stimulation indexes were higher in response to the whole virus than to the protein alone. Based on the above-mentioned, it was concludes that purified dengue 2 virus envelope protein was capable of generating specific and memory responses of antigen T-cell to dengue 2 type virus.
Subject headings: DENGUE VIRUS/inmunol; IMMUNIZATION; T-LYMPHOCYTES; VIRAL VACCINES/ /inmunol.
Recibido: 3 de abril de 1998. Aprobado: 11 de septiembre de 1998.
Dra. Beatriz Sierra Vázquez. Instituto de Medicina Tropical "Pedro Kourí". Apartado 601, Marianao 13, Ciudad de La Habana, Cuba.
E.mail:ciipk@infomed.sld.cu
1 Especialista de I Grado en Inmunología.
2 Máster en Virología. Licenciado en Microbiología. Aspirante a Investigador.
3 Máster en Virología. Licenciado en Microbiología.
]]> 4 Licenciado en Bioquímica.5 Doctora en Ciencias Biológicas. Especialista de II Grado en Microbiología. Investigadora Titular. Profesora Titular.