Valor obtenido U/mL/ Valor teórico U/mL x 100
Siendo el valor teórico = Concentración calculada x volumen de la muestra evaluada/ Volumen de la muestra evaluada + volumen de la muestra libre de anticuerpos.
Se consideró como óptimo un porcentaje de recuperación entre el 90-110 % y aceptable entre 80 - 90 % y 110 - 120 %.
- Paralelismo. Para la prueba de paralelismo se tomaron 5 muestras con concentraciones variables. A cada una se le realizaron diluciones seriadas desde 1:800 hasta 1:3 200 y se realizaron 4 repeticiones de cada dilución. Se consideró como óptimo si la dispersión de los valores era inferior al 10 %.
- Linealidad. Se tomaron 24 muestras que presentaban concentraciones entre 20 000 y 5 000 U/mL y se hicieron 12 parejas que combinaban las de mayor y menor concentración. Se aplicaron 4 veces las muestras individuales y las mezclas en la placa. Como excelente se consideraron los valores ±_10 % con respecto al valor teórico.
- Detectabilidad. Para el estudio del límite de detectabilidad se realizaron 18 repeticiones de blanco reactivo en 3 placas diferentes y se le calculó la media (
 ) y la desviación estándar (DE) para cada placa. La detectabilidad se calculó por la fórmula X ± 2 DE.
) y la desviación estándar (DE) para cada placa. La detectabilidad se calculó por la fórmula X ± 2 DE.
RESULTADOS
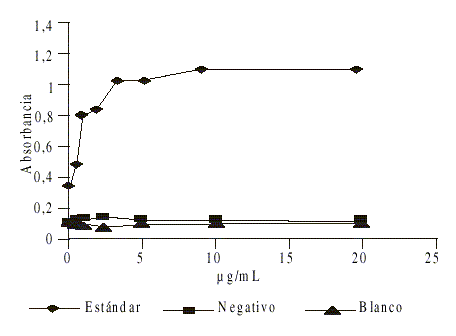
Los valores de absorbancia aumentan proporcionalmente a la concentración de recubrimiento hasta 10 m g/mL, a partir del cual se mantienen constantes, como concentración óptima de recubrimiento se tomó 20 m g/mL (fig. 1).
Fig. 1. Concentración óptima de recubrimiento.
El coeficiente de variación intraensayo (tabla 1) medido para 5 concentraciones y repetido en 3 placas diferentes es menor que el 10 % en el 2do., 3er. y 4to. segmentos de la curva y entre 10 y 15 % en el 1ro. y 5to. segmentos. Un comportamiento similar ocurre con el coeficiente de variación interensayo, como CV promedio se obtuvo 9,09 %. En el caso del coeficiente de variación total se logró un CV promedio de 12,30 % y en todos los casos el CV fue inferior al 20 % (tabla 2).
]]> TABLA 1. Precisión intraensayo del ELISA de proteína VA-MENGOC-BC®
TABLA 2. Precisión interensayo y total del ELISA de proteína VA-MENGOC-BC®
]]>
|
| Interensayo | Total | ||||
| Muestras |
CV (%) |
DE (U/mL) | ]]> CV (%) | |||
| 1 | 17 022 | 2 832 | 16,63 | 17 022 | 27,82 | 16,34 |
| 2 | 9 972 | ]]> 406 | 4,07 | 9 972 | 817 | 8,19 |
| 3 | 4 932 | 304 | 6,16 | 4 932 | ]]> 443 | 9,98 |
| 4 | 2 588 | 165 | 6,37 | 2 588 | 276 | 10,66 |
| 5 | ]]> 1 399 | 171 | 12,22 | 1 399 | 243 | 17,36 |
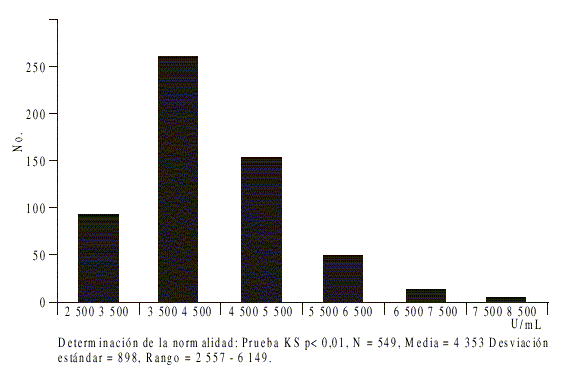
El rango del suero control fue entre 2 557 y 6 149 describiendo una distribución normal según la prueba de Kolmogorov Smirnov (fig.2). El rango de la curva se extiende desde 20 000 U/mL hasta 625 U/mL. El análisis de correlación entre el estándar secundario y el estándar de referencia mostró un coeficiente de correlación de 0,9958 con pendiente 1,0253 e intercepto de -132,47 (fig. 3).
Fig. 2. Rango del suero control del ELISA de proteína de VA-MENGOC-BC®.
]]>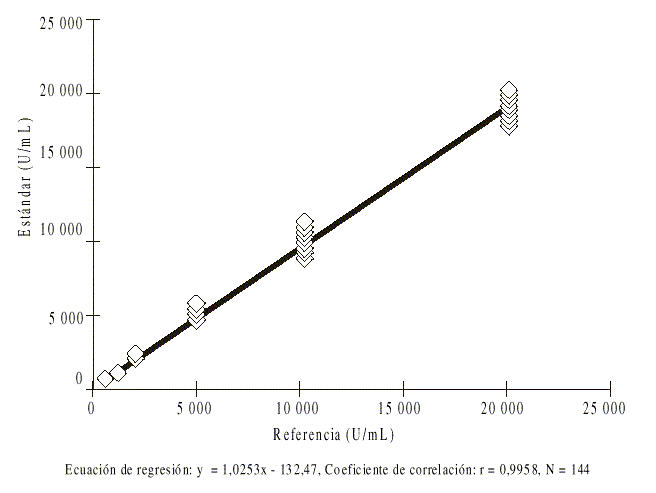
Fig. 3. Correlación entre el estándar secundario y el de referencia.
La recuperación del sistema entre los segmentos 2do., 3ro. y 4to. se encuentra dentro de los valores óptimos y en el 1ro. y 5to. segmentos discretamente superiores. La recuperación promedio fue de 99,78 % (tabla 3). La prueba de paralelismo realizada para 5 muestras en 3 diluciones diferentes mostró un comportamiento similar en el rango de medición evaluado (fig. 4). En todos los casos el CV fue menor que 10 %.
TABLA 3. Recuperación del ELISA de proteína VA-MENGOC-B®
|
| Valor esperado | Valor obtenido | Recuperación |
| ]]> Muestra | (U/mL) | (U/mL) | (%) |
| 1 | 20 000 | 17 022 | 85,11 |
| 2 | 10 000 | ]]> 9 772 | 99,72 |
| 3 | 5 000 | 4 932 | 98,64 |
| 4 | 2 500 | 2 588 | 103,54 |
| ]]> 5 | 1 250 | 1 399 | 111,92 |
En la prueba de linealidad se obtuvieron valores entre 93 y 108 % respecto al valor teórico (tabla 4). Se detuvo una detectabilidad de 700 U/mL, para una n = 54, X = 281 y DE = 209,5.
TABLA 4. Linealidad del ELISA de proteína VA-MENGOC-BC®
| Muestra X | ]]> Muestra Y | Valor esperado | Valor obtenido |
|
| (U/mL) | (U/mL) | X + Y (U/mL) | X + Y (U/mL) | % |
| 4 045 | ]]> 11 495 | 7 770 | 7 836 | 100,8 |
| 3 031 | 9 144 | 6 087 | 6 490 | 106,6 |
| 4 436 | ]]> 15 407 | 9 922 | 9 446 | 95,2 |
| 4 426 | 9 490 | 6 958 | 6 498 | 93,4 |
| 5 101 | ]]> 8 566 | 6 834 | 6 545 | 95,8 |
| 6 330 | 11 937 | 9 134 | 9 452 | 103,5 |
| 7 748 | ]]> 10 079 | 10 913 | 10 302 | 94,4 |
| 7 607 | 2 995 | 5 301 | 5 661 | 106,8 |
| 11 893 | ]]> 3 834 | 7 863 | 7 508 | 95,5 |
| 6 981 | 3 932 | 5 456 | 5 896 | 108,1 |
| 12 031 | ]]> 5 573 | 8 802 | 9 145 | 103,9 |
| 11 533 | 3 697 | 7 615 | 7 669 | 100,7 |
DISCUSIÓN
]]> VA-MENGOC-BC® es la única vacuna comercialmente disponible en el mundo para el serogrupo B,7 por este motivo fue necesario validar un ELISA de tipo indirecto que utiliza las vesículas de membrana externa de la vacuna como antígeno de captura, de ahí que sea el único ELISA con estas características disponible en la actualidad y útil para evaluar la efectividad y eficacia de este preparado vacunal.Para la validación del ELISA se analizaron diferentes parámetros como: concentración óptima de recubrimiento, selección de la curva estándar, correlación entre el estándar secundario y el de referencia, precisión y exactitud.
En los ELISA de tipo indirecto debe seleccionarse como concentración óptima de recubrimiento aquélla que se encuentre en la zona de meseta. En la figura 1 se muestran las densidades óptimas (DO) obtenidas con las diferentes concentraciones de recubrimiento. Las densidades más altas se observaron a partir de la concentración de 10 m g/mL y se mantuvieron luego constantes, lo que coincide con lo reportado por algunos autores.14 Tomando como base este resultado, se decidió utilizar 20 m g/mL para la sensibilización de las placas en nuestro ensayo, y garantizar así un recubrimiento óptimo.
La dispersión obtenida de los resultados de una muestra procesada varias veces se define como precisión y para su evaluación exploramos la intraensayo, interensayo y el total. Empleamos como criterio de calidad óptimo el alcanzar un CV menor que 10 % para el análisis intraensayo, y entre 10 y 20 % para el interensayo y el total, por lo que puede valorarse como buena la precisión alcanzada en esta prueba. En el interensayo, el 1er. y 5to. segmentos presentan una menor precisión, aunque menor que el 20 %, dada por la baja concentración de la muestra y por tanto, menores DO en el segmento inferior (5to. segmento) y por una menor pendiente en el caso del segmento superior (1er. segmento).
El rango del suero control mostró una distribución normal (fig. 2) y se ubicó entre el segundo y el cuarto puntos de la curva según la dilución de trabajo, siendo este segmento óptimo en términos de precisión y exactitud. Este rango permite controlar la calidad de la preparación de la curva estándar, ya que los ensayos sólo deben ser aceptados cuando el suero control muestre valores de concentración dentro de éste.
Se preparó una curva estándar de 6 puntos a partir de una dilución 1:200 hasta 1:6 400. El rango de la curva permitió cuantificar entre 20 000 y 625 U/mL con la dilución de trabajo de 1:200, a esta dilución, los valores de concentración de IgG anti-proteína B de la mayoría de las muestras de suero estudiadas con este sistema, se encuentran dentro del rango de valores de la curva estándar, lo que nos permite confirmar la utilidad de la dilución de trabajo seleccionada por nosotros. El análisis de correlación entre el estándar secundario y el estándar de referencia indica la similitud entre los 2 estándares y por tanto, las mediciones con ambos patrones (fig. 3). La exactitud es el grado de identidad de valores analíticos obtenidos con un método y el contenido real del parámetro.
La recuperación del sistema para 5 muestras diferentes se ubica desde 85 y 111 %; el valor promedio del recobrado es de 99,78 %, lo que permite afirmar la alta exactitud obtenida, aunque en la primera y última muestras correspondientes al primero y último puntos de la curva los valores son ligeramente superiores al 10 %, dada por la baja concentración de la muestra y por tanto menor DO en el segmento inferior, y por una menor pendiente en el caso del segmento superior.
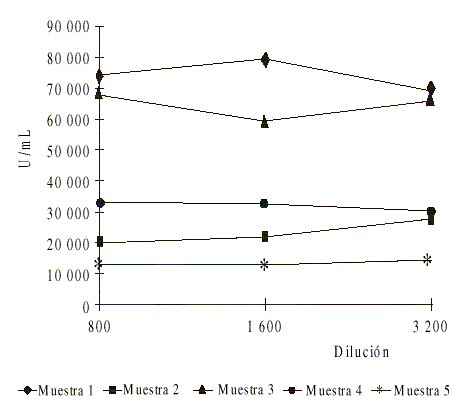
La prueba de paralelismo de las muestras ensayadas mostró una independencia del valor de la concentración de cada muestra de la dilución de trabajo utilizada, para el rango de medición evaluado. La prueba exhibió un coeficiente de variación entre las muestras inferior al 10 % (fig. 4).
Fig. 4. Paralelismo del ELISA de proteína VA-MENGOC-BC®.
]]> El análisis de la linealidad mostró que los valores observados se encontraban dentro del intervalo de ± 10 % con respecto al valor esperado (tabla 4).Estos resultados avalan la adecuada linealidad de la curva estándar y se corresponden con los reportados por otros autores para sistemas ELISA,15 lo cual posibilita confiar en estudios posteriores con esta técnica in vitro.
Se define como límite de detección o detectabilidad, a la mínima cantidad detectable por un método analítico, es decir, la cantidad mínima diferenciable de O, que en nuestro caso fue de 700 U/mL. Pensamos que este límite de detección es adecuado para nuestros propósitos, si se tiene en cuenta el rango de cuantificación empleado.
Para evaluar esta vacuna se han empleado los términos de seroconversión y serorrespondedor, dados por un incremento en la concentración de anticuerpos con respecto a los valores obtenidos previa vacunación, mayores que 4 en el primer caso y que 2 para el segundo.8,9 Aquellos valores inferiores al límite de detección deben sustituirse por su mitad,16 en este caso 350 U/mL, de esta manera la clasificación de la respuesta es más objetiva, sobre todo para aquellos valores extremadamente bajos detectados en las muestras tomadas antes de comenzar el esquema de vacunación.
Este ELISA de apropiada precisión y exactitud, caracterizado de forma adecuada, es útil para ser usado en la evaluación del componente proteico de VA-MENGOC-BC® y probablemente en estudios seroepidemiológicos para explorar la respuesta contra las proteínas de membrana externa del meningococo B cepa B4P1.15.
SUMMARY
An indirect ELISA test was optimised in which B meningoccocus outer membrane proteins included in the Cuban Vaccine known as VA-MENGOC-BC were used as capture antigents. Specific antibodies in serum samples from vaccinated individuals were detected using a human anti-IgG conjugate, i,e, alkalyne phosphatase, thus the reaction developed with a specific substrate called p-nitrophenilphophate. Standard serum was obtained from a reference standard, the gage curve range was 625 to 20 000/mL. The control serum was selected from the most interesting areas for the samples, hence, assay characteristics were determined. Intra-assay, inter-assay and total inaccuracies were lower than 10 % in the most linear area of the curve. Detectability was 700/mL. Recovery, paralelism and linearity studies showed an under 10 % innaccuracy.
Subject headings: NEISSERIA MENINGITIDIS; MENINGITIS; MENINGOCOCCAL/diagnosis; MENINGOCOCCAL/inmunol; MENINGOCOCCAL/therapy; ENZYM-LINKED; IMMUNO-SORBET ASSAY/methods; VACCINES.
REFERENCIAS BIBLIOGRÁFICAS
- Buckmaster ND, Boyce N. Two unusual presentations of N.m infection. Med J Aust 1993;58:266.
- Jones DM. Current and future trends in immunization against meningitis. J Antimicrob Chemothier 1993:31(Suppl B):93-9.
- Varcárcel M, Rodríguez R, Terry H. La enfermedad meningocócica en Cuba. Cronología de una epidemia. 1 rev. La Habana: Editorial Ciencias Médicas, 1991:111-229.
- Sierra VG, Campa C, Varcarcel M. Vaccine against group B Neisseria meningitidis: protection trial and mass vaccination results in Cuba. NIPH Ann 1991;14:195.
- Sierra VG, Campa C, García L, Sotolongo F, Izquierdo L. Efficacy evaluation of the Cuban vaccine VA-MENGOC-BC against disease caused by serogroup B Neisseria meningitidis. En: Achtman M, Kohl P, Marchal C, Morreli G, Seiler A, Thiesen B, eds. Neisseriae 1990. Berlin: Ed. Walter de Gruyter, 1991:129-34.
- Milagres LG, Ramos SR, Sacchi CT, Menes CA. Immune response of Brazilian children to a Neisseria meningitidis serogroup B outer membrane protein vaccine: comparison with efficacy. Infect Immun 1994;62:4419-24.
- Moraes JC, Perkins BA, Camargo MC. Protective efficacy of serogroup B meningococcal vaccine in Sao Paulo, Brazil Public Health. Lancet 1992;31:1071-8.
- Respuesta inmune humoral a las proteínas de una vacuna antimeningocócica en un ensayo realizado en Antioquia, Colombia. Bol of Sanit Panam 1995;118(4):285-94.
- Fernández J, Malberty J, Sotolongo F, Bacallao J, Camaraza M, et al. Cinética de la respuesta de anticuerpos bactericidas y de la IgG específica en individuos vacunados con VA-MENGOC-BC. Rev Cubana Hematol Inmunol Hemoter 1997;13(1):38-45.
- Statgraphics® plus for WindowsTM Version 1.0. Statistical Graphics. Corp. USA 1994.
- Plikaytis BD, Turner SH, Gheesling LL, Carlone GM. Comparisons of standard curve-fitting methods to quatitate Neisseria meningitidis group A polysaccharide antibody levels by enzyme-linked immunosorbent assay. J Clin Microbiol 1991;29:1439-46.
- Chaloner-Larsson G, Anderson R, Egan A. A WHO guide to good manufacturing practice (GMP) requirements. Part 2: Validation of analytical assays. Geneva: WHO, 1997:65-95.
- Broughton PMG, Bergonzi C, Lindstedt G, Loeber IG, Malan PG, Mathieu M, et al. Guidelines for a user laboratory to evaluate and select a kit for its own use. Part 1. Quantitative tests. European Committee for clinical laboratory Standard, 3;3,1986.
- Voller A, Bidwell DE, Bartlett A. The enzyme linked inmunosorbent assay (ELISA). London: Nuffield laboratories of comparative medicine: 1979:4-44.
- Kuhlmann WD, Rieger J. Diphtheria immunity of a West German population by measurement of antitoxin antibodies with enzyme-linked immunosorbent assay. Immunol Infect Dis 1995;5:10-4.
- Papaevangelou G, Karvelis E, Alexiou D, Kiossoglou K, Roumeliotou A, Safary A. Evaluation of a combined tetravalent diphteria, tetanus, whole cells pertussis and hepatitis B candidate vaccine administered to healthy infants according to a three-dose vaccination schedule. Vaccine 1995;13(2):175-8.
Recibido: 16 de marzo de 1998. Aprobado: 15 de noviembre de 1998.
Lic. Xenia Ferriol Marchena. Instituto "Finlay". Ave 27 No. 19805, AP 16017, La Lisa, La Habana, Cuba. CP 11600.
E.mail:inmunoquimica@finlay.edu.cu
1 Licenciada en Bioquímica. Aspirante a Investigadora.
2 Licenciada en Bioquímica. Investigadora Agregada. ]]>
4 Técnico Medio en Procesos Biológicos.
5 Especialista de I Grado en Inmunología.
6 Licenciado en Radioquímica. Aspirante a Investigador.