Instituto de Medicina Tropical Pedro Kourí
Lic. Ana M. Montalvo Álvarez,1 Lic. Lianet Monzote Fidalgo,2 Lic. Lisset Fonseca Géigel,3 Ing. Ivón Montano Goodridge,4 Dr. Luis Fonte Galindo,5 Dr. Manuel Soto6 y Dr. José M. Requena6
Se construyó una genoteca de Leishmania amazonensis en vector de expresión en células eucariotas (pEF1HisA, pEF1HisB, pEF1HisC). Se prepararon 2 subgenotecas con un número aproximado de 500 clones cada una y ratones BALB/c fueron inmunizados con 50 mg/0,1 mL de ADN de cada una; 2 inmunizaciones por vía IM, con 15 d de intervalo fueron realizadas. Grupos de ratones controles fueron inmunizados con ADN del plásmido vacío, con antígeno soluble del parásito (100 mg/0,1 mL) y solución salina fisiológica. Se midió el tamaño de las lesiones durante 12 semanas y al final del experimento, la carga parasitaria en los sitios de lesión fue determinada por el método de microtitulación en placas. Los ratones inmunizados con ADN 1, controlaron el tamaño de las lesiones, así como también los inmunizados con antígenos solubles, lo que alcanzó diferencia estadística (p< 0,05) en relación con el resto de los grupos, cuyas lesiones aumentaron de manera creciente. La carga de parásitos encontrada en los sitios de lesión corroboró los resultados anteriores, encontrando un número de promastigotes significativamente menor en aquellos que habían sido protegidos. Se concluyó que en la subgenoteca ADN1 deben existir genes, o fragmentos de genes, cuya expresión in vivo resulta protectora contra el reto, en el modelo murino empleado.
Palabras clave: Genoteca, genes, Leishmania amazonensis, ratones BALB/c, vacuna de ácidos nucleicos, inmunización con ADN.
Los protozoos del género Leishmania constituyen parásitos intracelulares obligados de los macrófagos y otras células mononucleadas del hospedero vertebrado. Estos causan un grupo de enfermedades en el hombre y los animales que van desde lesiones cutáneas simples de cura espontánea, hasta la diseminación visceral severa, que generalmente causa la muerte.1
Las leishmaniosis están ampliamente distribuidas en numerosas regiones geográficas de América, Asia, África y el sur de Europa. Diversos procedimientos han sido empleados en la búsqueda de protección contra algunas de sus formas clínicas,2 incluida la reciente tecnología de inmunización con ácidos nucleicos,3 sin que hasta el momento exista alguno completamente efectivo .
Se ha realizado la vacunación de ratones con ADN codificante para algunos antígenos de Leishmania, que incluyen la gp63,3 LACK,4 PSA-2,5 reportándose diferentes grados de protección, pero cada vez se hace más evidente la necesidad de utilizar más de un antígeno, o la acción cooperada de varios, para lograr una protección eficaz.
]]> Ejemplo de esto lo constituyen los resultados reportados por Dumonteil y otros,6 donde ratones inmunizados con plásmidos codificantes para los antígenos GP46, GP63 y CPb, mostraron estar mejor protegidos contra el reto con L. mexicana cuando fueron inmunizados con el conjunto de estos, que con los plásmidos individualmente. De igual forma, la vacunación con un cóctel de plásmidos que contenía los genes que codifican para las cisteíno proteinasas (CP) A y B de Leishmania, de reconocida acción protectora, evidenció un incremento en la respuesta inmune celular y humoral específicas, cuando se compara con la inmunización con el ADN de las CP, administrados individualmente.7Utilizando como inmunógeno ADN total de una genoteca de Lm. amazonensis construida en vector pcDNA3, se obtuvo previamente un control significativo y transitorio de las lesiones causadas en ratones susceptibles por parásitos infectivos,8 lo cual demostró que este acercamiento es aún explorable en la búsqueda de alternativas para la protección contra esta parasitosis. La utilización de grupos más pequeños de genes, de talla conocida, o fragmentos de estos, pudiera acercar a la identificación futura de potenciales inmunógenos.
Siguiendo aproximaciones enómicas, actualmente en boga, 2 trabajos, publicados recientemente, han demostrado que la utilización de genotecas de Leishmania y administradas como vacunas genéticas pueden en sí mismas constituir sistemas de protección9 o ser una aproximación interesante para identificar nuevas moléculas del parásito con capacidad de inducir inmunoprotección en el hospedero.10
Basados en estos trabajos, los autores de este estudio se propusieron inmunizar ratones BALB/c con ADN de subgenotecas de Leishmania amazonenzis y estudiar su efecto protector contra el reto de promastigotes infectivos de la misma especie de parásito.
Se utilizó la cepa MHOM/77/LTB0016 de Leishmania mexicana amazonensis, gentilmente cedida por el Instituto Oswaldo Cruz, Río de Janeiro, Brasil. Los parásitos fueron mantenidos en medio RPMI (Gibco), suplementado con 10 % de suero fetal bovino y una mezcla de ampicilina y estreptomicina a 250 mg/mL y 100 UI respectivamente, a 26 ºC.
La cepa de E. coli DH5a (New England Biolabs) fue utilizada para la construcción de la genoteca.
Los ratones isogénicos BALB/c, hembras, de 6 a 8 semanas de edad y peso entre 16 y 18 g, fueron suministrados por el Centro Nacional de Producción de Animales de Laboratorio (CENPALAB), Cuba.
El ADN genómico se obtuvo a partir de parásitos en su fase estacionaria de crecimiento, tras centrifugación y lavado con PBS (tampón fosfato 0,1 M; NaCl 0,15 M; pH 7,2 . El sedimento se resuspendió suavemente en tampón de lisis (0,15 M de NaCl, 0,1 M de EDTA y 0,5 % de SDS), al que se añadió proteinasa K hasta una concentración final de 0,1 mg/mL. Tras 30 min a 50 °C, se realizaron sucesivas extracciones con fenol/cloroformo, fenol /cloroformo /alcohol isoamílico, y posteriormente, se añadió al sobrenadante 0,1 vol de NaAc y 2,5 vol de etanol absoluto, dejando reposar en hielo. Después de la centrifugación, se lavó con etanol a 80 %. El sedimento se resuspendió en tampón TE (10 mM Tris HCl, 0,1 mM EDTA) y se digirió con RnasaI (20 mg/mL) para eliminar los restos de ácido ribonucleico (ARN), incubando 30 min a 37 °C. Después, se realizó una nueva extracción con fenol/cloroformo/alcohol isoamílico, para eliminar los restos de enzima. Al sobrenadante se le añadió ½ vol NH4Ac 7,5 M y 2 vol de etanol absoluto frío, incubando en hielo nuevamente, se centrifugó y lavó después con etanol 80 %. Por último, el sedimento de ADN se resuspendió en tampón TE.
La calidad del ADN se analizó por electroforesis en gel de agarosa 1 % en tampón de corrida trisborato-EDTA, aplicando las muestras disueltas en azul de bromofenol 0,25 % en solución de sacarosa 40 %.
El ADN genómico fue digerido con la enzima Sau 3A (Boehringer Mannheim). Numerosas concentraciones de enzima y tiempos de incubación fueron ensayados. Los productos de la digestión fueron sometidos a corrida electroforética, en las condiciones ya descritas, extrayendo los fragmentos de talla comprendida entre 4-5 kb, que fueron purificados utilizando el kit de extracción de bandas de ADN en geles de agarosa Concert Rapid TM Gel Extraction System (GIBCO BRL, Life Technologies), para realizar la ligasón.
La ligasón de los fragmentos de ADN genómico con el vector, en las proporciones adecuadas, se realizó utilizando la enzima T4 DNA ligasa (Boehringer Mannheim), dejando la mezcla a temperatura ambiente, toda la noche. El producto de la ligasón se transformó en células DH5a competentes, mediante choque térmico de 42 °C por 30 s, transfiriendo de inmediato a hielo por 3 min. Posteriormente, se añadieron 900 mL de medio SOB (2 % bactotriptona; 0,5 % extracto levadura; 0,05 % NaCl; 2,5 mM KCl; 10 mM MgCl2; pH 7,0) y se incubó a 37 °C por 45 min. Por último, las células se sembraron en placas LB-ampicilina, manteniéndose toda la noche en incubación a 37 °C. Se realizó el control de la transformación utilizando el plásmido pUC18.
Al día siguiente, se chequeó la calidad de la transformación, cuantificando el número de colonias obtenidas. Una muestra de 10 clones tomados al azar fue sembrada de forma independiente en 2 mL de medio LB y colocados en agitación a 37 °C toda la noche. Se realizó la extracción de ADN en cada caso, digiriendo posteriormente una alícuota de este con la enzima Eco RI, para conocer si dichos clones eran o no recombinantes. Los productos de la digestión fueron analizados por corrida electroforética en gel de agarosa. Todo el proceso de transformación se repitió 2 veces, partiendo de la misma mezcla de ligasón.
Todos los clones obtenidos en cada transformación fueron reunidos en 2 grupos diferentes (ADN1 y ADN2). Las colonias fueron cuidadosamente arrastradas a un erlenmeyer que contenía 10 mL de medio LB con 100 mg/mL de ampicilina, dejando crecer en agitación, a 37 °C por 4 h. Pasado este tiempo, se añadió medio LB en cantidad suficiente para completar 100 mL totales y 50 mg/mL de ampicilina, permitiendo crecer, en iguales condiciones, toda la noche. La purificación de cada grupo de clones se realizó utilizando el kit de purificación masiva de plásmidos Qiagen Maxi Kit, (QIAGEN). Igualmente, se realizó la purificación masiva del plásmido vacío, procediendo de la misma forma.
Para realizar los estudios de inmunización con las subgenotecas y el reto, los animales se dividieron de la forma siguiente:
A: grupo inmunizado con la subgenoteca ADN 1 ( 50 mg / 0,1 mL) n= 5
B: grupo inmunizado con la subgenoteca ADN 2 (50 mg / 0,1 mL) n= 5
C: grupo inmunizado con el plásmido vacío (50 mg/ 0,1 mL) n= 5
D: grupo inmunizado con antígenos solubles de L. amazonensis (100 mg/0,1 mL) n= 5
E: grupo inmunizado con solución salina fisiológica (0,1 mL) n= 5
Para determinar la carga parasitaria presente en la lesión, al finalizar el experimento anterior, se utilizó el método de microtitulación en placas.11 Brevemente, se tomaron las piezas musculares de los sitios de lesión en cada ratón, que fueron pesadas y luego homogenizadas en 4 mL de medio de cultivo de Schneider; se realizaron diluciones cuádruples seriadas, partiendo de 15 mL del homogenado y 225 mL de medio de cultivo. Las placas fueron incubadas a 26 ºC y examinadas luego de 7 y 15 d, utilizando un microscopio invertido, hasta encontrar la máxima dilución que contuviera, al menos, un promastigote vivo. El número de parásitos por gramo fue calculado según Gagneaux, mediante la fórmula siguiente:11
# de parásitos/gramo de tejido= 400 (1/ D+ ´ Po)
D+: última dilución positiva
Po: peso de la pieza muscular
Se calcularon las medias de la carga parasitaria de cada grupo de animales y se compararon por análisis de varianza mediante el Programa Statistica para Windows.
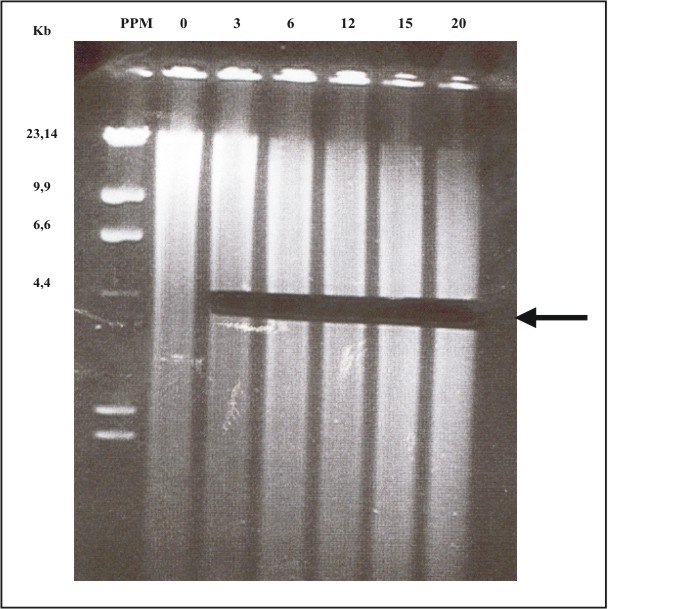
Se construyó una genoteca de expresión de Leishmania amazonensis, que fue altamente representativa del genoma del parásito, porque se utilizaron fragmentos de ADN de talla correspondiente a la densidad génica en esta especie (fig. 1). De los clones testados 100 % fue recombinante, lo que se comprobó en la corrida electroforética de los productos de la digestión de las colonias seleccionadas al azar (fig. 2) cuyo ADN fue extraído y digerido con EcoRI. La talla de las distintas bandas obtenidas indica, en todos los casos, que superan la talla del plásmido vacío, demostrando que todos los clones han incorporado secuencias de ADN del parásito. El ADN obtenido de las subgenotecas tuvo la calidad y concentración adecuadas para realizar las inmunizaciones que los autores de este trabajo se propusieron.
Fig. 1. Digestión de ADN genómico de Leishmania amazonensis con la enzima Sau3A. La flecha indica los fragmentos escogidos, cuya talla corresponde aproximadamente con la densidad génica de la especie. Los números 0, 3, 6, 12, 15 y 20, son los distintos tiempos (minutos) de incubación con la enzima. El patrón de peso molecular PPM, fue l Hind III.
]]>Fig. 2. Corrida electroforética de los productos de la digestión de 10 colonias escogidas al azar de la genoteca. El ADN de cada una fue digerido con la enzima EcoRI. La suma de los fragmentos en cada caso, demuestra que la talla es mayor que la del plásmido vacío, esto confirma que son clones recombinantes. PPM: patrón de peso molecular. Los números 1 al 10 corresponden a las colonias digeridas.
Los grupos de ratones A y D mostraron una disminución en el tamaño de las lesiones, con respecto al resto de los grupos, que alcanzó diferencia significativa para p< 0,05 (fig.3). En el grupo A esta diferencia se evidenció desde la semana 6 posterior al reto. En ambos casos, la diferencia se mantuvo hasta el final del experimento, la semana 12.
Fig. 3. Evolución de las lesiones en los distintos grupos de ratones inmunizados y retados con promastigotes infectivos. Los ratones inmunizados con ADN1 y antígenos solubles (grupos A y D) lograron controlar de manera significativa la talla de sus lesiones, a partir de la semana 6, hasta la 12. En el resto de los grupos (B, C y E) el tamaño de las lesiones aumentó de forma creciente durante todo el experimento.
En el grupo B, animales inmunizados con la subgenoteca G2, curiosamente no existió diferencia en la talla de las lesiones con respecto al control, ni tampoco con respecto al plásmido vacío, observándose en estos ratones un incremento continuo de las lesiones hasta el final del experimento.
]]> Estos resultados fueron corroborados al determinar la carga parasitaria en los sitios de las lesiones en los distintos grupos (fig. 4). En los ratones inmunizados con el grupo de clones ADN1, así como en el grupo inmunizado con antígenos solubles, se cuantificaron aproximadamente 100 parásitos/g, a diferencia del grupo inmunizado con ADN2 y los controles, en los cuales la cifra de promastigotes fue más de 2 veces superior. La diferencia entre los ratones inmunizados con ADN1 y ASL, con respecto al resto de los grupos, fue estadísticamente significativa (p< 0,01).
Fig. 4. Carga parasitaria en los sitios de lesión en los distintos grupos de animales, determinada al finalizar los experimentos. Las cifras corresponden al log10 del número de promastigotes cuantificados en cada caso.
La introducción por inyección intramuscular o intradérmica de ADN desnudo que codifica para antígenos de interés, la transcripción dentro de las células del hospedero y la presentación al sistema inmune de proteínas extrañas endógenamente generadas, son conocidos como vacunación con ADN.12
Esta tecnología tiene entre sus ventajas la simplicidad, bajo costo, estabilidad, plegamiento adecuado de la proteína antigénica y una adecuada presentación del antígeno, que conduce a una fuerte respuesta inmune, razones por las cuales muchos investigadores la han utilizado en la búsqueda de protección contra diversos agentes infecciosos.12-14
Algunos autores han demostrado la factibilidad de la inmunización con genotecas o bibliotecas de cDNA para lograr protección contra algunas enfermedades.14-16 En casi todos los casos este acercamiento ha sido utilizado para la búsqueda y el aislamiento de genes implicados en la obtención de una deseada respuesta inmune contra el patógeno.
Los autores de este estudio sustentan la conveniencia de la utilización de subgenotecas genómicas o grupos de genes para estos fines, dada la ventaja que representa evitar la selección de genes estadio-específicos en organismos digénicos, como Leishmania, o con un alto nivel de expresión, como ocurre en las bibliotecas de cDNA. Obviamente, esta aproximación es solo posible en organismos como Leishmania en el que los genes no poseen intrones y se encuentran agrupados con una elevada densidad en el genoma.17 Por otra parte, la mayor protección debería estar vinculada al efecto combinado de varios antígenos, por lo que la inmunización con la subgenoteca en sí representa, según la opinión de los autores de este trabajo, un acercamiento válido per se para lograr inmunocompetencia contra el parásito.
]]> Ha sido previamente reportado que ratones inmunizados con una mezcla de antígenos solubles de Leishmania spp. son protegidos contra el reto de parásitos infectivos,18,19 lo que se confirma con los resultados obtenidos en el grupo D. Pero también en el grupo A se obtuvo una respuesta protectora contra el reto.La existencia de diferencias estadísticamente significativas entre los animales de los grupos A y D, comparados con el resto, puso de manifiesto su capacidad de respuesta, al evidenciarse no solo un retardo en el crecimiento de las lesiones, sino también en su talla. Este hecho hace pensar que en la subgenoteca (ADN 1) existen genes o fragmentos de genes que al ser expresados in vivo, tras la inmunización, pudieran asumir la estructura nativa, e inducir protección para esta especie de Leishmania.
En el caso de los grupos controles: los animales inmunizados con el plásmido vacío y con SSF, ambos se comportaron de manera muy similar, alcanzando una talla de las lesiones que no difirió entre uno y otro, a pesar de que ha sido previamente reportado que el ADN plasmídico produce un efecto estimulador inespecífico de la respuesta inmune,20 pero en este caso, la protección no se hizo evidente, solamente, por la inmunización con el plásmido.
Esas propiedades inmunoestimulatorias plasmídicas se han relacionado con la secuencia del dinucleótido CpG, mucho más frecuente en bacterias que en vertebrados, que promueve respuestas de células B, T y T citotóxicas contra antígenos proteináceos;21,22 por lo que se considera como un nuevo y poderoso adyuvante.
Curiosamente, el grupo B de ratones no logró controlar sus lesiones en forma alguna. Una explicación a este hecho sería que en esta subgenoteca no existe ningún gen inductor de protectividad o, alternativamente, que en esta subgenoteca existan genes de Leishmania promotores de virulencia.
Sería interesante estudiar el nivel de inmunocompetencia generado por inmunizaciones como la realizada aquí, que implican la expresión de varios determinantes antigénicos, y la utilización además de un adyuvante que module la respuesta inmune celular hacia la población Th1, esencial en el control de esta enfermedad23 y otras parasitosis causadas por otros organismos intracelulares.
Finalmente, se quiere señalar que este es un reporte de la respuesta in vivo de ratones inmunizados con grupos no identificados de genes de Leishmania amazonensis, al reto con el parásito infectivo. Futuros trabajos llevarán a caracterizar esta respuesta al tiempo que se intentará identificar dentro de los clones presentes en la subgenoteca ADN1 aquellos responsables de la inmunoprotección del grupo. Estos estudios contribuirán a encontrar nuevas formas de combatir esta enfermedad que aún permanece sin control.
A genomic library of Leishmania amazonensis in expression vector of eukaryote cells (pEF1HisA, pEF1HisB, pEF1HisC) was prepared. Also two subgenomic libraries having each 500 clones approximately were created and BALB/c mice were immunized with 50 mg/0,1 mL of DNA from each. Two immunizations were administered intramuscularly at 15-day interval. Groups of control mice were immunized with DNA from empty plasmid pEF1His, with soluble parasite antigen (100 mg/0,1 mL) and saline solution. The size of lesions was measured for 12 weeks and at the end of the experiment, the parasite load at lesion sites was determined by plaque microtitration method. In mice immunized with subgenomic library DNA1 and with soluble antigens,the size of lesions was controlled, which reached an statistical difference (p< 0,05) in relation to the rest of groups whose lesions increased. The parasite load found in lesion sites confirmed the previous results; the number of promastigots was significantly lower in those mice already protected. It was concluded that in subgenomic library DNA1 there should be genes or gene fragments whose in vivo expression induces protective immune response against the challenge in the murine model used.
Key words: Leishmania amazonensis, expression genomic library, DNA immunization.
Recibido: 18 de febrero de 2004. Aprobado: 19 de marzo de 2004. ]]> Lic. Ana M. Montalvo Álvarez. Instituto de Medicina Tropical Pedro Kourí. Apartado 601, Marianao 13, Ciudad de La Habana, Cuba. Teléf: 2020426. Correo electrónico: amontalvo@ipk.sld.cu
1 Licenciada en Ciencias Biológicas. Investigadora Auxiliar. Profesora Instructora.