Conservación de cepas vacunales de Leptospira en nitrógeno líquido
Preservation for vaccinal strains of Leptospira at liquid nitrogen
]]>
Reinier Borrero MauraI; Niurka Batista SantiestebanII; Kirenia Blain TorresIII; Yolanda Valdés AbreuIV
ILicenciado en Microbiología. Instituto Finlay. Ciudad de La Habana, Cuba.
IIIngeniera Química. Instituto Finlay. Ciudad de La Habana, Cuba.
IIITécnico Medio en Química Industrial. Instituto Finlay. Ciudad de La Habana, Cuba.
IVTécnico Medio en Medicina Veterinaria. Instituto Finlay. Ciudad de La Habana, Cuba.
INTRODUCCIÓN: las cepas de Leptospira interrogans que integran la vacuna cubana vax-SPIRAL® son conservadas en medio semisólido de Fletcher, el cual garantiza el mantenimiento de la viabilidad de las células por pocos meses.
OBJETIVO: en este estudio, se evaluó la crioconservación en nitrógeno líquido de 6 variantes de crioprotectores como método de conservación a largo plazo de las cepas de Leptospira interrogans, utilizadas como antígenos en la vacuna antileptospirósica vax-SPIRAL®.
MÉTODOS: la viabilidad se evaluó periódicamente según el rendimiento celular alcanzado por las cepas recién descongeladas en medio EMJH. La estabilidad de la virulencia fue estimada en hámster. La antigenicidad antes y después de la crioconservación fue comparada mediante microaglutinación, frente a una batería de antisueros de referencia correspondientes a los serogrupos vacunales.
RESULTADOS: solo el empleo de dimetilsulfóxido a 2,5 y 5 %, y glicerol 2,5 % como agentes crioprotectores permitió una rápida recuperación de las 3 cepas, tras 19 meses de crioconservación sin afectación de su virulencia y antigenicidad.
CONCLUSIONES: los resultados obtenidos demuestran la factibilidad de la crioconservación en nitrógeno líquido con un apropiado agente crioprotector, como método de conservación de cepas vacunales de Leptospira.
Palabras clave: Leptospira interrogans, cepas vacunales, crioconservación.
INTRODUCTION: Leptospira interrogans strains of Cuban vaccine vax-SPIRAL®are preserved in Fletcher's semi-solid medium, which guarantees the preservation of the cell viability for a few months. ]]>
OBJECTIVE: to evaluate the cryopreservation at liquid nitrogen of 6 different cryoprotectors as a long-term preservation method for Leptospira interrogans strains used as antigens in vaccine vax-SPIRAL® against leptospirosis.
METHODS: viability was systematically evaluated according to the cell yield of the recently thawed strains in EMJH medium. Virulence stability was estimated in hamsters and antigenicity was evaluated by microscopic agglutination test using reference antisera from vaccinal serogroups.
RESULTS: the use of 2.5% and 5% dimethyl sulfoxide, and 2.5% glycerol allowed quick recovery of the three strains without virulence or antigenicity depletion after 19 months of cryopreservation.
CONCLUSIONS: the results showed the feasibility of the cryopreservation at liquid nitrogen using suitable cryoprotectant as a preservation method for vaccinal strains of Leptospira.
Key words: leptospira interrogans, vaccinal strains, cryopreservation.
]]>
INTRODUCCIÓN
La vacuna antileptospirósica trivalente vax-SPIRAL® es una suspensión de células enteras inactivadas de 3 cepas autóctonas de Leptospira interrogans pertenecientes a los serovares Canicola, Copenhageni y Mozdok.1 Por causa de la reconocida disminución de la antigenicidad con la atenuación de la virulencia de este microorganismo,2 resulta necesaria la disponibilidad de cultivos muy virulentos para ser utilizados como semillas durante la producción o para los ensayos de potencia de la vacuna en modelos animales. Tradicionalmente las cepas vacunales de Leptospira son conservadas en medio semisólido de Fletcher, el cual posee suero de conejo como constituyente esencial, que de modo potencial garantiza su viabilidad durante 4 o 5 meses. Periódicamente el microorganismo es inoculado y reaislado de animales de laboratorio susceptibles para emplear el sistema inmune animal como mecanismo de selección de las células muy virulentas y eliminar aquellas con una capacidad patogénica disminuida.3
Sin embargo, dada la alta variabilidad nutricional de los diferentes lotes de suero y como consecuencia la inconsistencia en el crecimiento del microorganismo, el medio de conservación tradicionalmente empleado no garantiza una óptima estabilidad de la viabilidad de las cepas vacunales. Además, los frecuentes pases por animales en ocasiones son inapropiados producto del gasto de materiales y recursos que conlleva, así como el riesgo que implica para el personal de laboratorio la manipulación de cepas virulentas. En tal sentido, resulta necesaria la búsqueda de un método de conservación de Leptospira que garantice una duradera y reproducible estabilidad en la viabilidad y virulencia del microorganismo, lo que permitirá incrementar la consistencia entre procesos productivos, disminuir los costos de producción y de las investigaciones y también minimizar los riesgos para el personal.
La crioconservación ha constituido uno de los principales métodos en la preservación de cepas bacterianas al nivel mundial. En la actualidad, la crioconservación constituye, un método tradicional pero efectivo para la conservación de ceparios de Leptospira al nivel internacional.4-7 Los cultivos con glicerol o dimetilsulfóxido (DMSO) almacenados a - 70 ºC o en nitrógeno líquido mostraron resultados satisfactorios en el mantenimiento de la viabilidad y virulencia de este microorganismo.4-7 Estudios recientes confirmaron que el empleo de glicerol o DMSO permiten mantener estables la viabilidad, virulencia y antigenicidad de las 3 cepas de Leptospira que conforman a la vacuna vax-SPIRAL® durante 7 meses de conservación en - 70 ºC como mínimo.8 En el presente trabajo se evalúa la efectividad del método de crioconservación en nitrógeno líquido usando cepas vacunales de Leptospira interrogans, así como la estabilidad del crecimento bacteriano, la virulencia y la antigenicidad de las cepas en estudio durante un período de 19 meses.
MÉTODOS
]]>
]]>
Cepa bacteriana
Se emplearon en el estudio las cepas vacunales 87, 169 y 108 de Leptospira interrogans, pertenecientes a los serovares Canicola, Copenhageni y Mozdok, respectivamente, las cuales fueron originalmente aisladas a partir de material remitido al Centro Nacional de Epizootiología y Diagnóstico Veterinario de Ciudad de La Habana y donadas al Instituto Finlay. Desde su aislamiento las cepas fueron conservadas en medio semisólido de Fletcher.9 La virulencia fue mantenida a través de pases periódicos en hámster según los métodos descritos por Faine y otros.9
Cultivo para los estudios de crioconservación
Las cepas fueron cultivadas en medio proteico EMJH9 durante 7 d bajo condiciones de agitación (130 rpm, 30 ºC). Se evaluaron características culturales como movilidad y uniformidad celular mediante observación directa bajo el microscopio de campo oscuro y pureza mediante tinción de Gram y siembra en caldo triptona soya y caldo tioglicolato. Los cultivos puros con buena movilidad y uniformidad celular fueron considerados apropiados para los estudios de crioconservación.
]]>
Crioprotectores y procedimiento de crioconservación
Se evaluó la capacidad crioprotectora de diferentes concentraciones de glicerol (MERCK) y DMSO (BDH). Cultivos de las 3 cepas de Leptospira fueron mezclados separadamente con glicerol o DMSO estériles, hasta lograr una concentración final de 2,5, 5 y 10 % de cada crioprotector. Las mezclas de cultivo y crioprotector fueron envasadas en volúmenes de 1 mL, empleando criotubos (Nalgene) de 2 mL de capacidad con tapa de rosca, bien rotuladas. Todo el procedimiento fue realizado en un tiempo máximo de 30 min. Los criotubos fueron congelados y mantenidos a - 70 ºC durante un día y después fueron transferidos a un tanque de conservación de nitrógeno líquido.
Estabilidad de la viabilidad
La viabilidad de cada cepa conservada con cada variante de crioprotector fue evaluada tras 24 h, 3, 6, 9, 12 y 19 meses de conservación. De cada variante cepa/crioprotector, 3 criotubos fueron descongelados empleando baño de agua a 37 ºC y el contenido total de cada uno fue inoculado individualmente en 5 mL de medio EMJH. Tras 7 d de incubación a 30 ºC (bajo condiciones estáticas), se determinó la concentración celular de cada cultivo mediante conteo en cámara de Petroff-Hausser y se evaluaron características culturales como movilidad y uniformidad celular, por observación directa bajo el microscopio de campo oscuro. En cada evaluación se incluyeron como controles de crecimiento las 3 cepas vacunales crecidas en medio EMJH de manera satisfactoria.
Estabilidad de la virulencia
]]>
Previo a la congelación fue determinada la dosis letal media (DL50) de cada cepa en hámsters según la metodología propuesta por Fajardo y otros.10 Tras cada descongelación y ulterior cultivo en medio EMJH, se evaluó además la estabilidad de la virulencia usando grupos de 6 animales de 45 a 50 g de peso, los que fueron inoculados por vía intraperitoneal con cada variante de cepa/crioprotector; de ellos 2 con dosis estimadas a 100 veces el valor de DL50 (según determinaciones previas), 2 con 10 000 veces el valor de DL50 y otros 2 con el cultivo puro. Los animales inoculados fueron observados sistemáticamente durante 14 d posinoculación, con el registro de los niveles de supervivencia en cada caso.
Estabilidad de la antigenicidad
Fue evaluada la antigenicidad de cada cepa antes y después de cada descongelación mediante la técnica de microaglutinación (MAT)11 frente a antisueros policlonales de referencia específicos a cada serogrupo vacunal.
RESULTADOS
]]>
]]>
Estabilidad de la viabilidad
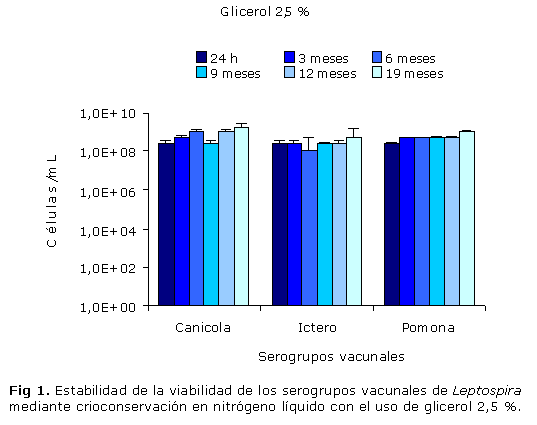
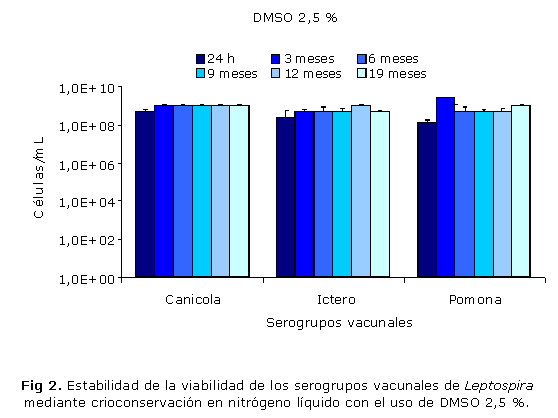
El uso de los agentes crioprotectores ensayados posibilitó el mantenimiento de la viabilidad de las cepas vacunales de Leptospira, en el tiempo con diferentes grados de eficiencia. De forma general, las variantes de agentes crioprotectores que garantizaron una completa estabilidad de la viabilidad de las 3 cepas fueron el DMSO a 2,5 y 5 %, y el glicerol 2,5 % (Figs. 1, 2 y 3), aunque la movilidad de los cultivos en todos los casos fue visiblemente superior con el empleo de DMSO. El glicerol 5 y 10 %, así como DMSO 10 % tuvieron un efecto variable en los diferentes serovares (Figs. 4, 5 y 6).
]]>
]]>
Los rendimientos celulares alcanzados por la cepa vacunal 87 del serovar Canicola, tras 7 d de incubación en medio EMJH luego de la descongelación, evidenciaron que no existieron diferencias apreciables en la estabilidad de la viabilidad con el empleo de los diferentes agentes crioprotectores (Figs. 1-6). Esta cepa fue capaz de sobrevivir en nitrógeno líquido tras 19 meses de conservación con cualquiera de las variantes de agente crioprotector empleados en este estudio.El glicerol 2,5 % y DMSO a 2,5 y 5 % resultaron ser las mejores variantes de agentes crioprotectores para la cepa 169 del serovar Copenhageni, porque permitieron mantener estable la viabilidad de dicha cepa durante todo el período evaluado (Figs. 1, 2 y 3). El glicerol 5 % solo garantizó la supervivencia de esta cepa vacunal hasta el noveno mes de conservación, porque en los siguientes meses no se observó crecimiento tras 7 d de incubación en medio EMJH luego de la descongelación (Fig. 4). En el caso del glicerol 10 % y DMSO 10 %, ninguna de las 2 variantes logró mantener la viabilidad de la cepa ni siquiera tras 24 h de conservación (Figs. 5 y 6).
La cepa vacunal 108 del serovar Mozdok mostró elevados grados de recuperación con cualquiera de las concentraciones de DMSO ensayadas o glicerol 2,5 y 5 % (Figs. 1, 2, 3, 4 y 6), por encima de 5 % el glicerol fue ineficiente como crioprotector tras 6 meses de evaluación (Fig. 5).
Estabilidad de la virulencia
Los procedimientos de crioconservación ensayados no condujeron a una disminución cuantitativa de la capacidad de las 3 cepas vacunales de Leptospira de producir infección letal en hámsters. Tras cada descongelación, todos los cultivos recuperados exitosamente e inoculados en animales con dosis equivalentes al valor de 100, 10 000 DL50 y cultivo puro de cada cepa produjeron la muerte por leptospirosis en la totalidad de los animales, sin variación aparente en el tiempo de aparición de los síntomas.
Estabilidad de la antigenicidad
]]>
Al comparar la antigenicidad de las cepas mediante MAT antes y después de cada descongelación, no se apreciaron diferencias en la capacidad de reaccionar con los respectivos antisueros policlonales. Durante todo el período de conservación evaluado las 3 cepas mantuvieron títulos idénticos a aquellos mostrados antes de la congelación (tabla).Tabla. Títulos de la técnica de microaglutinación de las 3 cepas vacunales de Leptospira interrogans frente a los antisueros
policlonales de referencia específicos a cada serogrupo en cada uno de los tiempos evaluados
| Cepas vacunales | T0 | 24 h | 1 mes | 3 meses | 6 meses | ]]> 9 meses | 12 meses | 19 meses |
| Canicola | 1/10480 | 1/10480 | 1/20960 | 1/10480 | 1/10480 | 1/20960 | ]]> 1/20960 | 1/10480 |
| Ictero | 1/10480 | 1/10480 | 1/10480 | 1/10480 | 1/10480 | 1/20960 | 1/20960 | ]]> 1/20960 |
| Pomona | 1/10480 | 1/10480 | 1/10480 | 1/20960 | 1/10480 | 1/10480 | 1/20960 | 1/10480 |
DISCUSIÓN
El objetivo fundamental de la conservación de cultivos bacterianos es mantener al microorganismo vivo en una condición lo más cercana posible al aislamiento original. La crioconservación permite detener las reacciones metabólicas y el deterioro biológico durante largos períodos, manteniendo la estabilidad genética del material crioconservado. Uno de los factores que posibilita la eficacia de la crioconservación como un método de conservación de cepas microbianas es la temperatura de almacenamiento, mientras la temperatura sea menor se logra con mayor eficiencia que el agua del medio se congele prácticamente toda, lo cual facilita que se detengan los procesos metabólicos de la célula que ocasionan su envejecimiento o deterioro.12 La conservación en nitrógeno líquido, donde se alcanzan temperaturas alrededor de los - 190 ºC, es superior en el mantenimiento de cepas bacterianas que la conservación a - 70 ºC. En este método resulta muy importante la adición de crioprotectores, grupo heterogéneo de sustancias de alta afinidad por el agua, que contribuyen a la supervivencia de la célula durante la crioconservación. Los crioprotectores disminuyen el punto de congelación del sistema y reducen la cantidad y el tamaño de los cristales de hielo durante el enfriamiento, lo cual contribuye a la protección física de las membranas y disminuye el incremento de la concentración iónica producto de la congelación del agua.13
Varios estudios avalan el empleo de la crioconservación como método eficaz para el mantenimiento de la viabilidad y virulencia de cepas de Leptospira interrogans por períodos prolongados,4,7 inclusive de las cepas empleadas en este estudio que han preservado estables sus características tras 7 meses de conservación en - 70 ºC.8 Aunque la mayoría de los daños a las células crioconservadas suelen ocurrir durante las etapas de congelación y descongelación, resulta necesario tener en cuenta el posible efecto citotóxico de los crioprotectores sobre el microorganismo, sobre todo a concentraciones elevadas donde un anhelado incremento del efecto crioprotector resulte superado por un letal efecto tóxico sobre la célula crioconservada.5
Ha sido estudiada con anterioridad la citotoxicidad del glicerol y el DMSO para varios serovares de Leptospira interrogans.4,5,8 Algunos de estos estudios demostraron que por encima de 10 % cualquiera de los 2 crioprotectores manifiesta determinado grado de citotoxicidad, con un efecto variable en dependencia del serovar incluido en el estudio. De cualquier forma, el glicerol ha mostrado 10 veces mayor capacidad citotóxica para Leptospira que el DMSO.5 Los resultados obtenidos en este trabajo sugieren igualmente una mayor toxicidad del glicerol en comparación con el DMSO, y se evidenció un efecto citotóxico del glicerol 10 % y DMSO 10 % a corto plazo sobre la cepa vacunal 169 del serovar Copenhageni, al no observarse crecimiento de la cepa tras 24 h de congelación (Figs. 5 y 6). El resultado anterior demuestra que la cepa del serovar Copenhageni es más sensible al efecto citotóxico de los agentes crioprotectores que las otras 2 cepas que conforman la vacuna vax-SPIRAL®.
La incrementada fragilidad de las células de Leptospira después de la congelación y descongelación, unido a la desventaja práctica de un lento crecimiento que dificulta la obtención de colonias tras el subcultivo en medio sólido, determinan que el crioprotector incorporado no pueda ser eliminado tras el proceso de crioconservación y posibilita su presencia en trazas en el producto final en el que son empleadas las cepas. El glicerol es un reactivo que está presente en algunos de los medios de cultivo para las leptospiras y, por lo tanto, su incorporación no afecta las características de la vacuna vax-SPIRAL®. En el caso del DMSO, sería un nuevo producto que se adicionaría en la confección de la vacuna, pero existen reportes de que el DMSO está permitido en trazas de hasta 50 mg en productos biofarmacéuticos para uso humano, al ser un solvente orgánico de origen vegetal con baja toxicidad.14 Por estas razones, el DMSO pudiera ser empleado como crioprotector en la criocoservación en nitrógeno líquido de cepas vacunales de Leptospira, destinadas para la producción de vacunas antileptospirosicas para uso humano. Tanto el DMSO 2,5 y 5 % permitieron la crioconservación de las 3 cepas vacunales de Leptospira interrogans durante los 19 meses de estudio. Por lo tanto, la mejor variante de crioprotector para la conservación de estas cepas en nitrógeno líquido lo constituye el DMSO 2,5 %, porque un incremento de la concentración hasta 5 % no ofrece diferencias en el mantenimiento de la viabilidad, virulencia y antigenicidad de este microorganismo.
Como resultado del presente estudio se logró comprobar que la crioconservación en nitrógeno líquido con el uso de un apropiado agente crioprotector permite mantener estable la viabilidad, virulencia y antigenicidad de las cepas vacunales de Leptospira durante 19 meses de conservación como mínimo, lo cual resulta un tiempo muy superior al logrado en el estudio con - 70 ºC.
]]>
REFERENCIAS BIBLIOGRÁFICAS
1. González M, Martínez R, Cruz de La Paz R, Infante JF, González I, Baró M, et al. Vax-Spiral®, vacuna antileptospirósica trivalente para uso humano; investigación, desarrollo e impacto sobre la enfermedad en Cuba. Biotecnología Aplicada. 2004;21(2):107-11.
2. Matsunaga J, Barocchi MA, Croda J, Young TA, Sanchez Y, Siqueira I, et al. Pathogenic leptospira species express surface-exposed proteins belonging to the bacterial immunoglobulin superfamily. Mol Microbiol. 2003;49(4):929-45.
3. Silva EF, Santos CS, Athanazio DA, Seyffer N, Seixas FK, Cerqueira GM, et al. Characterization of virulence of Leptospira isolates in a hamster model. Vaccine. 2008;26(31):3892-6.
4. Reed NE, Varney WC, Goddard RD, Wyeth PJ. The maintenance of challenge strains used in the potency test for canine Leptospira vaccines. Biologicals. 2000;28:25-8.
6. Palit A, Haylock LM, Cox JC. Storage of pathogenic leptospires in liquid nitrogen. J Appl Bacteriol. 1986;61:407-11.
6. Alexander A, Lessel E, Evans L, Frank E, Green S. Preservation of leptospiras by liquid-nitrogen refrigeration. Int J Syst Bacteriol. 1972;22:165-9.
7. Stalhein O. Viable, avirulent Leptospira interrogans serotype pomona vaccine: Preservation in liquid nitrogen. Appl Microbiol. 1971;22:726-7.
8. Borrero R, González A, del Puerto C, Batista N, Valdés Y. Conservación de cepas vacunales de Leptospira a -70 oC. Rev Cubana Med Trop. 2006;58(1):50-5.
9. Faine S, Adler B, Bolin C, Perolat P. Leptospira and leptospirosis. 2nd ed. Melbourne: MedSci; 1999.
10. Fajardo ME, Ortiz B, Chávez A, Gainza N, Izquierdo L, Hernández Y, et al. Normalización de la dosis letal 50 de las cepas de Leptospira interrogans utilizadas en el control de la vacuna antileptospirósica cubana para uso humano. Rev Cubana Med Trop. 1998;50:22-6.
11. Cole JR, Sulzer CR, Pursell AR. Improved microtechnique for the leptospiral microscopic agglutination test. Appl Microbiol. 1973;5:65-9.
12. del Puerto CA, García HM, Cedré B, Año G, Morales T, Alfaro A, Amat E, Mirabal M, Sotolongo F, Talavera A. Sistema de Lotes de Siembra de la cepa vacunal Vibrio cholerae 638. VacciMonitor. 2004;21(13).
13. Gherna R. Preservation. En: Gerhardt P, editor. Manual of Methods for General Bacteriology. 2nd ed. Washington DC: American Society for Microbiology; 1981. p. 208-17.
14. ICH Steering Committee. Guideline for residual solvents in pharmaceuticals for human use. International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Humans Use. FDA Federal Register. 1997;62(247):673-7.
]]>
Recibido: 28 de septiembre de 2009.
Aprobado: 15 de febrero de 2010.
Lic. Reinier Borrero Maura. Ave. 27 No. 19805, Lisa. AP 16017. CP 11600. Ciudad de La Habana, Cuba. Fax: (53-7) 208 6075; Teléf.: (53-7) 202 0986. Correo electrónico: rborrero@finlay.edu.cu ]]>